浅谈关于离子反应及共存问题的解题策略
江西省会昌县会昌中学(342600)
陈宗庭●
浅谈关于离子反应及共存问题的解题策略
江西省会昌县会昌中学(342600)
陈宗庭●
常见离子反应多在水溶液中进行,其可大致分为以下几个类型:(1)复分解型;(2)氧化还原型;(3)电离水解型.离子反应是高中化学的难点,题型简单、包含的知识面广、综合性强,在历年来各省份的高考题中频繁考这类题,这类题型的出题方式比较灵活,根据分值的大小,既可以出选择题,也可以夹杂在大题中,在大题目中的某一小问,这类题型因为既考验学生的基础扎不扎实,这种题往往涉及到的物质种类多,并且各种物质的电离、水解性质,都要考虑全面.本文就离子反应的题型介绍了几种解题技巧,以帮助同学学习.
离子反应;离子共存
水作为一种良好的溶剂,可以溶解大部分的反应物,反应物在水中溶解后,可以增大接触面,促进反应物充分反应.物质溶解在水里形成水溶液,有助于增大离子之间的接触面积、增加离子的碰撞概率.使得反应更加迅速快捷.在水溶液中发生的反应大部分属于离子反应,离子反应和离子共存问题是高考题中常考的题型,题目类型和分值分布都比较灵活,其主要考查离子共存、离子反应方程式书写与离子反应方程式正误判断、离子检验、溶液中离子浓度相对大小的比较等.
一、关于高中阶段离子方程式的题型汇总及解题方法归纳
1.书写离子方程式的要点
要点归纳:①离子方程式的前提条件(明确哪些可以写离子方程式);②准确把握物质的性质;③一切随条件变化而变化;④树立量的观点;⑤抓住主要矛盾改写化学式.
2.离子方程式正误判断
①违背客观事实;②化学符号书写错误,分子式写成离子,该用离子表示的写成分子式;③原子或电荷或得失电子不守恒,违反了电荷守恒,在溶液中离子反应前后,溶液均是电中性的;④化学计量数错误,或不约分或部分约分,离子反应方程也要遵循守恒定律.
二、溶液中离子共存问题解题方法归纳
离子共存问题要点归纳:

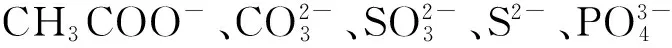
四反应,复分解反应,符合复分解反应就是说生成:沉淀、气体、水,这些都会改变溶液的组成.
规律总结:1.离子间能结合生成难溶性物质,则这些离子不能大量共存.

Ba2+Pb2+Ag+Ca2+Cu2+Mg2+Al3+Fe3+SO42-↓↓↓↓----CO2-3↓↓↓↓↓↓↓↓OH---↓↓↓↓↓↓
2.离子间能结合生成弱电解质,比如说常见的弱电解质:H2O、H2S、H2CO3那么这些离子不能在同一溶液中共存.
3.离子间能结合生成生成气体.常见的气体有:二氧化碳、二氧化硫、硫化氢、氨气.则这些离子不能大量共存.
4.溶液里的还原性物质与氧化性物质不能共存,溶液中的氧化性物质会氧化溶液中具有还原性的物质.
典例 (2012湖北卷)在氢离子浓度为1 mol/L的溶液中能大量共存的一组离子或分子是( ).

B.Ba2+、NH4+、Br-、Cl-


答案:B.
三、溶液中离子浓度大小的比较
溶液中离子浓度大小的比较技巧:①相等关系.一般依据是电荷守恒或物料守恒,在溶液中始终保持着阳离子的正电荷数等于阴离子所带的负电荷数.②大小关系.一般依据反应物过量,电离、水解等关系式求得.
综上所述,可以看出化学方程式的书写要注意特别细节,不可粗心大意,比如计量数的配平,沉淀或气体符号.同时,也可以看到离子共存和离子浓度的比较在本节是较难的内容,它涉及的离子广,反应多,这就要求对反应平衡和离子的性质掌握好.
G632
B
1008-0333(2016)31-0089-01

