重组抗人表皮生长因子受体人源化单克隆抗体注射液对Bcap37人乳腺癌细胞生长的抑制作用
曹玉婷,王珊珊,杨德宣,李琳娜,袁守军
◇基础医学研究◇
重组抗人表皮生长因子受体人源化单克隆抗体注射液对Bcap37人乳腺癌细胞生长的抑制作用
曹玉婷1,2,王珊珊2,杨德宣2,李琳娜2,袁守军1,2
目的 观察重组抗人表皮生长因子受体人源化单克隆抗体注射液(MIL41)对Her2高表达人乳腺癌细胞体内外的抑制作用。方法 通过流式细胞仪分析人乳腺癌细胞Bcap37中Her2受体的表达量,CCK8法测定MIL41在体外对乳腺癌细胞Bcap37生长的抑制作用;在体内研究中采用人乳腺癌细胞裸鼠皮下移植瘤模型的建立评价MIL41对肿瘤生长的抑制作用。结果 体外实验表明Bcap37为Her2受体过表达的人乳腺癌细胞,CCK8法检测结果显示MIL41对受试细胞Bcap37的生长有较强抑制作用。体内实验表明受试药MIL41对受试的人乳腺癌细胞Bcap37的裸鼠皮下移植瘤的生长有明显的抑制效应,同时呈现出良好的浓度依赖关系。分别给予3、6、12 mg/kg不同浓度的受试药,其瘤体积抑制率分别为33.7%、47.8%、59.0%,瘤重抑制率分别为29.6%、44.7%、55.6%。结论 MIL41对Bcap37人乳腺癌细胞在体内外的生长有较强的抑制作用。
表皮生长因子;单克隆抗体;Her2;Bcap37;乳腺癌;抗肿瘤活性
在女性群体中乳腺癌是所有恶性肿瘤中发病率及死亡率极高的癌症[1],其中20%~30%的乳腺癌患者的表皮生长因子受体2(human epidermalgrowth factor receptor-2,Her2)为阳性[2-4]。对于Her2阳性乳腺癌患者,恶性程度高、易发生转移、复发率高、预后较差。Her2受体是有受体酪氨酸激酶活性的跨膜糖蛋白,属于表皮生长因子受体家族[5],研究[6]表明其在多数恶性肿瘤细胞的转化中起关键性作用,以表皮生长因子受体Her2为单克隆抗体作用靶点的药物在临床中已成功运用,但是Her2其他抗原表位的单克隆抗体仍是研究中所关注的热点。北京天广实生物技术股份有限公司研发的重组抗人表皮生长因子受体人源化单克隆抗体注射液(MIL41)是靶向Her2受体新型抗原表位的单克隆抗体,其作用机制与Pertuzumab较为相似。该研究以Trastuzumab、Pertuzumab为阳性药,对MIL-41作用于Her2过表达乳腺癌细胞的体外及体内抗肿瘤作用进行药效学评价。
1 材料与方法
1.1 材料
1.1.1 药品与试剂 MIL-41购于北京天广实生物技术股份有限公司;Trastuzumab(上海罗氏制药有限公司,批号:B3457,稀释批号:B2040,分滤批号:SH0006);Pertuzumab(规格:30 mg/瓶,北京天广实生物技术股份有限公司无菌分装)。RPMI 1640培养液(美国Gibco公司);Her2/NEU PE荧光单克隆抗体[美国碧迪医疗器械(上海)有限公司)];CCK8检测液(武汉博士德生物工程有限公司)。
1.1.2 主要仪器 CO2气体培养箱(德国贺立氏仪器公司);倒置显微镜(重庆重光食品公司);流式细胞检测仪(美国Beckman Coulter公司);Multiskan Ascent酶标仪(芬兰Thermo Labsystems公司)。
1.1.3 实验动物 6~8周龄BALB/c裸鼠,SPF级,17.0~22.0 g,雌性,购自北京维通利华实验动物技术有限公司。受试动物饲养于无菌的独立送风IVC笼中,饲以专门为小鼠配制的消毒饲料,自由饮用纯净水。动物实验室内温度约25 ℃,相对湿度40%~70%,每日光照12 h。
1.1.4 肿瘤细胞株 Bcap37人乳腺癌细胞,购自中国医学科学院细胞中心,由军事医学科学院放射与辐射医学研究所肿瘤药理室传代、保存。
1.2 方法
1.2.1 细胞培养 接种细胞于含10%胎牛血清的DMEM培养液中(补充青、链霉素各100 μl/ml),置于37 ℃、5%CO2的细胞培养箱中,每隔1~2 d换液1次,0.25%胰蛋白酶消化,传代和收集细胞。
1.2.2 流式细胞仪检测 Her2受体将待检细胞用胰蛋白酶消化,取105~106个细胞1 000 r/min离心5 min,弃去上清液,收集细胞。PBS洗2遍,用0.05 ml PBS将细胞混悬备用。将Her-2 PE荧光素标记抗体5 μl加入细胞悬液中,室温下孵育30 min。将孵育好的细胞悬液3 000 r/min离心10 min,弃上清液,用0.05 ml PBS混悬检测。
1.2.3 CCK8法检测细胞增殖 将对数生长期细胞,用含10%胎牛血清的RPMI 1640细胞培养液配制成2.5×104/ml的细胞悬液,按每孔2 000~4 000个细胞(100 μl)加入到96孔细胞培养板中,培养24 h后,每孔加入含有不同浓度(1 500、750、375、187.5、93.75、46.875、23.437 5 μg/ml)受试药物的培养基100 μl,每个浓度设4个平行孔。培养72 h后,每孔加入10 μl CCK8检测液,37 ℃培养2~4 h后用酶标仪检测吸光度(optical density,OD)值,检测波长为450 nm。按方法进行一次重复性实验。
1.2.4 皮下移植瘤实验 将对数生长期的Bcap37细胞用胰酶消化收集,并用PBS洗涤重悬,悬液浓度>5×107个细胞/ml,将0.2 ml的肿瘤细胞悬液注射于裸鼠右腋皮下,建立传代荷瘤鼠模型。传代保种裸鼠皮下肿瘤生长体积至1 000~1 500 mm3时,无菌条件下取出瘤块,将其切成约(1.0×1.0×1.0) mm3,并接种于裸鼠右前肢腋部皮下。待皮下移植瘤体积达到100~150 mm3时,按照肿瘤体积随机分组。
MIL41对人乳腺癌细胞Bcap37细胞系裸鼠皮下移植瘤生长的影响,各受试药组药剂量为3、6 、12 mg/kg,尾静脉注射给药,每周给药2次,连续给药3周。每2~3 d测定动物体重及肿瘤体积,记录肿瘤体积变化。肿瘤瘤重生长抑制率(%)=(对照组瘤重-给药组瘤重)/对照组瘤重×100%。肿瘤体积=0.5ab2(a=肿瘤长径;b=肿瘤短径)

2 结果
2.1 流式检测Her2表达量结果 实验结果表明经过抗体标记Bcap37细胞的Her2表达量为95.0%;与Her2高表达细胞BT474相比,人乳腺癌细胞Bcap37为Her2受体表达量较高的细胞。见图1。
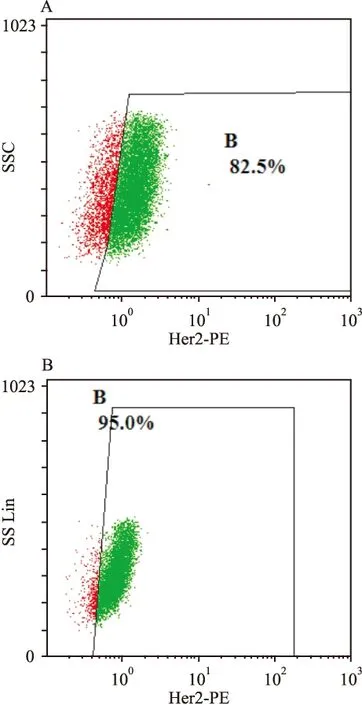
图1 流式细胞术检测Bcap37细胞Her2表达量
A:BT474细胞Her2受体表达量;B:Bcap37细胞Her2受体表达量
2.2 MIL41对Bcap37细胞增殖的影响 CCK8法实验结果表明MIL41对Her2受体过表达的细胞Bcap37的生长抑制作用呈现良好的浓度依赖关系,受试药物设置浓度基本涵盖了药物效应窗口。通过比较发现,MIL41对肿瘤细胞增殖抑制率与阳性药相当,差异无统计学意义。同时,MIL41对肿瘤细胞增殖的抑制呈现剂量依赖性。见表1。
2.3 MIL41抑制Bcap37细胞裸鼠皮下移植瘤生长 实验结果显示,MIL41对人乳腺癌Bcap37裸鼠皮下移植瘤生长有明显抑制作用。从体内的药效结果可以看出,在相同剂量情况下,MIL41在体内的抗肿瘤药效略高于阳性药组。在试验中动物未出现死亡,说明MIL41无毒性。见表2、图2~4。
3 讨论
人表皮生长因子受体Her2是有酪氨酸激酶活性的表皮生长因子家族中的一员,其受体的聚合作用会导致酪氨酸残基的磷酸化,启动多种信号通路导致细胞的增生和肿瘤的发生发展。Her2在25%的乳腺癌患者体内为高表达[7],Her2可以通过下游靶点来增加癌细胞的转移能力使得Her2阳性的乳腺癌更有侵袭能力[8]以及参与细胞的生长、增殖和凋亡等功能性调节[9]。随着分子生物学的发展,抗癌靶向药物成为研究的热点。在乳腺癌治疗中,除了传统的手术、放化疗等治疗方法外,靶向治疗成了一种新型的治疗手段[10],靶向药物也相继问世,如通过与HER2受体结合后干扰其自身磷酸化及阻碍相应异源二聚体形成的Trastuzumab,以及第一个被称作“HER二聚化抑制剂”的单克隆抗体Pertuzumab。因此在临床中凡检测到Her2过表达的患者都应接受抗Her2的治疗[11]。
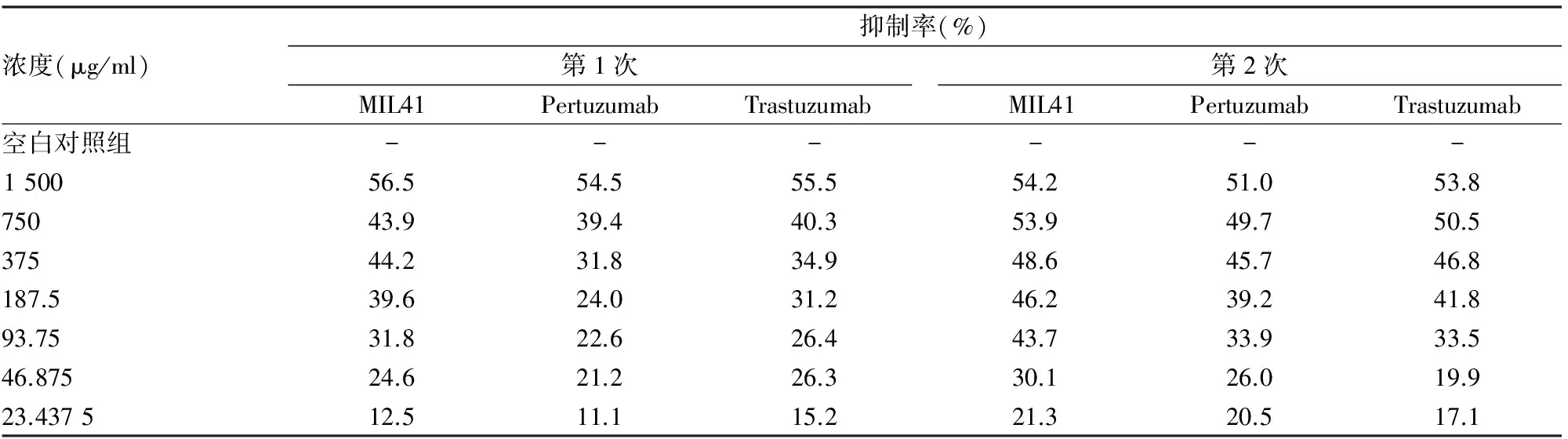
表1 MIL41对细胞生长的抑制效应

表2 MIL41对人乳腺癌细胞Bcap-37裸鼠皮下移植瘤生长抑制影响
与空白对照组比较:*P<0.05,**P<0.01

图2 MIL41对人乳腺癌细胞Bcap37裸鼠皮下移植瘤生长的抑制作用
A:空白对照;B:Trustuzumab;C:Pertuzumab;D:MIL41 3 mg/kg;E:MIL41 6 mg/kg;F:MIL41 12 mg/kg

图3 MIL41对人乳腺癌细胞Bcap-37裸鼠皮下移植瘤生长抑制作用

图4 MIL41对人乳腺癌细胞Bcap-37裸鼠皮下移植瘤体积生长的影响
本研究中将MIL41对乳腺癌Bcap37细胞体外及体内进行系统的药效评价。以Her2受体高表达细胞BT474作为检测Bcap37细胞Her2表达量的对照发现,Bcap37细胞中Her2高表达。体外实验结果显示,随着药物浓度的增加对Bcap37细胞生长抑制作用明显增强,体现出浓度依赖性。在体内实验中,荷瘤鼠给予MIL41药物治疗后,肿瘤生长明显缓解,通过瘤重抑制率来看,存在明显的统计学差异。实验结果表明MIL41对Her2过表达乳腺癌Bcap37的生长有较好的抑制作用,体现了良好的抗癌活性,为相关的基础研究提供了药效数据,同时也为临床研究提供依据。目前,MIL41已被批准进入临床阶段研究,有望成为治疗肿瘤中HER2高表达新型靶向药物。
[1] 周佳丽,颜蕴文,江巧玲,等. 全反式维甲酸及其衍生物对乳腺癌细胞株MDA-MB-231凋亡的影响[J]. 安徽医科大学学报,2015,50(2):154-7.
[2] Yin K, Cao Y J. Study on efficacy and safety of trastuzumab chemotherapy for the treatment of human epidermal growth factor receptor-2 positive breast cancer[J]. Chin J Clin Pharmacol, 2015, 31(9):725-7.
[3] Zhong A S. Clinical application of second-line scheme containing trastuzumab in HER2-positive breast cancer and security analysis[J].Practical J Cancer,2014, 29(9):1121-3.
[4] 刘 君,杨艳芳,顾 林. 曲妥株单抗在HER-2阳性乳腺癌新辅助治疗中的应用研究进展[J]. 中国肿瘤临床,2014,41(16):1065-8
[5] Li W,Pan Y,Li X J. Research progresses in resistance mechanisms to trastuzumab for HER 2 positive breast cancer and novel molecular targeted therapeutic strategies[J]. Chin J Clin Pharmacol,2014,30 (1):48-51.
[6] Liu P P, Liao H H, Liu W X, et al. Development method for determination of biological activity of anti-epithelial growth factor receptor monoclonal antibody[J].Chin J Biologicals, 2015,28(4):414-7.
[7] Recondo G Jr, Dìaz Canton E, Vega M, et al. Therapeutic options for HER-2 positive breast cancer:Perspectives and future directions[J]. World J Clin Oncol,2014,5(3):440-54.
[8] Zhang L, Sullivan P S, Goodman J C, et al. MicroRNA-1258 suppresses breast cancer brain metastasis by targeting heparanase[J]. Cancer Res, 2011, 71(3):645-54.
[9] Ren Y X, Wang G L. The mechanism of HER2-amplified breast cancer with trastuzumab resistance and the research for novel therapy[J]. Chinese Bulletin Life Sci, 2012, 24(5):421-7.
[10]徐 璐,曾 雪,张志强,等. 乳腺癌分子靶向治疗的现状与展望[J].中国实用外科杂志,2015,35(7):790-3.
[11]Mukai H.Treatment strategy for HER2-positive breast cancer[J]. Int J Clin Oncol, 2010, 15(4):335-40.
Evaluation of anti-cancer effect of anti-epithelial growth factor receptor monoclonal antibody on human breast cancer Bcap37 cells
Cao Yuting1,2, Wang Shanshan2,Yang Dexuan2,et al
(1SchoolofGraduateStudies,AnhuiMedicalUniversity,Hefei230032;2DeptofPharmacologyandToxicology,BeijingInstituteofRadiationMedicine,Beijing100850)
ObjectiveToinvestigatetheinhibitoryeffectofanti-epithelialgrowthfactorreceptormonoclonalantibody(MIL41)onhumanbreastcancerBcap37celllinein vitroandin vivo.MethodsTheflowcytometryinstrumentwasusedtoevaluatethelevelofHer2expressioninBcap37cells,theanti-canceractivityofMIL41 in vitrobyCCK8inspection,whiletheactivityin vivowasevaluatedbysubcutaneousimplantedtumorsinnudemicemodel.Results In vitroexperimentsshowedtheover-expressionofHer2inhumanbreastcancerBcap37cells,meanwhile,thereplicatedCCK8inspectionshowedtheMIL41hadinhibitoryeffectinBcap37cells.TheresultsshowedthatMIL41hadstronginhibitoryeffectindose-dependentmanneronhumanbreastcancerBcap37xenotransplantedinnudemice.Theinhibitionratesoftumorvolumewere33.7%,47.8%and59.0%whentheadministratedconcentrationwas3,6,12mg/kg;moreover,theinhibitionratesoftumorweightwere29.6%,44.7%and55.6%.ConclusionMIL41couldefficientlyinhibittheproliferationofhumanbreastcancerBcap37 in vivoandin vitro.
epithelialgrowthfactorreceptor;monoclonalantibody;Her2;Bcap37;humanbreastcancer;anti-canceractivity
国家重大新药创新科技重大专项综合新药研究开发技术大平台项目(编号:2012ZX09301003-001)
1安徽医科大学研究生院,合肥 2300322军事医学科学院放射与辐射医学研究所,北京 100850
曹玉婷,女,硕士研究生; 袁守军,男,研究员,博士生导师,责任作者,E-mail:ysjyuan@139.com
时间:2016-10-12 13:23:00
http://www.cnki.net/kcms/detail/34.1065.R.20161012.1323.001.html
R 965.1
A
1000-1492(2016)11-1555-04
10.19405/j.cnki.issn1000-1492.2016.11.001
2016-07-10接收

