ELISA法检测食蟹猴血浆中rhCNB多肽的方法学评价①
邵继平 张彩云 胡不为 谢学立 田树红 王日超 黄道隆 符 健
(海南医学院药物安评中心,海口571199)
·免疫学技术与方法·
ELISA法检测食蟹猴血浆中rhCNB多肽的方法学评价①
邵继平 张彩云 胡不为②谢学立 田树红 王日超 黄道隆 符 健
(海南医学院药物安评中心,海口571199)
目的:酶联免疫吸附法(ELISA)定量测定食蟹猴血浆中rhCNB多肽的方法学评价。方法:利用双抗体夹心ELISA法,对rhCNB多肽的方法学灵敏度、线性范围、精密度与准确度和回收率进行方法学验证。结果:该方法特异性高,在0.195~12.5 ng/ml的线性范围内,线性关系良好,标准曲线方程为Y = 15.1X-0.26,R2=0.996 8,定量下限(LLOQ)为0.195 ng/ml;该方法的批内精密度CV分别为3.55%、1.39%和4.71%;批间精密度CV分别为1.59%、3.2%和3.8%,均<5%,准确度在91.9%~108.8%之间,方法回收率在88.5%~108.3%之间,<110%,说明该ELISA方法的准确度较高。符合验证要求。结论:双抗体夹心ELISA法灵敏度高、通量大、重复性、准确度及精密度好,可用于生物样品中rhCNB多肽的定量检测。
酶联免疫吸附法;食蟹猴;rhCNB多肽;方法学评价
肝癌(Liver cancer)是严重危害我国人民健康的恶性肿瘤之一,其发病率和死亡率仅次于胃癌和食道癌,耐药、复发和转移成为肝癌患者死亡的主要原因。晚期患者往往陷入无药可救的绝境,在我国中位生存期仅3~6个月,在欧美也仅6~9个月,预后很差。
虽然治疗肝癌的药物众多,但大多数药物毒副作用大。目前临床上肝癌药物最大的缺点是缺乏组织选择性,在体内广泛分布,在发挥疗效的同时产生严重的全身性毒副作用。因此寻找高效低毒的新型抗癌药迫在眉睫。
钙调磷酸酶(Calcineurin,CN)是目前唯一一种依赖Ca/CaM(钙调素)的蛋白磷酸酶,由A、B亚基以1∶1的比例组成异二聚体,A亚基(CNA)是催化亚基,B亚基(CNB)是调节亚基。CNB作为该酶的调节亚基,能促进CNA的活性,且相对分子质量小,性质稳定。CN在免疫激活通路中发挥重要作用,是T细胞活化的关键酶。临床前研究表明rhCNB(重组人钙调磷酸酶B亚基,recombinant human calcineurin B subunit)能刺激T细胞和NK细胞增殖以及增强NK细胞的杀伤活性,增强巨噬细胞吞噬能力等免疫功能,且rhCNB对H22肝癌有显著的抑制作用,疗效确切,是高效低毒的新型抗肝癌生物药[1]。
酶联免疫吸附法(ELISA)是蛋白类生物技术药物常用的分析方法,具有操作简单,灵敏度高、特异性好,易于标准化,易被临床采用等优点[2-4]。rhCNB作为开发中的一种创新药,本文采用ELISA方法来评价其疗效,并从线性、灵敏度、精密度和准确度、回收率等方面进行方法学验证,旨在为该ELISA方法在临床上快速、准确、方便地定量检测人生物样本中的rhCNB奠定基础,为评价rhCNB用于肝癌治疗的临床疗效提供行之有效的检测手段。
1 材料与方法
1.1 材料
1.1.1 试剂 rhCNB ELISA试剂盒(批号:A21503 115D,南京金斯瑞公司生产)和rhCNB供试品(批号:20140807)均由海口奇力制药股份有限公司提供。
1.1.2 仪器 TECAN酶标仪(奥地利TECAN有限公司生产),Centrifuge 5810高速离心机(德国Eppendorf公司生产)。
1.1.3 实验动物 食蟹猴6只,普通级,海南新正源生物科技有限公司提供(合格证号:SCXK琼2011-0002),雌雄各半,体重(2.4~4.5)kg。饲养于海南医学院药物安评中心动物房。
1.2 方法
1.2.1 食蟹猴血浆样品制备方法 从食蟹猴肘正中静脉取血0.3 ml置于肝素钠抗凝真空管内,静置1 h后,用3 000 r/min离心20 min,分离后的血浆标本保存于-20℃冰箱备用。
1.2.2 ELISA方法 双抗夹心ELISA法的原理是在酶标板上预先包被rhCNB抗体,待rhCNB抗原与抗体发生特异性结合反应,再加入HRP标记rhCNB多抗,然后用TMB底物显色,显色强度与rhCNB浓度成正比。通过酶标仪检测吸光度(OD值),根据rhCNB标准品制定的标准曲线,用线性拟合方式计算rhCNB的含量。试剂盒操作步骤:将rhCNB蛋白加入96孔板内,室温孵育1 h,洗板4次;加一抗,孵育1 h,洗板4次;再加入辣根过氧化酶偶联的二抗,孵育0.5 h,洗板4次。加入四甲基联苯胺(TMB)底物,避光室温孵育5~15 min,最后加终止液终止反应,酶标仪450nm处读取吸光度[5,6]。
1.2.3 方法学评价 对建立的rhCNB双抗夹心ELISA法分别进行线性和范围、灵敏度、准确度和精密度、回收率等方法学验证[7-9]。(1)线性范围:线性是指在设计的剂量范围内,测试结果与试样中被测物质浓度呈正比关系的程度。应在规定的范围内测定线性关系[10,11]。参照试剂盒标准品溶液的配制方法将标准品母液从1 mg/ml倍比稀释为:12.5 ng/ml、6.25 ng/ml、3.125 ng/ml、1.56 ng/ml、0.78 ng/ml、0.39 ng/ml、0.195 ng/ml、0 ng/ml。检测其信号值,并绘制标准曲线,观察是否呈线性。(2)定量下限:以零浓度溶液重复测定20次。然后计算空白值均值和空白值十倍标准差所对应的浓度,最后统计实验所测得的平均值为定量下限[12-14]。(3)准确度:取线性范围内高、中、低三个浓度的溶液进行方法学准确度的考察。将标准品母液依次稀释成10 000 ng/ml、5 000 ng/ml、1000 ng/ml。每个浓度的溶液各取2 μl分别加到2 μl猴空白血浆中,用1996 μl 1×稀释液分别稀释成10 ng/ml、5 ng/ml、1 ng/ml高中低三个浓度。每一浓度制备6份样品。然后按照试剂盒说明书检测其信号值,最后通过计算回收率比较测定值与真实值之间的差异。(4)精密度:取线性范围内高、中、低三个浓度的溶液进行方法学批内和批间精密度的考察。同一批内求RSD计算批内精密度,连续测3 d,测其批间差异。标准品母液稀释方法见1.2.3(1)。(5)回收率:选已知含量的血清样本,分别加入三个浓度的等体积的标准品溶液(浓度为10 ng/ml、5 ng/ml、1 ng/ml),混匀后再用本法进行测定。回收率=实际浓度/理论浓度×100%。
1.3 数据处理 结果用药动学软件(BAPP)进行线性拟合求回归方程并绘制标准曲线。Microsoft Excel XP软件进行一般计算。
2 结果
2.1 线性范围 对12.5、6.25、3.125、1.56、0.78、0.39、0.195、0 ng/ml一系列标准品溶液进行ELISA检测。以标准品浓度为横坐标,以吸收值为纵坐标进行线性拟合并绘制标准曲线。以阴性对照的2.1倍为cut off 值,确定该方法的阳性值。从图1可见,线性方程Y=15.1X-0.26,R2=0.996 8。在0~12.5 ng/ml的浓度范围内,本方法的线性关系良好,符合验证要求。
2.2 定量下限 定量下限是标准曲线上的浓度最低点,以零浓度溶液重复测定16次。然后计算空白值均值和空白值十倍标准差所对应的浓度,最后统计实验所测得的平均值为定量下限。本方法测得的定量下限为0.195 ng/ml。符合验证要求。
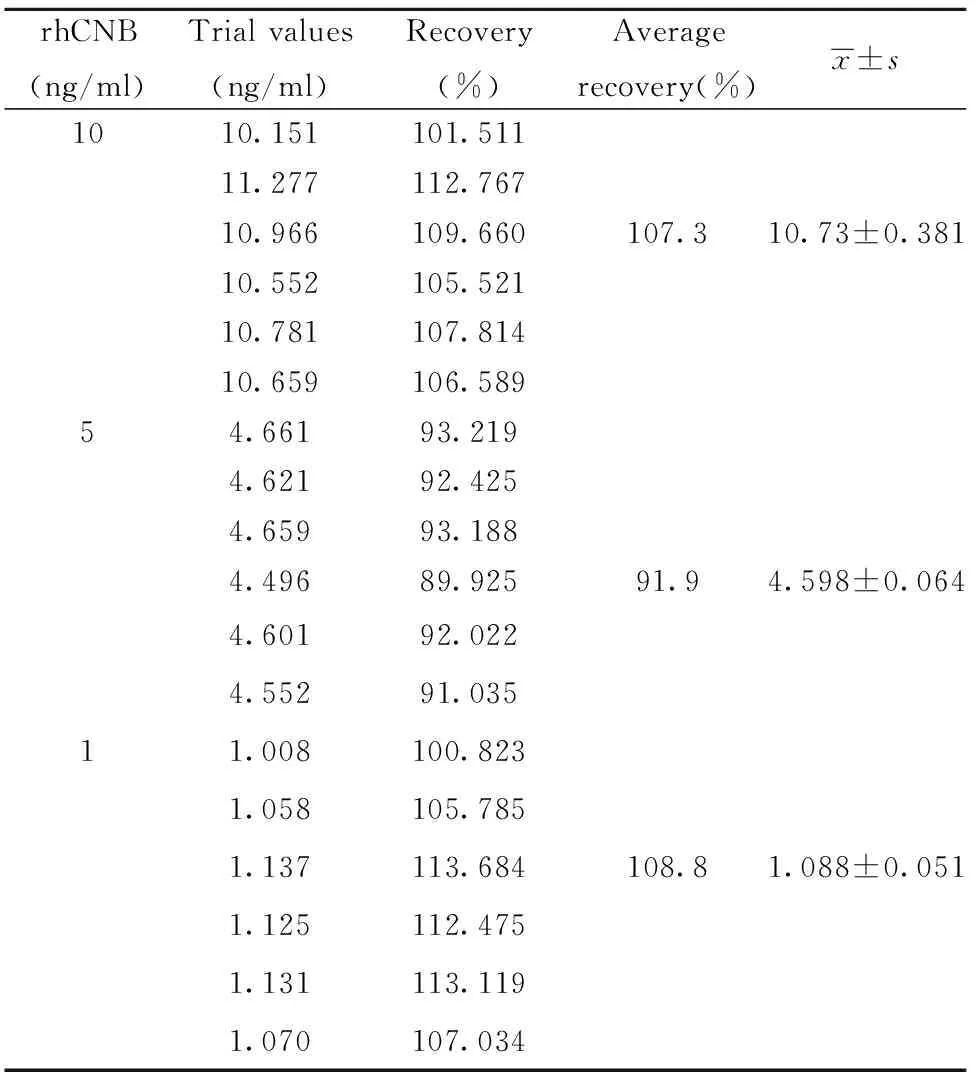
2.3 准确度 在rhCNB标准品线性范围内,选择高、中和低3个标准品浓度:10、5和1 ng/ml,每一个浓度做6份平行样品,计算每一浓度的回收率。表1准确度分析结果表明该方法高、中、低浓度的回收率分别为107.3%、91.9%和108.8%,均在80%~120%可接受范围内。可见,本方法的准确度符合验证要求。
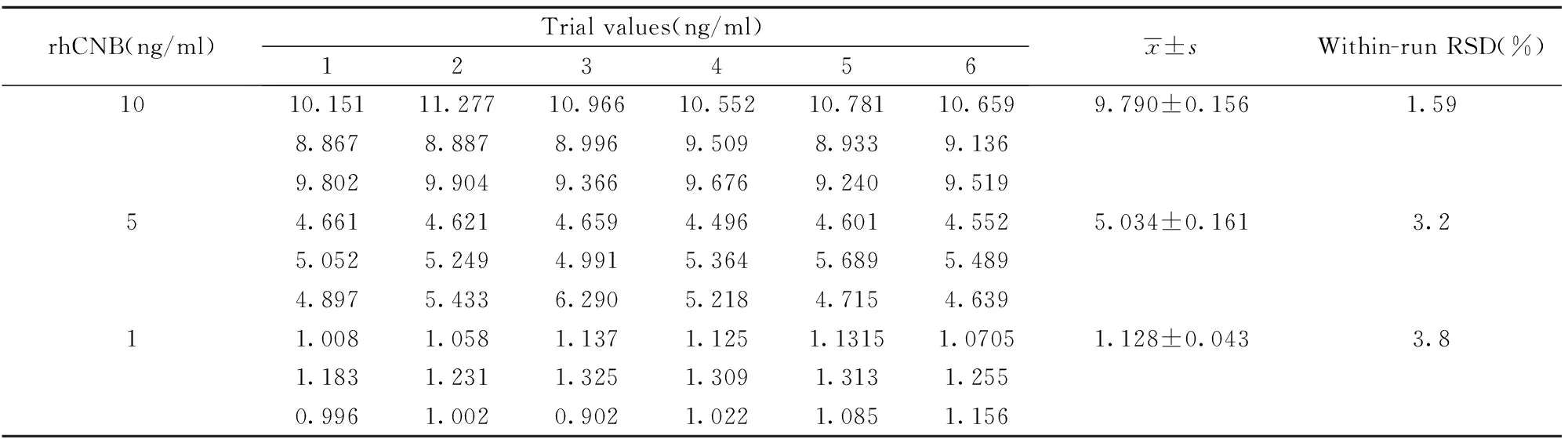
2.4 精密度 在rhCNB标准品线性范围内,选择高、中和低3个标准品浓度:10、5和1 ng/ml,每一个浓度做6份平行样品,连续测定3 d,计算每一浓度的均值、标准差和变异系数。表2和表3批内和批间精密度结果显示该方法的批内精密度CV分别为3.55%、1.39%和4.71%;批间精密度CV分别为1.59%、3.2%和3.8%,均<10%。可见,本方法的批内和批间精密度均符合验证要求。

图1 rhCNB标准曲线Fig.1 Standard curve of rhCNBNote: rhCNB ELISA method had high linearity within 0.195-12.5 ng/ml,the working curve of rhCNB was Y=15.1x-0.26,R2 = 0.996 8.
表1 rhCNB ELISA方法准确度
Tab.1 Accuracy of rhCNB ELISA method
rhCNB(ng/ml)Trialvalues(ng/ml)Recovery(%)Averagerecovery(%)x±s1010.151101.51111.277112.76710.966109.660107.310.73±0.38110.552105.52110.781107.81410.659106.58954.66193.2194.62192.4254.65993.1884.49689.92591.94.598±0.0644.60192.0224.55291.03511.008100.8231.058105.7851.137113.684108.81.088±0.0511.125112.4751.131113.1191.070107.034
表2 rhCNB ELISA方法批内精密度(n=18)
Tab.2 Inter-precision of rhCNB ELISA method(n=18)
表3 rhCNB ELISA方法批间精密度(n=48)
Tab.3 Intra-precision of rhCNB ELISA method(n=48)
rhCNB(ng/ml)Trialvalues(ng/ml)123456x±sWithin-runRSD(%)1010.15111.27710.96610.55210.78110.6599.790±0.1561.598.8678.8878.9969.5098.9339.1369.8029.9049.3669.6769.2409.51954.6614.6214.6594.4964.6014.5525.034±0.1613.25.0525.2494.9915.3645.6895.4894.8975.4336.2905.2184.7154.63911.0081.0581.1371.1251.13151.07051.128±0.0433.81.1831.2311.3251.3091.3131.2550.9961.0020.9021.0221.0851.156
表4 rhCNB ELISA方法回收率
Tab.4 Recovery of rhCNB ELISA method

rhCNB(ng/ml)Trialvalues(ng/ml)Recovery(%)Averagerecovery(%)RSD(%)108.77687.78.56685.68.22782.288.55.69.55795.59.11491.155.415108.35.419108.45.039100.8105.82.395.070101.45.529110.511.056105.61.042104.21.122112.2108.35.501.175117.41.021102.1
2.5 回收试验 由表4结果可见,高中低浓度样品的回收率分别为:88.5%、105.8%、108.3%,方法回收率<110%,说明该ELISA方法的准确度较高。符合验证要求。
3 讨论
酶联免疫吸附法是高通量筛选和定量检测生物技术药物的一种常用方法,其原理是利用抗原抗体特异性结合进行检测,灵敏度高达纳克甚至皮克级,以灵敏度高、特异性好、操作简便、安全而广泛应用于临床诊断[15-17]。但ELISA法也存在一定的局限性:如重复性较差、受自身抗体或内源性酶等干扰;此外,影响因素多,较明显的是温度和时间等,都会带来误差。因此用ELISA法定量检测生物样本中的药物,对分析方法的灵敏度、线性范围、精密度与准确度等都有严格的要求。本文采用双抗夹心ELISA技术对rhCNB试剂盒进行方法学评价,结果表明,血浆中杂质不干扰样品的测定,在0.195 ng/ml~12.5 ng/ml的线性范围内,线性关系良好,标准曲线方程为Y=15.1X-0.26,R2=0.996 8;高、中、低三个浓度的准确度高,批内和批间精密度均小于10.0%,有良好的精密度;方法回收率<110%。综上所述:该方法特异性、准确度和精密度、线性及范围、定量下限等均符合验证可接受标准,能够快速、灵敏、准确地对生物样品中的rhCNB多肽进行定量检测。
[1] 高 锦,赵文军,王艳丽,等.注射用重组人钙调磷酸酶B亚基稳定性的初步研究[J].中国新药杂志,2008,17(8):675-678.
[2] 杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008:142-167.
[3] 中国生物制品标准化委员会.中国生物制品规程[M].2000年版.北京:化学工业出版社,2000:620-623.
[4] 沈关心,周汝麟.现代免疫学实验技术[M].武汉:湖北科技出版社,200l:34-35.
[5] Savino E,Hu B,Sellers J,etal.Development of an In-House,Process-Specific ELISA for Detecting HCP in a Therapeutic Antibody,Part 2[J].Bio Process International,2011,9:68-75.
[6] Huisman H,Wynveen P,Nichkova M,etal.Novel ELISAs for screening of the biogenic a mines GABA,glycine,beta-phenylethyla mine,agmatine,and taurine using one derivatization procedure of whole urine samples[J].Anal Chem,2010b,82:6526-6533.
[7] Fengqiang Wang,Dennis Driscoll,Daisy Richardson,etal.The comparison of chemilu minescent and colorimetric-detection based ELISA for chinese hamster ovary host cell proteins quantification in biotherapeutics[J].J Bioproces Biotechniq,2013,3(2):1000136.
[8] Nichkova M,Huisman H,Wynveen P,etal.Evaluation of a novel ELISA for serotonin:urinary serotonin as potential biomarker for depression[J].Anal Bioanal Chem,2012,402:1593-1600.
[9] Nichkova M,Wynveen PM,Marc DT,etal.Validation of an ELISA for urinary dopa mine:applications in monitoring treatment of dopa mine-related disorders[J].J Neurochem,2013,125:724-735.
[10] Schenauer MR,Flynn GC,Goetze AM.Identification and quantification of host cell protein impurities in biotherapeutics using mass spectrometry[J].Anal Biochem,2012,428:150-157.
[11] Tscheliessnig AL,Konrath J,Bates R,etal.Host cell protein analysis in therapeutic protein bioprocessing-methods and applications[J].J Biotechnol,2013,8:655-670.
[12] Huisman H,Wynveen P, Setter PW.Studies on the immune response and preparation of antibodies against a large panel of conjugated neurotransmitters and biogenic a mines:specific polyclonal antibody response and tolerance[J].J Neurochem,2010,112(3):829-841.
[13] Liu N,Brevnov M,Furtado M,etal.Host cellular protein quantification[J].Bio Process International,2012,10:44-50.
[14] Wang X,Schomogy T,Wells K,etal.Improved HCP quantitation by minimizing antibody cross-reactivity to target proteins[J].Bio Process International,2010,8:18-24.
[15] Roda A,Guardigli M.Analytical chemilu minescence and biolu minescence:latest achievements and new horizons[J].Anal Bioanal Chem,2012,402:69-76.
[16] Dotsikas Y,Loukas YL.Improved performance of antigen-HRP conjugate-based immunoassays after the addition of Anti-HRP antibody and application of a liposomal chemilu minescence marker[J].Anal Sci,2012,28:753-757.
[17] Edgeworth JA,Farmer M,Sicilia A,etal.Detection of prion infection in variant Creutzfeldt-Jakob disease:a blood-based assay[J].Lancet,2011,377:487-493.
[收稿2015-10-12 修回2015-10-27]
(编辑 倪 鹏)
Methodological evaluation of rhCNB in long-tailed macaque sera detected by Enzyme-linked Immunosorbent Assay(ELISA)
SHAO Ji-Ping,ZHANG Cai-Yun,HU Bu-Wei,XIE Xue-Li,TIAN Shu-Hong,WANG Ri-Chao,HUANG Dao-Long,FU Jian.Hainan Medical University,Haikou 571199,China
Objective:To validate an enzyme linked immunosorbent assay(ELISA) method for the quantification of rhCNB in long-tailed macaque sera.Methods: The linear,sensitivity,accuracy,precision and recovery were determined using ELISA.Results: The present ELISA method had high linearity within 0.195 ng/ml-12.5 ng/ml,the working curve of rhCNB was Y= 15.1X-0.26,R2=0.996 8, the method showed good sensitivity of 0.195 ng/ml,the accuracy were in the range of 91.9%-108.8%,and the Coefficient of variation(CV) for inter-assay were 3.55%,1.39% and 4.71%,the intra-assay were 1.59%,3.2% and 3.8%,all less than 10%,the recoveries were in the range of 88.5%-108.3%,<110%.Thus the method was coincidence with requirement.Conclusion: Double antibody sandwich ELISA assay of rhCNB in long-tailed macaque sera has good sensitivity,accuracy,precision and recovery and it can be used to measure rhCNB concentration in biological samples.
Enzyme linked immunosorbent assay(ELISA);Long-tailed macaque;Recombinant human calcineurin B subunit(rhCNB); Methodological evaluation
10.3969/j.issn.1000-484X.2016.04.017
①本文为国家自然科学基金资助项目(81160408)。
邵继平(1971年-),女,博士,副教授,主要从事新药安全性评价的研究,E-mail:jpshaosl@163.com。
及指导教师:符 健(1959年-),男,博士,教授,主任,主要从事新药安全性评价的研究。
R969.1 R917
A
1000-484X(2016)04-0528-04
②西交利物浦大学,苏州215123。