可离子化有机污染物对大型溞的毒性及QSAR研究
包信,张栩嘉,,赵元慧
1. 哈尔滨师范大学 地理科学学院,哈尔滨 150028 2. 东北师范大学 环境学院,长春 130024
可离子化有机污染物对大型溞的毒性及QSAR研究
包信1,张栩嘉1,,赵元慧2
1. 哈尔滨师范大学 地理科学学院,哈尔滨 150028 2. 东北师范大学 环境学院,长春 130024
取代苯酚、苯胺和苯甲酸类化合物是在环境水体中具有较强生物毒性的芳香族可离子化有机化合物,它们在水体中对水生生物和水生生态系统都有较大危害。测定此类化合物在pH值为6、7.8和9的条件下对大型溞的24 h急性毒性,计算化合物在不同pH值条件下的中性态分子所占比例F0。研究毒性与F0的相关性,结果表明F0对取代苯酚和苯甲酸类化合物的毒性的影响较大而对取代苯胺毒性的影响很小。对于卤代苯甲酸类化合物,毒性与疏水性的相关性较好,但是羟基苯甲酸类化合物的毒性与疏水性参数的相关性很差,引入量子化学参数EHOMO和取代羟基个数NOH,可以改进苯甲酸类化合物的模型的质量。
可离子化有机污染物;大型溞;急性毒性;QSAR
Received 22 November 2015 accepted 21 January 2016
取代苯酚、苯胺和苯甲酸类化合物是在环境水体中普遍存在的具有较强生物毒性的芳香族可离子化有机化合物,它们在水体中对水生生物和水生生态系统都有较大危害。苯酚和苯胺类化合物是有机化工的基本原料,被大量用于酚醛树酯、离子交换树酯、高分子材料、合成纤维、石料、燃料、香料、炸药、农药及染料等工业当中[1-2],进而有大量的含有苯酚和苯胺类化合物的废水排放到环境水体当中,这是一类对人类危害严重的工业废水[3]。取代苯甲酸类化合物是一类重要的植物生长调节剂,被广泛应用在农业生产当中,进而大量进入到水体。目前已经有一些研究证明了苯甲酸类化合物对细菌、无脊椎动物、大型溞和鱼类都存在一定的毒性作用[4]。
取代苯酚、苯胺和苯甲酸类化合物共同具有的特点就是它们都是可离子化有机化合物,在水中有2种存在形态:离子态和非离子态。在不同pH条件下,取代苯酚、苯胺和苯甲酸类化合物的离子态和非离子态的所占比例不同。赵元慧等[5]研究了不同pH条件下(6.0,7.8,9.0) 9种苯甲酸类化合物对大型溞的24 h急性毒性,并通过建立了定量构效关系证明,苯甲酸类化合物对大型溞的毒性可通过引入疏水性参数和一个可以表征化合物离子化程度的参数进行合理准确的预测,这说明苯甲酸类化合物的离子态和非离子态对生物吸收和毒性的贡献不同。于瑞莲等[6-8]研究了不同pH条件下(6.0,7.8,9.0)苯酚和苯胺类化合物对大型溞的急性毒性,研究表明随着pH的变化苯酚和苯胺类化合物对大型溞的毒性有所变化,苯酚类化合物的毒性随pH的升高而减小,苯胺类化合物的毒性随pH的升高而增大,这说明可离子化有机化合物的分子态被生物吸收的速度要比离子态大,分子态所占比例越大,对生物的毒性越大[6-8]。另外,不同的水生生物由于其自身组织结构不同,对离子态和非离子态的吸收也有所差别,张栩嘉等[9]研究了有机化合物对8种水生生物的种间关系,研究表明,对于疏水性化合物的毒性,发光菌与大型溞有很好的种间相关性,而对于可离子化有机化合物,发光菌与大型溞的相关性很差,且发光菌的毒性显著大于大型溞毒性,这一方面说明发光菌和大型溞对可离子化有机化合物的吸收机制不同,发光菌是单细胞水生生物,无论是离子态还是非离子态都相对容易被单细胞细菌吸收,进而破坏细胞的正常功能,但是离子态化合物却很难进入到大型溞体内,多细胞水生生物的皮肤和脂质层能够阻止其对可离子化有机化合物的吸收,因此也说明了大型溞对离子态和非离子态的吸收不同。
为了进一步深入研究取代苯酚、苯胺和苯甲酸类化合物在水中的电离程度对其毒性的影响,本研究测定了38种不同pH条件下(6.0,7.8,9.0)苯酚、苯胺和苯甲酸类化合物对大型溞的毒性,研究pH对可离子化有机化合物毒性的影响,进而解释可离子化有机化合物的毒性作用机理,并选用适当的物理化学参数分别对苯酚、苯胺和苯甲酸类化合物建立QSAR模型。
1 材料与方法(Materials and methods)
1.1 受试化合物
本研究共测试了38种有机化合物对大型溞的生物毒性,受试化合物如表1所示。
1.2 试验材料
试验生物为大型溞(Daphnia magna),甲壳纲,枝角亚目。本研究使用的大型溞取自北京王子健教授实验室,再进行扩大培养。扩大培养使用的容器是容积大约为8 L的圆玻璃缸,培养用水是经自然曝气3 d以上的人工配制稀释水,温度控制在17~25 ℃,pH为6~9。使用实验室培养的栅藻为大型溞的饵料,每周更换一次大型溞培养液,每天追加1次浓缩悬浮藻液,控制培养液中栅藻的的浓度,一般为106个·L-1左右,呈淡苹果绿色,避免晚间缺氧引起大型溞死亡。控制大型溞的密度在50个·L-1,以保持大型溞在孤雌生殖的状态下。
毒性实验选用实验室培养3代以上的出生6~24 h的幼溞。为了获得6~24 h的幼溞,在实验前从储备缸中挑去适量的怀孕母溞放入2 L的大少杯中单独培养。每个大少杯中方母溞20~30个。18 h后,用自制软头的吸管取走母溞,24 h时,此繁殖缸中的幼溞即为6~24 h的幼溞,可直接用于实验。
1.3 毒性试验
有机化合物的贮备液用人工稀释水配制,定容到棕色容量瓶中,难容的化合物先用微量丙酮(不超过0.1 mL·L-1)助溶或者用超声波清洗机溶解后定容。化合物的贮备液浓度均在其水中溶解度以下,实验期间水温为18~24 ℃。根据预实验,按等对数间距取一系列不同体积的储备液于50 mL具塞比色管中,用人工配制稀释水稀释到50 mL,加入HCl溶液或NaOH溶液调节到pH=6.0、7.8或9.0。每个化合物在不同pH下设置5个浓度点和1个空白对照,每个点作3个平行。每个比色管中放10个同龄且健康的6~24 h幼溞,观察并计录24 h活动被抑制的数目。使用SPSS13.0统计分析软件将受试浓度对数和大型溞死亡数进行回归分析,求出24 h-IC50值。实验过程中试液中的溶解氧达到饱和时的60%以上,且对照点无死亡,实验数据有效。
1.4 毒性数据集的建立
本实验一共获得了38种化合物在3个不同pH值条件下的毒性24 h-IC50值,通过文献中获得了在相同条件下测定的35种取代苯酚、苯胺和苯甲酸类化合物在3个与本实验相同的pH值条件下的毒性24 h-IC50值,其中有4种重复化合物,它们是:2-硝基苯胺、2、4-二硝基苯胺、2-硝基苯酚和2、4-二硝基苯酚。共有12组重复数据,重复数据的绝对平均误差为0.04个log单位。由于使用的试验方法相同,重复数据的误差很小,所以将实验数据和文献数据合并,建立了1个一共含有69种化合物的3个不同pH值条件下的毒性24 h-IC50值数据集,其中包括6种非可离子化有机化合物、17种取代苯胺、19种取代苯酚、3种氨基苯酚和24种取代苯甲酸类化合物。
1.5 分子描述符
本研究对全部69种化合物计算了总共17种描述符。其中包括疏水性参数log KOW、酸性解离常数pKa,在给定pH值下某种化合物中性态和离子态所占百分比,Abraham溶剂化参数(E, S, A, B, V)。 这些参数是使用ACD/Labs程序(Advanced Chemistry Development, Inc., http: // www.acdlabs.com)计算的。另外还有量子化学参数最高占据轨道能EHOMO和最低未占轨道能ELUMO,是使用程序MOPAC2009 (Stewart Computational Chemistry, USA, openmopac. Net)计算的,使用AM1的方法对于化合物结构进行能量最小化。附表1中列出了取代苯酚、苯胺和苯甲酸类化合物的描述符计算结果。
1.6 统计分析
本研究所使用的统计分析软件是Minitab (version 14),建立QSAR方程的方法是最小二乘回归分析法和逐步回归分析法。每个回归分析方程都给出了如下信息:样品数量n,相关系数的平方R2,估计值的标准误差S和Fisher检验值F。用于筛选有效描述符的逐步回归分析方法也是使用Minitab软件进行的。

表1 受试化合物名称、纯度和生产厂家
2 结果(Results)
2.1 pH为6.0、7.8和9.0的条件下取代苯酚化合物对大型溞的毒性
表1中列出了在pH为6、7.8和9的条件下,苯酚、苯胺和苯甲酸类化合物对大型溞的24 h急性毒性log 1/IC50值。观察它们的毒性发现化合物的毒性随着取代基数量、种类和取代位置的不同而变化。毒性随着取代基数量的增加而增加,如2,3-二甲基苯酚﹥单甲基苯酚、2,4-二硝基苯酚﹥单硝基苯酚、五氯酚﹥2,4,6-三氯苯酚﹥2,4-二氯苯酚﹥一氯苯酚、三氯苯胺﹥二氯苯胺﹥一氯苯胺﹥苯胺。卤代苯甲酸类的毒性随着卤素取代基数量的增加而增加,即四氯取代﹥三氯取代﹥二氯取代﹥一氯取代。取代基的不同也会影响毒性,苯酚类化合物的变化规律为:NO2≈CH3﹤Cl﹤Br﹤OH。苯胺类化合物的变化规律为NO2≈CH3﹤Cl﹤Br﹤OH。卤素取代基的不同也会影响卤代苯甲酸的毒性,其变化规律为:Br﹥Cl﹥F。对于具有相同个数的同种基团取代的化合物,取代位置的变化也会影响苯酚类化合物的毒性。对于卤代苯酚而言,毒性顺序为间位﹥对位﹥邻位,而卤代苯甲酸的毒性顺序为对位﹥间位﹥邻位。本研究还测定了6种羟基苯甲酸类化合物的毒性,6种化合物的毒性顺序为:3,4,5-三羟基苯甲酸﹥2,5-二羟基苯甲酸﹥2,4-羟基苯甲酸﹥2-羟基苯甲酸﹥4-羟基苯甲酸﹥3-羟基苯甲酸。这说明羟基苯甲酸的毒性也随着羟基取代数目的增加而增强。对于单羟基取代苯甲酸而言,邻位取代的毒性最强,而2,5-二羟基苯甲酸的毒性大于2,4-羟基苯甲酸,这说明邻位上的羟基取代对苯甲酸类化合物的毒性有增强作用。Kamaya等[10]研究了羟基苯甲酸类化合物对大型溞的48 h急性毒性,也发现了相同结果。
观察pH值为6.0、7.8和9.0时化合物对大型溞的毒性-logIC50值发现,苯酚和苯甲酸类化合物的毒性值随着pH的增大而减小,苯胺类化合物的毒性随着pH的增大而增大。对于可离子化有机化合物而言,随着取代基种类和数量的改变,化合物的离子化程度也不相同。表1列出了在pH为6、7.8和9的条件下,取代苯酚、苯胺和苯甲酸类化合物在水溶液中非离子态所占的比例F0。对于酸性化合物而言非离子态化合物随着溶液pH的增大而减小,对于碱性化合物而言非离子态化合物随着溶液pH的增大而增大。这说明可离子化有机化合物对大型溞的毒性随着非离子态化合物的增多毒性增强,非离子态对毒性贡献较大。
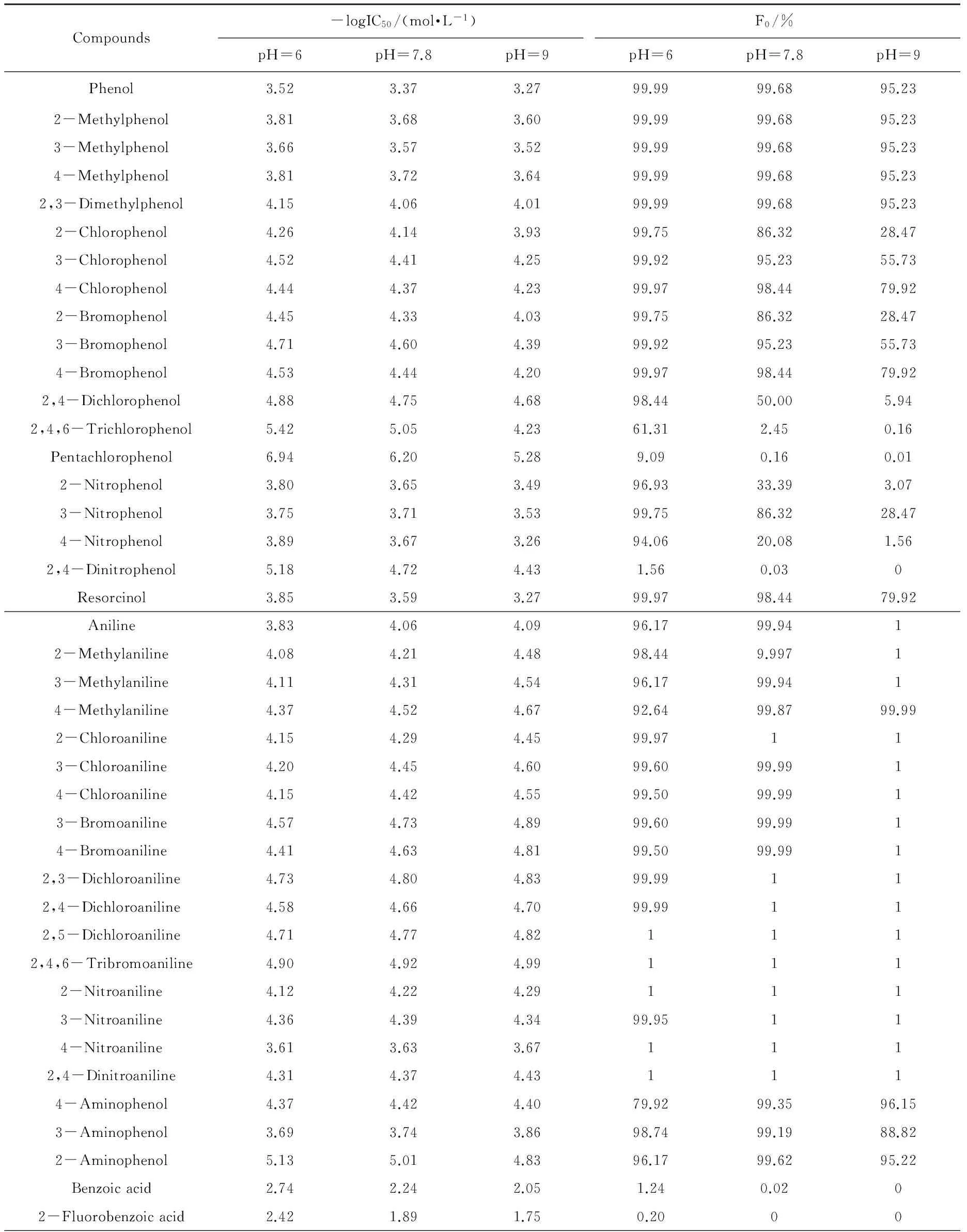
表2 不同pH值下取代苯酚、苯胺和苯甲酸类化合物对大型溞的毒性
在pH从6~9的范围内,不同化合物的电离程度并不相同。如苯酚类化合物,若环上有强吸电子基团,例如卤素或者硝基,会使酚羟基上的电子密度下降,进而增大苯酚的电离能力,而中性基团取代苯酚,如甲基则对电离能力无影响。因此,苯酚和甲基苯酚的电离能力相对较差,在pH为6~9的范围内,仍然主要以非离子态形式存在,虽然非离子态所占比例随着pH的增大有所下降,但是变化很小,同时甲基苯酚类化合物的毒性随pH的下降也很小。卤代苯酚和硝基苯酚类化合物(2,4,6-三氯苯酚、五氯酚和2,4-二硝基苯酚除外)在pH=6时仍然主要以非离子态形式存在,但是非离子态所占比例随着pH的增大而显著下降,下降的程度根据化合物结构有所不同,但是非离子态化合物所占比率明显低于甲基苯酚类化合物。这类化合物毒性随pH的下降比甲基苯酚类化合物的程度要大,但是仍然不十分显著,同时其毒性随pH的下降也不十分显著。2,4,6-三氯苯酚、五氯酚和2,4-二硝基苯酚由于吸电子基团的能力很强,在pH=6时已经有很高的电离程度,在pH为6~9的范围内都主要以离子态形式存在,这3种化合物的毒性随着pH的增大而下降非常显著。这说明苯酚类化合物的离子化程度越高,其毒性受pH影响越显著。对于苯胺类化合物,在pH从6~9的范围内都主要以分子态形式存在,分子态所占比例随pH变化较小,因此毒性随pH的变化并不显著。本研究设定的3个pH值6.0、7.8和9.0均大于所测定苯甲酸类化合物的pKa,所以在测定条件下取代苯甲酸类化合物主要呈离子态形式。非离子态化合物随着溶液pH的增大而减小,毒性值也随着pH的增大而减小。
2.2 不同pH值下取代苯酚、苯胺和苯甲酸对大型溞毒性的QSAR研究
有机污染物对水生生物的致毒过程是一个复杂的过程,包括有机物传输到作用靶位和有机污染物与作用靶位发生反应2个部分。假设我们所研究的可离子化有机化合物不具有反应性,或者放映性很弱,那么其毒性与其传输到作用靶位的能力有很大关系,有机物传输到作用靶位的能力与化合物的疏水性有关,因此我们分别建立了不同pH条件下的苯酚、苯胺和苯甲酸类化合物的疏水性方程。应用逐步回归方法,对计算的17种描述符进行筛选,结果如表3。
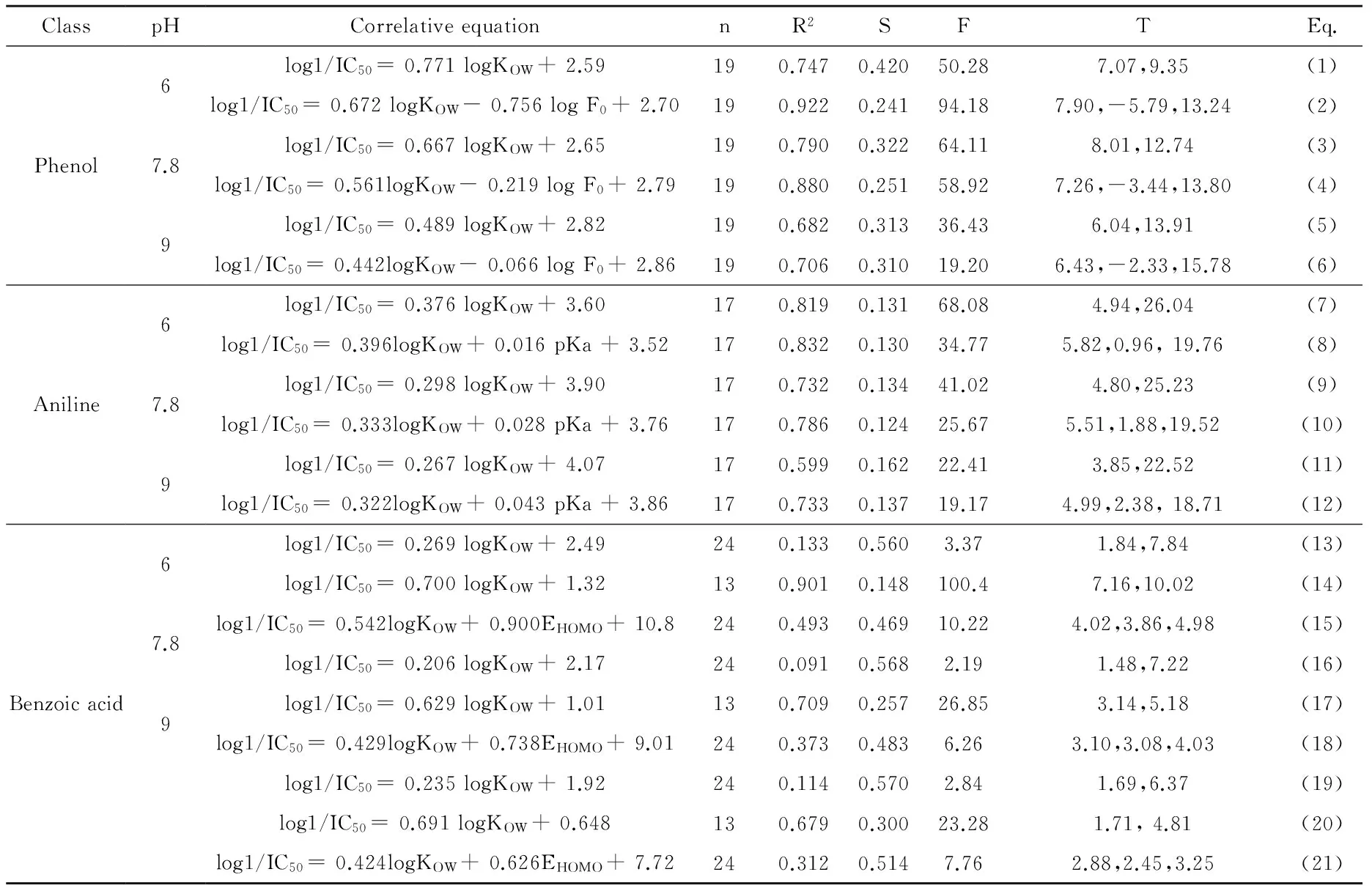
表3 不同pH值下取代苯酚、苯胺和苯甲酸对大型溞毒性的QSAR回归方程
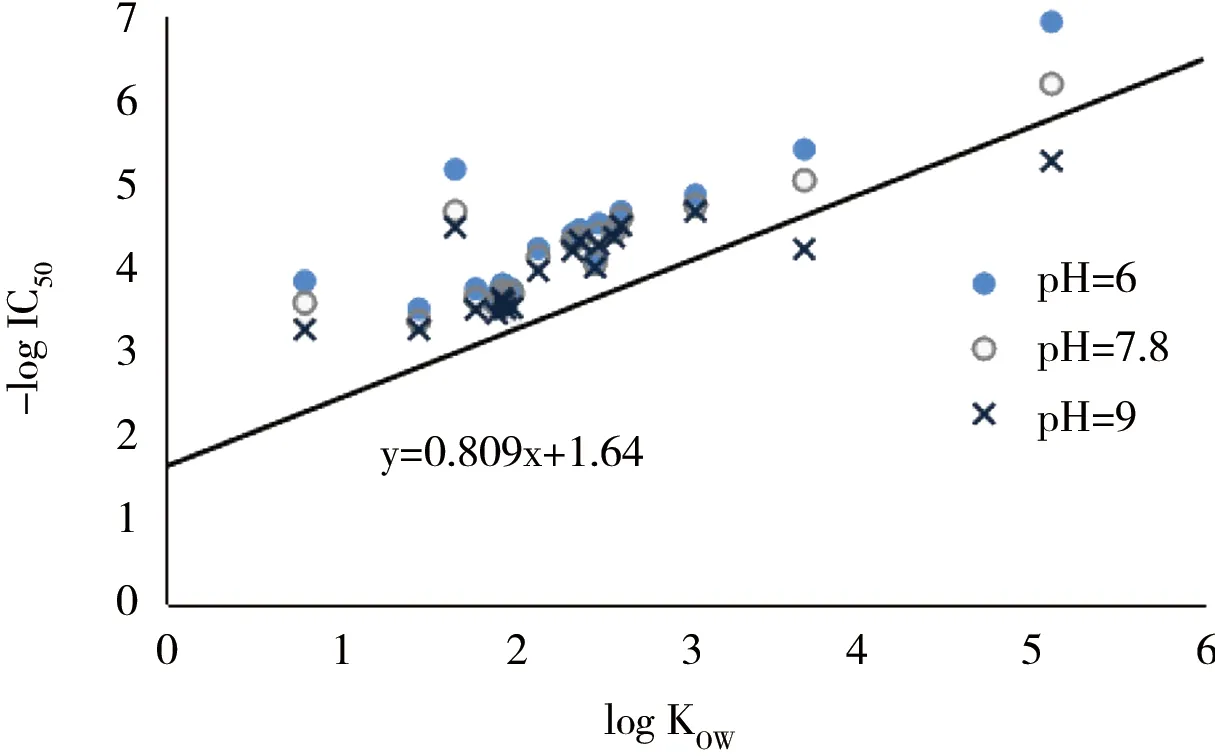
图1 苯酚类化合物log1/IC50与logKOW散点图Fig. 1 Plot of log 1/IC50 against logKOW for phenols
如图1所示,图中实线是根据大型溞基线毒性方程建立的[4],大部分苯酚类化合物在pH从6~9的范围内的毒性都高于基线毒性,2,4,6-三氯苯酚和五氯酚在pH=9的情况下毒性显著低于基线毒性。除各别离群点之外苯酚类化合物与log KOW表现出了较好的相关性。因此我们对取代苯酚类化合物在3个pH条件下对大型溞的毒性建立了log KOW单参数模型,见表3中方程(1)、(3)和(5)。单参数模型具有显著性,但是拟合优度不高。为了改进模型,逐步回归方程引入了可离子化有机化合物在水溶液中非离子态所占比例参数logF0,与log KOW建立了二元线性回归模型,见表3中方程(2)、(4)和(6)。在引入logF0后模型的决定系数得到较大改善。

图2 苯胺类化合物log1/IC50与logKOW散点图Fig. 2 Plot of log 1/IC50 against logKOW for anilines
如图2所示,取代苯胺类化合物的毒性与基线毒性相比表现出了较高的剩余毒性,尤其是邻羟基苯胺和对羟基苯胺。这是由于这2种化合物在环境或者生物有机体中很容易被氧化成苯醌类化合物,而苯醌可以与生物亲核试剂发生迈克尔加成反应,有很高的毒性。我们应用取代苯胺类化合物(氨基苯酚除外)在3个pH条件下对大型溞的毒性建立了logKOW单参数模型,见表3中方程(7)、(9)和(11)。单参数模型具有一定显著性,但是拟合优度不高。苯胺类化合物对大型溞具有反应性,因此我们引入能够在一定程度上代表亲电-亲核反应的参数pKa,与log KOW建立了二元线性回归模型,见表3中方程(8)、(10)和(12)。在引入pKa后,pH=9的模型的决定系数得到显著改善,而pH=6 和pH=7.8的模型的决定系数提高的并不显著。
本研究尝试用logKOW与取代苯甲酸类化合物对大型溞的毒性建立QSAR模型,但是得到的相关方称的结果很差,R2均小于0.2,见表3中方程(13)、(16)和(19)。但是我们发现卤代苯甲酸类化合物毒性与logKOW的相关性较好,见表3中方程(14)、(17)和(20)。在pH=6的条件下,相关方程的决定系数R2高达0.9以上,但随着pH的增高,相关方称的决定系数相应降低。这说明随着pH的增高,疏水性对卤代苯甲酸类化合物的毒性贡献减小。图3是取代苯甲酸类化合物在不同pH条件下毒性与log KOW的散点图。从图中可以看出,在pH=6、pH=7.8和pH=9的条件下,卤代苯甲酸和苯二甲酸都表现出了低于基线毒性的毒性作用。

图3 苯甲酸类化合物log 1/IC50与log KOW散点图Fig. 3 Plot of log 1/IC50 against log KOW for acids
在图3中,我们也发现了部分取代苯甲酸类化合物表现出了较高的剩余毒性,这部分化合物主要是羟基苯甲酸类。这说明羟基苯甲酸类化合物可能具有反应型毒性。应用疏水性参数logKOW和电性参数EHOMO与毒性建立QSAR模型,结果见表3中方程(15)、(18)和(21)。引入电性参数EHOMO,虽然能够使方程的决定系数有所改进,但是并不显著。
取代羟基的个数显著影响羟基苯甲酸类化合物的毒性,如图4所示。因此,将取代羟基的数量(NOH)引入回归方程,见方程(22)、(23)和(24)。结果表明:引入NOH之后,方程的决定系数得到明显改善。
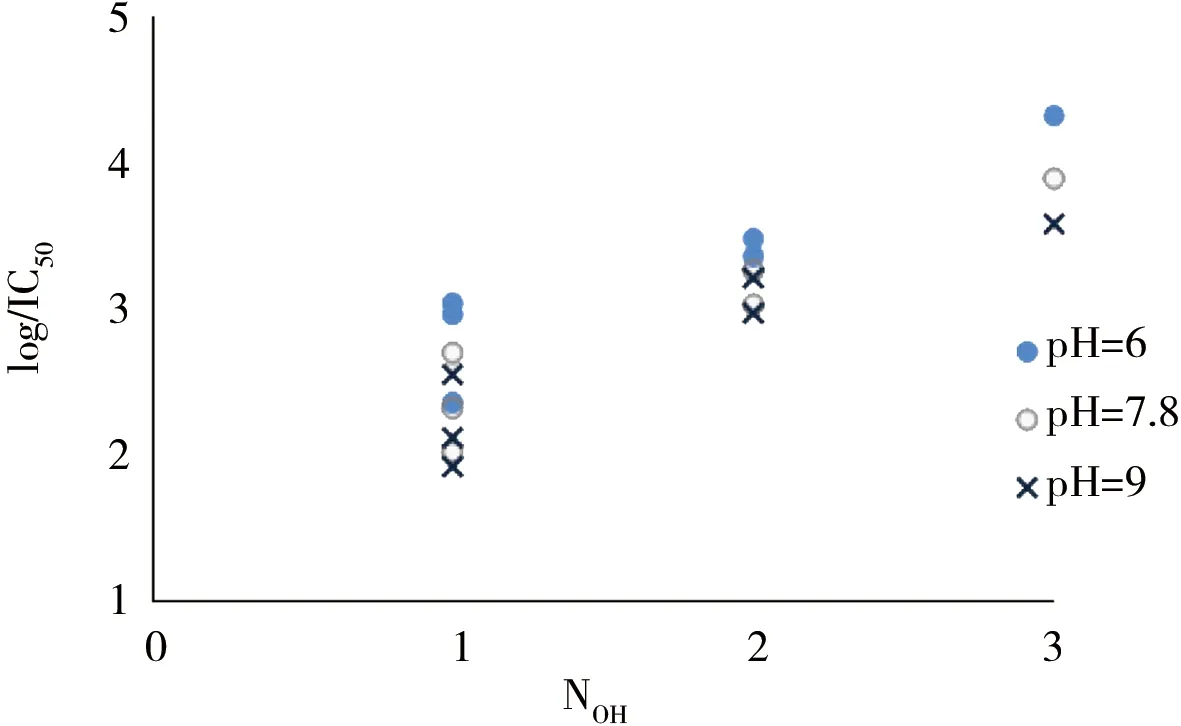
图4 苯甲酸类化合物log 1/IC50与NOH散点图Fig. 4 Plot of log 1/IC50 against NOH for acids
pH=6: log1/ IC50= 0.694 log KOW+ 0.835 EHOMO+ 0.194 ( NOH)2+ 9.72
n=24 R2=0.84 S=0.265 F=36.52
(22)
pH=7.8: log1/ IC50= 0.589 log KOW+ 0.670 EHOMO+ 0.203 ( NOH)2+ 7.58
n=24 R2=0.825 S=0.292 F=24.94
(23)
pH=9: log1/ IC50= 0.591 log KOW+ 0.555 EHOMO+ 0.194 ( NOH)2+ 6.51
n=24 R2=0.789 S=0.261 F=31.43
(24)
3 讨论(Discussion)
大型溞的pH耐受范围是5.5~9.5,在此范围内大型溞可以正常生存,因此本研究在此范围内设定了6、7.8和9三个pH节点。为了证明pH值对可离子化有机化合物毒性的影响是由离子化带来的,我们测定了6种中性化合物在pH为6、7.8和9的条件下对大型溞的毒性,见表4。结果证明,中性化合物在pH从6~9的范围内都以中性态形式存在,不随着pH的变化而变化,而中性化合物在pH从6~9的范围内对大型溞的毒性差异很小,无规律,我们认为这种差异是由试验误差带来的。因此,pH对中性有机物的毒性无影响。
研究结果表明,取代苯酚和苯甲酸类化合物的毒性随着pH的升高而减小,而苯胺类化合物的毒性随着pH的升高而增大,这主要是由于化合物的离子化造成的。有机弱酸和弱碱在水中会发生电离作用,对于一元弱酸来说:
HA=A-+H+
同理,对于一元弱碱来说:
pKb=14-pKa, pOH=14-pH
因此:

表4 不同pH值下中性化合物对大型溞的毒性
所以,当pH = pKa时,有机弱酸或者弱碱的非离子态和离子态所占比例各为50%;对于有机弱酸而言,当pH > pKa时离子态占优势,反之则非离子态占优势;对于有机弱碱而言,当pH > pKa时非离子态占优势,反之则离子态占优势;pH与pKa差值的绝对值越大,离子态或非离子态所占比例越高。Rendal等[11]认为,对酸性化合物而言,当pH-pKa在 -1 ~ 3的范围内时,离子化率对化合物毒性影响较大;对碱性化合物而言,当pH-pKa在 -3 ~ 1的范围内时,离子化率对化合物毒性影响较大。
在本研究中,取代苯酚类化合物随着取代基的不同,离子化率的影响也不相同。苯酚和烷基取代苯酚pH从6~9的范围内pH-pKa均小于-1,所以离子化率对其影响也不显著,平均毒性变化仅为0.18个log单位。而对于卤代酚和硝基苯分类化合物,由于卤素和硝基是吸电子基团,会降低酚羟基上的电子密度,使酚羟基更容易电离。苯酚环上连接的卤素或者硝基越多,吸电子能力就越强,苯酚就越容易水解。一卤代、二卤代苯酚和一硝基苯酚在pH=6时,pH-pKa均小于-1,但是在pH=9时卤代苯酚均大于-1,而由于硝基的吸电子能力更强,单硝基苯酚的pH-pKa都在1左右,因此离子化率对毒性的影响比烷基苯酚类化合物显著,平均毒性变化为0.32个log单位,其中pH从6~7.8平均毒性变化为0.1 log单位,pH从7.8~9平均毒性变化为0.22 log单位。2, 4, 6-三氯苯酚的pH-pKa为-0.2~2.8,在-1~3的范围之内,因此其毒性变化较大为1.19个log单位。五氯酚在pH从6~9的范围内毒性变化最大,为1.66 log单位,这不仅是由于其pH-pKa为1~4,接近-1~3的范围,更重要的是五氯酚和2, 4-二硝基苯酚与以上其他苯酚类化合物的毒性作用机理不同,它们具有氧化磷酸化解偶联效应,既它们进入到生物体细胞内,增加了细胞基质中的质子浓度,破坏了线粒体内外的质子浓度势,阻碍了线粒体的信号传导,使氧化作用和磷酸化作用解偶联,对生物造成很高毒性。因此,毒性随pH值的变化程度不仅与离子化率有关,还与可离子化有机化合物的作用类型和其与生物受体靶位的反应的程度有关。苯胺类化合物的pH-pKa均大于1,所以离子化率F0值对苯胺类化合物的影响并不显著,在pH从6~9 的范围内,平均毒性增长仅为0.24个log单位。
苯胺类化合物的pH-pKa均大于1,所以离子化率F0值对苯胺类化合物的影响并不显著,在pH从6~9的范围内,平均毒性增长仅为0.24个log单位。苯胺类化合物整体对大型溞都表现出了较高毒性,这是由于苯胺类化合物具有反应性。苯胺本身是亲核试剂,氨基上的孤对电子使苯胺很容易与生物大分子中的缺电子基团发生取代反应,如果苯胺的环上连有烷基等给电子基团,则这种反应会增强,毒性也随之增强。如果苯胺环上连有吸电子基团,则这种反应就会减弱,但是如果苯胺环上连着强吸电子基团,如2, 4, 6- 三溴苯胺和2,4-二硝基苯胺,那么氨基将会呈现缺电子状态,使苯胺变成亲电试剂,使毒性增强。在基团活化理论中,邻位的作用最强,其次是对位,间位取代由于有空间位阻效应,活化效果最差。观察一卤代苯胺的毒性发现,间卤代苯胺的毒性最高,这是由于间位卤素与邻对位卤素比,吸电子能力相对较差,对苯胺的亲核性质降低较小,所以毒性较高。
比较取代苯甲酸在pH值为6.0、7.8和9.0情况下的毒性值,我们发现:pH=6和pH=7.8两种条件下的毒性值的平均差值为0.45个log单位,而pH=7.8和pH=9两种条件下的pH-pKa均大于3,毒性值的平均差值仅为0.19个log单位。这是因为取代苯甲酸类化合物大部分在pH=7.8的情况下已经达到了很高的解离程度,因此,在pH从7.8~9的范围内,离子化率对毒性没有影响,但是毒性还是随着pH的降低有所下降,这说明pH除了影响苯甲酸类化合物的离子化率以外,可能还产生了一些其他方面的影响。大型溞的脂质外壳对离子态化合物有很强的阻碍作用,因此大部分苯甲酸类化合物的毒性都在基线毒性以下,但是羟基苯甲酸类化合物对大型溞确表现出了较高的剩余毒性。这可能是由于羟基苯甲酸类化合物在水溶液中可以形成具有较高疏水性的酯类化合物,进而增强了其生物富集能力,大量进入到水生生物体内。而在酯基上连有苯环的酯类化合物在有机体内可以与生物大分子发生双分子历程的亲核取代反应,使毒性增强。由于空间位阻效应,间硝基苯甲酸生成酯类比较困难,所以其毒性相对较低。
综上可知,为了探讨离子化率对化合物毒性的影响,本研究通过实验测定了取代苯酚、苯胺和苯甲酸类化合物在pH值为6、7.8和9的条件下对大型溞的24 h急性毒性。得出以下结论:取代苯酚和苯甲酸类化合物的毒性随着pH的升高而降低,而取代苯胺类化合物的毒性随着pH的升高而升高。氨基苯酚类化合物对大型溞表现出了较高毒性,毒性随pH值变化无规律。离子化率是影响苯酚类化合物毒性的重要因素,可以引入log F0进入到苯酚类化合物的疏水性模型,改进模型的决定系数。苯胺类化合物的离子化程度较低,在设定pH值内主要以非离子态形式存在,离子化率对毒性的影响很小,引入可以代表亲电性质的参数pKa,也不能使模型得到较好改进。氯代苯甲酸类化合物与疏水性的相关性较好,但是羟基苯甲酸类化合物与疏水性参数的相关性很差,引入量子化学参数EHOMO和取代羟基个数NOH,可以改进苯甲酸类化合物的模型的质量。
致谢:感谢哈尔滨师范大学地理科学学院高梅香副教授在文章修改中给予的帮助。
[1] Yangjeh A H, Jenagharad M D, Nooshyar M. Application of artificial neural networks for predicting the aqueous acidity of various phenols using QSAR [J]. Journal of Molecular Modeling, 2006, 12: 338-347
[2] 金相灿. 有机化合物污染化学[M]. 北京: 清华大学出版社, 1990
Jin X C. Chemistry of Organic Compounds [M]. Beijing: Tsinghua University Press, 1990 (in Chinese)
[3] 王红娟, 奚红霞, 夏启斌, 等. 含酚废水处理技术的现状与开发前景[J]. 工业水处理, 2002, 22(6): 6-9
Wang H J, Xi H X, Xia Q B, et al. Present situation and future development of phenol-containing wastewater treatment [J]. Industrial Water Treatment, 2002, 22(6): 6-9 (in Chinese)
[4] Layton A C, Lajoie C A, Easter J P, et al. Molecular diagnostics for polychlorinated biphenyl degradation in contaminated soils [J]. Annals of the New York Academy of Sciences, 1994, 721: 407-421
[5] Zhao Y H, Ji G D, Cronin M T D, et al. QSAR study of the toxicity of benzoic acids to Vibrio fischeri, Daphnia magna and carp [J]. Science of the Total Environment, 1998, 216(3): 205-215
[6] 于瑞莲, 赵元慧, 袁星, 等. 取代苯胺和苯酚类化合物对大型溞的毒性及pH值对其毒性的影响[J]. 环境化学, 1998, 17(5): 451-456
Yu R L, Zhao Y H, Yuan X, et al. Effect of pH Daphnia magna toxicity of substituted anilines and phenals [J]. Environmental Chemistry, 1998, 17(5): 451-456 (in Chinese)
[7] 于瑞莲, 胡恭任. 苯胺类化合物在不同pH值下对大型溞的急性毒性及QSAR研究[J]. 重庆环境科学, 2002, 24(6): 47-49
Yu R L, Hu G R. Acute toxicities of organic acids and bases to photobacterium phosphoreum at different pH [J]. Chongqing Environmental Science, 2002,24(6): 47-49 (in Chinese)
[8] 于瑞莲, 赵元慧, 胡恭任. 酚类对大型溞的急性毒性及QSAR研究[J]. 华侨大学学报:自然科学版, 2003, 24(1): 44-47
Yu R L, Zhao Y H, Hu G R. Acute toxicity of phenol chemicals to Daphnia magna at different pH values and the QSAR study [J]. Journal of Huaqiao University: Natural Science, 2003, 24(1): 44-47 (in Chinese)
[9] Zhang X J, Qin H W, Su L M, et al. Interspecies correlations of toxicity to eight aquatic organisms: Theoretical considerations [J]. Science of the Total Environment, 2010, 408: 4549-4555
[10] Kamaya Y, Fukaya Y, Suzuki K. Acute toxicity of benzoic acids to the crustacean Daphnia magna [J]. Chemosphere, 2005, 59: 255-261
[11] Rendal C, Kusk K O, Tarrp S. Optimal choice of pH for toxicity and bioaccumulation studies of ionizing organic chemicals [J]. Environmental Toxicology and Chemistry, 2011, 30(11): 2395-2406
The Toxicities of Ionized Organic Compounds toDaphniamagnaand QSAR Study
Bao Xin1, Zhang Xujia1,*, Zhao Yuanhui2
1. College of Geographical Sciences , Harbin Normal University, Harbin 150028, China 2. School of Environmental, Northeast Normal University, Changchun 130024, China
The ionization organic compounds of substituted phenols, anilines and benzoic acids are ubiquitous with strong biotoxicity in environmental water and quite harmful to aquatic organisms and aquatic ecosystems. The 24 h acute immobilization toxicity of the three kinds of compounds was determined for the freshwater crustacean Daphnia magna under the condition of pH equal to 6, 7.8 and 9 respectively. The proportion of neutral form (F0) was consequently calculated for the three kinds of compounds at three different pH conditions. Based on the correlation between toxicity and F0, the results showed that it was an important influencing factor of ionization to the toxicity of phenols; and neutral form accounts for absolute advantage, so the effect of ionization on anilines was smaller than phenols. The correlation between the toxicity of halogenated benzoic acids and hydrophobicity parameter was strong, while, the correlation between the toxicity of hydroxyl benzoic acids and hydrophobicity parameter was much weaker. Moreover, the results suggested that inclusion of EHOMOand the number of hydroxyl (NOH) with log KOWcan improve the determinate coefficient of the models.
ionized organic compounds; Daphnia magna; acute toxicity; QSAR

◆
10.7524/AJE.1673-5897.20151122001
黑龙江省自然科学基金(C201022);哈尔滨师范大学博士启动基金项目(kxb201314)
包信(1989-),女,硕士研究生,研究方向为水生生态毒理学,E-mail: 317499292@qq.com
*通讯作者(Corresponding author), E-mail: zhangxj957@nenu.edu.cn
2015-11-22 录用日期:2016-01-21
1673-5897(2016)2-720-12
X171.5
A
简介:张栩嘉(1983-),女,环境科学博士,讲师,主要研究方向为有机污染物毒性作用机理及构效关系,发表学术论文10余篇。
包信, 张栩嘉, 赵元慧. 可离子化有机污染物对大型溞的毒性及QSAR研究[J]. 生态毒理学报,2016, 11(2): 720-731
Bao X, Zhang X J, Zhao Y H. The toxicities of ionized organic compounds to Daphnia magna and QSAR study [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 720-731 (in Chinese)

