5-磺酸间苯二甲酸铜配位聚合物的合成、结构及性能研究
刘 冰, 郭 凯, 何婷婷, 苗卫妮
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
5-磺酸间苯二甲酸铜配位聚合物的合成、结构及性能研究
刘 冰, 郭 凯, 何婷婷, 苗卫妮
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
5-磺酸间苯二甲酸单纳(NaH2SIP)和Cu(Ac)2按照不同比例,通过水热反应合成一个2D铜配位聚合物[Cu3(SIP)(OH)2(Ac)(H2O)2].其结构中包含了一个椅式构型的[Cu4(OH)4]4+单元及一个四边形的[Cu2(Ac)2]2+单元.两类结构单元相互连接形成一条沿c轴[Cu6(Ac)2(OH)4(H2O)4]无机链,通过SIP3-桥联相邻无机链,形成2D层状结构.并通过氢键和π…π堆积作用形成3D超分子框架.该2D层可简化为(6,4)位结点连接的4,6L26{32.42.52}{34.44.54.63}拓扑网络.该配合物的热分解温度为277 ℃,在462 nm处有一荧光发射峰,归属为配体内的π…π*跃迁,PXRD表明样品与化合物1单晶物相相同.
5-磺酸间苯二甲酸; 荧光光谱; 晶体结构; 拓扑
0 引言
金属-有机框架(Metal-organic frameworks,MOFs)材料作为一类多孔性材料,已广泛应用于催化[1]、离子交换[2]、药物传递[3]、气体吸附与分离[4]等研究领域,也是材料科学和配位化学的研究热点之一.MOFs材料是无机金属离子与有机配体通过配位键连接形成具有孔洞结构的一类多维聚合物,相对分子筛等无机多孔性材料,具有结构可调性、通用性及柔韧性等优点[5].当前对MOFs材料的研究主要集中在结构的设计优化、性能表征和构效关系研究上.对MOFs材料构效关系的深入研究有助于对MOFs材料的设计原则的理解,也有助于提高设计特定性能的MOFs材料的准确性[6].但目前研究还不能准确预测MOFs材料的结构及性能[7].MOFs材料设计原则之一是选用多功能有机配体与特定金属中心反应[8].5-磺酸间苯二甲酸(常以5-磺酸间苯二甲酸单钠盐(NaH2SIP)的形式出售)为一个多功能刚性配体,常用于MOFs材料的合成,具有以下优点:(1)5-磺酸间苯二甲酸中包含了配位能力较强的两个处于间位的羧基,可作为桥联配位基团;(2)配位能力较弱的磺酸基可作为分子间氢键的受体,用于搭建超分子网络[9];3)苯环可作为羧基与磺酸基间的空间连接体,也可通过π…π堆积作用组织超分子网络[10].5-磺酸间苯二甲酸不对称的构型较易形成具有非心空间群的结构,从而易于获得非线性光学功能材料[11].5-磺酸间苯二甲酸基MOFs材料金属中心来源广泛,涵盖了主族金属[12]、过渡金属[13]及稀土金属[9,14].
本文以NaH2SIP为有机配体与Cu(Ac)2按不同比例水热合成一2D层状化合物[Cu3(SIP)(OH)2(Ac)(H2O)2](1).通过X-射线单晶衍射、X-射线粉末衍射(PXRD)、热重(TG)、FT-IR、荧光光谱等表征了该化合物的单晶结构及性能.
1 实验部分
1.1 原料与仪器
(1)主要试剂及原料:本文实验所用药品未做进一步纯化.NaH2SIP购自梯希爱(上海)化成工业发展有限公司,Cu(Ac)2和DMF购自国药集团化学试剂有限公司,全氟聚醚真空油(FOMBLIN Y LVAC 25/6)购自西宝生物有限公司,均为分析纯.红外光谱所用KBr为光谱纯,购自国药集团化学试剂有限公司.
(2)主要仪器型号及测试条件:傅立叶红外光谱(Bruker Tensor 27,布鲁克)采用KBr压片法,测量范围4 000~400 cm-1.热重分析仪(SDT Q600 V8.3 Build 101,美国TA仪器):样品在N2氛下测试,N2流速为20 cm3·min-1,升温速率为10 ℃·min-1,测量温度为20 ℃~800 ℃.X-射线粉末衍射(Rigaku D/Max-3c,日本理学株式会社),辐射源为Cu Kα射线(λ1=1.540 598 Å;λ2=1.544 426 Å),测试条件为:室温下连续模式,工作电压为40 kV,工作电流为50 mA,2θ扫描范围为3 °~60 °,步进为0.02 °,扫描速度为4 °min-1.固态荧光光谱(Hitachi F-4600,日本日立株式会社)室温下测试,以氙灯作激发光源,发射和激发狭缝均为2.5 nm,步进为2.0 nm,积分时间为0.1 s.
1.2 [Cu3(SIP)(OH)2(Ac)(H2O)2](1)的合成
0.1 mmol,0.026 8 g NaH2SIP,0.2 mmol,0.039 9 g Cu(Ac)2·H2O与10 mL水混合置于25 mL聚四氟乙烯水热罐中,160 ℃加热5天,自然降温获得蓝色棱柱状晶体,依次用水和乙醇洗涤,50 ℃干燥24 h,收集产物22.9 mg,产率为60.94%.
不同比例的Cu(Ac)2和NaH2SIP (Cu(Ac)2∶NaH2SIP =0.1∶0.1-0.5,间隔为0.1 mmol)在相似反应条件下同样可获得化合物1;当Cu(Ac)2∶NaH2SIP=0.1∶0.2时,在H2O/DMF (5 mL∶5 mL)混合溶剂中,相似反应条件下反应可制备化合物1.
1.3 X-射线单晶衍射
使用全氟聚醚真空油在显微镜下挑选适合X-射线单晶衍射用的晶体.将挑选的晶体置于Bruker X8 Kappa APEX II CCD面探衍射仪上,使用APEX2软件包收集X-射线单晶衍射照片.室温下利用石墨单色化的Mokα射线(λ=0.710 73 Å),以ω扫描方式收集一定角度的衍射数据.利用SAINT+程序进行衍射数据的指标化和还原,使用SADABS软件包对衍射数据进行洛仑兹和极化影响的强度校正及经验吸收.化合物1的晶体结构通过使用SHELXTLTM晶体软件包由直接法解出,并基于F2函数对非氢原子经全矩阵最小二乘法进行精修.所有非氢原子的热参数进行各向异性修正.氢原子由理论加氢得到,只计算不修正.化合物1的晶体学数据详见表1,主要键长和键角列于表2中.
化合物1的晶体学数据(不包含结构因子)已经上传到剑桥晶体学数据库中,CCDC号为1438100,可通过网址免费获取:www.ccdc.cam.ac.uk/data_request/cif.

表1 化合物1的晶体学数据
R1=(Σ||Fo|-|Fc||/Σ|Fo|). wR2=[Σ(w(Fo2-Fc2)2)/Σ(w|Fo2|2)]1/2
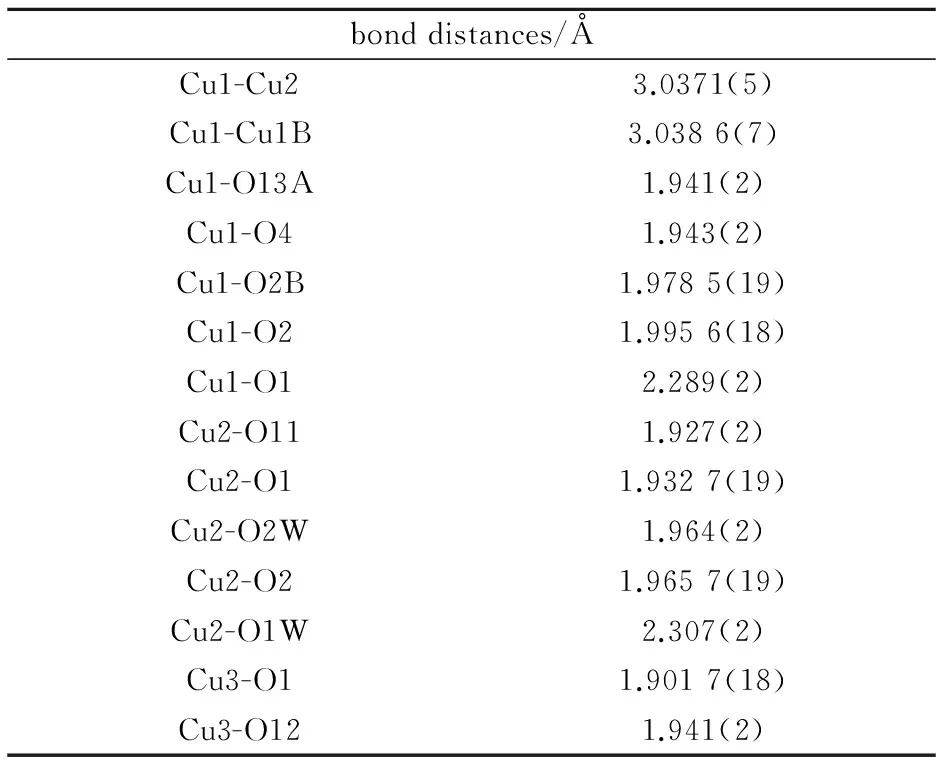
表2 化合物1的主要键长(Å)和键角(°)
续表2

bonddistances/ÅCu3-O14A1.9416(19)Cu3-O3C1.9821(19)Cu3-O32.268(2)O13A-Cu1-O496.40(10)O13A-Cu1-O2B94.97(9)O4-Cu1-O2B159.46(9)O13A-Cu1-O2171.33(9)O4-Cu1-O290.35(9)O2B-Cu1-O280.26(8)O13A-Cu1-O197.00(8)O4-Cu1-O1101.58(8)O2B-Cu1-O193.93(7)O2-Cu1-O176.24(7)O13A-Cu1-Cu2135.25(6)O4-Cu1-Cu286.30(7)O2B-Cu1-Cu297.53(5)O2-Cu1-Cu239.58(5)O1-Cu1-Cu239.50(5)O13A-Cu1-Cu1B134.88(7)O4-Cu1-Cu1B127.86(7)O2B-Cu1-Cu1B40.34(5)O2-Cu1-Cu1B39.92(6)O1-Cu1-Cu1B83.60(5)Cu2-Cu1-Cu1B65.110(13)O11-Cu2-O196.57(8)O11-Cu2-O2W86.64(9)O1-Cu2-O2W171.05(11)O11-Cu2-O2169.49(10)O1-Cu2-O285.85(8)O2W-Cu2-O289.54(9)O11-Cu2-O1W103.93(10)O1-Cu2-O1W86.30(8)O2W-Cu2-O1W101.08(10)O2-Cu2-O1W86.41(8)O11-Cu2-Cu1137.30(6)O1-Cu2-Cu148.88(6)O2W-Cu2-Cu1124.16(8)O2-Cu2-Cu140.31(5)O1W-Cu2-Cu198.43(6)O1-Cu3-O1293.42(9)O1-Cu3-O14A93.86(8)O12-Cu3-O14A160.06(11)O1-Cu3-O3C177.28(8)O12-Cu3-O3C84.50(9)O14A-Cu3-O3C88.67(8)O1-Cu3-O398.74(8)O12-Cu3-O3100.39(10)O14A-Cu3-O396.81(9)O3C-Cu3-O379.95(8)
对称码:A=x+1, y-1, z; B=-x+3, -y+2, -z-2; C=-x+3, -y+2, -z-1; D=x-1, y+1, z.
1.4 拓扑分析
根据A.F.Wells拓扑网络结点的定义[15]及化合物1的结构特征,[Cu4(OH)4]4+、[Cu2(Ac)2]2+次级构筑单元(SBUs)和SIP3-3体分别虚拟为6-、6-、4-连接结点,通过拓扑结构分析软件包TOPOS 4.0中的ADS程序计算化合物1拓扑结构.
2 结果与讨论
2.1 合成
Cu(Ac)2与NaH2SIP的比例由0.1∶0.1-0.5(间隔为0.1 mmol)在相同条件下反应均得到化合物1,表明在指定反应条件下,化合物1是主要产物.化合物1还可以通过使用等体积混合溶剂H2O/DMF获取,但在乙醇或甲醇中产物为粉末,表明溶剂在产物结晶过程中起着重要作用.使用其他铜盐重复相类似的实验时,并不能得到类似产物.例如,Cu(NO3)2与NaH2SIP在反应比例0.1∶0.1-0.5(间隔为0.1 mmol)得到均为绿色澄清溶液.使用CuSO4时,当CuSO4∶NaH2SIP=0.1∶0.1-0.5时,产物为蓝色溶液;当CuSO4∶NaH2SIP=0.4-0.2∶0.1时,产物为蓝色沉淀.若使用CuCl2,当CuCl2∶NaH2SIP= 0.1∶0.1-0.5时,则产物均为棕色沉淀.上述现象表明阴离子在产物结晶过程中有重要影响.化合物1的反应条件也运用到其他过渡金属盐的反应中,如Ag+,Ni2+的产物为沉淀,Co2+在高比例金属时为沉淀,高比例配体时为粉色溶液,且自然挥发母液没有得到合适的单晶,表明金属中心在配合物的合成起着关键作用.
2.2 晶体结构
化合物1是一个由SIP3-配体支撑的2D层状结构,该2D层由一条[Cu6(Ac)2(OH)4(H2O)4]无机链与SIP3-配体连接而成.化合物1的不对称单元包含了3个独立的Cu(II),一个完全去质子化的SIP3-配体,一个Ac-离子及2个独立的μ3-OH-离子(如图1所示).正负电荷可完全中和,使化合物1保持电中性.O1和O2的键价和(BVS)通过计算分别为1.243和1.329,接近1,表明O1和O2均为OH-离子,与电荷分析相符.Cu1为五配位畸形四方锥构型,由O2,O2B,O4和O13A(A=x+1,y-1,z;B=-x+3,-y+2,-z-2)构成四方锥的基面,O1为四方锥顶点.Cu1偏离四方锥最小二乘基面的最大偏离度为0.187 3 Å.Cu2与Cu3的配位构型均为四方锥,其偏离四方锥最小二乘基面的最大偏离度分别为0.063 3 Å和0.1615 Å.Cu1、Cu2、Cu3的CuO5四方锥的畸形度τ分别为0.066,0.009,0.096(τ=(β-α)/60,α、β分别为Cu原子基面中最大的二个键角.理想四方锥的α=β=180 °,τ=0).
Cu1与Cu2通过O1和O2桥联形成四边形[Cu2(OH)2]2+单元.每两组[Cu2(OH)2]2+被Cu1-O2键连接形成椅式[Cu4(OH)4]4+次级单元,其中Cu1…Cu2与Cu1…Cu1距离分别为3.037 1(5) Å和3.038 6(7) Å.Ac-离子通过单齿桥联的O3原子将Cu3及其对称原子连接形成[Cu2(Ac)2]2+次级单元.上述[Cu4(OH)4]4+及[Cu2(Ac)2]2+次级单元通过Cu1-O4和Cu3-O1键相互连接形成了一条沿c轴方向无机[Cu6(Ac)2(OH)4(H2O)4]链(图2).SIP3-配体中二个间位羧基以μ4-二(双齿桥联)模式(图3)分别连接Cu2-Cu3、Cu1-Cu3形成沿bc平面的2D层(图2).在2D层中,配位水与磺酸基之间形成了分子间氢键(O1W-H1WA…O16=2.846(3) Å 139(3) °;O1W-H1WB…O17=2.790(3) Å,175(3) °;O2W-H2WB…O17=2.715(3) Å,169(4) °),苯环间形成了π…π堆积作用(π…π=3.619 Å,π为苯环的质心).通过上述分子间作用力,2D层构筑为3D超分子网络(图4).
根据化合物1的结构特征,通过TOPOS 4.0拓扑结构软件分析包,将[Cu4(OH)4]4+、[Cu2(Ac)2]2+次级构筑单元和SIP3-配体分别虚拟为6-、6-、4-位节点.[Cu4(OH)4]4+、[Cu2(Ac)2]2+结点的点符号均为{34.44.54.63},SIP3-结点为{32.42.52},因此化合物1的整体结构可简化为一个(6,4)连接的4,6L26{32.42.52}{34.44.54.63}拓扑网络(图2).

对称码:A=x+1,y-1,z;B=-x+3,-y+2,-z-2;C=-x+3,-y+2,-z-1.图1 化合物1中Cu(Ⅱ)原子的配位环境图

图2 化合物1的结构构建图及拓扑结构图

图3 SIP3-配体的配位方式图

图4 化合物1的3D超分子网络图
2.3 性能表征
2.3.1 X-射线粉末衍射
水热反应使用水或混合溶剂H2O/DMF做溶剂均可获得化合物1,其X-射线粉末衍射(PXRD)图样与通过单晶数据拟合的PXRD图样一致,表明产物为化合物1的单一物相,性能测试样品与单晶样品一致(图5).
2.3.2 固态荧光光谱
室温条件下测试化合物1、NaH2SIP的固态荧光光谱.在285紫外光的激发下,NaH2SIP在321 nm处产生一个较宽的的发射光谱,该发射峰可归属于π*→n跃迁[16].文献报道的H3SIP激发波长为320 nm,但发射波长为467 nm.H3SIP去质子形成单钠盐NaH2SIP,发射波长有146 nm的红移.373 nm紫外光激发化合物1,在467 nm处产生浅蓝色的荧光(如图6(a)所示).CIE 1931软件分析其色温坐标图,证实其荧光为淡蓝色(如图6(b)所示).与NaH2SIP的荧光光谱比较,可观测到约141 nm的红移.该类红移在苯羧酸基和SIP基配合物较为常见.例如,在文献报道的SIP基配合物的发射光谱常在410~430 nm,可归属于配体到金属的跃迁(ligand-to-metal-charge transfer,LMCT)[11,12,16,17].化合物1与H3SIP的荧光光谱非常相似,表明化合物的发射光谱可归属为配体内电荷跃迁(intraligand charge transfer,ILCT),即配体内π…π*跃迁.化合物1与NaH2SIP发射光谱的不同,表明金属中心与(H)SIP配体的相互作用将影响其荧光光谱.金属与苯环的作用,影响苯环间的π…π堆积作用,进而影响其荧光光谱.

图5 化合物1的实验测试PXRD图样与单晶数据拟合PXRD图样比较

(a)化合物1、NaH2SIP的固态荧光光谱图

(b)化合物1的色温图图6 化合物1及NaH2SIP的荧光光谱图及CIE软件计算的色温图
2.3.3 热重分析
化合物1的热重分析表明其失重分为2个步骤.第一步出现在174 ℃~277 ℃,失重约8.0%,归属为配位水的失去,与理论值6.4%接近.在随后277 ℃~595 ℃温度范围内,有约57.3%较大失重出现,归属为金属-有机框架内的各成分(包括SIP3-配体、Ac-和OH-离子)的氧化导致2D框架的坍塌(如图7所示).框架内各成分的同步分解亦表明该2D金属-机框架具有较好的热稳定性.

图7 化合物1的热重曲线图
3 结论
本文通过反应物的不同比例、不同溶剂水热合成2D[Cu3(SIP)(OH)2(Ac)(H2O)2](1)MOFs材料.该2D化合物包含一椅式构型的[Cu4(OH)4]4+及四边形[Cu2(Ac)2]2+次级构筑单元.其相互连接形成一条沿从c轴方向的无机链[Cu6(Ac)2(OH)4(H2O)4],并通过分子间氢键及苯环间π…π堆积作用构建3D超分子框架.该化合物的拓扑结构分析表明,将[Cu4(OH)4]4+、[Cu2(Ac)2]2+次级构筑单元和SIP3-配体分别虚拟为6-、6-、4-位节点,化合物1简化为(6,4)连接的4,6L26{32.42.52}{34.44.54.63}拓扑网络.实验测试的PXRD图样与由单晶数据拟合的PXRD图样一致,表明样品性能测试的样品与单晶结构测试样品物相同.固态荧光光谱表明化合物在373 nm光激发下,在462 nm产生一较宽的发射峰,与H3SIP固态荧光相似,表明该发射峰应归属为配体内的π…π*电子跃迁.TG分析表明化合物1的失重分为两步:第一步发生在174 ℃~277 ℃,主要失去配位水;第二步发生在277 ℃~595 ℃,为SIP3-配体、Ac-和OH-离子同步氧化,导致2D框架的坍塌.
[1] Corma H,Garcia F X,Llabres I X.Engineering metal organic frameworks for heterogeneous catalysis[J].Chemistry Review,2010,110(8):4 606-4 655.
[2] Seo J S,Whang D,Lee H,et al.A homochiral metal-organic porous material for enantioselective separation and catalysis[J].Nature,2000,404:982-986.
[3] An J,Geib S J,Rosi N L.Cation-triggered drug release from a porous zinc-adeninate metal-organic framework[J].Journal of American Chemistry Society,2009,131(24):8 376-8 377.
[4] Vaidhyanathan R,Iremonger S S,Shimizu G K H,et al.Competition and cooperativity in carbon dioxide sorption by amine-functionalized metal-organic frameworks[J].Angewandte Chemie International Edition,2012,51(8):1 826-1 829.
[5] Xu H,Gao J K,Wang J P,et al.Surfactant-thermal method to synthesize a new Zn(II)-trimesic MOF with confined Ru(bpy)32+complex[J].Journal of Solid State Chemistry,2015,226:295-298.
[6] Gao J K,Miao J W,Li P Z,et al.A p-type Ti(IV)-based metal-organic framework with visible-light photo-response[J].Chemical Communications,2014,50:3 786-3 788.
[7] Ouellette W,Hudson B S,Zubieta J.Hydrothermal and structural chemistry of the zinc(II)-and cadmium(II)-1,2,4-triazolate systems[J].Inorganic Chemistry,2007,46(12):4 887-4 904.
[8] Nagarathinam M,Vittal J J.Anisotropic movements of coordination polymers upon desolvation:Solid-state transformation of a linear 1D coordination polymer to a ladderlike structure[J].Angewandte Chemie International Edition,2006,45(26):4 337-4 341.
[9] Liu Q Y,Xu L.Novel structure evolution of lanthanide-SIP coordination polymers (NaH2SIP=5-sulfoisophthalic acid monosodium salt) from a 1D chain to a 3D network as a consequence of the lanthanide contraction effect[J].European Journal of Inorganic Chemistry,2005,17:3 458-3 466.
[10] Dalrymple S A,Parvez M,Shimizu G K H.Intra-and intermolecular second-sphere coordination chemistry:Formation of capsules,half-capsules,and extended structures with hexaaquo- and hexaamminemetal ions[J].Inorganic Chemistry,2002,41(26):6 986-6 996.
[11] Liu Q Y,Wang Y L,Zhang N,et al.Spontaneous resolution in the ionothermal synthesis of homochiral Zn(II) metal-organic frameworks with (10,3)-a topology constructed from achiral 5-sulfoisophthalate[J].Crystal Growth & Design,2011,11(9):3 717-3 720.[12] Li P,Yu Q,Chen J,et al.Supramolecular coordination complexes with 5-sulfoisophthalic acid and 2,5-bipyridyl-1,3,4-oxadiazole:Specific sensitivity to acidity for Cd(II) species[J].Crystal Growth & Design,2010,10(6):2 650-2 660.
[13] Yang E C,Zhang Y Y,Liu Z Y,et al.Diverse self-assembly from predesigned conformationally flexible pentanuclear clusters observed in a ternary copper(II)-triazolate-sulfoisophthalate system:Synthesis,structure and magnetism[J].Inorganic Chemistry,2014,53(1):327-335.
[14] Song J L,Lei C,Mao J G.Syntheses,crystal structures,and luminescent properties of novel layered lanthanide sulfonate-phosphonates[J].Inorganic Chemistry,2004,43(18):5 630-5 634.
[15] Wells F.Three-dimensional nets and polyhedra[M].New York:Wiley-Interscience,1977.
[16] Liu Q Y,Xu L.Synthesis,crystal structures and photophysical properties of two supramolecular complexes of cadmium(II)[J].Inorganic Chemistry Communications,2005,8(4):401-405.
[17] Wu G,Yin F J,Wei H,et al.Synthesis,structure,luminescent and thermal properties of ytterbium(III) and dysprosium(III) complexes with 5-sulfoisophthalic acid sodium salt[J].Zeitschrift für Anorganische and Allgemeine Chemie,2011,637(5):602-607.
【责任编辑:蒋亚儒】
Synthesis,structure and property of a 2D 5-sulfoisophthalate-based copper coordination polymer
LIU Bing, GUO Kai, HE Ting-ting, MIAO Wei-ni
(College of Chemistry and Chemical Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China)
A 2D copper-sulfoisophthalate compound,[Cu3(SIP)(OH)2(Ac)(H2O)2] (1),was synthesized from the hydrothermal reactions of 5-sulfoisophthalic acid monosodium salt (NaH2SIP) with Cu(Ac)2at different ratios. Compound 1 distinguishes itself as a 2D layered network, in which a [Cu4(OH)4]4+subunit of chair configuration and a quadrangular Cu2(Ac)2subunit were formed.The interconnection of [Cu4(OH)4]4+and [Cu2(Ac)2] subunits shapes into a inorganic [Cu6(Ac)2(OH)4(H2O)4] chain along the c-direction.With the linkage of SIP3-spacer,a 2D layered compound is constructed,and further fabricated into 3D supermolecular architecture based on the connections of hydrogen bindings and π…π stacking interactions. Compound 1 is simplified as a (6,4)-connected 4,6L26 {32.42.52}{34.44.54.63} topological network.The thermal stability of 1 is up to ca. 277 ℃,and the fluorescence of 1 shows an emission at 462 nm assigned to π…π*intraligand transfer.PXRD of compound 1 confirms the phase purity of the bulk sample.
sulfoisophthalic acid; fluorescence; crystal structure; topology
2016-06-25
教育部留学归国人员科研基金项目(2015); 国家级大学生创新创业训练计划项目(201610708029); 陕西科技大学博士科研启动基金项目(BJ14-02)
刘 冰(1975-),男,湖南益阳人,副教授,博士,研究方向:配位化学
1000-5811(2016)06-0104-06
O614.121
A

