鸡肉组织中磺胺氯达嗪钠的高效液相色谱法检测
王小柱
(辽宁省畜产品安全监察所,辽宁 沈阳 110003)
鸡肉组织中磺胺氯达嗪钠的高效液相色谱法检测
王小柱
(辽宁省畜产品安全监察所,辽宁沈阳110003)
本试验通过引入磺胺嘧啶钠、磺胺二甲基嘧啶、磺胺间甲氧嘧啶、磺胺甲恶唑、磺胺二甲氧嘧啶、磺胺喹恶啉、磺胺氯吡嗪等7种磺胺药与磺胺氯达嗪钠进行高效液相色谱残留对比分析,建立了一种在鸡肉组织中磺胺氯达嗪钠的高效液相色谱检测法。这对控制鸡肉组织中磺胺类药物残留、保障人类健康具有重要意义。
磺胺氯达嗪钠;鸡肉组织;高效液相色谱法;检测
磺胺类药物(Sul fonamides,Sas)是指具有对氨基苯磺酰胺结构的一类药物的总称,主要用于预防和治疗细菌感染性疾病的化学治疗,对危害家禽的某些原虫也有作用。但磺胺类药物在服用后可引起恶心、呕吐、头晕、全身无力等不良反应,易在肾小管、肾盂、输尿管、膀胱等处形成结晶,引起腰痛、血尿、尿路阻塞等,长期服用甚至可以形成结石。驾驶员、高空作业者等群体更需慎服。
磺胺类药物在体内代谢缓慢,因此,磺胺类药物的残留也日益引起人们对食物安全的关注。食物中磺胺类药物的残留可引起过敏性体质人的过敏反应,使病原菌产生抗药性等,因此,许多国家对食品中磺胺类药物的最大残留量作了严格的限定,如欧洲和美国肉类产品的最大残留量为100 ng/g,牛奶中为10 ng/g[1]。
鸡肉是磺胺类药物残留的靶组织,研究鸡肉组织中磺胺类药物残留分析方法对其残留的监控具有重要的价值。目前对于SAs残留分析的报道很多,主要是各种高效液相色谱法(HPLC),采用恒溶剂或梯度分离的方式,通过直接紫外法(UV)、荧光衍生化法或比色法进行检测,这些方法通常需要多个液-液分配(LLF)、浓缩等步骤[2],操作比较复杂,并且针对鸡肉组织样品的残留分析资料较少。本试验选择国内较常见的7种磺胺类药物与磺胺氯哒嗪钠作为比照对象[3],以碱性氧化铝柱固相萃取(SPE)和恒溶剂洗脱HPLC为基础[4],建立了鸡肉组织中的磺胺氯哒嗪钠的残留分析方法,对控制鸡肉组织中该药的残留、保证鸡肉的正常出口、保障人类身体健康具有重要意义。
1 材料与方法
1.1试验材料鸡肉样品由沈阳市商检所提供,4℃保存待用。
1.2试验方法
1.2.1色谱条件色谱柱:C18柱,250㎜×4.6㎜i.d.
流动相:乙腈-磷酸(0.017 mol/L)(20+80)
流速:1.0 mL/min
检测波长:270 nm
进样量:20μL
保留时间:14.653~15.128 min
1.2.2标准溶液的制备
1.2.2.1磺胺嘧啶钠准确称取将磺胺嘧啶钠标准品10 mg,置于100 mL容量瓶中,用甲醇溶液定容、摇匀,作为储备液。C=105ng/mL。
1.2.2.2磺胺二甲基嘧啶准确称取将磺胺二甲基嘧啶标准品10 mg,置于100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.3磺胺间甲氧嘧啶准确称取将磺胺间甲氧嘧啶标准品10 mg,置于100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.4磺胺甲恶唑准确称取将磺胺甲恶唑标准品10 mg,置于100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.5磺胺二甲氧嘧啶准确称取将磺胺二甲氧嘧啶标准品10 mg,放入100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.6磺胺喹恶啉准确称取将磺胺喹恶啉标准品10 mg,放入100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.7磺胺氯吡嗪准确称取将磺胺氯吡嗪标准品10 mg,放入100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.8磺胺氯达嗪钠准确称取将磺胺氯达嗪标准品10 mg,放入100 mL容量瓶中,用甲醇溶液定容,摇匀。作为储备液。C=105ng/mL。
1.2.2.98种药物的混合液从已配制好的上述8种溶液各吸取1 mL置于100 mL容量瓶中,用流动相溶解,定容,摇匀。
1.2.3样品处理将鸡肉组织解冻、绞碎,用分析天平准确称取鸡肉组织5.0 g,量取乙腈25 mL,加入4.0 g无水硫酸钠,一起置于匀浆杯中,用玻璃棒搅拌。匀浆机匀浆后,将样液倒入50 mL离心管中,3 000 r/min离心5 min;将分离后的残渣再用25 mL乙腈处理,玻璃棒搅拌,振荡10 min后,3 000 r/min离心5 min;合并两次上清液置于分液漏斗中,加入正己烷30 mL,同向手动振荡10 min后,取下层液体,置于旋转蒸发瓶中,再加入正丙醇10 mL,在54℃下用旋转蒸发仪浓缩,残留物用3 mL 95%的乙腈溶解。摇动1 min后,过Sep-Pak氧化铝柱(需预先用95%的乙腈10 mL平衡柱体),残留物再加95%的乙腈5 mL溶解,摇动1 min后过柱,不收集样液。用70%的乙腈10 mL洗脱,收集洗脱液并加入5 mL正丙醇。于54℃条件下用旋转蒸发仪浓缩干燥。残留物用2 mL已超声过的流动相溶解,溶解后的液体用带过滤膜的注射器收集。所制样液用高效液相色谱仪进行检测。
1.3标准曲线
1.3.1绘制标准曲线的原理由磺胺氯达嗪钠的系列浓度与图谱显示的峰面积绘制标准曲线,浓度与峰面积成正向关系(线性关系)。本试验的药物添加浓度在标准曲线线性范围之内,说明本试验方法可行。
1.3.2储备液的稀释及进样稀释过程
1.3.2.1磺胺氯达嗪钠C=500 ng/mL的配置从磺胺氯达嗪的原液中用刻度吸管各吸取1 mL放入200 mL容量瓶中,用流动相溶解,摇匀,定容至刻度。所得样液为所要稀释的浓度。
1.3.2.2磺胺氯达嗪钠C=400 ng/mL的配置从磺胺氯达嗪的原液中用刻度吸管各吸取1 mL放入250 mL容量瓶中,用流动相溶解,摇匀,定容至刻度。
1.3.2.3磺胺氯达嗪钠C=200 ng/mL的配置从C=400 ng/mL的容量瓶中,用25 mL的移液管吸取25 mL的溶液放到50 mL的容量瓶中,用流动相溶解,摇匀,定容至刻度。
1.3.2.4磺胺氯达嗪钠C=100 ng/mL的配置从C=500 ng/mL的容量瓶中,吸取5 mL的溶液置于25 mL容量瓶中,用流动相溶解,摇匀,定容至刻度。
1.3.2.5磺胺氯达嗪钠C=50 ng/mL的配置从C= 500 ng/mL的容量瓶中,吸取5 mL溶液置于50 mL容量瓶中,用流动相溶解,摇匀,定容至刻度
1.3.2.6磺胺氯达嗪钠C=20 ng/mL的配置从C= 400 ng/mL的容量瓶中,吸取5 mL的溶液置于100 mL的容量瓶中,用流动相溶解,摇匀,定容至刻度。
1.3.2.7磺胺氯达嗪钠C=10 ng/mL的配置从C= 500 ng/mL的容量瓶中,吸取1 mL的溶液置于50 mL的容量瓶中,用流动相溶解,摇匀,定容至刻度。
1.3.3标准曲线的绘制根据磺胺氯达嗪钠的系列浓度与相应图谱的峰面积(S)确定标准曲线,建立回归方程。
1.4样品添加回收率的测定按照样品处理方法进行制备样液,用高效液相色谱仪进行检测。在0.05~0.5 mg/kg添加浓度范围内,每个浓度梯度的样品设置5次重复。
1.5变异系数的测定将空白组织中添加磺胺氯达嗪钠(浓度为500 ng/mL)标准品,按此浓度的50%、100%、200%添加,按标准各测定3次(每次5个平行),由测出的回收率进行检测其变异系数,变异系数=标准差/平均数×100%。
2 结果与分析
2.188种药物标准溶液的色谱检测结果8种药物混合标准液经高液相色谱仪检测,图谱显示,磺胺氯达嗪钠与其他7种磺胺类药物的图谱峰形互不重叠(图1)。说明磺胺氯达嗪钠与其他7种磺胺类药物的添加可以明显区分,各药物互不干扰。
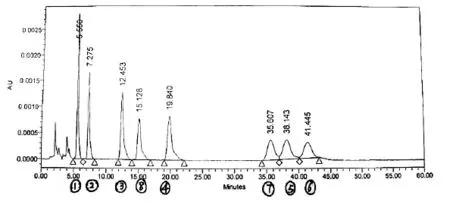
图1 8种药物的混合液的色谱图Fig.1 Chromatogram o f 8 kinds o f drug m ixtures
药物保留时间顺序:磺胺嘧啶钠;磺胺二甲基嘧啶;磺胺间甲氧嘧啶;磺胺氯达嗪钠;磺胺甲恶唑;磺胺氯吡嗪;磺胺二甲氧嘧啶;磺胺喹恶啉。
药物保留时间:磺胺嘧啶钠5.550 min;磺胺二甲基嘧啶7.275 min;磺胺间甲氧嘧啶12.453 min;磺胺氯达嗪钠15.128 min;磺胺甲恶唑19.840 min;磺胺氯吡嗪35.607 min;磺胺二甲氧嘧啶38.143 min;磺胺喹恶啉41.445 min。
2.2线性回归方程根据磺胺氯达嗪的系列浓度与相应图谱的峰面积确定标准曲线,建立回归方程(表1)。
2.3样品添加回收率与相关数据的结果分为添加样和阴性样(不含磺胺氯达嗪钠)两组,在阴性样中按50%、100%、200%添加磺胺氯达嗪钠对照品,按标准各测定3次(每次5个平行)(表2)。磺胺氯达嗪钠的平均回收率在55.0%~81.3%之间,阴性样响应值为0,说明其组织成分无干扰,方法可行。
按照检测限的定义,磺胺氯哒嗪钠的检测限为0.005 mg/kg,定量限低于0.01 mg/kg,50%浓度添加的变异系数(RSD)为4.17%~7.35%,100%浓度添加的变异系数为4.60%~7.96%,200%浓度添加的变异系数为2.32%~7.28%。
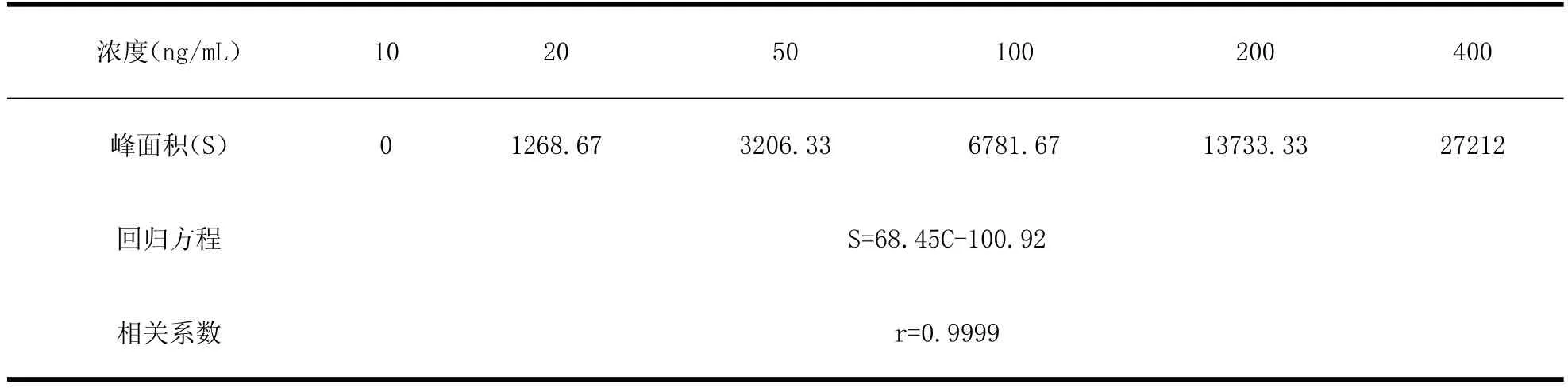
表1 回归方程及相关系数Table1 The regression equation and correlation coe fficient
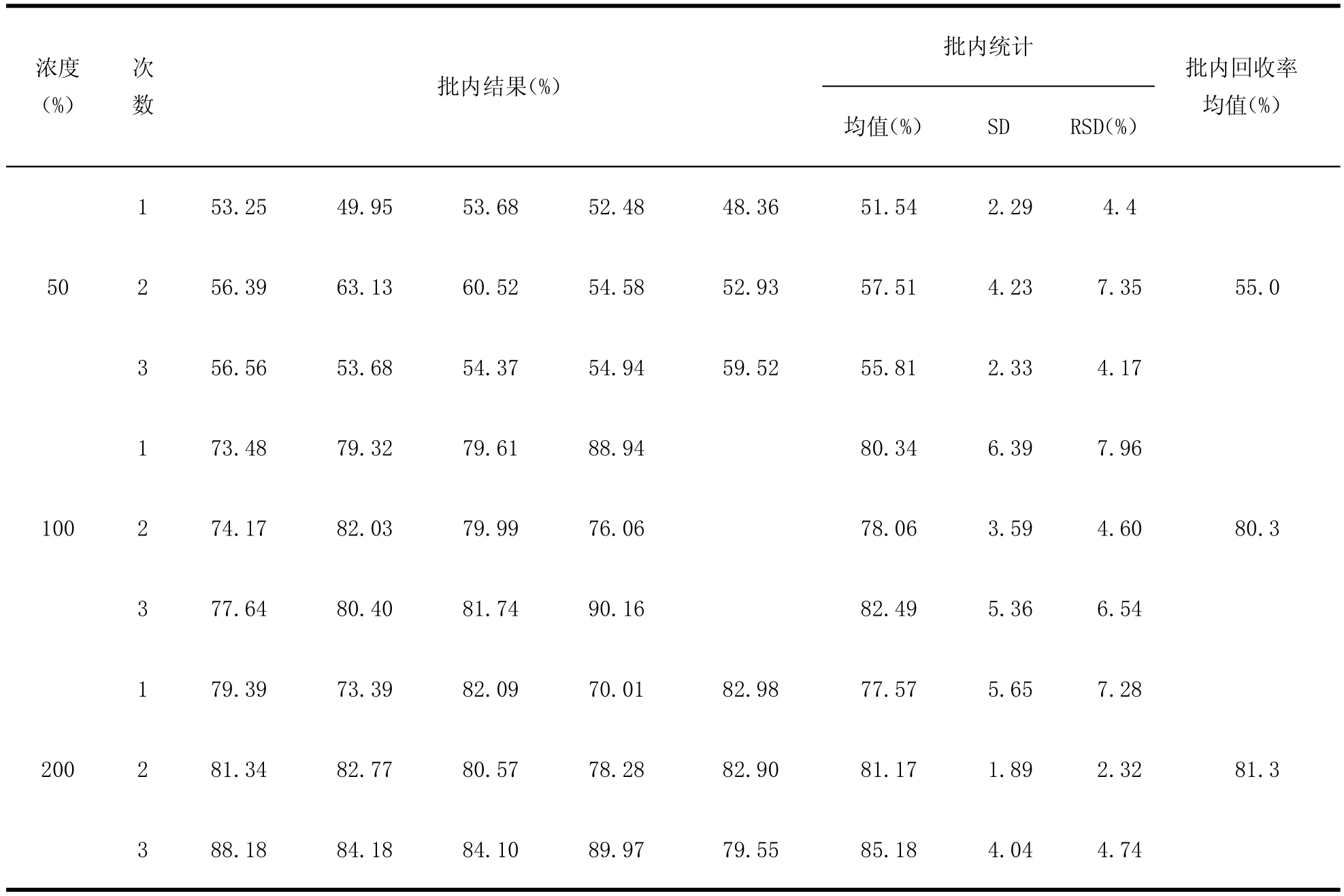
表2 回收率结果Table2 Recovery results
3 讨论
3.1样品的选取空白鸡肉组织的选取对试验的成功起重要的作用。如果鸡肉组织中含有磺胺类药物,那么试验得出的图谱就无法进行有效区分。故而在添加药物之前,必须确保鸡肉空白样品不含有任何磺胺类药物,以免影响试验结果。
3.2样品处理方法SAs属于碱性两性药物,主要呈弱酸性,等电点范围为pH 3~5,极性较高,一般采用极性溶剂提取和碱性溶液与溶剂反萃取净化的方法处理样品。曾用氯仿、二氯甲烷或乙酸乙酯做提取溶剂,0.1 mol/L氢氧化钠和溶剂反萃取净化,但大部分参试的SAs回收率低(低于60%),并且样品干扰和乳化严重。
3.3测定方法的选择食用畜产品中磺胺药物残留的分析检测方法有多种,包括滴定法[5]、气相色谱[6]、液相色谱、毛细管电泳[7]及生物分析方法[8]等,最常用的是液相色谱法,液相色谱常用的检测方法有紫外吸收[9]、荧光[10]、电化学检测[11]及质谱法[12]等方法。最终试验选择HPLC法。HPLC是SAs最常用、最方便的测定方法。采用C18柱分离和直接紫外法检测。试验表明,该方法同样适合肠衣、肝、肾中磺胺类药物残留量的测定,如改变色谱分离条件,该方法可推广应用到磺胺间氧哒嗪等其他磺胺类药物残留量的检测。
3.4流动相的选择根据SAs的理化性质,有机溶剂和pH都对SAs的保留有重要的影响。为便SAs获得有效保留和分离,并且防止固定相表面残余的硅醇基导致SAs色谱峰脱尾,一般采用酸性流动相(离子抑制)。8种磺胺类药物的出峰顺序和保留时间依次为:磺胺嘧啶钠、磺胺二甲基嘧啶、磺胺间甲氧嘧啶、磺胺氯达嗪钠、磺胺甲恶唑、磺胺氯吡嗪、磺胺二甲基嘧啶、磺胺喹恶啉。
3.5检测波长的选择利用二极管阵列检测器检测,得到8种成分的吸收光谱图,判断出各成分的最大吸收波长,为了兼顾8种成分的同时测定,选择紫外检测法进行检测,检测波长为270 nm,利用保留时间进行定性。
4 结论
4.1本试验建立了鸡肉组织中磺胺氯达嗪钠的提取、净化方法。
4.2本试验建立了鸡肉组织中磺胺氯达嗪钠的HPLC法色谱条件;色谱柱为C18柱(250㎜×4.6㎜ i. d)、流动相为乙腈-磷酸(0.017 mol/L)(20+80)、流速为1.0 mL/min、检测波长270 nm、进样量20μL,保留时间为14.653~15.128 min。
4.3本试验建立的鸡肉组织中磺胺氯达嗪钠的HPLC检测法最低检测限为0.005 mg/kg,定量限低于0.01 mg/kg,变异系数为2.32%~7.96%。此法适用于磺胺类药物的残留检测,并为磺胺类药物残留检测的进一步研究奠定了基础。
[1]王向勇,张磊,李敬光.持久性有机污染物膳食摄入的研究进展[J].食品安全质量检测学报,2014,5(2):438-444.
[2]吴景,刑书霞,曹进.食品中维生素检测技术进展[J].食品安全质量检测学报,2015,6(8):2882-2889.
[3]李晓雯,迟秋池,夏苏捷,等.高效液相色谱-四极杆-飞行时间质谱法检测猪肉中22种磺胺类兽药残留[J].食品安全质量检测学报,2015,6(5):1736-1742.
[4]段语晖,卫引茂.基于新型硼酸固相萃取柱的多巴胺色谱分析方法[J].分析化学研究报告,2013,41(3):406-411.
[5]李润丰,赵希艳,高亚弟.2,6-二氯靛酚反滴定法测定红色早疏中红色还原型VC[J].营养学报,2012,34(5):507-509.
[6]王建玲,候学会,王国庆.气相色谱-质谱联用法在食品安全分析中的应用[J].食品研究与开发,2013,34(8):110-114.
[7]董亚蕾,陈晓佼,胡敬,等.高效毛细管电泳在食品安全检测中的应用的进展[J].色谱,2012,30(11):1117-1126.
[8]刘斌,张印兵,岑小波.生物分析方法验证在药物非临床评价中的应用[J].中国药理学与毒理学杂志,2013,27(3):480-485.
[9]韦日伟,王昆,吴先富,等.药物中有关物质检测方法的研究进展及应用[J].中国药师,2015,18(5):851-855.
[10]于长泳.IBV荧光定量PCR检测方法的建立及对感染鸡体内病毒的检测[J].现代畜牧兽医,2014,12:1-6.
[11]兰小淞,吕延成.碳纳米管技术在食品安全检测中的应用进展[J].食品科学,2014,35(21):344-349.
[12]刘凯,王丽那,李建忠.饲料和鸡肉中利巴韦林的测定——超高效液相色谱—串联质谱法[J].现代畜牧兽医,2014,5:15-19.
Detection of Sulfachloropyridazine sodium in Chicken tissues w ith established HPLC
Wang Xiaozhu
(Liaoning Institute of safety supervision for animal products,LiaoningShenyang110003)
In this experiment,with the residual comparison of 7 kinds of sul fa drugs:sul fadiazine,sul famethazine,sul famonomethoxine,sul famethoxazole,sul fadimethoxine,sul faquinoxaline, sul faclozines with sul fachloropyridazine sodium,we establ ished a new HPLC method to detect the residual of Sul fachloropyridazine sodium in chicken tissues.This method could have a signi f icant impor tance in the detection of Sul fachloropyridazine sodium residual and protection of human heal th.
Sul fachloropyridazine sodium;Chicken tissues;HPLC;Detection
O657.1
B
1672-9692(2016)02-0010-05
2015-12-23
王小柱(1983-),男,辽宁辽阳人,硕士研究生,中级畜牧师,主要从事饲料、兽药、畜产品安全监督执法工作。

