HbA1c在不同检测系统及不同储存条件下结果的比较
采 云
(武警北京总队医院检验科,北京100027)
·方法研究·
HbA1c在不同检测系统及不同储存条件下结果的比较
采 云
(武警北京总队医院检验科,北京100027)
目的 探讨全血标本在不同温度、存放时间及不同检测系统下检测糖化血红蛋白(HbAlc)结果和稳定性差异。方法 对采集的30例来自我院内科门诊体检人群全血标本采用乙二胺四乙酸二钾(EDTA-K2)抗凝后分装于A、B、C、D、E五组试管中,A组立即检测、B组在4~8℃下冷藏1d后检测、C组在4~8℃下冷藏10d后检测、D组在-20℃下冷藏1d后检测、E组在-20℃下冷藏10d后检测,检测系统分别为:Bio-Rad variant II Turbo HbAlc检测仪、Primus Ultra2HbAlc检测仪、Roche Modular PPI全自动生化检测仪。结果 在同一种种检测系统下,A组立即检测结果与B组全血样本在4~8℃下冷藏1d后检测结果比较差异不具有统计学意义(P<0.05)。在同一种检测系统下,C组样本在4~8℃下冷藏10d后检测、D组样本在-20℃下冷藏1d后检测、E组样本在-20℃下冷藏10d后检测结果与A组检测结果差异均具有统计学意义(P<0.05)。在同一种种检测系统下,随着存放时间、存放温度的变化(B、C、D、E组),检测结果的CV值均高于A组。在同一温度下、存放时间条件下,Roche Modular PPI检测系统的检测结果的CV值最小。结论 温度和放置时间会对全血标本糖化血红蛋白(HbAlc)结果和稳定性造成影响,Roche Modular PPI检测系统的检测结果的稳定性相对较好。
全血标本; 不同温度; 存放时间; 检测系统; 糖化血红蛋白
现如今,糖尿病的发病率日益升高,已成为危害人类健康的一大顽疾[1]。在临床中,常规评价糖尿病诊疗和并发症控制效果的标准为糖化血红蛋白A1c(glycosylated hemoglobin A1c,HbA1c),通过降低其血清内浓度可显著减少糖尿病患者出现大血管和微血管类疾病的概率[2],且其表达水平的变化和患者预后具有密切相关性,因此寻找特异性高的HbA1c检测方法对提高糖尿病诊断及评价治疗效果的准确率具有极其重要的意义[3]。目前,在我国医院中,尚无有统一检测HbA1c标准及方法,且检测方法纷繁复杂,错误率较高[4],同时温度、存放时间及检测系统均可致HbA1c检测结果出现差异,本研究通过利用不同检测系统测定不同温度及存放时间下HbAlc,以分析各检测结果和稳定性差异,探讨标准化HbA1c检测方法的可能性。
材料与方法
1 全血样本采集
选取2016年2月期间来我院内科体检人群30例。其中男性18例,女性12例;年龄为19~42岁,平均年龄为31.7±12.6岁。患者于清晨空腹及餐后2h各取5份4mL静脉血样本,注入乙二胺四乙酸二钾(EDTA-K2)抗凝试管中。
2 检测系统
Bio-Rad variantII Turbo HbAlc检测仪,配套试剂批号:AA00618NU,400次测试后换防护柱,2000次测试后换分析柱,且更换柱子后应做活化定标。Primus Ultra2HbAlc检测仪及配套试剂、分析柱。校准品及质控品购自Bio-Rad公司,需按照系统说明书反转更换柱子,并定期清洗试剂酶样品。Roche Modular PPI全自动生化检测仪及配套测定试剂、校准品及质控品均购自Roche公司。三种检测系统均采用标准样品进行校对后应用,检测结果的一致性达到98%。
3 实验操作方法
使用Bio-Rad variantⅡTurbo糖化血红蛋白检测仪以阳离子交换高效液相色谱法(HPLC)、使用Primus Ultra2HbAlc检测仪以亲和层析HPLC法及使用Roche Modular PPI全自动生化检测仪以免疫抑制比浊法测定5组全血样本内HbAlc。其中A组样本制备后即检测,B组4~8℃冷藏1d后检测,C在4~8℃冷藏10d后检测,D组-20℃冷藏1d后检测,E组-20℃冷藏10d后检测。
4 质控标准
根据美国糖化血红蛋白标准化计划(National Glycohemoglobin Standardization Program,NGSP)储存校准品及质控品的稳定性标准,进行全血样本的稳定性评价。NGSP规定:HbA1c测定结果以-70℃或更低温度±3s为可接受范围,在±3s范围内结果稳定,否则为不稳定。
5 统计学方法
数据分析及统计在专业软件SAS9.0软件包中处理,HbAlc检测结果采用均数±标准差(±s)表示;多间比较采用单因素方差分析,组间两两比较采用LSD-t检验;检测结果稳定性采用变异系数(CV)值表示[5],CV=s/x。P<0.05表示两组指标差异具有统计学意义。
结 果
1 在不同温度下、不同存放时间及不同检测系统下检测结果的差异性分析
三种检测系统下,A、B、C、D、E五组标本检测出的HbAlc结果进行比较差异均具有统计学意义(P<0.05),见表1。
在同一种检测系统下,A组立即检测结果与B组全血样本在4~8℃下冷藏1d后检测结果比较差异不具有统计学意义(P<0.05),见表1。
在同一种检测系统下,C组样本在4~8℃下冷藏10d后检测、D组样本在-20℃下冷藏1d后检测、E组样本在-20℃下冷藏10d后检测结果与A组检测结果差异均具有统计学意义(P<0.05)。见表1。
表1 不同温度下、不同存放时间及不同检测系统下检测结果的差异性分析(±s)

表1 不同温度下、不同存放时间及不同检测系统下检测结果的差异性分析(±s)
注:与Bio-Rad variant II Turbo系统结果比较,*P<0.05;与Primus Ultra2系统结果比较,#P<0.05;与同一检测系统下A组结果比较,▲P<0.05
检测系统A组B组C组D组E组Bio-Rad variant II Turbo5.22±0.155.27±0.185.38±0.21▲5.44±0.25▲5.48±0.26▲Primus Ultra25.32±0.14*5.38±0.16*5.49±0.20*▲5.57±0.23*▲5.60±0.25*▲Roche Modular PPI5.47±0.14*#5.49±0.15*#5.59±0.22*#▲5.68±0.23*#▲5.72±0.23*#▲F值7.0937.4847.8307.7427.096 P值0.0260.0220.0180.0200.025
2 在不同温度下、不同存放时间下不同检测系统下检测结果的稳定性比较
三种检测系统下,A、B、C、D、E五组标本检测出的HbAlc结果的变异系数(CV)见表2、图1。
在同一种种检测系统下,随着存放时间、存放温度的变化(B、C、D、E组),检测结果的CV值均高于A组,见表2。
在同一温度下、存放时间条件下,Roche Modular PPI检测系统的检测结果的CV值均小于Bio-Rad variant II Turbo系统、Primus Ultra2,Primus Ultra2检测结果的CV值均小于Bio-Rad variant II Turbo系统。见表2。
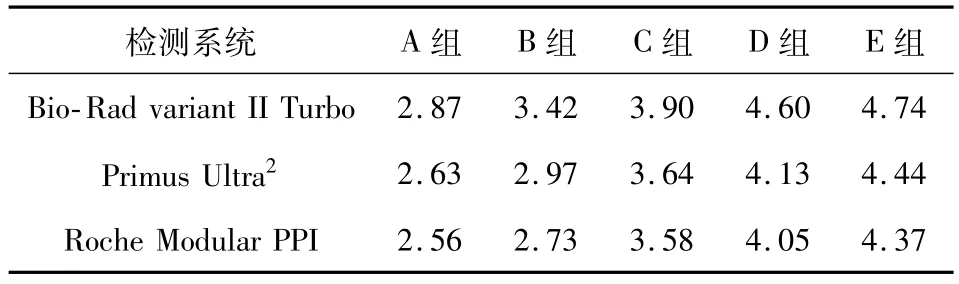
表2 在不同温度下、不同存放时间下不同检测系统下检测结果的稳定性比较(%)
讨 论
临床研究显示[6],糖化血红蛋白水平能够反映人体3个月内血糖状态,而且不会受到短期血糖浓度波动影响,因此HbA1c检测已成为一些国家诊断及评价糖尿患者病情状况或发展的“金标准”。然而在我国,HbA1c的检测方法众多,且结果差异性较大,故其仍未被广大医疗结构接纳为诊断糖尿病标准[7],仅作为一项辅助检查指标。随着我国医学检测标准化进程的不断推进,关于HbA1c检测的统一化标准也在逐步制定中,且呈现检测方法及各项指标逐一清晰化、制度化的态势,我们认为其必将在不久以后成为我国诊断糖尿病的通行标准之一。
研究显示,要想树立HbA1c检测的科学标准,首先要保证检测结果的准确性,这就需要对其实验步骤和检测系统的稳定性进行充分的掌握和把控[8]。在检测系统中,我们分别选取Bio-Rad variant II Turbo HbAlc检测仪+HPLC法、Primus Ultra2HbAlc检测仪+亲和层析HPLC法和Roche Modular PPI全自动生化检测仪+免疫抑制比浊法等三个常规系统联合三种实验方法进行HbA1c检测。研究显示,抽取的全血标本的质量和实验检验结果准确性和可靠性具有密切关系[9],因此在对患者抽血后,应将血液样本及时进行抗凝处理后冷藏,并应尽早检测以保证样本的质量符合检测要求。目前,由于医疗纠纷的概率较高,多数医疗机构为避免日后因检测结果错误而引发医患纠纷,都会保存每日的检测标本以待复查[10]。在研究中,我们分别选取立即检测、4~8℃下冷藏1d后检测、4~8℃下冷藏10d后检测、-20℃下冷藏1d后检测和-20℃下冷藏10d后检测五种检测时间及冷存温度组合对全血标本进行监测,以探讨不同保存时间及保存条件与HbA1c检验结果间的关系。
在本研究中,在三种检测系统下,A、B、C、D、E五组标本检测出的HbAlc结果的比较差异均具有统计学意义(P<0.05),在同一种种检测系统下,A组立即检测结果与B组全血样本在4~8℃下冷藏1d后检测结果比较差异不明显,且C组样本在4~8℃下冷藏10d后检测、D组样本在-20℃下冷藏1d后检测、E组样本在-20℃下冷藏10d后检测结果显著高于A组检测结果(P<0.05)。结果显示,在同等实验方法和检测系统下,抽取患者全血样本抗凝后立即检测c和待1d后检测HbA1c的结果具有可比性,前提是将样本进行合理的冷存。有研究建议应在获取血样应先立即检测HbAlc,但在实际条件下,由于部分医院患者人数较多或实验环境制约,较难充分实现全部实验当天抽血即可完成检测[11],因此我们认为也可将4~8℃下冷藏1d血样的HbA1c检测结果作为选择。在研究中,在同一种种检测系统下,随着存放时间、存放温度的变化,B~E组的检测结果的CV值均高于A组,且CV值呈现随着冷存时间和冷存温度升高而逐渐增大的趋势,检测结果稳定性和冷存时间及冷存温度可能存在负相关性。同时,在研究中,我们发现在同一温度下、存放时间条件下Roche Modular PPI系统的检测结果的CV值最小,其次为 Primus Ultra2系统,Bio-Rad variant II Turbo系统最高。结果显示Roche Modular PPI系统检测稳定性最高,且在-20℃下冷藏10d条件下,其
CV值仅为4.37%。该系统高稳定性也可能和免疫抑制比浊法,该方法根据血红蛋白分子结构设计,可针对HbA1c与血液内血红蛋白单抗间的凝集反应特性进行定性检测[12],稳定性较高,研究已证明,其灵敏度可精确到μL数量级,应作为HbA1c检测首选检测方法。
本研究中评价了三种不同方法、不同仪器、不同浓度样本和不同存放条件对检测结果的干扰,结果确实存在差异。Bio-Rad variant II Turbo测定样本常温可稳定7d,4℃可稳定
14d,-30℃可稳定35d;而亲和层析HPLC不受温度、氨基甲酰糖化血红蛋白和胎儿血红蛋白的干扰,结果可靠。免疫抑制比浊法是依据血红蛋白上糖化基团的结构特点而设计,原理是根据HbA 1c与相应的单抗结合发生凝集反应的特性,受干扰因素也较小。
综上所述,我们认为全血样本的冷存温度和放置时间与HbAlc检测结果和稳定性具有密切关系,研究显示应选取Roche Modular PPI系统作为检测系统首选。
[1]温冬梅,张秀明,张德才,等.Hb E变异体对5种糖化血红蛋白检测系统测定结果的干扰评价.中华检验医学杂志,2014,37(12):921-927.
[2]徐安平,夏勇,纪玲.血红蛋白变异体对不同糖化血红蛋白检测系统的干扰.中华检验医学杂志,2014,37(12):890-892.
[3]曾洁,张传宝,赵海建,等.应用六西格玛管理方法评估糖化血红蛋白检测系统性能.现代检验医学杂志,2014,29(4):17-20.
[4]索明环,温冬梅,张秀明.HbA1 c在三种检测系统及不同储存条件下结果的稳定性.检验医学,2014(8):813-816.
[5]赵芳,张芳,邱玲,等.酶法测定糖化白蛋白的方法性能验证及其初步临床应用.中华检验医学杂志,2013,36(4):343-347.
[6]沈默宇,石立,叶新华.影响糖化血红蛋白检测系统的因素.医学研究生学报,2013,26(9):1004-1006.
[7]俞叶夫,包国祥,赵国民,等.赋值传递与方法学比对对提高糖化血红蛋白可比性的观察.中国糖尿病杂志,2013,21(3):264-266.
[8]He H,Lv R,Li S,et al.Reference intervals and factors contributing to serum glycated albumin levels in West China.Clin lab,2014,60(1):119-124.
[9]刘慧,王蓓.3种检测系统测定糖化血红蛋白测量不确定度的评估.现代医学,2012,40(5):520-523.
[10]童华诚,刘慧,张美,等.三种检测系统测定糖化血红蛋白相关性分析及偏倚评估.中国实验诊断学,2011,15(7):1156-1158.
[11]Ayyagari R,Wei W,Cheng D,et al.Effect of Adherence and Insulin Delivery System on Clinical and Economic Outcomes among Patients with Type 2 Diabetes Initiating Insulin Treatment.Value Health,2015,18(2):198-205.
[12]向阳,姜艳,张琼.2种糖化血红蛋白检测方法的比对和结果一致性评价.新疆医科大学学报,2013,36(7):979-980.
(李 凌编辑)
Comparison of the Results of HbA1c by Different Detection Systems and Under Different Storage Conditions
CAI Yun
(Department of Clinical Laboratory,The Hospital of Wujing Beijing Command,Beijing 100027,China)
Objective To investigate the test results and the stability of glycosylated hemoglobin(HbAlc)in whole blood samples under different temperature,storage time and by different detection systems.Methods We collected 30 cases of whole blood samples with ethylene diamine tetraacetic acid dipotassium(EDTAK2)anticoagulant packaging.The samples were divided into A,B,C,D,E groups,five samples in each group.Group A was given immediate detection.Group B was refrigerated under 4-8℃ for one day before detection.Group C was stored under 4-8℃ for 10 days.Group D was stored at-20℃ freezer for one day and group E in-20℃ freezer for 10 days before detection.We used the following detection systems:Bio-Rad variant II turbo HbAlc detector,Primus ultra2 HbAlc detector and Roche modular PPI full automatic biochemical analyzer.Results Under the same detection system,the results of group A and group B had no statistical difference(P<0.05).Under the same detection system,the results of group C,group D and group E were significantly different than that of group A(P<0.05).Under the same detection system,the CV values of groups B,C,D,and E were higher than those of group A.At the same temperature and storage time,the Roche Modular PPI detection system had the minimum of the CV value.Conclusion Temperature and time will have an effect on the stability of HbAlc,Roche Modular PPI system provides relatively reliable testing results.
Whole blood sample; Different temperature; Storage time; Testing system;Glycosylated hemoglobin
10.11748/bjmy.issn.1006-1703.2016.11.030
2016-02-23;
2016-10-14

