培门冬酶治疗结外NK/T细胞淋巴瘤的效果与安全性分析
任小晶
(安阳市人民医院 血液肿瘤科 河南 安阳 455000)
培门冬酶治疗结外NK/T细胞淋巴瘤的效果与安全性分析
任小晶
(安阳市人民医院 血液肿瘤科 河南 安阳 455000)
目的 探讨培门冬酶治疗结外NK/T细胞淋巴瘤(ENKTL)的效果与安全性。方法 选择2010年1月至2016年1月安阳市人民医院收治的ENKTL患者60例作为研究对象,将其随机分为对照组与研究组,各30例。对照组应用吉他西滨、奥沙利铂、地塞米松与左旋门冬酰胺酶治疗,研究组应用吉他西滨、奥沙利铂、地塞米松与培门冬酶治疗。比较两组近期疗效及不良反应。结果 两组患者近期疗效比较,差异无统计学意义(P>0.05)。研究组消化道反应、过敏反应发生率低于对照组,差异具有统计学意义(P<0.05);两组血小板计数降低、细胞计数降低及高血糖的发生率比较,差异无统计学意义(P>0.05)。结论 培门冬酶治疗ENKTL具有显著的近期疗效,可以有效缓解疾病进展,降低消化道与过敏反应的发生率,安全性高,适于临床应用。
培门冬酶;结外NK/T细胞淋巴瘤;安全性
结外NK/T细胞淋巴瘤(ENKTL)是非霍奇金淋巴瘤中十分少见的一种类型,具有进展快、侵袭性高、预后差等特点。多项研究发现,该病对常规药物治疗收效甚微,主要与ENKTL具有多药耐药基因有关,使得多药耐药蛋白水平升高[1-2]。然而,左旋门冬酰胺酶类药物不受多药耐药蛋白的影响。培门冬酶属于门冬酰胺酶制剂,现已广泛应用于淋巴细胞白血病的治疗中,且疗效较佳,无明显的毒副作用。目前,临床对于培门冬酶治疗ENKTL的报道较少。本研究旨在观察ENKTL患者应用培门冬酶治疗的临床效果。
1 资料与方法
1.1 一般资料 选择2010年1月至2016年1月安阳市人民医院收治的ENKTL患者60例作为研究对象。入组标准:所有患者均经免疫组化分型与病理形态学确诊为ENKTL;无化疗禁忌证;体力ECOG评估分值在2分以下;患者及其家属对本次研究内容知情,已签署同意书。排除标准:合并严重脏器功能不全;肿瘤侵犯脑部。将其随机分为对照组与研究组,各30例。对照组男16例,女14例;年龄24~67岁,平均(56.7±8.5)岁;病程10~48 d,平均(28.4±5.4)d。研究组男17例,女13例;年龄24~68岁,平均(56.8±8.3)岁;病程12~47 d,平均(27.5±5.9)d。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法 ①对照组第1、8天静脉滴注1 000 mg/m2吉他西滨;第1天静脉滴注130 mg/m2奥沙利铂;第1~7天静脉滴注10 mg地塞米松;第1~7天静脉滴注5 000 U/m2左旋门冬酰胺酶(由协和发酵麒麟制药有限公司提供,国药准字J20100137)。②研究组第1、8天静脉滴注1 000 mg/m2吉他西滨;第1天静脉滴注130 mg/m2奥沙利铂;第1~7天静脉滴注10 mg地塞米松;第1天静脉滴注培门冬酶(由江苏恒瑞医药股份有限公司提供,国药准字H20090015)。1个周期为3周,通常情况下患者需要接受2~3个周期的治疗。两组在此基础上均实施放疗,放疗后继续实施药物治疗方案,共6个周期。
1.3 观察指标 ①参照世界卫生组织制定的实体瘤评判标准[3]对比两组患者的近期疗效。CR:病灶生物学与影像学异常消失,且未见新发病灶;PR:病变缩小在50%以上,且未见新发病灶;SD:病灶缩小在50%以下或增大在25%以下或无明显变化;PD:病灶增大在25%及25%以上或最小病灶增加在50%或50%以上,发现新病灶。有效率=(CR+PR)/例数×100%。②观察两组患者治疗期间的不良反应。
1.4 统计学方法 采用SPSS 17.0统计学软件进行数据处理分析,定性资料的组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效 两组患者近期疗效比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患者近期疗效对比(n,%)
2.2 不良反应 研究组消化道反应、过敏反应发生率低于对照组,差异具有统计学意义(P<0.05);两组血小板计数降低、细胞计数降低及高血糖的发生率比较,差异无统计学意义(P>0.05)。见表2。
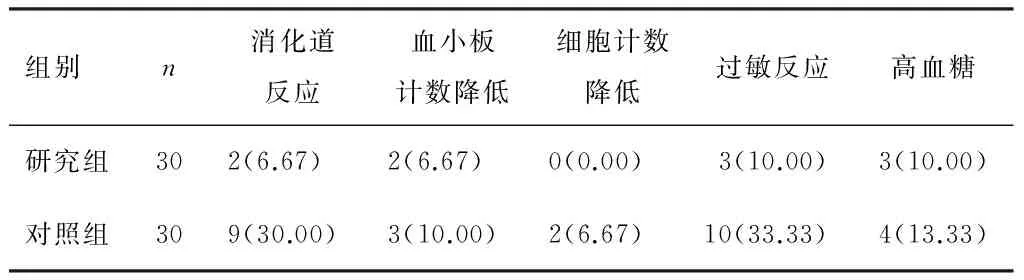
表2 两组患者治疗期间的不良反应比较[n(%)]
3 讨论
ENKTL属于非霍奇金淋巴瘤的一种特殊类型,约占7%左右,具有恶性程度高、预后差、进展快速等特点[4]。有研究报道显示,早期患者放化疗综合治疗或放疗的5年生存率为30%~40%,由于缺少对该病发生原因、发生机制的相关认知,所以仍未有标准、统一的治疗方案[5]。目前,针对化疗不敏感与早期病灶局限的患者主要采取放射治疗,近70%的患者可以有效缓解症状,然而此类方法的复发率却高达50%,且在治疗1 a内易出现全身远处转移或局部复发[6]。有学者认为,常规蒽环类化疗药物治疗ENKTL效果欠佳,5年生存率仅为7%~25%[7]。ENKTL对化疗药物不敏感可能与血管损伤所致的药物分布不佳、多药耐药基因有关[8]。所以,采用不受多药耐药基因影响的抗肿瘤药物是改善ENKTL治疗效果与预后的关键。
左旋门冬酰胺是用于降解门冬酰胺的细菌酶类,在淋巴细胞白血病中已发挥出了显著的治疗作用。目前,左旋门冬酰胺化疗方案已在临床应用了30 a,可以有效提高患者的疗效与生存期。然而,由于左旋门冬酰胺酶类化疗方案不良反应发生率较高,使其临床应用范围受到了一定的限制[9]。
培门冬酶是由聚乙二醇、左旋门冬酰胺酶及磷脂双分子层聚集而成,其中聚乙二醇能够通过包裹使机体免疫功能免受攻击,降低过敏风险;磷脂双分子层具有显著的稳定性,保护酶类免受水解,继而延长半衰期[10]。本文研究结果显示,两组患者近期疗效比较,差异无统计学意义(P>0.05)。可见左旋门冬酰胺酶与培门冬酶对于ENKTL均有显著的治疗效果。研究组消化道反应、过敏反应发生率低于对照组,差异具有统计学意义(P<0.05)。提示培门冬酶治疗ENKTL的安全性更佳,对消化道与过敏反应的毒性更低,这与部分研究结果相符[11-12]。需要注意的是,临床为了保证患者的治疗安全,给药治疗前应提前备好急救药品,预防过敏性反应,保证治疗质量。
总之,培门冬酶治疗ENKTL具有显著的近期疗效,可以有效缓解疾病进展,降低消化道与过敏反应的发生概率,安全性高,适于临床应用。
[1] 赵涵,胡晓晔,邹青峰.早期鼻自然杀伤细胞/T细胞淋巴瘤治疗进展[J].中国全科医学,2014,20(8):964-968.
[2] 汪春秀,张智慧.结外NK/T细胞淋巴瘤L-GEMOX方案治疗的临床观察[J].现代肿瘤医学,2014,15(6):1434-1437.
[3] 徐小红,杨磊,谭清和,等.改良SMILE方案治疗结外NK/T细胞淋巴瘤初探[J].现代肿瘤医学,2014,22(6):1438-1440.
[4] 燕玮,何晓薇,杨威.培门冬酶治疗三例T细胞淋巴瘤病例报道并文献回顾[J].实用药物与临床,2014,17(9):1100-1103.
[5] 梁绍平,王华庆,张会来,等.培门冬酶联合GEMOX方案治疗初治鼻腔NK/T细胞淋巴瘤临床疗效观察[J].中国肿瘤临床,2014,34(19):1225-1228.
[6] 万纯黔.培门冬酰胺酶联合吉西他滨治疗结外NK/T细胞淋巴瘤的安全性和疗效观察[J].实用临床医药杂志,2015,15(11):19-22.
[7] 向永胜,徐晓东,王龙,等.培门冬酶联合放化疗治疗鼻型NK/T细胞淋巴瘤临床疗效观察[J].临床药物治疗杂志,2015,20(6):51-53.
[8] 马军,沈志祥,朱军,等.培门冬酶治疗急性淋巴细胞白血病和恶性淋巴瘤中国专家共识[J].中国肿瘤临床,2015,18(24):1149-1158.
[9] 刘隽,唐勇,程毅敏,等.培门冬酶联合地塞米松治疗老年进展期结外NK/T细胞淋巴瘤的临床研究[J].中国癌症杂志,2013,10(4):298-301.
[10]俞远东,喻雄杰,曹风军.AspaMetDex方案治疗早期鼻腔NK/T细胞淋巴瘤的临床研究[J].湖北医药学院学报,2016,25(2):134-137.
[11]彭志强,董涵之,双跃荣.含培门冬酶的化疗方案治疗淋巴瘤的安全性分析[J].江西医药,2016,14(6):507-510.
[12]聂波,曾云,李云涛,等.结外NK/T细胞淋巴瘤鼻型34例临床分析[J].昆明医科大学学报,2016,18(6):123-126.
R 733
10.3969/j.issn.1004-437X.2016.11.013
2016-05-14)

