CuFe2O4纳米粒子催化芳香酮的不对称硅氢化反应
朱洁莲, 夏晓峰, 梁敏婷, 刘 湘, 李和兴
(1. 江南大学化学与材料工程学院, 食品胶体与生物技术教育部重点实验室, 无锡 214122;2. 上海师范大学资源化学教育部重点实验室, 上海 200234)
CuFe2O4纳米粒子催化芳香酮的不对称硅氢化反应
朱洁莲1, 夏晓峰1, 梁敏婷1, 刘 湘1, 李和兴2
(1. 江南大学化学与材料工程学院, 食品胶体与生物技术教育部重点实验室, 无锡 214122;2. 上海师范大学资源化学教育部重点实验室, 上海 200234)
分别采用共沉淀法、 溶胶-凝胶法和溶剂热法制备得到CuFe2O4纳米粒子, 以(R)-联萘二苯基膦[(R)-BINAP]为手性配体、 聚甲基氢硅氧烷(PMHS)为硅氢化试剂, 将制得的CuFe2O4纳米粒子用于催化芳香酮的不对称硅氢化反应. 结果表明, 溶剂热法能制得分散性好、 粒径小且分布均匀的CuFe2O4纳米球, 其催化活性明显优于其它2种方法. 在添加剂t-BuOK和t-BuOH的共同作用下, CuFe2O4纳米粒子的催化活性得以明显改善, 最终得到一种高效的非均相催化体系CuFe2O4/t-BuOK/t-BuOH. 在室温和空气氛围下, 用于催化芳香酮的不对称硅氢化反应, 底物转化率和产物对映体过量值分别高达99%和92%. 研究证实底物芳环上取代基的电子效应和空间位阻明显影响不对称硅氢化反应的结果. CuFe2O4纳米催化剂在外加磁场的作用下能较易从反应体系中分离回收, 且催化剂经4次循环利用后仍具有较高的催化活性.
不对称硅氢化反应; 芳香酮; CuFe2O4纳米粒子; 聚甲基氢硅氧烷
芳香族手性醇是一类重要的有机合成中间体, 广泛应用于医药、 农药及添加剂等物质的合成[1~4]. 从反应效率、 原子经济性以及环境友好等方面综合考虑, 不对称硅氢化还原酮类化合物[5~8]是获取手性醇的有效方法之一, 它具有无需耐高压设备、 反应条件温和及操作简便等优势, 具有广泛的应用前景. 目前, 酮的不对称硅氢化反应主要采用过渡金属和手性配体所形成的手性配合物作为催化剂, 以均相催化反应进行[9~12]. 而均相催化剂经反应后难以回收, 容易引起金属流失, 增加成本以及环境污染等问题, 在一定程度上制约了其发展和应用. 发展非均相催化剂和实现催化剂的回收再利用是解决以上问题的方法之一. 纳米粒子具有高比表面积, 存在大量易于接近的活性位点, 且无毒性, 可回收利用, 是作为非均相催化剂的首选材料. 通过纳米粒子与手性配体的相互作用形成具有催化活性的非均相催化剂, 从而实现不对称催化合成各种手性化合物[13,14]. Lipshutz课题组[15,16]和Kantam课题组[17~19]在非均相催化不对称硅氢化反应的研究上做了很多工作. 然而, 与均相Cu(Ⅱ)催化的不对称硅氢化反应[11,20,21]相比, 非均相催化反应的效率还有待提高. 这可能是由于此类纳米催化剂在制备方法上的缺陷所致. 共沉淀法[22]制备的纳米粒子分散性不好, 容易发生团聚, 造成催化活性位点的减少, 从而降低其催化活性. 吴静等[23,24]尝试利用介孔材料的负载技术以改善CuFe2O4纳米粒子的分散性, 但由于有机物质会堵塞介孔孔道, 使得催化剂循环催化的效果明显下降. 由此看来, CuFe2O4纳米粒子本身的制备方法是改善其催化效果的关键. 除了共沉淀法, 溶胶-凝胶法[25,26]和溶剂热法[27,28]也是制备铜铁氧体纳米粒子的常用方法. 这2种方法所制得的CuFe2O4纳米粒子在粒径分布、 颗粒分散性和尺寸控制上均优于共沉淀法, 理论上有望改善其催化效果. 事实上, 关于这2种方法制得的CuFe2O4纳米粒子催化不对称硅氢化反应的效果尚未被证实.
本文分别采用共沉淀法、 溶胶-凝胶法和溶剂热法制备CuFe2O4纳米粒子, 比较其对不对称硅氢化反应的催化活性, 并选取高催化活性的CuFe2O4纳米粒子用于非均相催化体系的研究, 考察添加剂和底物芳环上取代基等因素对不对称硅氢化反应的影响. 另外, 对CuFe2O4纳米催化剂进行回收和重复使用的研究. 结合可行的不对称反应机理阐明该催化反应的实质, 探讨各反应因素的影响.
1 实验部分
1.1 试剂与仪器
2′-氯苯乙酮和3′-氯苯乙酮购于上海璞光实业有限公司; 4′-氯苯乙酮、 4′-甲基苯乙酮、 4′-甲氧基苯乙酮和正十三烷购于Fluka公司; (R)-联萘二苯基膦[(R)-BINAP]、 聚甲基氢硅氧烷(PMHS)和t-BuOK购于上海晶纯试剂有限公司; 苯乙酮和4′-硝基苯乙酮等均购于国药集团化学试剂公司. 气相色谱检测采用装有Varian公司CP-Chirasil-Dex手性毛细管色谱柱的FMLI 9790型气相色谱仪(浙江温岭市福立分析仪器有限公司); 比旋光度测定采用WZZ-2A型数字自动旋光仪(上海物理光学仪器厂).
1.2 CuFe2O4纳米粒子的制备
1.2.1 共沉淀法制备CuFe2O4纳米粒子 参考文献[17]方法, 按Cu(Ⅱ)和Fe(Ⅱ)摩尔比1∶2分别称取CuCl2·2H2O和FeCl3·6H2O, 将其溶解于去离子水中, 配制成0.1 mol/L Cu2+和0.2 mol/L Fe2+的均匀混合溶液. 在机械搅拌下, 用恒压滴液漏斗缓慢滴加0.1 mol/L NaOH水溶液, 直至反应体系pH值为9~10, 停止滴加. 反应结束后, 继续搅拌30 min. 通过抽滤, 分离出沉淀物, 并用去离子水多次洗涤, 然后置于80 ℃烘箱内干燥. 干燥后研磨, 再于700 ℃下焙烧2 h得到黑色粉末样品.
1.2.2 溶胶-凝胶法制备CuFe2O4纳米粒子 参考文献[25]方法, 称取5 mmol CuCl2·2H2O和10 mmol FeCl3·6H2O溶解于50 mL去离子水中, 混合均匀后, 将其置于80 ℃水浴中, 并在强烈搅拌下用滴液漏斗逐滴滴加100 mL浓度为0.3 mol/L的柠檬酸水溶液, 得到透明的溶胶, 继续保持加热搅拌至产生凝胶后停止. 将凝胶物质放置在130 ℃烘箱中干燥3 h, 经研碎后, 再将其置于700 ℃焙烧2 h, 即可得到产品.
1.2.3 溶剂热法制备CuFe2O4纳米粒子 参考文献[27]方法, 分别称取6 mmol CuCl2·2H2O, 12 mmol FeCl3·6H2O, 1.5 g NaOAc和1.5 g PVP置于圆底烧瓶中, 加入90 mL乙二醇后持续搅拌, 使其完全溶解且混合均匀, 得到红棕色透明油状溶液. 将混合液转移至容积为100 mL聚四氟乙烯内胆的不锈钢反应釜中, 于160 ℃烘箱中反应24 h. 反应结束后, 自然冷却至室温, 利用磁铁将黑色固体分离, 分别用去离子水和无水乙醇多次洗涤. 将固体置于70 ℃真空干燥12 h, 即可得到样品.
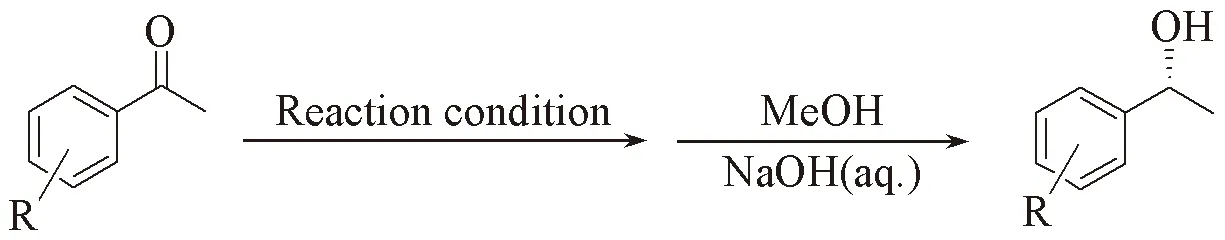
1.3 CuFe2O4纳米粒子催化芳香酮的不对称硅氢化反应及纳米催化剂的回收再利用
在25 mL圆底烧瓶中, 依次加入 10 mg CuFe2O4纳米粒子、 0.01 mmol 手性配体(R)-BINAP、 0.03 mmolt-BuOK和3 mL甲苯, 于25 ℃下搅拌1 h. 加入3 mmol PMHS后继续搅拌30 min. 再加入1 mmol底物芳香酮和3 mmolt-BuOH. 采用薄层色谱法监控反应的进程. 反应结束后, 利用磁铁将CuFe2O4纳米粒子固定在烧瓶底部, 待反应液变得澄清透明后将反应液倾倒于另一个干净的圆底烧瓶中, 纳米催化剂则放置一边待用. 在强烈搅拌下, 于反应液中加入1 mL甲醇和3 mL 2.5 mol/L的NaOH水溶液, 并持续搅拌3 h. 混合液分别用二氯甲烷萃取(5 mL×3), 收集油层, 并依次用15 mL饱和NaCl溶液和15 mL去离子水洗涤, 用无水硫酸钠干燥后减压浓缩, 采用快速柱层析法(展开剂为石油醚、 二氯甲烷和乙酸乙酯的混合液)分离提纯, 采用气相色谱仪测定底物芳香酮的转化率和反应所得手性醇的对映体过量(e.e.)值.
催化反应后回收得到的纳米催化剂分别用乙醇和去离子水洗涤3次, 真空干燥后, 通入氮气, 使催化剂在室温(25 ℃)下活化1 h, 回收所得催化剂无需进一步处理即可用于下一次催化反应.
2 结果与讨论
2.1 CuFe2O4纳米粒子的表征

Fig.1 SEM images of CuFe2O4 prepared by different methods(A) Coprecipitation method; (B) sol-gel method; (C) solvothermal method.
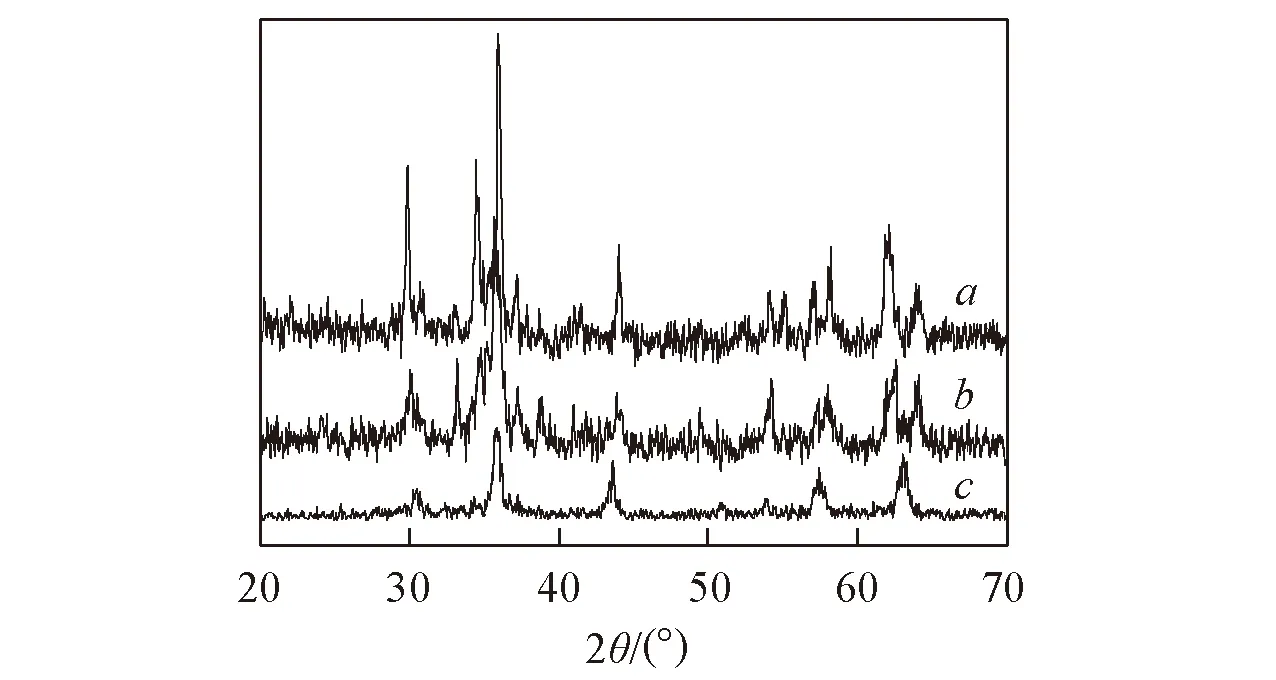
Fig.2 XRD patterns of CuFe2O4 prepared by sol-gel(a), coprecipitation(b) and solvothermal(c) methods
图1(A)~(C)分别为共沉淀法、 溶胶-凝胶法和溶剂热法制得的CuFe2O4的SEM照片. 从图1可见, 3种方法制备的样品形貌分别为球状与块状、 块状和球状. 从分散性来看, 共沉淀法和溶胶-凝胶法制备的样品分散都不均匀, 团聚现象严重, 而溶剂热法制备的样品分散均匀. 3种方法所制备样品的粒径尺寸分别为50~150, 200和100 nm. 共沉淀法和溶胶-凝胶法均需要高温焙烧处理, 在焙烧过程中, 小粒子由于自身的高表面容易产生聚结而形成大颗粒, 导致颗粒的分散性不好. 另外, 在溶胶-凝胶法中, 凝胶的特殊网状结构使得反应前驱体间相互紧密靠近, 因此相对于共沉淀法, 溶胶-凝胶法制得的CuFe2O4纳米粒子更趋向形成块状大颗粒. 溶剂热法不需要高温焙烧处理, 所制得的CuFe2O4呈球形, 无论是粒径分布均匀性还是分散性, 该样品都明显优于其它2种方法.
图2为溶胶-凝胶法、 共沉淀法和溶剂热法制得的CuFe2O4的XRD谱图. 对照立方晶系CuFe2O4的标准谱图(JCPDS No.25-0283), 本文制得的样品在2θ=29.8°, 35.9°, 43.9°, 57.1°和62.1°处明显出现了CuFe2O4的特征衍射峰, 其对应的晶面分别为(220), (311), (400), (511)和(440), 这表明所得样品主要为CuFe2O4.
2.2 比较3种CuFe2O4纳米粒子催化不对称硅氢化反应的活性
以苯乙酮为底物, 价廉无毒的PMHS为还原剂, 商品化(R)-BINAP为手性配体, 考察了3种方法制得的CuFe2O4纳米粒子催化不对称还原苯乙酮反应的催化活性, 结果见表1. 由表1可见, 由共沉淀法和溶胶-凝胶法制得的CuFe2O4纳米粒子的催化活性较差, 需要较长时间并提高反应温度才能使反应基本完全(表1 Entries 1~4). 该结果与纳米粒子的表征结果相对应. 由于其颗粒尺寸较大和粒子团聚严重, 大大减少了纳米粒子的比表面积及表面上的活性位点, 从而减弱了纳米催化剂的活性. 另外, 纳米粒子的形貌也影响其催化活性. 溶胶-凝胶法制得的CuFe2O4成块状的大颗粒, 不仅其比表面积少, 而且相对于球状粒子, 块状纳米粒子的活性位点更难以接近, 使得溶胶-凝胶法制得的CuFe2O4纳米催化剂的活性最差. 溶剂热法制得的CuFe2O4纳米催化剂(表1 Entry 5)具有很好的催化活性, 在25 ℃下仅需2 h即可完成反应, 转化率和e.e.值分别达99%和77%. 与文献[17]的结果相比, 催化效率有了较大提高, 这与溶剂热法制得的纳米粒子的高比表面积、 高分散性、 粒子均一性和球状小粒径等因素密切相关. 另外, 同一反应温度下, 3种方法制得的CuFe2O4纳米粒子催化的不对称硅氢化还原苯乙酮所获得产物的e.e.值基本相近. 因此, 在后续的实验中选用溶剂热法制备的CuFe2O4纳米粒子作为催化剂.

Table 1 Asymmetric hydrosilation of acetophenone catalyzed by CuFe2O4 nanoparticles via different methodsa
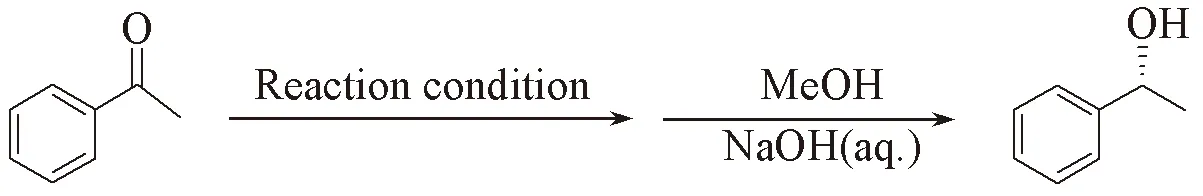
2.3 添加剂对酮的不对称硅氢化反应的影响
为进一步改善非均相催化剂CuFe2O4的催化活性, 考察了添加剂t-BuOK和t-BuOH对苯乙酮不对称硅氢化反应的影响, 结果见表2. 由表2可知, 在无添加剂的情况下, 反应2 h时底物的转化率能达到66%(表2 Entry 1). 当体系中添加了t-BuOK, 反应效率有明显上升, 苯乙酮的转化率提高至89%(表2 Entry 2), 同时添加t-BuOK和t-BuOH对该反应的促进作用更为明显, 2 h内反应的底物转化率就能达到99%, 且所得产物(R)-1-苯基乙醇的e.e.值能达到77%(表2 Entry 3). 这是由于t-BuOK有利于具有催化还原活性Cu—H的生成,t-BuOH有利于最后产物醇的生成. 然而, 当体系中只添加t-BuOH时, 转化率却下降至24%(表2 Entry 4), 单独t-BuOH反而不利于Cu—H的生成. 为了进一步说明CuFe2O4纳米催化剂的活性, 进行了一组对照实验(表2 Entry 5), 即只添加t-BuOK 和t-BuOH , 不添加CuFe2O4纳米催化剂, 结果发现, 经过10 h后反应基本未进行, 这说明添加剂单独用于该硅氢化反应不能起到催化作用, 真正起到催化作用的是CuFe2O4纳米催化剂.
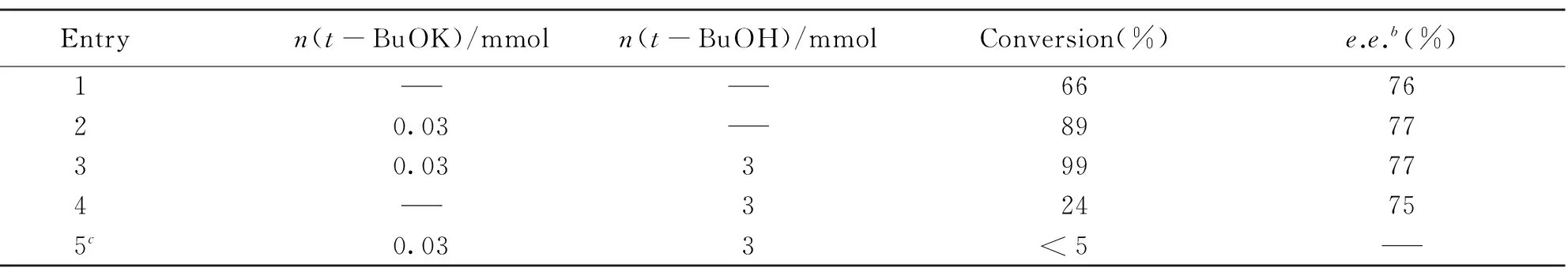
Table 2 Effects of additives on the asymmetric hydrosilation of acetophenonea
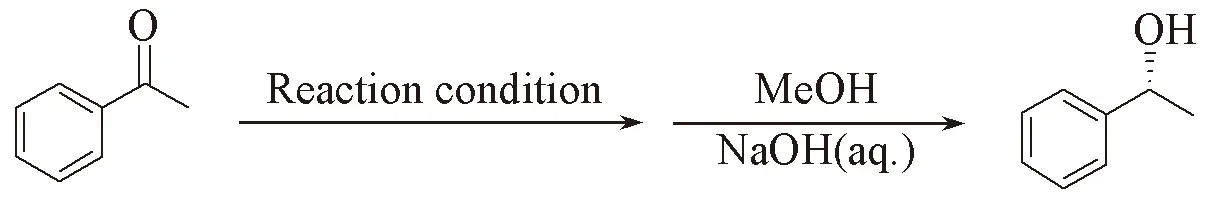
2.4 底物酮苯环上的取代基对不对称硅氢化反应的影响
根据文献[29~31]报道, 底物酮苯环上取代基的电子效应及空间位阻对不对称反应有较大影响. 本文考察了底物苯环上不同取代基对芳香酮不对称硅氢化转化率和产物手性醇e.e.值的影响, 结果见表3. 由表3可见, 在室温(25 ℃)和空气环境下, CuFe2O4纳米粒子能有效催化一系列芳香酮的不对称硅氢化反应. 底物酮苯环上的电子效应在反应中有重要影响. 底物酮苯环上的吸电子基团(除了2′-Cl—)有利于该非均相催化反应, 一方面吸电子基团有利于活性化合物Cu—H的进攻, 从而提高转化率, 另一方面吸电子基团还略有利于手性配体与底物的契合, 从而提高产物的e.e.值(表3 Entries 3~5), 最高的转化率和e.e.值分别为99%和92%. 而底物酮苯环上的供电子基团则会降低活性化合物Cu—H的进攻效率, 导致底物转化率降低, 同时其反应的对映选择性基本不受影响(表3 Entries 6~9). 当底物酮苯环上的取代基处于邻位时, 由于邻位取代基的空间阻碍, 不利于底物羰基与配体的契合, 其相应产物的e.e.值会明显下降(表3 Entry 2), 这与Shimizu等[32]所报道的结果恰恰相反. 表明在该不对称硅氢化反应中, 底物酮苯环上取代基的空间位阻抑制了对映选择性的提高.
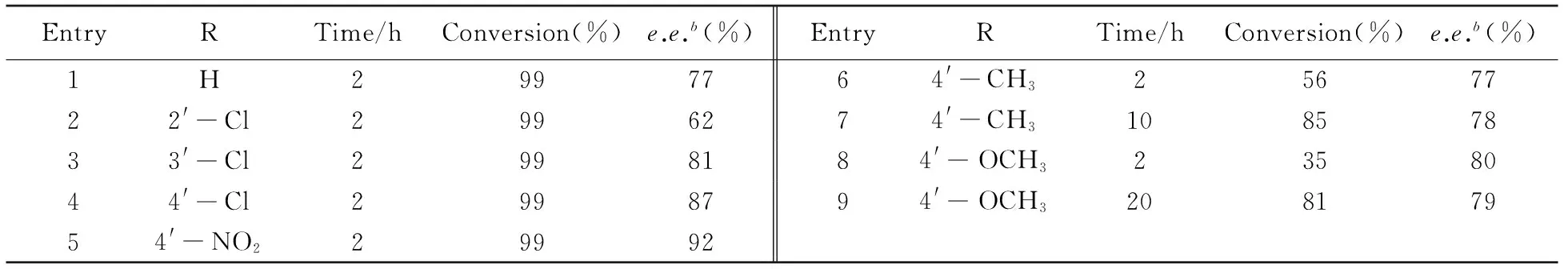
Table 3 Effects of substrates on the asymmetric hydrosilationa
2.5 CuFe2O4纳米催化剂的循环利用

Fig.3 Magnetic separation of CuFe2O4nanoparticles
发展非均相催化剂主要是为了实现催化剂的回收和循环利用, 本文对CuFe2O4纳米催化剂的分离, 回收以及重复使用进行了研究. 图3(a)给出了反应后CuFe2O4纳米粒子分散于反应液中的情况, 说明该纳米粒子能很好地分散于反应液中, 可与反应物充分接触, 有利于催化反应的进行. 而图3(b)是外加磁场分离CuFe2O4纳米粒子的情况. 说明该CuFe2O4纳米粒子具有很好的磁性, 在磁铁作用下纳米粒子基本聚集在外加磁场周围, 与反应液彻底分离, 使得反应液变得澄清透明. 鉴于CuFe2O4磁性纳米粒子具有易分离的特性, 可进一步对其回收和循环利用进行研究.
表4分别列出了4次循环利用后CuFe2O4纳米粒子催化苯乙酮不对称硅氢化还原的结果. 从表4可知, 第1次循环利用后的CuFe2O4纳米催化剂对苯乙酮的转化率没有影响, 仍能获得高达99%的底物转化率, 在第2~4次循环中, 不对称催化反应的底物转化率依次降低, 这可能是因为催化剂在回收过程中其活性部位减少, 或催化剂形貌发生了变化导致催化活性下降. 因此, 对回收利用后的CuFe2O4纳米粒子进行了SEM表征, 图4是第2次回收后的CuFe2O4纳米催化剂的SEM照片. 从图4可知, 回收和循环利用前后的CuFe2O4纳米催化剂在形貌和粒子尺寸方面并没有发生明显变化, 但回收后的CuFe2O4纳米粒子有少量局部团聚的现象, 导致其活性部位略有减少, 降低了催化活性, 导致转化率的缓慢下降. 而e.e.值主要与底物和配体有关, 所以并没有受到影响.
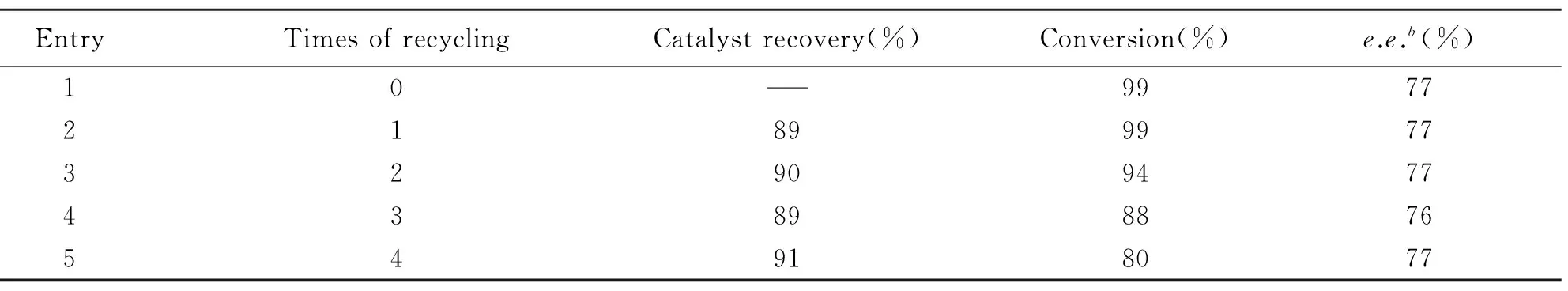
Table 4 Recycling of CuFe2O4 nanoparticles catalyst for the asymmetric hydrosilation of acetophenonea
a. Reaction conditions: 0.010 g CuFe2O4nanoparticles, 1%(molar fraction)(R)-BINAP, 3 mmol PMHS, 0.03 mmolt-BuOK, 3 mmolt-BuOH, 3 mL toluene, 2 h, 25 ℃, air;b. absolute configuration was determined to be (R).
2.6 CuFe2O4纳米粒子催化酮的不对称硅氢化反应的机理

Fig.5 Plausible mechanism of the asymmetric hydrosilation of aromatic ketones catalyzed by CuFe2O4 nanoparticles
图5给出了CuFe2O4纳米粒子催化不对称硅氢化还原芳香酮的可能反应机理. 在反应初期, CuFe2O4, (R)-BINAP和t-BuOK通过配位等作用生成一种手性配合物Ⅰ, 并继续与还原剂PMHS作用形成了具有催化还原活性的Cu—H化合物Ⅱ. 其中t-BuO—基团的亲核作用有利于Si—H键的断裂, 从而促进Cu—H化合物的生成. 这可能是整个非均相催化反应的决速步骤. 随着底物酮的加入, 物质Ⅱ的Cu—H键与酮羰基在一定的电子效应及空间位阻的作用下相互定位嵌合, 从而生成具有一定立体构型的Cu—O中间体Ⅲ, 这可能是决定整个不对称硅氢化反应的立体选择性的步骤. 在催化过程的后期, 体系中添加的t-BuOH能为物质Ⅲ提供质子, 使其质子化[33], 促进产物醇Ⅳ的生成, 并使配合物Ⅰ重新产生以进入下一轮的循环催化. 这就解释了为什么添加剂t-BuOK和t-BuOH的共同作用能有效改善该非均相催化体系的活性. 此外, 芳基上吸电子基团有利于羰基氧上电荷向碳上转移, 从而有利于Cu—H上氢的进攻, 最终有利于反应的进行, 从而提高转化率. 而苯环邻位取代基的空间阻碍, 不利于底物与配体的相互定位嵌合, 会导致e.e.值的下降.
综上所述, 本文将溶剂热法制得的CuFe2O4纳米催化剂用于催化芳香酮的不对称硅氢化反应, 在室温(25 ℃)和空气环境下该CuFe2O4纳米催化剂显示了良好的催化活性, 通过添加剂t-BuOK和t-BuOH的共同作用可使催化活性进一步提高, 且非均相催化体系CuFe2O4/t-BuOK/t-BuOH对底物芳香酮的适用范围具有一定的广泛性. 底物苯环上取代基的电子效应和空间位阻对芳香酮的不对称硅氢化反应的结果具有明显的影响. 此外, 磁性CuFe2O4纳米催化剂能有效实现回收和循环利用, 使得该非均相催化体系更具发展潜力.
[1] Denard C. A., Hartwig, J. F., Zhao H.,ACSCatalysis, 2013, 3(12), 2856—2864
[2] Liu X., Pan Z. G., Xu J. H.,Prog.Chem., 2011, 23(5), 87—96(刘湘, 潘争光, 许建和. 化学进展, 2011, 23(5), 87—96)
[3] Zhang X. C., Wu Y., Yu F., Wu F. F., Wu J., Chan A. S.,Chemistry, 2009, 15(24), 5888—5891
[4] Riant O., Mostefai N., Courmarcel J.,Synthesis-Stuttgart, 2004, 18(12), 2943—2958
[5] Perez M., Qu Z. W., Caputo C. B., Podgorny V., Hounjet L. J., Hansen A., Dobrovetsky R., Grimme S., Stephan D. W.,Chem.Eur.J., 2015, 21(17), 6491—6500
[6] Kawabata S., Tokura H., Chiyojima H., Okamoto M., Sakaguchi S.,Adv.Synth.Catal., 2012, 354(5), 807—812
[7] Moser R., Boskovic Z. V., Crowe C. S., Lipshutz B. H.,J.Am.Chem.Soc., 2010, 132(23), 7852—7853
[8] Yao J. S. Wu Y. S.,Chem.J.ChineseUniversities, 2002, 23(1), 68—70(姚金水, 吴佑实. 高等学校化学学报, 2002, 23(1), 68—70)
[9] Wu F. F., Zhou J. N., Fang Q., Hu Y. H., Li S., Zhang X. C., Chan A. S., Wu J.,Chem.AsianJ., 2012, 7(11), 2527—2530
[10] Liu L. J., Wang F. J., Shi M.,Organometallics, 2009, 28(15), 4416—4420
[11] Issenhuth J. T., Dagorne S., Bellemin-Laponnaz S.,Adv.Synth.Catal., 2006, 348(14), 1991—1994
[12] Sirol S., Courmarcel J., Mostefai N., Riant O.,Org.Lett., 2001, 3(5), 4111—4113
[13] Ji Y. G., Wu L., Fan Q. H.,ActaChim.Sinica, 2014, 72(7), 798—808(季益刚, 吴磊, 范青华. 化学学报, 2014, 72(7), 798—808)
[14] Ranganath K. V. S., Glorius F.,Catal.Sci.Technol., 2011, 1(1), 13—22
[15] Lee C. T., Lipshutz B. H.,Org.Lett., 2008, 10(19), 4187—4190
[16] Lipshutz B. H., Frieman B. A., Tomaso A. E. Jr.,Angew.Chem.Int.Ed., 2006, 45(8), 1259—1264
[17] Kantam M. L., Yadav J., Laha S., Srinivas P., Sreedhar B., Figueras F.,J.Org.Chem., 2009, 74(12), 4608—4611
[18] Kantam M. L., Laha S., Yadav J., Likhar P. R., Sreedhar B., Jha S., Bhargava S., Udayakiran M., Jagadeesh B.,Org.Lett., 2008, 10(19), 4391—4391
[19] Kantam M. L., Laha S., Yadav J., Likhar P. R., Sreedhar B., Choudary B. M.,Adv.Synth.Catal., 2007, 349(10), 1797—1802
[20] Issenhuth J. T., Dagorne S., Bellemin-Laponnaz S.,C.R.Chim., 2010, 13(3), 353—357
[21] Lee D. W., Yun J.,TetrahedronLett., 2004, 45(28), 5415—5417
[22] Pandya P. B., Joshi H. H., kulkarni R. G.,J.Mater.Sci.Lett., 1991, 10(8), 474—476
[23] Li M., Li B., Xia H. F., Ye D., Wu J., Shi Y.,GreenChemistry, 2014, 16(5), 2680—2688
[24] Li B., Li M., Yao C., Shi Y., Ye D., Wu J., Zhao D.,J.Mater.Chem.A, 2013, 1(23), 6742—6749
[25] Yang H., Yan J., Lu Z., Cheng X., Tang Y.,J.AlloysCompd., 2009, 476(1/2), 715—719
[26] Tao S. W., Gao F., Liu X. Q., Sφrensen O. T.,Mater.Sci.Eng.B, 2000, 77(2), 172—176
[27] Zhang W., Quan B., Lee C., Park S. K., Li X., Choi E., Diao G., Piao Y.,ACSAppl.Mater.Interfaces, 2015, 7(4), 2404—2414
[28] Yang L. X., Xu Y. B., Jin R. C., Wang F., Yin P., Li G. H., Xu C. P., Pan L. B.,Ceram.Int., 2015, 41(2, Part A), 2309—2317
[29] Qi S. B., Li M., Li S., Zhou J. N., Wu J. W., Yu F., Zhang X. C., Chan A. S., Wu J.,Org.Biomol.Chem., 2013, 11(6), 929—937
[30] Liu X., Zhang B. L., Xia Y. M., Xu J. H.,ActaChim.Sinica, 2009, 67(13), 1492—1496(刘湘, 张宝立, 夏咏梅, 许建和. 化学学报, 2009, 67(13), 1492—1496)
[31] Kantam M. L., Laha S., Yadav J., Likhar P. R., Sreedhar B., Jha S., Bhargava S., Udayakiran M., Jagadeesh B.,Org.Lett., 2008, 10(14), 2979—2982
[32] Shimizu H., Igarashi D., Kuriyama W., Yusa Y., Sayo N., Saito T.,Org.Lett., 2007, 9(9), 1655—1657
[33] Zhang X. C., Wu F. F., Li S., Zhou J. N., Wu J., Li N., Fang W., Lam K. H., Chan A. S. C.,Adv.Synth.Catal., 2011, 353(9), 1457—1462
(Ed.: V, Z)
Asymmetric Hydrosilation of Aromatic Ketones Catalyzed by CuFe2O4Nanoparticles†
ZHU Jielian1, XIA Xiaofeng1, LIANG Minting1, LIU Xiang1*, LI Hexing2
(1.KeyLaboratoryofFoodColloidsandBiotechnology,MinistryofEducation,SchoolofChemicalandMaterialEngineering,JiangnanUniversity,Wuxi214122,China; 2.KeyLaboratoryoftheChineseMinistryofEducationinResourceChemistry,ShanghaiNormalUniversity,Shanghai200234,China)
CuFe2O4nanoparticles were synthesized by coprecipitation, sol-gel and solvothermal methods, respectively. The asymmetric hydrosilation of aromatic ketones was catalyzed by CuFe2O4nanoparticles, employing (R)-BINAP[2,2′-bis(diphenylphosphino)-1,1′-binaphthalene] as chiral ligand and polymethylhydrosiloxane as hydrosilating reagent. The results showed that compared to the others, the CuFe2O4nanoparticles prepared by solvothermal method had spherical shape, small size, better dispersion, uniform distribution and excellent catalytic activities. Meanwhile, it was found that the catalytic activity of the CuFe2O4nanoparticles was significantly improved with the addition oft-BuOK andt-BuOH. An efficient heterogeneous catalytic system CuFe2O4/t-BuOK/t-BuOH was finally obtained. Under room temperature and air atmosphere, the conversion of the aromatic ketones and the enantiomeric excesses of the (R)-1-arylethanols were up to 99% and 92%, respectively, with the heterogeneous catalytic system. It was also confirmed that the electronic effect and steric hindrance of the groups on the aromatic ring distinctly affected the results of hydrosilation. And a possible mechanism was presented to explain the influence of some key factors on the reaction. Furthermore, it was demonstrated that the CuFe2O4nanocatalyst could be easily separated from reaction system under an external magnetic field. And after recycling for four times, the catalyst could also have a high catalytic activity for the asymmetric hydrosilation.
Asymmetric hydrosilation; Aromatic ketone; CeFe2O4nanoparticles; Polymethylhydrosiloxane
10.7503/cjcu20150650
2015-08-14.
日期: 2016-01-06.
国家自然科学基金(批准号: 21402066)资助.
O643.32; O621.3+4
A
联系人简介: 刘 湘, 男, 副教授, 主要从事催化不对称合成研究. E-mail: liuxiang@jiangnan.edu.cn
† Supported by the National Natural Science Foundation of China(No.21402066).

