具有超快吸附能力的(C,N)-TiO2光催化材料
何琴玉, 吴泽宏, 黄伟源, 陈晓媚, 魏玉蕊, 刘俊明, 杜 纯, 周江山, 李方舟
(1. 华南师范大学物理与电信工程学院, 广东省量子工程与量子材料重点实验室, 广州 510006;2. 华南师范大学华南先进电子研究院, 先进材料实验室, 广州 510006)
具有超快吸附能力的(C,N)-TiO2光催化材料
何琴玉1,2*, 吴泽宏1, 黄伟源1, 陈晓媚1, 魏玉蕊1, 刘俊明2, 杜 纯1, 周江山1, 李方舟1
(1. 华南师范大学物理与电信工程学院, 广东省量子工程与量子材料重点实验室, 广州 510006;2. 华南师范大学华南先进电子研究院, 先进材料实验室, 广州 510006)
采用“溶胶-凝胶与微波二步法”合成了碳、氮掺杂的锐钛矿(C,N)-TiO2光催化材料. 首先采用溶胶-凝胶方法制备了TiO2前驱物凝胶粉末,然后将其与盐酸胍混合微波制备(C,N)-TiO2纳米材料. 对该材料进行X射线衍射(XRD)、扫描电子显微镜(SEM)、紫外-可见漫反射光谱(UV-Vis DRS)等表征,并测试在甲基橙溶液(100 mg/L)中的黑暗吸附以及饱和黑暗吸附后的甲基橙光催化降解等性能. 结果表明,获得的材料为纯锐钛矿相的二氧化钛. 颗粒分散好,平均粒径约20 nm. 具有大的比表面积. 随着C、N含量的增加,可见光区域的吸收增加,而紫外光区域的吸收基本不随C、N的含量变化;所制备的(C,N)-TiO2对甲基橙溶液具有超快的黑暗吸附能力(t<1 min);在微波处理中,随着盐酸胍的添加量增加,光催化的量子效率先增加后减小. 最好的样品能在20 min内对甲基橙的降解效率达到93%. 在可见光区域的吸收与黑暗吸附2个因素中,黑暗吸附的作用更大. 文章认为微波处理光催化材料的方法简单、快速、节能,是提高光催化速率的有效途径,值得推广.
碳、氮掺杂二氧化钛; 黑暗吸附; 光催化; 甲基橙
随着环境的恶化,低成本、高效率的光催化材料成为近几年研究的热点[1-2]. TiO2由于优秀的光催化性能而成为最具有商业化应用前景的光催化材料,尤其是碳(C)、氮(N)掺杂的TiO2(简称:(C,N)-TiO2),能较多利用可见光部分的能量成为催化材料的新星[3-4]. 但(C,N)-TiO2的制备成本较高,光催化效率还有待改善. 因此,提高光催化速率、降低其制备成本是(C,N)-TiO2商业化需要解决的问题.
本文首次尝试采用溶胶-凝胶法[5-6]制备TiO2前驱物凝胶粉末,采用微波辐射该前驱体与盐酸胍的混合物,快速制备了(C,N)-TiO2纳米粉体. 微波操作可制备很小的(C,N)-TiO2纳米颗粒,获得高比表面积的光催化粉末. 制备的(C,N)-TiO2纳米颗粒具有非常快速的黑暗吸附能力和光催化速度. 即使将黑暗吸附的时间计算在内,将甲基橙降解93%以上仅需要20 min. 这是到目前为止降解甲基橙速率最快的一种光催化材料. 另外,该方法制备(C,N)-TiO2纳米粉体具有能耗低、时间短、成本低,具有非常好的商业应用价值.
1 样品制备与分析测试方法
1.1 溶胶凝胶法制TiO2前驱物凝胶粉
以钛酸丁酯作为前驱物,无水乙醇做溶剂,采用冰醋酸和去离子水来调节凝胶的形成. 钛酸丁酯、无水乙醇、冰醋酸和水的质量比为 1∶18∶3∶5. 先将钛酸丁酯溶解在无水乙醇中,然后加入冰醋酸,搅拌约10 min. 再将去离子水逐滴滴入以上溶液形成溶胶. 静置4~20 h可得到凝胶. 将所得凝胶置于干燥箱中60 ℃干燥得到干凝胶,所得淡黄色样品研磨20 min得到TiO2前驱凝胶粉.
1.2 微波法制备(C,N)-TiO2纳米粉末
本文通过增加微波前驱体中盐酸胍的添加量来增加(C,N)-TiO2中C,N的含量(掺杂量). 将所得的二氧化钛前驱物凝胶粉与盐酸胍混合,研磨10 min,然后装入石英坩埚中,并置于微波炉中. 微波炉功率选为50 W,微波一定时间得到(C,N)-TiO2纳米粉末. 二氧化钛前驱物凝胶粉与盐酸胍混合的质量比分别为:3∶0、3∶0.2、3∶0.4、3∶0.6、3∶0.8、3∶1.0、3∶1.2、3∶1.4和3∶1.6. 对应盐酸胍的质量分数分别为0%、6.25%、11.76%、16.67%、21.05%、25.00%、28.57%、31.82%和34.78%.分别用NCT00、NCT02、NCT04、NCT06、NCT08、NCT10、NCT12、NCT14和NCT16来表示上述比例制备的(C,N)-TiO2纳米粉末.
1.3 黑暗吸附及光催化
黑暗吸附和光催化均在石英反应装置(图1)中进行. 石英反应器外围包裹一层锡纸避光以提供黑暗环境. 同时锡纸可隔离光源(模拟的太阳光)以外的光,以便于光强的控制. 石英反应器夹层采用冷却循环水保温,以避免光照引起甲基橙溶液的升温. 将光源(350 W的氙灯)固定于反应器正上方的10 cm高度处. 反应器放置在磁搅拌器托盘上.

图1 光催化实验装置照片
1.3.1 黑暗吸附 取100 mL质量浓度为20 mg/L的甲基橙溶液放入图1的反应器中. 取0.1 g样品加入甲基橙溶液中. 磁搅拌1 min后静置. 盖上锡纸防止光线进入溶液中. 每隔1 min取样1次, 在5 000 r/min下离心5 min,取上清液测试紫外可见吸收光谱.
由于甲基橙在464 nm附近有1个较强的吸收峰,对应甲基橙的官能团(—NN—)的振动吸收[7]. 根据Beer-Lambert定律,该峰的吸收强度与甲基橙溶液浓度成正比[8]. 故通过对比不同时间所取溶液的紫外可见光谱中464 nm附近吸收峰的强弱可以得到甲基橙溶液的浓度C[9],可进一步计算出甲基橙溶液由于黑暗吸附获得的降解率[10]:
Ed=((C0-C)/C0)×100%=((A0-A)/A0)×100%,
(1)其中,C0为甲基橙溶液的初始质量浓度;C黑暗吸附时间t时刻的甲基橙质量浓度;A0是初始甲基橙溶液的紫外-可见光谱中464 nm附近吸收峰的强度;A是黑暗吸附t时刻所取甲基橙溶液在464 nm处吸收峰的强度;Ed是黑暗吸附对甲基橙溶液中甲基橙的降解率. 1.3.2 光催化 取100 mL质量浓度为20 mg/L的甲基橙溶液放入图1的反应器中. 取0.1 g样品加入甲基橙溶液中, 搅拌1 min静置20 min, 使黑暗吸附至吸附饱和. 然后打开模拟太阳光(紫外-可见光)光源光照, 每隔20 min取样1次, 并在5 000 r/min下离心5 min,取上清液测试紫外可见吸收光谱. 步骤与黑暗吸附方法一致,测定上清液甲基橙在464 nm附近的峰强可确定甲基橙的质量浓度,再根据式(1)计算出光催化降解率.
1.4 其他的分析测试方法
采用X射线衍射((XRD, X’Pert Pro, Panalytical)来分析制备样品的相,扫描速度是2°/min. 用扫描电子显微镜(SEM,Zeiss Ultra 55, Carl Zeiss)来观察制备粉末的分散情况与颗粒大小. 用紫外-可见光谱仪测试所制备粉末的漫反射谱(UV-Vis DRS,Shimadzu 2550 PC spectrophotometer).
2 结果与讨论
图2是微波6.0 min制备的不同样品的XRD谱. 用快速微波法将锐钛矿TiO2与盐酸胍的混合物处理后得到的物质是单相,与纯的锐钛矿TiO2的XRD衍射峰一致[11].
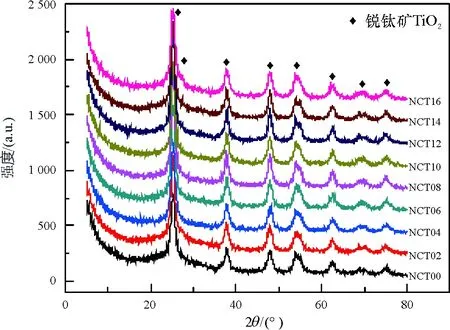
图2 微波6.0 min制备的不同样品的XRD谱
Figure 2 XRD patterns of as-prepared samples with microwave irradiation time of 6.0 min
图3是微波6.0 min制备的NCT12粉末的SEM图. 颗粒的分散性较好. NCT12的颗粒平均粒径为20 nm左右,而且颗粒分布较均匀.

图3 NCT12粉末的SEM照片
图4是微波6.0 min制备的不同样品的UV-VIS DRS谱. 对于所有样品,随着TiO2前驱物凝胶粉末与盐酸胍混合质量比的增加,(C,N)-TiO2粉末对可见光的吸收边红移,且吸收增加. NCT16对可见光的吸收达到最大. 这些结果和文献[12-13]的结果相符. 文献[12-13]的工作中,当N、C掺入量不大时,随着N、C掺入量的增加,对可见光的吸收边红移,吸收越强. 这个结果也间接证明了N、C在TiO2中的掺入量随着微波前TiO2前驱物凝胶粉与盐酸胍质量比的增加而增加.

图4 不同样品的紫外可见漫反射光谱
所有样品均在1 min内达到吸附平衡(黑暗吸附达到饱和)(图5),说明吸附相当快. 这是因为凝胶颗粒中包含Ti—O以外的键,在微波作用下,盐酸胍与凝胶粉末的混合物在短时间产生大量气体,造成纳米颗粒的分散而不是团聚,分散性好,生成的(C,N)-TiO2颗粒小(约20 nm),在吸附甲基橙过程中,材料的有效吸附面积大. 因此,黑暗吸附迅速. 1 min内即可达到吸附平衡. 这应该是到目前为止最快的黑暗吸附速度,比活性炭[14-15]的快. 快速的黑暗吸附使得在实际的污水处理过程中污水处理速度提高. 因此,利用微波方法配合适当的气体产生剂(如盐酸胍),可以在光催化材料中产生孔洞[16],或者产生颗粒之间的分散效果,以增加光催化剂的比表面积.
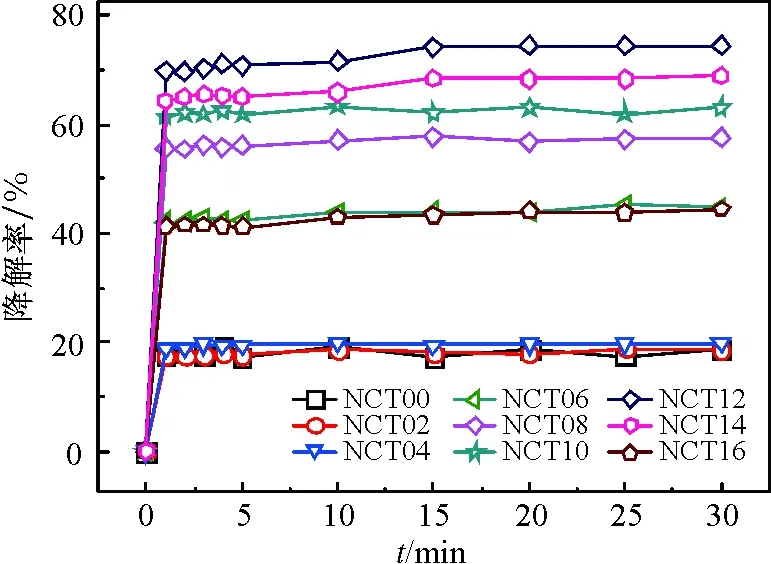
图5 不同样品的黑暗吸附曲线
图6是微波6.0 min制备的不同样品的光催化曲线. 先在黑暗下吸附20 min(充分吸附),再通过光催化实验得到. 从NCT00到NCT12,随着混合物中盐酸胍质量比的增加,其达到饱和甲基橙降解率的时间缩短,NCT00需要近120 min,NCT12仅需要20 min,其饱和甲基橙降解率随盐酸胍的增加而增加. NCT00在黑暗吸附20 min. 光催化20 min后的甲基橙降解率为84%,而NCT12在黑暗吸附20 min并光催化40 min后的甲基橙光催化降解率高达93%. 由于这些降解率是以在吸附20 min后溶液的浓度作为参考浓度(甲基橙浓度小于2 mg/L),其光催化率由于受到初始质量浓度的影响比100 mg/L甲基橙的光降解率低[9,17]. NCT12的甲基橙光降解率最高. 从NCT12到NCT16,其光催化降解率逐渐减小. 虽然NCT12对可见光的吸收率不高,但其具有远高于其他样品的黑暗吸附,故NCT12具有最好的甲基橙光降解率. 虽然NCT16的可见光吸收率是NCT12 的2倍,但其光降解率仍然比NCT12低近80%. 可见,黑暗吸附比可见光吸收率对光催化效率的影响大.

图6 不同样品的光催化曲线
微波时间对NCT12的黑暗吸附和光催化性能的影响不大(图7). 但对黑暗吸附20 min后甲基橙溶液(2 mg/L)在光照1 h内的降解率能达到80%以上(此时的降解率以黑暗吸附后的质量浓度作为起始质量浓度). 微波处理6.0 min的样品对甲基橙的光降解率最高,黑暗吸附20 min的甲基橙溶液(2 mg/L)光照1 h的降解率能达到90%以上,该结果与图6的光催化结果相吻合. 从图6的结果可推测,黑暗吸附性能起主导作用,微波处理后样品的黑暗吸附很大,但微波时间对NCT12的黑暗吸附和光催化性能的影响不大.
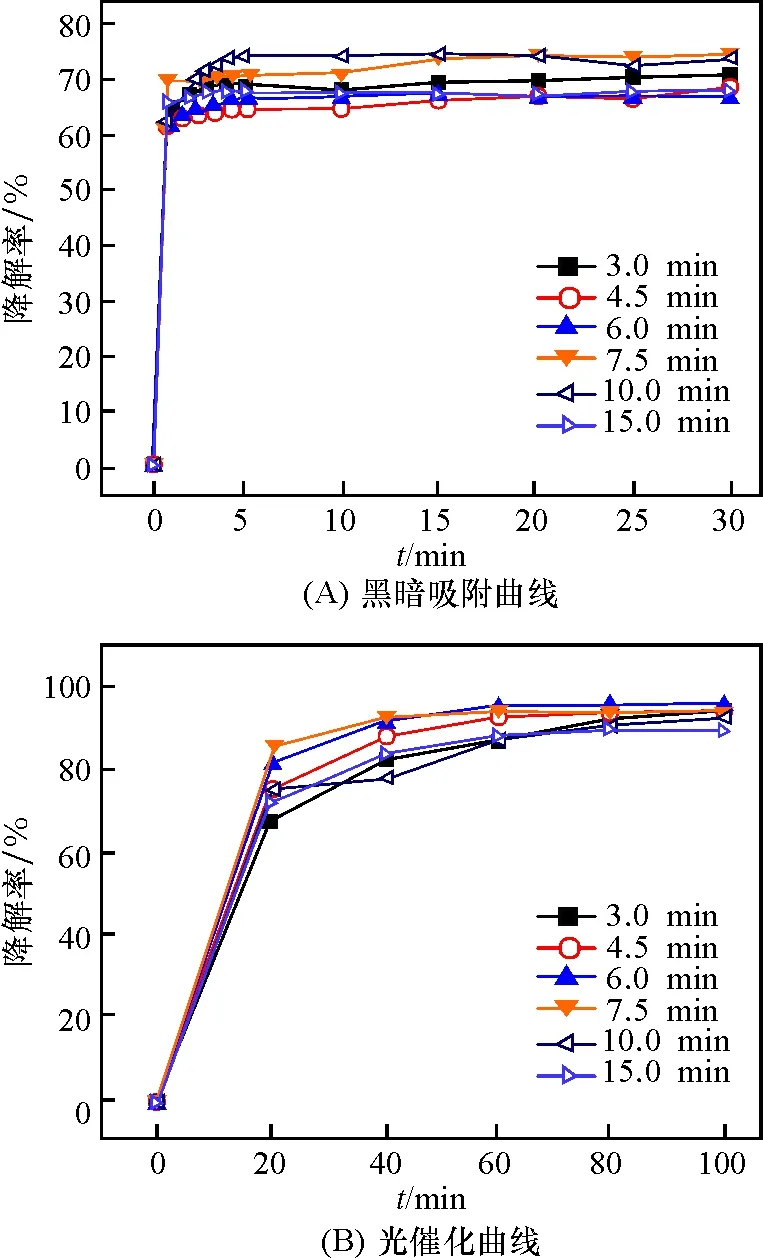
图7 不同微波时间对样品NCT12的黑暗吸附和光催化性能的影响
Figure 7 Effects of microwave irradiation time on the dark adsorption and photodegradation of NCT12
微波时间对NCT08的光催化性能的影响较大(图8). 随着微波时间的增加,其光催化的光降解效率增加;但微波6.0 min的样品其饱和光降解率最大. 原因可能是吸附量最多.

图8 不同微波时间对NCT08的光催化性能的影响
Figure 8 Effect of microwave irradiation time on the photode-gradation of NCT08
微波时间对NCT10的光催化性能的影响不大(图9). 但在光催化1 h后对黑暗吸附20 min的甲基橙溶液(2 mg/L)的降解率能达到90%以上. 微波4.5 min的样品其光降解率最高,能对黑暗吸附20 min的甲基橙溶液(2 mg/L)在光照1 h后的降解率能达到90%以上,该结果和图6、图7B的光催化结果吻合. 微波后的各个样品的黑暗吸附很大,但微波时间对NCT10的光催化性能影响不大.

图9 不同微波制备时间对NCT10的光催化性能的影响
Figure 9 Effect of microwave irradiation on the photodegradation of NCT10
从图7B、图8、图9可以看出,微波处理前TiO2纳米粉混合物中盐酸胍的添加量质量分数较大(如大于25%)时,微波处理时间对黑暗吸附和光催化性能的影响不大. 这可能是在微波处理TiO2纳米粉与盐酸胍混合物时,有大量的气体释放出来,在生成纳米TiO2颗粒过程中起到很好的分散作用. 微波时间增加,对纳米TiO2的分散时间越长,对纳米TiO2颗粒的分散效果越好,分散颗粒越小. 同时,盐酸胍质量分数的增加,对纳米TiO2颗粒的分散有利. 但当盐酸胍质量分数增加到一定量(即NCT12,28.57%)时,其对纳米TiO2颗粒的分散效果最佳. 当继续增加盐酸胍的添加量时,纳米TiO2颗粒的分散效果变差. 此时,微波时间对黑暗吸附和光催化的性能的影响较小.
3 结论
采用简单、快速的方法在溶胶-凝胶方法制备的TiO2纳米颗粒中掺入C、N元素, 获得了对甲基橙溶液具有超快黑暗吸附能力(1 min达到饱和吸附)的纯锐钛矿相的掺杂C、N的(C,N)-TiO2纳米材料. 颗粒分散好,尺寸均匀(平均粒径约20 nm). 随着C、N掺杂量的增加,可见光区域的吸收增加,而紫外光区域基本不变. 但在可见光区域的吸收与黑暗吸附2个因素中,黑暗吸附因素的作用较大. 随着微波处理前纳米TiO2混合物中盐酸胍质量分数的增加,光催化的量子效率先增加后减小. 样品NCT12的饱和光催化降解率最大;在20 min内达到饱和,其光催化降解率高达93%. 因此,微波处理光催化材料的方法是提高光催化速率的有效途径,值得推广.
[1] SU Y F,WANG G B,DAVE T F,et al. Photoelectrocatalytic degradation of the antibiotic sulfametho-xazole using TiO2/Ti photoanode[J]. Applied Catalysis B: Environmental,2016,186:184-192.
[2] SAMIRA B,HIR Z A M,YOUSELF A T,et al. Photocatalytic performance of activated carbon-supported mesoporous titanium dioxide[J]. Desalination and Water Treatment,2016,57(23):10859-10865.
[3] XU Q C,WELLIA D V,YAN S,et al. Enhanced photocatalytic activity of C-N-codoped TiO2films prepared via an organic-free approach[J]. Journal of Hazardous Materials,2011(1/2/3),188:172-180.
[4] WU K R,HUNG C H. Characterization of N,C-codoped TiO2films prepared by reactive DC mag-netron sputtering[J]. Applied Surface Science,2009,256(5):1595-1603.
[5] NOLAN N T,SYNNOTT D W,SEERY M K,et al. Effect of N-doping on the photocatalytic activity of sol-gel TiO2[J]. Journal of Hazardous Materials,2012,211/212:88-89.
[6] 黄剑锋. 溶胶-凝胶原理与技术[M]. 北京:化学工业出版社,2005:58-60.
[7] HUO Y N,JIN Y,ZHU J,et al. Highly active TiO2-x-yNxFyvisible photocatalyst prepared under supe-rcritical conditions in NH4F/EtOH fluid[J]. Applied Catalysis B:Environmental,2009,89:543-550.
[8] YOGI C,KOJIMA K,WADA N,et al. Photocatalytic degradation of methylene blue by TiO2film and Au particles-TiO2composite film[J]. Thin Solid Films,2008,516:5881-5884.
[9] ZHONG W,YU L,DU C,et al. Characterization and high pollutant removal ability of buoyant (C,N) -TiO2/PTFE flakes prepared by high-energy ball-milling[J]. RSC Advances,2014,4(75):40019-40028.
[10]CHENG X W,YU X J,XING Z P. One-step synthesis of visible active C-N-S-tridoped TiO2photocatalyst from biomolecule cystine[J]. Applied Surface Science,2012,258:7644-7650.
[11]CHEN J F,ZHONG J B,LI J Z,et al. Photoinduced charge separation and simulated solar-driven p-Hotocatalytic performance of C-N-co-doped TiO2prepared by sol-gel method[J]. Journal of Sol-Gel Science and Technology,2015,76(2):332-340.
[12]QIN H L,GU G B,LIU S,et al. Study on preparation of nitrogen-doped titania by sol-gel technique and its visible light activity [J]. Acta Energiae Solaris Sinica,2007,28(4):363-367.
[13]MALGORZATA W,DIANA D,ANTONI M,et al. Carbon-modified TiO2for photocatalysis[J]. Nanoscale Research Letters,2012,7:1-6.
[14]KHALED M,KHALED H,NOUREDDINE H,et al. Kinetics and equilibrium studies on removal of methylene blue and methyl orange by adsorption onto activated carbon prepared from data pits-a comparative study[J]. Journal of Chemical Engineering,2015,32(2):274-283.
[15]WU Y H,YU Q,XU H D,et al. Adsorption behavior and kinetics of methyl orange in water on activated carbon[J]. Advanced Materials Research,2012,549:318-321.
[16]ZHAO Z X,LI Z,XIA Q B,et,al. Microwave irradiation preparation and properties of PNIPAAm Copolymer hydrogel[J]. Chinese Journal of Materials Research,2008,22(4):405-410.
[17]XU S B,ZHU Y F,JIANG L,et al. Visible light induced photocatalytic degradation of methyl orange by polythiophene/TiO2composite particles[J]. Water,Air and Soil Pollution,2010,213:151-159.
【中文责编:成文 英文责编:李海航】
Preparation and Photocatalytic Properties of Nitrogen and Carbon Co-doped Titanium Dioxide by Combining Sol-gel Method and Microwave-assisted Method
HE Qinyu1,2*, WU Zehong1, HUANG Weiyuan1, CHEN Xiaomei1, WEI Yurui1, LIU Junming2, DU Chun1, ZHOU Jiangshan1, LI Fangzhou1
(1. Guangdong Provincial Key Laboratory of Quantum Engineering and Quantum Materials, School of Physics and Telecommunication Engineering, South China Normal University, Guangzhou 510006, China; 2. Institute for Advanced Materials, South China Academy of Advanced Optoelectronics, South China Normal University, Guangzhou 510006, China)
A kind of nitrogen and carbon co-doped titanium dioxide ((N,C)-TiO2) was prepared by a simple, fast and energy-saving method, by which composite consisting of TiO2precusor (fabricated by sol-gel method) and guanidine hydrochloride was irradiated by microwave. X-Ray diffraction (XRD), scanning electron microscopy (SEM), UV-visible diffuse reflection spectra (UV-Vis DRS), dark adsorption of methylene orange and photo-catalysis were employed to characterize the prepared samples. It is shown that the prepared samples are pure anatase TiO2with large specific area and good disperse, homogeneous nanosized particle size (20 nm). The Vis absorption of prepared powders increases with increased content of guanidine hydrochloride in above-said composite. In the meantime, a very fast and high dark adsorption is found in as-fabricated powders. The time when the dark adsorption reaches to saturation is less than 1 min. And the photocatalytic degradation firstly increases, then decreases with increased content of guanidine hydrochloride in above-said composite. The best saturated photocatalytic degradation is 93% within 20 min. It is also found that between the two factors -Vis absorption and dark adsorption, the dark adsorption plays more important role in photocatalytic activity. It can be concluded that the microwave-assisted method can introduce pores or lead to smaller particle size in as-prepared powdered photocatalysts.
C,N co-doped TiO2; dark adsorption; photocatalysis; methylene orange
2016-04-07 《华南师范大学学报(自然科学版)》网址:http://journal.scnu.edu.cn/n
国家自然科学基金项目(51372092);华南师范大学2014—2015年自然科学类“高校创新强校工程”特色创新类项目
O64
A
1000-5463(2016)05-0025-06
*通讯作者:何琴玉,教授,Email:gracylady@163.com.

