冻融期去根处理对小兴安岭6种林型土壤微生物量的影响
林尤伟,金光泽
东北林业大学生态研究中心, 哈尔滨 150040
冻融期去根处理对小兴安岭6种林型土壤微生物量的影响
林尤伟,金光泽*
东北林业大学生态研究中心, 哈尔滨 150040
春季冻融期,在小兴安岭的阔叶红松(Pinuskoraiensis)林、谷地云冷杉(Piceakoraiensis-Abiesnephrolepis)林、阔叶红松择伐林、白桦(Betulaplatyphylla)次生林、红松人工林、兴安落叶松(Larixgmelinii)人工林的去根处理样地和对照样地进行野外取土实验,分析了根去除对上述林型土壤微生物量的影响以及与土壤环境因子的关系。结果表明:冻融循环期间对照样地和去根处理样地的林型、土壤层次、取样时间均显著地影响土壤微生物量碳(MBC) (P<0.05),对照样地中各林型的土壤微生物量氮(MBN)差异显著,而去根处理样地中各林型的MBN没有显著差异(P>0.05);冻融循环期间去根处理显著地减少了大部分林型及土层(谷地云冷杉林0—10 cm及择伐林外)的MBC,而去根处理对大部分林型及土层(阔叶红松林0—10 cm,谷地云冷杉林和择伐林的10—20 cm除外)的MBN没有显著影响。说明在小兴安岭春季冻融期根系对土壤微生物量的影响不可忽视。
冻融循环;土壤微生物量碳氮;根切除;微生物含量变化;森林土壤
在高纬度地区的春季,土壤反复冻融是常见的温度变化现象[1]。冻融通过破坏土壤团聚体和有机质结构,杀死土壤中的微生物,加快植物残体破碎化而释放出植物生长所需要的营养物质[2]。土壤的冻结速度、冻融交替次数、土壤含水量和微生物不同生长阶段等造成土壤微生物的致死程度不同,从而影响微生物群落生理功能和群落结构[3]。土壤覆盖的植被类型不同,地下生长的根和地表凋落物类型也有所不同,导致土壤有机碳的分布状况也有很大差异[4]。在多次单尺度(白天2℃,5 h;晚上-4℃,19 h)冻融循环后,较大的土壤温差交替加快了不同森林植被类型的土壤微生物碳氮转化速率[5]。
植物根系和凋落物在化学性质、向土壤输入有机质的量和方式的不同,其在土壤生态系统中的作用也有所差异[6]。冬春季土壤中植被的凋落物分解过程在土壤碳输入中起着重要作用,因此国内外相关研究多集中于该期间凋落物分解对土壤碳素循环的影响[7- 8]。近年来,人们开始关注植物根系和凋落物对CO2释放量、微生物生物量碳和土壤酶活性的影响。Schaefera等[9]发现,植物根系去除后导致土壤分解凋落物的速率下降;张伟东等[10]研究发现,土壤微生物量的季节动态由地下部分的碳输入决定,而非地上的新鲜凋落物;Clemmensen等[11]发现在北方森林中的碳含量占很大比例是通过根和它们相关的菌根真菌进行储存,并得出了在生态系统养分循环过程中,落叶、树枝等和植物根系对土壤的碳输入量大小的比较中根和真菌占优势这一结论。另外,Campbell等[12]研究表明,冬春季节根系对土壤的养分吸收有着明显的影响。然而受试验方法所限, 对植物根系(凋亡细根和根系分泌物)在碳输入过程中的作用研究较少,现有的报道也大都采用模拟方法,将细根或有机物质添加到土壤中模拟根系周转和根系分泌物的作用[13]。随着温室效应的持续与森林的覆盖率降低,冻融周期的缩短,根系在冻融循环期间对森林土壤养分循环和对微生物活性的影响逐渐被人们所重视。目前,冻融期去根处理对同一气候区不同林型的土壤微生物量的影响的研究较为匮乏。
小兴安岭是我国重要的林区之一,地处北方气候变化敏感地区。本研究以东北东部山区的顶极植被-阔叶红松(Pinuskoraiensis)林、阔叶红松林经过择伐后形成的阔叶红松择伐林(简称择伐林)、阔叶红松林皆伐后天然更新的白桦(Betulaplatyphylla)林、皆伐后人工造林的红松人工林和兴安落叶松(Larixgmelinii)人工林以及非地带性顶极植被-谷地云冷杉(Piceakoraiensis-Abiesnephrolepis)林为研究对象,探讨冻融循环期不同演替阶段的林型的土壤微生物量动态变化特征及其影响因子,分析根系对6种林型土壤微生物量的影响,为了解冻融循环期该地区不同演替阶段的森林中根系对土壤微生物碳氮循环过程的影响及其作用机制提供基础数据与科学依据。
1 材料与方法
1.1 研究区概况
本研究在黑龙江凉水国家级自然保护区(47° 0′ 50″ N, 128° 53′ 20″ E)进行。保护区位于黑龙江省伊春市带岭区,地处小兴安岭南部达里带岭支脉的东坡,属于典型的低山丘陵地貌。本地区的气候属于温带大陆性夏雨季风气候,春季到来较晚,降水较少;夏季比较短而且过得快,温凉多雨;秋季迅速降温,并带有早霜现象;冬季漫长且寒冷,干燥。年平均气温-0.3℃,年均最高气温7.5℃,年均最低气温-6.6℃,年平均降水量676 mm,年平均蒸发量805 mm,无霜期100—125 d,积雪期130—150 d。主要植被类型为我国东北东部山区的顶极植被-阔叶红松林。
1.2 实验设计与方法
本研究选取方圆2 km 内的阔叶红松林、择伐林、白桦次生林、兴安落叶松人工林、红松人工林,以及谷地云冷杉林为研究对象。阔叶红松林、择伐林、白桦次生林位于中坡(海拔分别为460 m,450 m和370 m),兴安落叶松人工林和红松人工林位于中上坡(海拔为400 m和380 m),云冷杉林位于谷地(海拔350 m);各个林型坡向相似;平均坡度 10—15°。各个林型植被的根系主要集中于0—20 cm土层[14];地带性土壤为暗棕色森林土壤。样地植被组成及概况如表1所示。
土壤含水率(Ws)采用Trime-Pico土壤水分分析仪测定;土壤温度(Ts)采用土壤温度仪连续测定,土壤有机碳(SOC)采用multi N/C 3000 TOC分析仪(Analytic Jena AG, Germany)测定;土壤全氮(TN)采用KjeltecTM2300凯氏定氮仪(Foss Teactor AB, Sweden)进行测定;土壤微生物量采用氯仿熏蒸浸提法进行提取,提取液采用multi N/C 3000分析仪(Analytic Jena AG, Germany)进行测定。土壤微生物量碳(MBC)和土壤微生物量氮(MBN)分别用下式求得[15-16]。
MBC=Ec/0.45
MBN=En/0.45
式中,Ec和En分别为熏蒸和未熏蒸土样浸提液有机碳,全氮的差值;0.45为校正系数。
1.3 数据分析
采用方差分析(ANOVA)检验林型、土壤层次、采样时间及其交互作用对MBC和MBN的影响(MBC和MBN均经过对数转换后服从正态分布)。采用Duncan检验比较MBC和MBN在林型、土壤层次和采样日期之间的显著性差异。用Pearson 相关系数评价MBC和MBN与土壤含水量、TOC、TN之间的关系。上述统计分析均使用 SPSS19. 0 统计软件完成。

表1 小兴安岭6种林型样地概况和树种构成
*起测胸径为1 cm
2 结果
2.1 冻融循环期间6种林型的土壤理化性质
冻融循环期间各个林型之间对照样地和去根处理样地0—10 cm层温度与10—20 cm层温度动态如图所示 (图1)。

图1 冻融循环期间样地内土壤温度动态变化(2013年)Fig.1 Dynamic changes of soil temperature in sampling site during the freeze-thaw cycle (2013)Ⅰ:阔叶红松林Mixed broadleaved-Korean pine forest;Ⅱ: 谷地云冷杉林Spruce-fir valley forest; Ⅲ:择伐林Selection cutting forest; Ⅳ:白桦次生林Secondary birch forest;Ⅴ: 红松人工林Korean pine plantation; Ⅵ: 落叶松人工林Dahurian larch plantation
冻融循环期间对照样地的林型间以及土层间的有机碳无显著差异(P>0.05);而去根处理样地的林型间的有机碳差异显著(P<0.05),土层间的有机碳无显著差异。对照样地以及去根处理样地的总氮(TN)含量均表现出相同的趋势,即林型间没有显著差异,而土层间差异显著。对照样地的林型之间以及土层间的含水率有显著差异;去根处理样地的林型之间的含水率差异显著,而土层间含水率没有显著差异(表2)。
冻融循环期间对照样地的谷地云冷杉林、落叶松人工林的0—10 cm层的土壤有机碳和落叶松人工林、谷地云冷杉林的0—20 cm层的土壤有机碳显著高于去根处理样地;红松人工林0—10 cm、10—20 cm和0—20 cm的含水率以及择伐林的0—20 cm层的含水率显著低于去根处理样地,而阔叶红松林0—10 cm层的含水率显著高于去根处理样地。去根处理对全氮含量无显著影响(表2)。

表2 冻融循环期间小兴安岭6种林型的土壤理化性质
F: 林型; S: 土层; W: 取样时间; 不同大写英文字母表示0—10 cm土层同一处理不同林型间差异显著, 不同小写罗马字母表示10—20 cm土层同一处理不同林型差异显著, 不同大写罗马字母表示0—20 cm土层同一处理不同林型间差异显著, 不同小写英文字母分别表示同一林型不同处理间差异显著(N=15,ɑ=0.05)
2.2 冻融循环期间不同林型土壤微生物量碳氮的差异
冻融循环期间对照样地和去根处理样地的林型、土壤层次、取样时间均显著地影响土壤微生物量碳(MBC)。对照样地0—20 cm层阔叶红松林的MBC与谷地云冷杉林的MBC差异显著(P<0.05),对照样地的林型间土壤微生物量氮(MBN)、C/N均差异显著,而土层间差异不显著(P>0.05)。去根处理样地中林型对MBN影响不显著,而土层对MBN的影响显著,林型、土层对C/N均无显著影响。
冻融循环期间去根处理显著地减少了大部分林型及土层(除谷地云冷杉林0—10 cm层,择伐林0—20 cm层和10—20 cm层外)的MBC,而去根处理对大部分林型及土层(阔叶红松林0—10 cm层和0—20 cm层,谷地云冷杉林的10—20 cm层和0—20 cm层除外)的MBN没有显著影响,并对大部分林型和土层(白桦次生林的0—10 cm层和0—20 cm层,落叶松人工林的0—10 cm层和0—20 cm层除外)的C/N也没有显著影响(表3)。
2.3 冻融循环期间不同林型土壤微生物量碳氮的动态
0—10 cm土层中,对照样地所有林型的MBC的动态变化基本呈现“W”型,即:冻融循环伊始(4月22日)开始下降,随土壤冻融循环持续而上升,至第3次、第5次冻融循环达到峰值(图2)。与对照样地相比,去根处理样地0—10 cm土层的MBC波动幅度相对较小,而在10—20 cm层则波动幅度更小(图2)。
与MBC相比,冻融期去根处理和对照样地的MBN的动态变化在林型和土层间的差异不大(图3,图4)。在0—10 cm土层,对照样地的MBN变化呈现“M”型。到第4次冻融循环(5月7日)出现第2次高峰。去根处理样地的MBN动态则呈现从冻融初期开始上升,在之后一直下降的格局(图3)。与0—10 cm土层相比,10—20 cm 土层的MBN波动更大,大部分林型都在第3次、第4次冻融循环期间有所回升,而在冻融末期又继续降低(图3)。
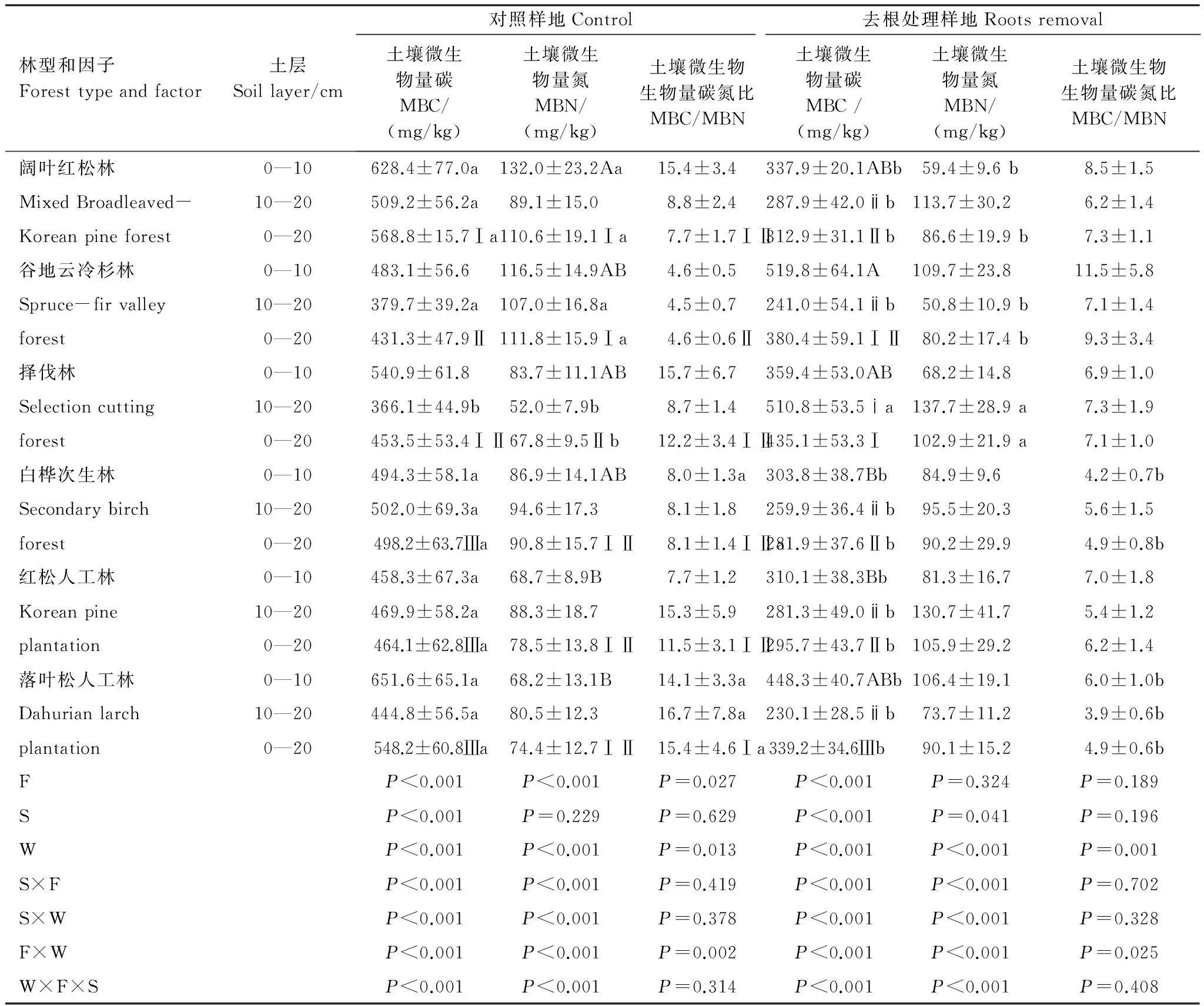
表3 冻融循环期间小兴安岭6种林型的土壤微生物生物量碳、氮和碳氮比
Table 3 Soil microbial biomass carbon, nitrogen and carbon/nitrogen ratio in 6 forest types in Xiaoxing′an Mountains during the freeze-thaw cycle
林型和因子Foresttypeandfactor土层Soillayer/cm对照样地Control去根处理样地Rootsremoval土壤微生物量碳MBC/(mg/kg)土壤微生物量氮MBN/(mg/kg)土壤微生物生物量碳氮比MBC/MBN土壤微生物量碳MBC/(mg/kg)土壤微生物量氮MBN/(mg/kg)土壤微生物生物量碳氮比MBC/MBN阔叶红松林0—10628.4±77.0a132.0±23.2Aa15.4±3.4337.9±20.1ABb59.4±9.6b8.5±1.5MixedBroadleaved-10—20509.2±56.2a89.1±15.08.8±2.4287.9±42.0ⅱb113.7±30.26.2±1.4Koreanpineforest0—20568.8±15.7Ⅰa110.6±19.1Ⅰa7.7±1.7ⅠⅡ312.9±31.1Ⅱb86.6±19.9b7.3±1.1谷地云冷杉林0—10483.1±56.6116.5±14.9AB4.6±0.5519.8±64.1A109.7±23.811.5±5.8Spruce-firvalley10—20379.7±39.2a107.0±16.8a4.5±0.7241.0±54.1ⅱb50.8±10.9b7.1±1.4forest0—20431.3±47.9Ⅱ111.8±15.9Ⅰa4.6±0.6Ⅱ380.4±59.1ⅠⅡ80.2±17.4b9.3±3.4择伐林0—10540.9±61.883.7±11.1AB15.7±6.7359.4±53.0AB68.2±14.86.9±1.0Selectioncutting10—20366.1±44.9b52.0±7.9b8.7±1.4510.8±53.5ⅰa137.7±28.9a7.3±1.9forest0—20453.5±53.4ⅠⅡ67.8±9.5Ⅱb12.2±3.4ⅠⅡ435.1±53.3Ⅰ102.9±21.9a7.1±1.0白桦次生林0—10494.3±58.1a86.9±14.1AB8.0±1.3a303.8±38.7Bb84.9±9.64.2±0.7bSecondarybirch10—20502.0±69.3a94.6±17.38.1±1.8259.9±36.4ⅱb95.5±20.35.6±1.5forest0—20498.2±63.7ⅠⅡa90.8±15.7ⅠⅡ8.1±1.4ⅠⅡa281.9±37.6Ⅱb90.2±29.94.9±0.8b红松人工林0—10458.3±67.3a68.7±8.9B7.7±1.2310.1±38.3Bb81.3±16.77.0±1.8Koreanpine10—20469.9±58.2a88.3±18.715.3±5.9281.3±49.0ⅱb130.7±41.75.4±1.2plantation0—20464.1±62.8ⅠⅡa78.5±13.8ⅠⅡ11.5±3.1ⅠⅡ295.7±43.7Ⅱb105.9±29.26.2±1.4落叶松人工林0—10651.6±65.1a68.2±13.1B14.1±3.3a448.3±40.7ABb106.4±19.16.0±1.0bDahurianlarch10—20444.8±56.5a80.5±12.316.7±7.8a230.1±28.5ⅱb73.7±11.23.9±0.6bplantation0—20548.2±60.8ⅠⅡa74.4±12.7ⅠⅡ15.4±4.6Ⅰa339.2±34.6ⅠⅡb90.1±15.24.9±0.6bFP<0.001P<0.001P=0.027P<0.001P=0.324P=0.189SP<0.001P=0.229P=0.629P<0.001P=0.041P=0.196WP<0.001P<0.001P=0.013P<0.001P<0.001P=0.001S×FP<0.001P<0.001P=0.419P<0.001P<0.001P=0.702S×WP<0.001P<0.001P=0.378P<0.001P<0.001P=0.328F×WP<0.001P<0.001P=0.002P<0.001P<0.001P=0.025W×F×SP<0.001P<0.001P=0.314P<0.001P<0.001P=0.408
F: 林型Forest type; S: 土层Soil layer; W: 取样时间Sampling times;不同大写英文字母表示0—10 cm土层同一处理不同林型间差异显著, 不同小写罗马字母表示10—20 cm土层同一处理不同林型差异显著, 不同大写罗马字母表示0—20 cm土层同一处理不同林型间差异显著, 不同小写英文字母分别表示同一林型不同处理间差异显著(N=15,ɑ=0.05)
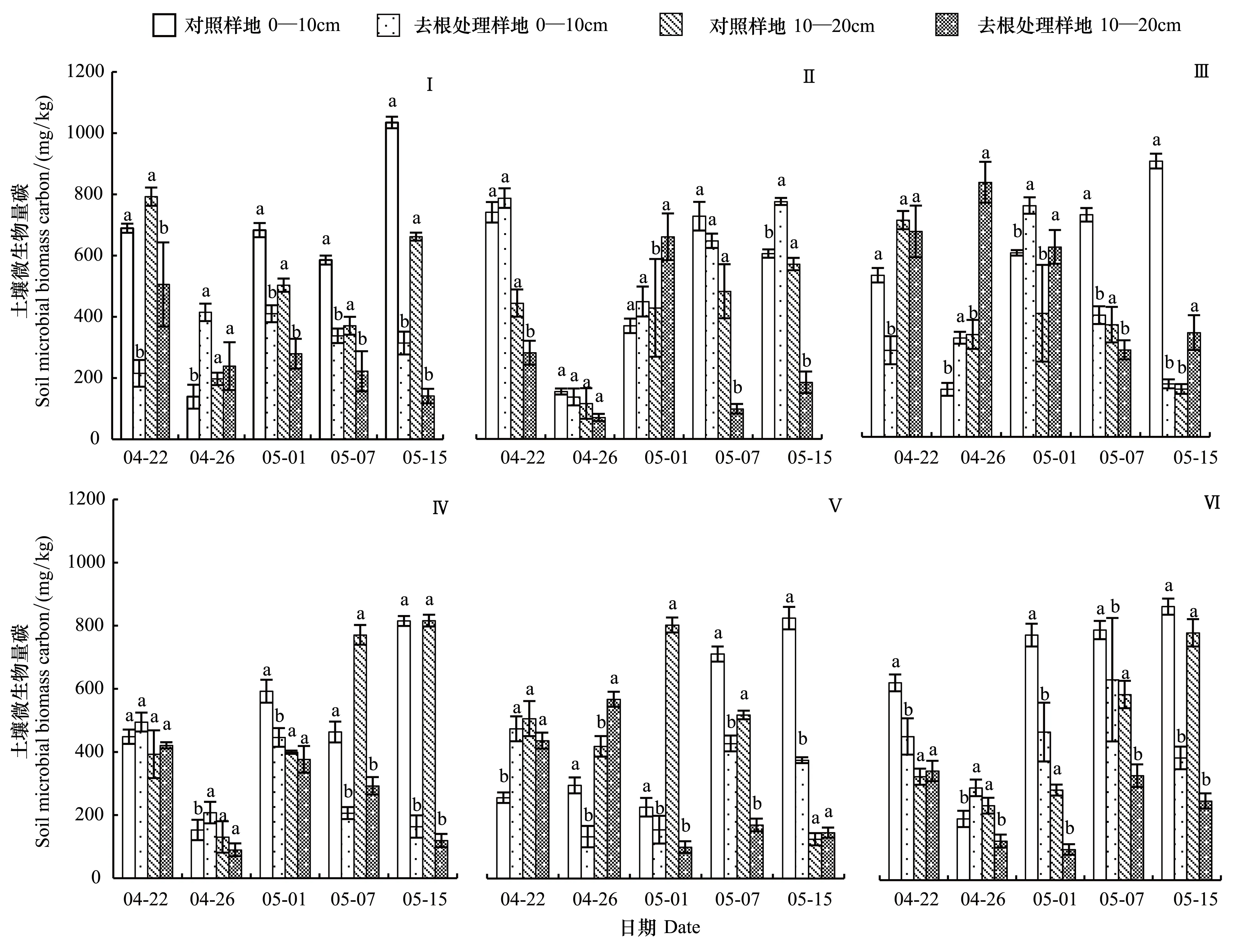
图2 冻融循环期间小兴安岭6种林型的土壤微生物量碳的动态变化(2013年)Fig.2 The change of 6 forest types soil microbial biomass carbon in Xiaoxing′an Mountains during the freeze-thaw cycle (2013)Ⅰ:阔叶红松林Mixed broadleaved-Korean pine forest; Ⅱ: 谷地云冷杉林Spruce-fir valley forest; Ⅲ:择伐林Selection cutting forest; Ⅳ:白桦次生林Secondary birch forest;Ⅴ: 红松人工林Korean pine plantation; Ⅵ: 落叶松人工林Dahurian larch plantation;不同小写字母分别表示同一土层不同处理间差异显著(N=15,ɑ=0.05)

图3 冻融循环期间小兴安岭6种林型的土壤微生物量氮的动态变化(2013年)Fig.3 The change of 6 forest types soil microbial biomass nitrogen in Xiaoxing′an Mountains during the freeze-thaw cycle (2013)
2.4 冻融循环期土壤微生物量与土壤理化性质的关系
冻融期对照样地MBC与土壤有机碳、全氮显著负相关,微生物量碳氮和微生物碳氮比均与温度显著正相关,含水率均与MBC、MBN和MBC/MBN之间关系均不显著;去根处理样地的MBC与土壤温度则显著负相关,MBC、MBN和MBC/MBN与土壤有机碳和全氮之间关系均不显著(P>0.05)(表3)。
3 讨论
冻融循环期间剧烈温差变化将导致0—20 cm层土壤微生物和植物根系的大量死亡,微生物分解底物的速率下降,造成冻融循环期间不同林型内土壤有机碳和土壤全氮均没有显著差异(表2),与Brooks等[17]、Shanley和Chalmers[18]研究相符;随着冻融循环的持续,土壤冰水相变和部分残留的微生物进行繁殖,将降低土壤有机碳和全氮含量[19- 22],导致在本研究中取样时间显著影响对照样地的土壤有机碳含量、土壤全氮含量和土壤含水率(表2),这与Fitzhugh等[23]在冻融期的研究结果相同。冻融循环也使不同土壤层中N的吸收程度相异[8,24],造成土层之间的全氮含量差异显著(表2)。
冻融循环增加土壤微生物繁殖所需的底物,冻融循环末期随着土壤温度的回升(图1),微生物开始恢复繁殖,造成本研究中各个林型内土壤微生物量碳氮动态基本呈现“W”型变化(图2,图3),与Henry[1]的研究结果相似。本研究中土壤微生物量碳氮含量波动在54—1051 mg/kg与2.7—494.2 mg/kg之间,低于温带其他地区的研究结果[25-26],造成这一的差异的原因可能是由于林型不同和取样时间差异导致。冻融循环期间土壤微生物逐渐适应强烈的温差变化,导致土壤中养分含量不断地被微生物利用分解,导致对照样地和去根样地内土壤微生物量产生动态波动[27]。同时冻融循环期植物和土壤微生物对养分的利用存在相互促进和竞争的关系[6],本研究中阔叶红松林和白桦次生林生态系统代谢旺盛(表2),同时根系和土壤微生物之间的相互作用,刺激了土壤微生物的生长和繁殖,土壤微生物含量比其他林型较大。谷地云冷杉林是本地区的非地带性顶极群落,其受到针叶分泌物的影响引起微生物分解速率降低[28],同时冻融环境下较低的土壤温、湿度又限制了土壤微生物的活动,造成其微生物量碳相对较低,这种差异是森林植被种类和环境因子共同作用的结果。
对照样地的MBC含量与TOC含量极显著负相关(P<0.01),与TN含量显著负相关(P<0.05)(表4),MBC和MBN受到温度影响显著(表4),与其他相关研究结果相符[25,29],表明冻融循环期间在本研究区有根系的土壤中,土壤有机碳、全氮和温度是影响土壤微生物量碳氮的关键因子;而去根样地在冻融循环期间,由于0—10 cm土层中微生物含量受到环境因子的影响程度较大,且去根样地内缺乏根系对土壤的保护作用,导致各林型0—10 cm的土壤微生物量碳氮显著低于对照样地(表3),与其他相关研究结果相符[29-30]。尽管有研究指出土壤有机碳和全氮是影响土壤微生物量的主要因子[31],但本研究中去根处理样地的土壤微生物量碳仅受到土壤温度的显著影响(表4),与Li等[32]在生长季节的研究结果相符合。缺乏根系保护的去根处理样地内土壤环境受到冻融循环的影响将更加剧烈,且土壤环境条件的剧烈变化会改变土壤中有机质含量对微生物量的影响[33],这可能是去根处理样地内土壤微生物量碳氮和土壤有机碳和全氮之间无显著关系的原因(表4)。
土壤微生物生物量碳氮比(MBC/MBN)在一定程度上反映了土壤中真菌和细菌的比例[34]。本研究中对照样地各林型的土壤微生物MBC/MBN存在显著差异,而去根处理样地的各林型的MBC/MBN没有显著差异(表3),表明和对照样地相比,去根样地内的微生物的生长方式和生存策略存在差异,与其他相关研究结果相符[32,35],但导致去根处理样地中微生物群落的组成、结构与功能发生改变的深层原因有待研究。Feng等[36]在研究生长季节期间地上和地下碳输入影响比较中,也发现根系去除使其含量发生改变。张伟东等[10]发现杉木(Cunninghamialanceolata)林根系对土壤微生物量的增长具有明显的促进作用;但是在美国和匈牙利的DIRT(detritus input and removal treatments)实验中[35],去除根系没有影响季节动态下土壤微生物量碳氮的变化。这些研究表明根系的去除对土壤微生物量的影响因所处区域和植被类型而存在差异。本研究还发现去根处理样地各林型之间的MBN无显著差异,可能与缺乏根系分泌物对土壤中N的分解作用有关[13,37]。关于在冻融期植物根系的缺失是如何引起微生物群落组成的改变,需加入微观数据来揭示其内在机制。
表 4 冻融循环期间土壤微生物量碳、氮和土壤理化性质的相关分析
Table 4 Correlation coefficients between soil microbial biomass carbon, nitrogen, soil microbial carbon/nitrogen, and soil physicochemical properties

因子Factor对照样地Control去根处理样地Rootsremoval总有机碳Totalorganiccarbon全氮Totalnitrogen含水率Soilwatercontent温度Soiltemperature总有机碳Totalorganiccarbon全氮Totalnitrogen含水率Soilwatercontent温度Soiltemperature土壤微生物量碳Soilmicrobialbiomasscar-bon-0.202**-0.193*-0.0660.211**-0.0920.1340.129-0.249**土壤微生物量氮Soilmicrobialbiomassnitrogen0.0410.09-0.0200.246**-0.0370.1430.114-0.111土壤微生物量碳氮比Soilmicrobialbiomasscarbon/nitrogen0.07-0.12-0.0260.163*-0.013-0.032-0.063-0.037
*P<0.05; **P<0.01
[1] Henry H A L. Soil freeze-thaw cycle experiments: Trends, methodological weaknesses and suggested improvements. Soil Biology and Biochemistry, 2007, 39 (5): 977- 986.
[2] Urakawa R, Shibata H, Kuroiwa M, Inagaki Y, Tateno R, Hishi T, Fukuzawa K, Hirai K, Toda H, Oyanagi N, Nakatai M, Nakanishi A, Fukushima K, Enoki T, Suwa Y. Effects of freeze-thaw cycles resulting from winter climate change on soil nitrogen cycling in ten temperate forest ecosystems throughout the Japanese archipelago. Soil Biology and Biochemistry, 2014, 74: 82- 94.
[3] Sharma S, Szele Z, Schilling R, Munch J C, Schloter M. Influence of freeze-thaw stress on the structure and function of microbial communities and denitrifying populations in soil. Applied and Environmental Microbiology, 2006, 72 (3): 2148- 2154.
[4] Tan B, Wu F, Yang W, He X H. Snow removal alters soil microbial biomass and enzyme activity in a Tibetan alpine forest. Applied Soil Ecology, 2014, 76: 34- 41.
[5] Shama V, Hussain S, Sharma K R, Arya V M. Labile carbon pools and soil organic carbon stocks in the foothill Himalayas under different land use systems. Geoderma, 2014, 232: 81- 87.
[6] Wang M, Hua C, Li Z, Lewis J B, Yu Y, Tian J, Li G, Dai L. Effect of freezing thawing on nitrogen mineralization in vegetation soils of four landscape zones of Changbai Mountain. Annals of Forest Science, 2011, 68: 943- 951.
[7] Almagro M, Martínez-Mena M. Litter decomposition rates of green manure as affected by soil erosion, transport and deposition processes, and the implications for the soil carbon balance of a rain fed olive grove under a dry Mediterranean climate. Agriculture, Ecosystems and Environment, 2014, 196: 167- 177.
[8] 何洁, 蒋先敏, 杨万勤, 倪祥银, 徐李亚, 李晗, 吴福忠. 雪被斑块对川西高山森林凋落叶N和P释放的影响. 应用生态学报, 2014, 25 (8): 2518- 2116.
[9] Schaefer D A, Feng W, Zou X. Plant carbon inputs and environmental factors strongly affect soil respiration in a subtropical forest of southwestern China. Soil Biology and Biochemistry, 2009, 41 (5): 1000- 1007.
[10] 张伟东, 汪思龙, 颜绍馗, 杨会侠, 徐广标. 杉木根系和凋落物对土壤微生物学性质的影响. 应用生态学报, 2009, 20 (10): 2345- 2350.
[11] Clemmensen K E, Bahr A, Ovaskainen O, Dahlberg A, Ekblad A, Wallander H, Stenlid J, Finlay R D, Wardle D A, Lindah B D. Roots and associated fungi drive long-term carbon sequestration in boreal forest. Science, 2013, 339(6127): 1615- 1618.
[12] Campbell J L, Socci A M, Templer P H. Increased nitrogen leaching following soil freezing is due to decreased root uptake in a northern hardwood forest. Global Change Biology, 2014, 20 (8): 2663- 2673.
[13] Landi L, Valori F, Ascher J, Renella G, Falchini L, Nannipieri P. Root exudates effects on the bacterial communities, CO2evolution, nitrogen transformations and ATP content of rhizosphere and bulk soils. Soil Biology and Biochemistry, 2006, 38 (3): 509- 516.
[14] 史宝库. 小兴安岭6种林型土壤呼吸特征. 哈尔滨:东北林业大学, 2012.
[15] Wu J, Joergensen R G, Pommerening B, Chaussod R, Brookes P C. Measurement of soil microbial biomass C by fumigation-Extraction: an automated procedure. Soil Biology and Biochemistry, 1990, 22 (8) : 1167-1169.
[16] Joergensen R G, Brookes P C. Ninhydrin-reactive nitrogen measurements of microbial biomass in 0.5 mol, K2SO4soil extracts. Soil Biology and Biochemistry, 1990, 22 (8) : 1023-1027.
[17] Brooks P D, Williams M W, Schmidt S K. Inorganic nitrogen and microbial biomass dynamics before and during spring snowmelt. Biogeochemistry, 1998, 43(1): 1- 15.
[18] Shanley J B, Chalmers A. The effect of frozen soil on snowmelt runoff at Sleepers River, Vermont. Hydrological Processes, 1999, 13(12‐13): 1843- 1857.
[19] 谭波, 吴福忠, 杨万勤, 杨玉莲, 王奥, 康丽娜. 雪被去除对川西高山森林冬季土壤温度及碳、 氮、磷动态的影响. 应用生态学报, 2011, 22(10): 2553- 2559.
[20] 任伊滨. 冻融对小兴安岭湿地土壤微生物碳氮和氮转换的影响. 哈尔滨工程大学学报, 2013, 34(4): 530- 535.
[21] Schmil J P, Billbrough C, Welker J M. Increased snow depth affects microbial activity and nitrogen mineralization in two Arctic tundra communities. Soil Biology and Biochemistry, 2004, 36 (2): 217- 227.
[22] Pregitzer K S, Burton A J, Zak D R, Talhelm A F. Simulated chronic nitrogen deposition increases carbon storage in northern temperate forests. Global Change Biology, 2008, 14 (1): 142- 153.
[23] Fitzhugh R D, Driscoll C T, Groffman P M, Tierney G L, Fahey T J, Hardy J P. Effects of soil freezing, disturbance on soil solution nitrogen, phosphorus, and carbon chemistry in a northern hardwood ecosystem. Biogeochemistry, 2001, 56 (2): 215- 238.
[24] Groffman P M, Hardy J P, Driscoll C T, Fahey T J. Snow depth, soil freezing and fluxes of carbon dioxide, nitrous oxide and methane in a northern hardwood forest. Global Change Biology, 2006, 12 (9): 1748- 1760.
[25] Warren M, Zou X M. Seasonal nitrogen retention in temperate hardwood forests: The “vernal dam” hypothesis and case studies. Acta Phytoecologica Sinica, 2003, 27(1): 11- 15.
[26] Zhang D, Zhang Y, Qu L, Ma K, Dai S. Effects of slope position on soil microbial biomass ofQuercusliaotungensisforest in Dongling Mountain. Acta Ecologica Sinica, 2012, 32(20): 6412- 6421.
[27] Santos V B, Araújo A S, Leite L F, Nunes L A, Melo W J. Soil microbial biomass and organic matter fractions during transition from conventional to organic farming systems. Geoderma, 2012, 170: 227- 231.
[28] 杨刚, 何寻阳, 王克林, 黄继山, 陈志辉, 李有志, 艾美荣. 不同植被类型对土壤微生物量碳氮及土壤呼吸的影响. 土壤通报, 2008, 39(1): 189- 191.
[29] Tierney G L, Fahey T J, Groffman P M, Hardy J P, Fitzhugh R D, Driscoll C T. Soil freezing alters fine root dynamics in a northern hardwood forest. Biogeochemistry, 2001, 56 (2): 175- 190.
[30] Larsen K S, Jonasson S, Michelsen A. Repeated freeze-thaw cycles and their effects on biological processes in two arctic ecosystem types. Applied Soil Ecology, 2002, 21 (3): 187- 195.
[31] Herrmann A, Witter E. Sources of C and N contributing to the flush in mineralization upon freeze-thaw cycles in soils. Soil Biology and Biochemistry, 2002, 34(10): 1495- 1505.
[32] Li Y, Xu M, Sun O, Cui W. Effects of root and litter exclusion on soil CO2efflux and microbial biomass in wet tropical forests. Soil Biology and Biochemistry, 2004, 36(12): 2111- 2114.
[33] Lovell R D, Jarvis S C, Bardgett R D. Soil microbial biomass and activity in long-term grassland: effect s of management changes. Soil Biology and Biochemistry, 1995, 27 (7): 969- 975.
[34] Fauci M F, Dick R P. Soil microbial dynamics: short-and long-term effects of inorganic and organic nitrogen. Soil Science Society of America Journal, 1994, 58(3): 801- 806.
[35] Brant J B, Myrold D D, Sulzman E W. Root controls on soil microbial community structure in forest soils. Oecologia, 2006, 148 (4): 650- 659.
[36] Feng W, Zou X, Schaefer D. Above- and belowground carbon inputs affect seasonal variations of soil microbial biomass in a subtropical monsoon forest of southwest China. Soil Biology and Biochemistry, 2009, 41 (5): 978- 983.
[37] 吴林坤, 林向民, 林文雄. 根系分泌物介导下植物-土壤-微生物互作关系研究进展与展望. 植物生态学报, 2014, 38 (3): 298- 310.
Effects of root resectioning on soil microbial biomass in six forest types in the Xiaoxing′an Mountains during freezing-thawing cycles
LIN Youwei, JIN Guangze*
CenterforEcologicalResearch,NortheastForestryUniversity,Harbin150040,China
Freeze-thaw cycles are the key drivers of soil carbon cycling in cold zone ecosystems. Recent theoretical and empirical work suggests that roots enhance the sequestration of soil carbon and the stability of soil microbial biomass. The rhizosphere—the layer of soil influenced by plant roots—is considerably richer in microbial diversity than the surrounding bulk soil. However, the effects of roots on microbial ecological processes and the potential mechanisms remain unclear. Investigating the effects of rhizosphere microbial changes in soils without roots in the northeast forests can therefore provide scientific support for vegetation restoration and ecological reconstruction in this region. This study focused on the changes in microbial biomass in forest soils without plant roots in the Xiaoxing′an Mountains during the freeze-thaw cycle. The experiment was conducted in six typical forest types: virgin mixed broadleaved-Korean pine (Pinuskoraiensis) forest, spruce-fir (Piceakoraiensis-Abiesnephrolepis) valley forest, secondary birch (Betulaplatyphylla) forest, Korean pine plantation, and Dahurian larch (Larixgmelinii) plantation. In 2010, we randomly selected three plots (20 m × 30 m) each of which contained three root-trenched subplots (2 m × 2 m) in each forest type. Soil samples from 0—10 cm and 10—20 cm soil layers were randomly selected weekly in the six forest types from April to May 2013 (the freeze-thaw cycle). We used trenching methods, randomly set three subplots (2 m × 2 m) without roots inside of each 20 m × 30 m plot. Furthermore, we randomly set three (2 m × 2 m) control plots; with the root resection plots about 1 m apart. We measured the variability of rhizosphere microbial biomass in different soil layers associated with six forest types during the freeze-thaw cycle. We preformed the fumigation-extraction method to collect samples, and used the Analytic Jena 3000 to analyze soil microbial carbon and nitrogen contents. We observed significant differences in soil microbial biomass and soil nutrient stability between the root resection and control plots. The microbial biomass carbon (MBC) of the root resection plots was significantly different than that of the control plots. However, no significant difference was observed in microbial biomass nitrogen (MBN) between these two treatments in each forest type (P> 0.05). In the control plots, the MBC was significantly negatively correlated with soil organic carbon, and total nitrogen (P< 0.05); MBC, MBN, and the microbial carbon and nitrogen ratio (MBC/MBN) were all significantly positively related to temperature; and soil water content between MBC, MBN, and MBC/MBN were not significantly different. In the root removal plots, MBC and soil temperature had a significant negative correlation, and the influence of soil organic carbon and total nitrogen were not significant (P> 0.05) on MBC, MBN, and MBC/MBN. Our results suggest that forest areas lacking root and soil protection would see reductions in soil MBC, and the microbial biomass sequestration in these forest soils would be negatively influenced during the freeze-thaw cycle. The capacity of rhizobacteria to metabolize carbon sources was stronger in communities associated with roots than without roots. Our results also suggest that rhizobacteria from associated species have distinct carbon metabolism characteristics.
freeze-thaw cycles; microbial biomass carbon; microbial biomass nitrogen; root resection; microbial content changes; forest soils
林业公益性行业科研专项资助项目(201204320);长江学者和创新团队发展计划(IRT_15R09)
2015- 01- 30;
日期:2016- 01- 15
10.5846/stxb201501300246
*通讯作者Corresponding author.E-mail: taxus@126.com
林尤伟,金光泽.冻融期去根处理对小兴安岭6种林型土壤微生物量的影响.生态学报,2016,36(19):6159- 6169.
Lin Y W, Jin G Z.Effects of root resectioning on soil microbial biomass in six forest types in the Xiaoxing′an Mountains during freezing-thawing cycles.Acta Ecologica Sinica,2016,36(19):6159- 6169.

