谢尔宾斯基三角分形结构的STM研究
顾高臣李 娜张 雪侯士敏,*王永锋,2,*吴 凯
(1北京大学电子系,纳米器件物理与化学教育部重点实验室,北京 100871;2北京大学(天津滨海)新一代信息技术研究院,天津 300457;3北京大学化学与分子工程学院,北京分子科学国家实验室,北京 100871)
谢尔宾斯基三角分形结构的STM研究
顾高臣1李 娜1张 雪1侯士敏1,*王永锋1,2,*吴 凯3,*
(1北京大学电子系,纳米器件物理与化学教育部重点实验室,北京 100871;2北京大学(天津滨海)新一代信息技术研究院,天津 300457;3北京大学化学与分子工程学院,北京分子科学国家实验室,北京 100871)
分形结构因其特殊的数学和美学意义受到科学家们长期以来的广泛关注。化学家更是试图利用共价键和配位键等来合成各类分子分形结构,但由于溶解性的限制,始终无法实现高级别、无缺陷的分子分形结构的构筑。最近我们采用超高真空表面制备方法,成功获得了基于卤键与配位键的谢尔宾斯基三角分形结构,并使用扫描隧道显微镜(STM)对其生长机制进行了研究。4,4′′-二溴-1,1′:3′,1′:4′,1′′-四联苯分子在Ag(111)表面通过自组装形成了一系列无缺陷卤键分形结构。由于卤键作用较弱,该结构只能稳定在液氮温度以下。在Au(111)表面共沉积4,4′-二氰基-1,1′:3′,1′-三联苯分子与铁原子可以制备出更稳定的配位分形结构。密度泛函理论计算揭示了分形结构的成像机制。蒙特卡洛计算表明,表面三节点的形成对谢尔宾斯基三角分形结构的生长具有重要意义。
分形;谢尔宾斯基三角形;分子自组装;表面科学;扫描隧道显微镜
1 引 言
小到雪花,大到土星环,分形结构广泛存在于自然界内,它们具有自相似性质和非整数维度填充空间的形态特征1。对其研究于美学、数学、自然科学、工程技术都具有非常重要的意义。因此,分形结构的制备得到了科学界的广泛关注。人们已经在溶液中合成了少量的分形体,但是由于溶解性差等因素限制,通过液相方法尚未实现高级别的、无缺陷的分子分形结构的制备2–7。谢尔宾斯基三角形(ST)是一种典型的分形结构,由波兰数学家谢尔宾斯基在1915年提出。理论预言,这种形式的分子结构有非常奇特的力学、电学、磁学和光学等方面的功能8,9。最近我们采用超高真空表面制备方法,成功获得了基于卤键与配位键的ST分形结构,并使用扫描隧道显微镜对其生长机制进行了研究10,11。过去表面制备的树枝状分形结构通常热稳定性差,经过退火之后会聚集成岛,而我们制备的这种有序分形结构退火后仍保持分形状态。
实验中我们使用的衬底是Ag(111)与Au(111)单晶表面,它们具有与ST一样的三重旋转对称性,有利于生长分形结构。要满足ST结构要求,采用的分子需为骨架角度为120°的折线形小分子,并且两端的官能团要以环三键方式链接。基于这样的考虑,我们设计并合成了4,4′′-二溴-1,1′:3′,1′:4′,1′′-四联苯(B4PB)和4,4′-二氰基-1,1′:3′,1′-三联苯(C3PC),它们的化学结构图如图1所示。利用B4PB分子之间的卤键与氢键的协同作用以及C3PC分子与过渡金属原子Fe之间的配位键相互作用,我们制备了一系列ST分形结构10,11。实验中样品制备是在超高真空系统中完成的,表征手段为扫描隧道显微镜(STM)。
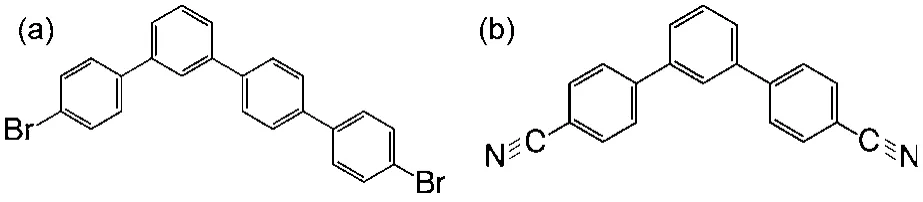
图1 B4PB (a)与C3PC (b)分子结构示意图Fig.1 Structure diagrams of B4PB (a) and C3PC (b)molecules
2 基于卤键的谢尔宾斯基三角分形结构
B4PB分子从温度为363 K的钽舟中热蒸发到处于室温的Ag(111)单晶表面后,将样品传入低温STM中,待温度稳定后进行扫描,观察到样品表面为一系列不同尺寸的等边三角形结构所覆盖10。这一系列结构与谢尔宾斯基三角的分形原型(图2(a))非常相似。因此,本文将它们记作B4PB-ST-n(n = 0, 1, 2, 3, 4) (图2(b)),更高级数的ST结构尚未观察到。从示意图可以看出,高级数三角形由三个全等的次级三角形堆砌而成,并在结构中央围出一个(倒)三角形孔,这些次级结构也依照同样的规律构成,从而形成一系列尺寸呈指数规律变化的三角形分子组装结构和三角形孔,并且结构本身具有三重旋转对称性。实验图像的三角形的边由分子组成,而它的顶点则是由三个分子的环卤键组成的结点。这种与理想的顶点和线的差异使得其豪斯多夫维数与理论值(1.59)略有偏差,约为1.68。
B4PB分子的投影长度大约1.55 nm,每个ST-n结构的边长约为2n+2nm,由3个ST-(n – 1)次级结构构成,次级结构呈“品”字型排列、两两之间以一个B4PB桥接,因此每个ST-n包含Tn个B4PB分子(式(1),

组成结构的分子数目在图2(b)每张STM图像的右上角标出。例如,B4PB-ST-3结构边长约为23+2nm = 32 nm,共由(33+2+ 3)/2 = 123个B4PB分子组成。此外,每个ST-n结构还包括(3n+1– 1)/2个由B4PB分子围成的三角形孔,其中第m级孔的数目为3n–m(m = 0, 1, ··, n)个,尺寸约为2m+1nm。
生长动力学过程的控制对晶体的高级数ST分形结构的形成具有重要的作用。对覆盖度约为0.17ML(monolayer)的样品进行一系列对照实验表明,样品降温速率越低,参与形成高级数分形结构(如B4PB-ST-3)的分子比例越大(图3)。例如,样品温度从室温迅速下降到液氦温度(4 K),降温速率约为13 K·min–1,那么此条件下得到的样品只有不足5%的分子参与形成B4PB-ST-3结构(图3(a)。而对同一个样品,以0.02 K·min–1的极低降温速率通过温度窗口,那么便可以成功制备由B4PB-ST-3结构主导的样品(图3(e))。此时,参与形成B4PB-ST-3结构的分子比例高达55%以上(图3(f))。特别地,在该样品上还得到了更高级但尚未完全形成的B4PB-ST-4结构(图3(e)),这显示了基于分子间弱相互作用的可逆和可控分子自组装方法的进一步调控,可能得到更高级数的ST分形结构。
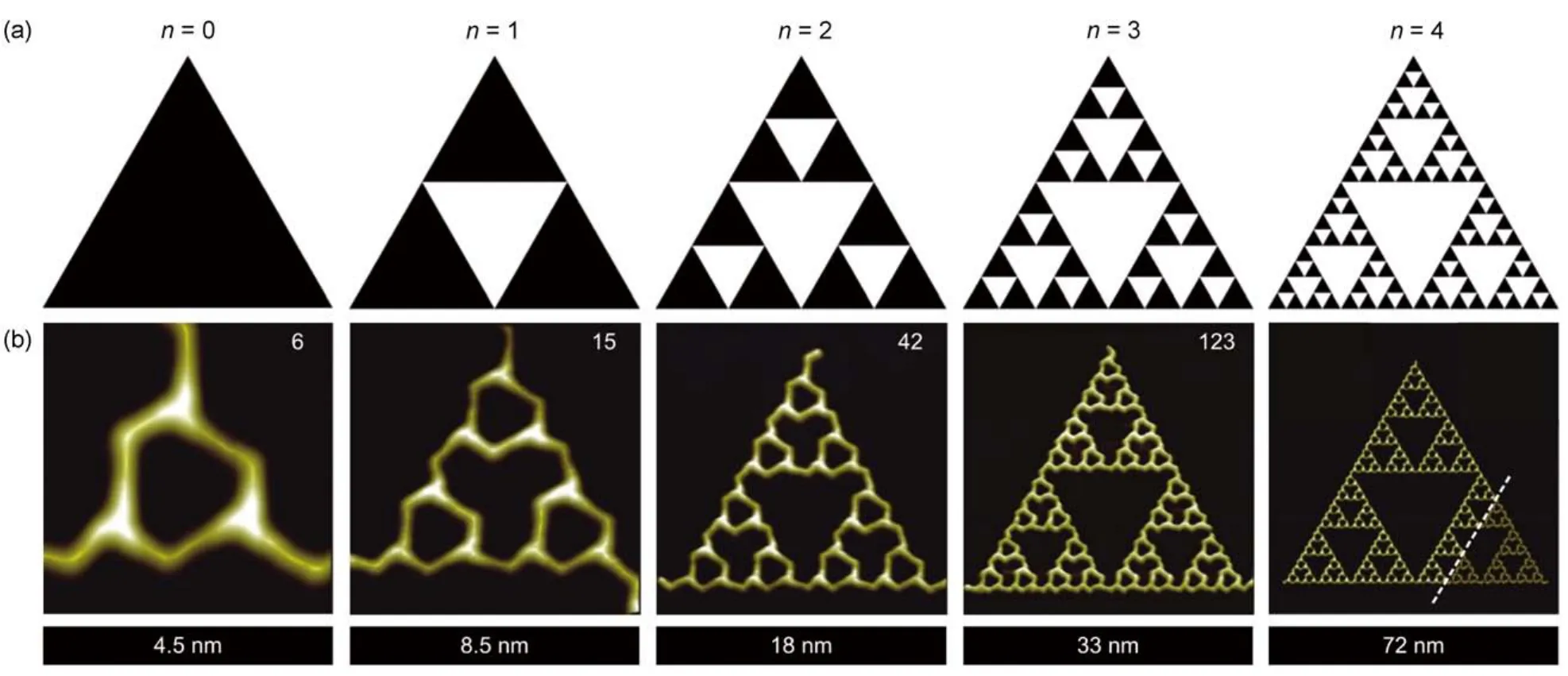
图2 所有不同级数的基于B4PB分子的ST结构10Fig.2 The whole family of the observed B4PB molecular ST structures10
3 金属有机配位的谢尔宾斯基三角分形结构
由于B4PB分子间卤键的相互作用较弱,上述ST分形结构只能稳定于液氮温度以下。为了提高稳定性,需要更强的分子间相互作用存在,同时如果分子之间的作用力太强,会降低分形结构的可逆性,使其中的缺陷不易修复,不利于高级数分形结构的制备。综合以上考虑,我们设计了氰基为取代基的分子C3PC(图1b),通过其与Fe原子之间的配位相互作用,我们制备了室温稳定的ST分形结构。同时由于金属原子的引入,使得它在分子的分离、筛选、以及反应催化领域的应用成为可能12–19。
配位ST分形结构也是采用真空表面制备方法获得的。先后将C3PC分子和铁原子热蒸发到干净的Au(111)表面,之后将样品在大约373 K的温度退火0.5 h,使得金属和分子充分迁移和配位,最后将样品转移到低温STM腔内进行STM表征11。
对于任意的Fe-ST-n分形结构,其所包含的分子数(Mn)和原子数(An)分别为:
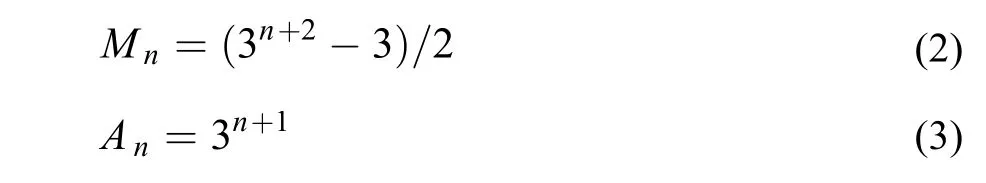
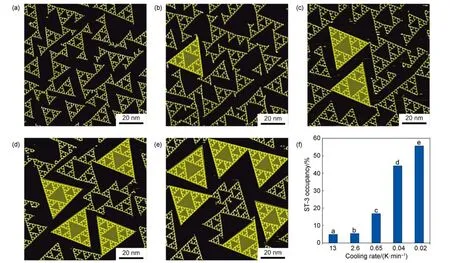
图3 B4PB-ST-3生长动力学过程的调控与优化10Fig.3 Adjustment and optimization of growth kinetics of the B4PB-ST-310
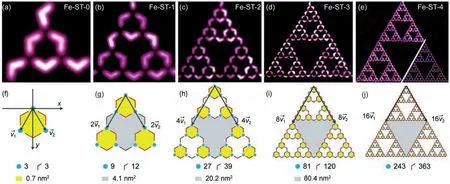
图4 铁原子和C3PC分子配位后形成的一系列ST结构11Fign.41 Thne 2whole family of ST structures constructed by Fe and C3PC molecule11
这两个数字以及每个ST中的最大孔的面积都标记于图4中。特别需要指出的是,用这种方法得到的分形结构中的磁原子数目可以精确调控,分别为3、9、27与81。采用传统的溶液合成方法,得到含3或9个金属原子的分子是比较容易实现的,但要制备含有27或者81个金属原子的分子是有很大难度的。所以,通过生长分形结构的方法,我们可以制备具有幻数磁原子数目的分子,这对于系统研究金属原子之间的自旋耦合奠定了基础。为了进一步简化ST的结构,了解它的拼接规则,可以将C3PC分子简化为一条120°的折线。假设一个蓝色的圆圈代表一个金属原子,最多与3条折线相连。由此每个ST-n能够由3个低一级的ST-(n – 1)和3个辅助分子(紫色)构成。三个低一级的ST-(n – 1)中的一个固定,另外两个分别按照和进行平移。其中两个大小相等,方向相差60°。然后再将3个辅助分子加入其中,从而实现低级别的三角形三个顶点的饱和配位。
在STM图像中(图4),我们只看到参与配位的分子,并没有看到铁原子。为了阐明其机制,我们对这个体系进行了包含范德华力的密度泛函理论(DFT)方法计算。图5(a)是Au(111)表面上一个Fe原子与三个C3PC分子组成的配位基元优化后的结构俯视图。由于Au表面的重构过于复杂,体系过于庞大,之前对于其DFT计算都不考虑鱼骨重构,其正确性也获得了实验验证。我们这里也采用了类似方法,从优化结构可以看出Fe原子吸附于fcc位,另外,Fe-N的键长约为0.188 nm,与之前文献中的计算结果相同20。从侧视图(图5(b)可以看出,Fe原子相对于C3PC分子距离针尖更远,这样在成像的过程中,Fe原子波函数与针尖波函数不易交叠,这很可能是我们没有看到Fe原子的原因。超高真空中有一氧化碳,氢气,水等残余气体,在偶然的情况下,这些气体分子会吸附在针尖顶部,这样的修饰针尖在成像中可以与Fe原子靠的很近,增强波函数交叠,从而使我们可以看到铁原子(图5(c))。这也证实了我们看到的分形结构确实是靠配位键来稳定的。
最近的蒙特卡罗模拟21,22和上面的实验都表明,形成分子谢尔宾斯基三角需要两个必要条件,分子具有120°的骨架结构并且顶点和分子的连接数为3。对于直线分子的组装,无论是利用环卤键,还是金属有机配位,都只能得到二维的孔状的网格23–25。另外的影响因素还包括衬底的三重对称性。它在分子之间的相互作用比较弱的时候,是一个非常重要的因素。将B4PB分子沉积于四重对称性的Ag(100)表面,就无法获得分形结构10。但是当分子之间的相互作用特别强时,这个因素的影响可能就没有那么明显,这个现象有待于实验的进一步验证。当120°骨架分子与顶点的连接数为2或4时,分子会在表面形成常规晶体。当连接数为3与4共存的时候,就可能实现分形结构与传统晶体的共存,这在最近的实验中得到验证。120°端羟基分子通过氢键可以形成三聚体与四聚体,两者能量相近,前者倾向于形成谢尔宾斯基三角分形结构,后者倾向于形成二维晶体,故可以在表面观测到分形与晶体的共存,从而通过改变基底、覆盖度与分子结构,得以实现二者的竞争调控26。
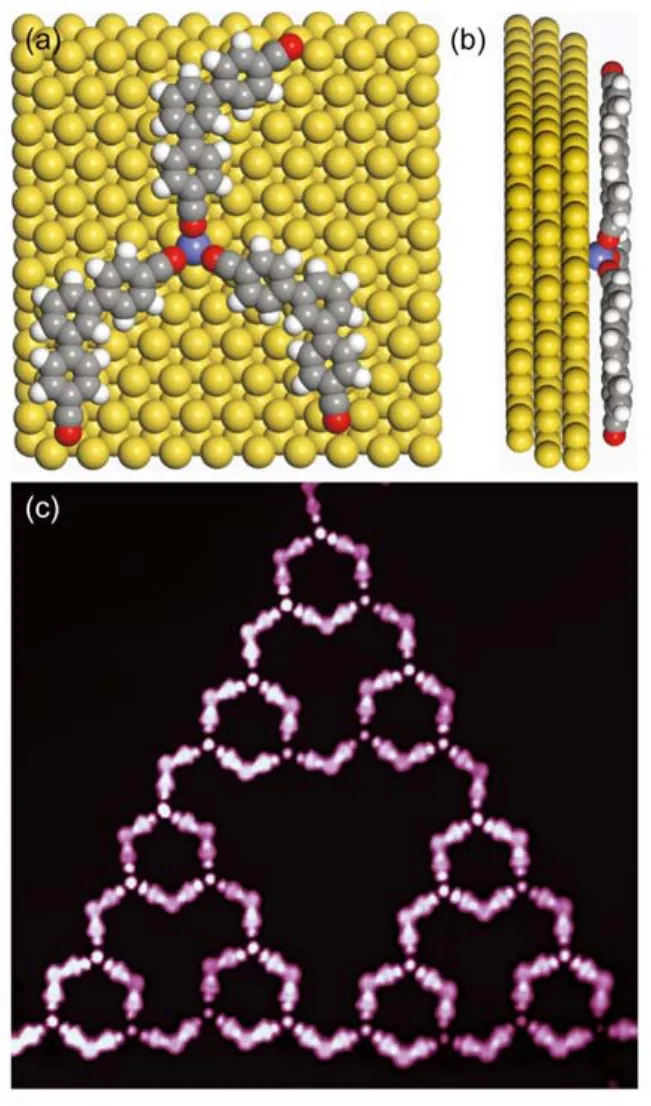
图5 Au(111)表面上由一个铁原子和三个C3PC分子组成的结构优化的模型图和Fe-ST-2的高分辨STM图11Fig.5 Optimized structures comprising one Fe atom and three C3PC molecules on Au(111) surface and high resolution image of Fe-ST-211
4 结 论
综上,我们利用卤键和金属有机配位键在金属表面构筑了一系列谢尔宾斯基三角分形结构。制备这种分形结构的两个必要条件分别是分子骨架120°和顶点分子连接数为3。除此之外,还有衬底对称性、分子和分子之间的相互作用、表面覆盖度、温度窗口等也会对分形结构生长产生影响。我们制备的分形结构具有热稳定性与宏观整体对称性。目前我们对其生长机制,物理性质,潜在应用等的认识都处于初步阶段,需要进一步结合高精密实验与理论计算进行更深入的研究。
(1)Mandelbrot, B. B. The Fractal Geometry of Nature; Freeman, W. H. Company: New York, 1982; pp 1–495.
(2)Newkome, G. R.; Shreiner, C. Chem. Rev. 2010, 110, 6338. doi: 10.1021/cr900341m
从麻疹监测信息报告管理系统可见,285份IgM抗体阳性病例中,214例有病例信息,其中只有29例有免疫史,高达61.68%的病例无免疫接种史,无免疫史的病例中,8月~6岁组病例占53.03%(70/132),且均为非本县区户籍,这充分说明本地区麻疹免疫工作还存在较大漏洞,特别是对外来人口的免疫接种工作,应该要加强对6岁以内儿童和22岁以上青年的麻疹免疫接种和信息管理工作,消除免疫空白地带,为早日实现消除麻疹的目标打下坚实的基础。
(3)Sugiura, K. I.; Tanaka, H.; Matsumoto, T.; Kawai, T.; Sakata, Y. Chem. Lett. 1999, 28, 1193.
(4)Newkome, G. R.; Wang, P.; Moorefield, C. N.; Cho, T. J.;Mohapatra, P. P.; Li, S.; Hwang, S. H.; Lukoyanova, O.;Echegoyen, L.; Palagallo, J. A.; lancu, V.; Hla, S. W. Science 2006, 312, 1782. doi: 10.1126/science.1125894
(5)Fujibayashi, K.; Hariadi, R.; Park, S. H.; Winfree, E.; Murata, S. Nano Lett. 2008, 8, 1791. doi: 10.1021/nl0722830
(6)Sarkar, R.; Guo, K.; Moorefield, C. N.; Saunders, M. J.;Wesdemiotis, C.; Newkome, G. R. Angew. Chem. Int. Edit. 2014,53, 12182 doi: 10.1002/anie.201407285
(7)Wang, M.; Wang, C.; Hao, X. Q.; Liu, J.; Li, X.; Xu, C.; Lopez, A.; Sun, L.; Song, M. P.; Yang, H. B.; Li, X. J. Am. Chem. Soc. 2014, 136, 6664. doi: 10.1021/ja501417g
(8)Wang, A.; Zhao, M. Phys. Chem. Chem. Phys. 2015, 17, 21837. doi: 10.1039/C5CP03060A
(9)van Veen, E.; Tomadin, A.; Katsnelson, M. I. ; Yuan, S.; Polini, M. arXiv: 1504.00628.
(10)Shang, J.; Wang, Y.; Chen, M.; Dai, J.; Zhou, X.; Kuttner, J.;Hilt, G.; Shao, X.; Gottfried, J. M.; Wu, K. Nat. Chem. 2015, 7, 389. doi: 10.1038/nchem.2211
(12)Chui, S. S. Y.; Lo, S. M. F.; Charmant, J. P. H.; Guy Orpen, A.;Williams, I. D. Science 1999, 283, 1148. doi: 10.1126/science.283.5405.1148
(13)Li, H.; Eddaoudi, M.; O'Keeffe, M.; Yaghi, O. M. Nature 1999,402, 276. doi: 10.1038/46248
(14)Wilmer, C. E.; Leaf, M.; Lee, C. Y.; Farha, O. K.; Hauser, B. G.;Hupp, J. T.; Snurr, R. Q. Nat. Chem. 2012, 4, 83.
(15)Bloch, E. D.; Queen, W. L.; Krishna, R.; Zadrozny, J. M.;Brown, C. M.; Long, J. R. Science 2012, 335, 1606. doi: 10.1126/science.1217544
(16)Herm, Z. R.; Wiers, B. M.; Mason, J. A.; van Baten, J. M.;Hudson, M. R.; Zajdel, P.; Brown, C. M.; Masciocchi, N.;Krishina, R.; Long, J. R. Science 2013, 340, 960. doi: 10.1126/science.1234071
(17)Inokuma, Y.; Yoshioka, S.; Ariyoshi, J.; Arai, T.; Hitora, Y.;Takada, K.; Matsunaga, S.; Rissanen, K.; Fujita, M. Nature 2013,495, 461. doi: 10.1038/nature11990
(18)Furukawa, H.; Cordova, K. E.; O'Keeffe, M.; Yaghi, O. M. Science 2013, 341, 1230444. doi: 10.1126/science.1230444
(19)Deria, P.; Mondloch, J. E.; Karagiaridi, O.; Bury, W.; Hupp, J. T.; Farha, O. K. Chem. Soc. Rev. 2014, 43, 5896. doi: 10.1039/C4CS00067F
(20)Vargas, A.; Krivokapic, I.; Hauser, A.; Daku, L. M. L. Phys. Chem. Chem. Phys. 2013, 15, 3752.
(21)Nieckarz, D.; Szabelski, P. J. Phys. Chem. C 2013, 117, 11229.
(22)Nieckarz, D.; Szabelski, P. Chem. Commun. 2014, 50, 6843. doi: 10.1039/c4cc01344a
(23)Stepanow, S.; Lin, N.; Payer, D.; Schlickum, U.; Klappenberger, F.; Zoppellaro, G.; Ruben, M.; Brune, H.; Barth, J. V.; Kern, K. Angew. Chem. Int. Edit. 2007, 46, 710.
(24)Schlickum, U.; Decker, R.; Klappenberger, F.; Zoppellaro, G.;Klyatskaya, S.; Ruben, M.; Silanes, I.; Arnau, A.; Kern, K.;Brune, H.; Barth, J. V. Nano Lett. 2007, 7, 3813. doi: 10.1021/nl072466m
(25)Schlickum, U.; Klappenberger, F.; Decker, R.; Zoppellaro, G.;Klyatskaya, S.; Ruben, M.; Kern, K.; Brune, H.; Barth, J. V. J. Phys. Chem. C 2010, 114, 15602. doi: 10.1021/jp104518h
(26)Zhang, X.; Li, N.; Gu, G. C.; Wang, H.; Nieckarz, D.; Szabelski, P.; He, Y.; Wang, Y.; Xie, C.; Shen, Z. Y.; Lü, J. T.; Tang, H.;Peng, L. M.; Hou, S. M.; Wu, K.; Wang, Y. F. ACS Nano 2015,doi: 10.1021/acsnano.5b04427
Sierpiński Triangle Fractal Structures Investigated by STM
GU Gao-Chen1LI Na1ZHANG Xue1HOU Shi-Min1,*WANG Yong-Feng1,2,*WU Kai3,*
(1Key Laboratory for the Physics and Chemistry of Nanodevices, Department of Electronics, Peking University, Beijing 100871, P. R. China;2Beida Information Research (BIR), Tianjin 300457, P. R. China;3Beijing National Laboratory for Molecular Sciences, College of Chemistry and Molecular Engineering, Peking University, Beijing 100871, P. R. China)
Self-similar fractals haνe been extensiνely inνestigated because of their importance in mathematics and aesthetics. Chemists haνe attempted to synthesize νarious molecular fractal structures through sophisticated design. But because of poor solubility, synthesis of defect-free fractals with large sizes in solution usually proνes difficult. Recently, we reported the formation of extended and defect-free Sierpiński triangle fractals by halogen or coordination bonds on surfaces under ultrahigh νacuum conditions. Their growth mechanism has been systematically studied by scanning tunneling microscopy. Using 4,4′′-dibromo-1,1′:3′,1′:4′,1′′-quaterphenyl molecules, a series of Sierpiński triangles were successfully prepared on Ag(111)through self-assembly. A slow cooling rate is crucial for growing fractals of higher order. These fractals are only obserνed below liquid-nitrogen temperature because of the weak interactions in halogen bonds. More stable metal-organic Sierpiński triangles were fabricated by depositing 4,4″-dicyano-1,1′:3′,1″-terphenyl molecules and Fe atoms on Au(111) and annealing at around 100 °C for 10 min. The fractals are stabilizedthrough coordination interaction between Fe atoms and N atoms in molecules. Density functional theory calculations reνealed their imaging mechanism. Monte Carlo simulations displayed the formation process of surface-supported fractal structures. Three-fold nodes are belieνed to dominate the structure formation of Sierpiński triangles.
Fractal; Sierpiński triangles; Self-assembly; Surface science; Scanning tunneling microscopy
O647
10.3866/PKU.WHXB201511261
Received: October 27, 2015; Revised; November 26, 2015; Published on Web: November 26, 2015.
*Corresponding authors. WANG Yong-Feng, Email: yongfengwang@pku.edu.cn; Tel: +86-10-62762722. HOU Shi-Min,
Email: smhou@pku.edu.cn; Tel: +86-10-62762722. WU Kai, Email: kaiwu@pku.edu.cn; Tel: +86-10-62754005.
The project was supported by the National Natural Science Foundation of China (21522301, 21373020, 21403008, 61321001, 21433011, 21133001, 913000002), National Key Basic Research Program of China (973) (2014CB239302, 2013CB933404, 2011CB808702), and Specialized Research
Fund for the Doctoral Program of Higher Education, China (20130001110029).
国家自然科学基金(21522301, 21373020, 21403008, 61321001, 21433011, 21133001, 913000002), 国家重点基础研究发展规划项目(973)
(2014CB239302, 2013CB933404, 2011CB808702)及高等学校博士学科点专项科研基金(20130001110029)资助
©Editorial office of Acta Physico-Chimica Sinica

