脑蛋白水解物的提取工艺优化
黄 洁,王孝功,单 敏,田福元(.西安市食品药品检验所,西安 70054;.西安迪赛生物药业有限责任公司,西安 7006;.陕西万信医药采购供应站,陕西咸阳 70065)
脑蛋白水解物的提取工艺优化
黄洁1*,王孝功2,单敏1,田福元3(1.西安市食品药品检验所,西安710054;2.西安迪赛生物药业有限责任公司,西安710016;3.陕西万信医药采购供应站,陕西咸阳710065)
目的:优化脑蛋白水解物的提取工艺。方法:以pH约为9的碱性提取液进行提取;以总氮含量、与脑蛋白水解物(丽珠赛乐)肽图的相似度的综合评分为指标,通过L9(34)正交试验优化猪脑(1 kg)水解工艺中胰蛋白酶的加入量、胃蛋白酶的加入量及水解时间,并进行工艺验证试验。结果:最优提取工艺为胰蛋白酶加入量8 g、胃蛋白酶加入量5 g、水解时间12 h;验证试验中所制脑蛋白水解物的总氮含量分别为5.20、5.18、5.20 mg/ml(RSD=2.22%,n=3),肽图相似度分别为93%、94%、96%(RSD=1.62%,n=3),综合评分分别为0.911、0.917、0.932(RSD=1.18%,n=3)。结论:优化的生产工艺合理、提取效率高,产物肽图相似度高。
脑蛋白水解物;提取工艺;正交试验;总氮含量;肽图相似度
脑蛋白水解物注射液是一种猪脑蛋白水解提取物,为多种游离氨基酸和低分子肽的混合注射液,是一种神经保护剂。其具有神经营养和神经保护的类似神经生长因子的作用[1],主要用于治疗颅脑外伤及脑血管病等引起的记忆力减退及注意力集中障碍,辅助治疗脑功能不全,也用于治疗神经衰弱、蛋白质缺乏及蛋白质消化吸收障碍等[2]。本文以总氮含量和与脑蛋白水解物(丽珠赛乐)肽图的相似度为指标,优化了从猪脑中提取脑蛋白水解物的工艺,以期建立一种重现性好、脑蛋白水解物活性更高的生产工艺。
1 材料
1.1仪器
1260型高效液相色谱仪(美国Agilent公司);MK3型酶标仪(美国Thermo公司);DK-S420型电热恒温水箱(上海慕航仪器设备有限公司);Pall minimate超滤系统(美国Pall公司);L-600型离心机(湘仪离心机仪器有限公司,离心半径:16 cm);DS-1型组织粉碎机(上海比朗仪器有限公司)。
1.2药品与试剂
脑蛋白水解物注射液(商品名:丽珠赛乐,丽珠集团丽珠制药厂,批号:20140809321,规格:5 ml/支);胰蛋白酶(批号:141043,活性:>2 500 U/mg)、胃蛋白酶(批号:140821,活性:>3 800 U/mg)均购自四川德博尔制药有限公司;乙腈为色谱纯;乙醇、盐酸、氢氧化钠、三氟乙酸均为分析纯。
1.3其他
猪脑(方欣肉联厂)。
2 方法与结果
2.1滴定法测定总氮含量
参照注射用脑蛋白水解物征求意见稿[3],取脑蛋白水解物,加水稀释至适宜浓度,作为供试品溶液,依法测定[4]。精密量取供试品溶液约2 ml,置于烧瓶中,加入硫酸铜试液2滴,再加入浓硫酸5 ml,小火消化4 h,放冷。全部转移至蒸馏瓶中,加入40%氢氧化钠溶液10 ml。取2%硼酸溶液10 ml,置于100 ml锥形瓶中,加甲基红-溴甲酚绿混合指示液5滴,将冷凝管尖端插入液面下,加热,进行蒸汽蒸馏,至硼酸溶液开始由酒红色变为蓝绿色时起,继续蒸馏约10 min后,将冷凝管尖端提出液面,使蒸汽继续冲洗约1 min,用水淋洗尖端后停止蒸馏。馏出液用硫酸滴定液(0.005 mol/L)滴定至溶液由蓝绿色变为灰紫色,并将滴定的结果用空白试验校正。每1 ml硫酸滴定液(0.005mol/L)相当于0.1401mg的氮。
2.2高效液相色谱法测定脑蛋白水解物的条件
参照注射用脑蛋白水解物征求意见稿[3],精密取丽珠赛乐适量,加水溶解并稀释制成每1 ml中约含总氮6 mg的溶液,作为对照品溶液。色谱条件:C18(250 mm×4 mm,5 μm),以0.1%三氟醋酸溶液为流动相A,0.085%三氟醋酸乙腈溶液-0.1%三氟醋酸溶液(80∶20)为流动相B,梯度洗脱,流速为0.8 ml/min,检测波长为276 nm,进样量为20 μl。精密量取供试品或对照品溶液各20 μl,分别注入液相色谱仪,记录色谱图,以中药指纹图谱相似度评价系统[4]考察其相似度。梯度洗脱程序见表1。

表1 梯度洗脱程序Tab 1 Conditions of gradient elution
2.3以总氮含量和肽图相似度为指标筛选脑蛋白水解物提取试剂
按照猪脑-提取试剂1∶3的比例向猪脑中分别加入pH约为3~4的盐酸溶液(酸性提取试剂)、pH近中性的纯化水(中性提取试剂)及pH约为9的氢氧化钠溶液(碱性提取试剂),于37水浴孵化30 min,4 000 r/min(离心半径为16 cm)离心20 min,取上清液。
2.3.1总氮含量按“2.1”项下方法分别测定经酸性、中性、碱性提取试剂提取后的上清液中的总氮含量。结果分别为1.16、4.98、5.21 mg/ml,表明碱性提取试剂提取的上清液中总氮含量最高。
2.3.2肽图相似度按“2.2”项下方法分别测定酸性、中性、碱性提取试剂提取后的上清液和丽珠赛乐的高效液相色谱图,色谱图见图1。

图1 高效液相色谱图Fig 1 HPLC chromatograms
经中药指纹图谱相似度评价系统评价,酸性、中性、碱性提取试剂提取后的上清液与丽珠赛乐的相似度分别为8%、9%、13%,表明碱性条件下相似度最高。最终确定提取试剂为pH约为9的氢氧化钠溶液。
2.4正交试验优化脑蛋白水解物提取工艺
2.4.1因素与水平的确定为了进一步提高提取后上清液中总氮含量,将提取后上清液分别采用胰蛋白酶、胃蛋白酶水解一定时间。取提取后的上清液用氢氧化钠溶液调pH为8.5~9.5,加入胰蛋白酶水解t1时间,再用稀盐酸调节pH至1~2,加入胃蛋白酶水解t2时间。胰蛋白酶和胃蛋白酶水解总时间(t1+ t2)即水解时间,t1∶t2=3∶1。采用L9(34)正交试验优化猪脑(1 kg)水解工艺中胰蛋白酶的加入量(A,g)、胃蛋白酶的加入量(B,g)及水解时间(C,h),因素与水平见表2。

表2 因素与水平Tab 2 Factors and levels
2.4.2正交试验设计与结果根据“2.4.1”项下因素与水平,以总氮含量与丽珠赛乐肽图的相似度的综合评分为指标优化提取工艺,其中总氮含量权重占30%,相似度权重占70%。将含总氮6 mg/ml作为1,测定出的总氮含量按此标准换算并乘以权重占有比例即为总氮的分值。将肽图输入中药指纹图谱相似度评价系统,给出的相似度作为肽图的分值,乘以权重占有比例即为肽图的分值。2项分值之和即为综合评分结果。正交试验设计与结果见表3,方差分析结果见表4。
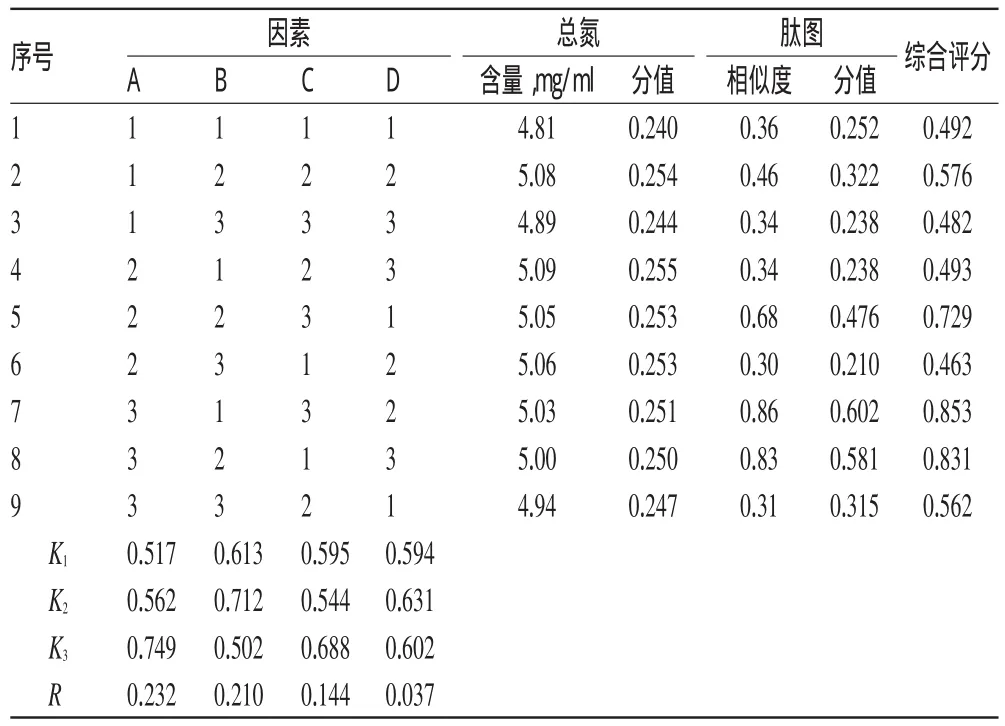
表3 正交试验设计与结果Tab 3 Orthogonal design and results

表4 方差分析结果Tab 4 Result of variance analysis
由表3和表4可知,3因素对综合评分影响的强弱依次为A>B>C,其中A和B对综合评分有显著影响(P<0.05)。综合考虑,最优提取工艺为A3B2C3,即猪脑(1 kg)水解工艺中胰蛋白酶加入8g、胃蛋白酶加入5g、水解时间12h。
2.4.3验证试验按照最优提取工艺提取猪脑蛋白水解物,重复试验3次,分别测定提取液中总氮含量,比较与丽珠赛乐肽图的相似度,计算综合评分。结果平均总氮含量为5.19 mg/ml(RSD=2.22%,n=3),平均肽图相似度为94.33%(RSD=1.62%,n=3),平均综合评分为0.92(RSD=1.18%,n=3)。验证试验结果见表5。
2.5纯化工艺
脑蛋白水解物提取液首先采用5 kDa超滤膜包超滤,收集透过液后进一步层析柱纯化。首先采用反相色谱,C8柱(250 mm×21.2 mm,10 μm),以0.1%三氟醋酸溶液为流动相A,0.085%三氟醋酸乙醇溶液-0.1%三氟醋酸溶液(85∶15)为流动相B(先以B相流洗2个柱体积,再以A相平衡5个柱体积,上样,A相流洗约2个柱体积,12%B洗脱约1.5个柱体积,洗脱峰丢弃,35%B相洗脱约2个柱体积,收集洗脱峰),流速为100 ml/min。收集的洗脱液继续采用G25层析柱进行脱盐,先用流动相注射用水平衡色谱柱约10个柱体积,上样,继续用注射用水流洗,收集色谱峰,即为脑蛋白水解物提取液样品。测定其总氮含量并与丽珠赛乐肽图进行比较,结果,总氮含量为10.52 mg/ml(RSD=1.1%,n=3),肽图相似度均大于95%。

表5 验证试验结果Tab 5 Results of verification test
2.6脑蛋白水解物活力的比较
参照注射用脑蛋白水解物征求意见稿[3]进行测定。比较丽珠赛乐与按本文方法制备的3批脑蛋白水解物的活力,结果进行配对t检验。结果显示,上述脑蛋白水解物的活力分别为(57.96±4.44)%、(95.77±7.09)%、(97.23±8.08)%、(92.51± 6.74)%,与丽珠赛乐比较的P均小于0.05,表明本文方法制备的脑蛋白水解物的活力更高。
3 讨论
脑蛋白水解物注射液是以新鲜的猪脑为原料,经过提取、酶解、超滤等过程制成的无菌制剂,主要成分为脑神经肽、各种氨基酸,临床上主要用于颅脑损伤、脑血管后遗症状的改善等,疗效确切,临床应用广泛[5-6]。原国家食品药品监督管理局于2008年12月15日发布的《关于加强脑蛋白水解物注射液监督检查的通知》(国食药监办〔2008〕734号)[7]指出在全国开展的注射剂类药品生产工艺和处方核查工作中发现,脑蛋白水解物注射剂在药品标准和执行工艺处方等方面存在着较为突出的问题,主要是企业选用猪脑原料的质量标准不完善;企业之间现行生产工艺差别较大;猪脑水解所用的蛋白酶种类、酶量及水解温度、时间等不一致,甚至有补加氨基酸的行为。这些行为大大降低了脑蛋白水解物注射液的疗效,同时导致不良反应大大增加[8]。本研究以丽珠赛乐作为对照品,以肽图相似度、总氮含量为指标,通过对提取试剂的选取、水解工艺的优化,结合层析工艺,生产出了比丽珠赛乐总氮含量更高、活力更强的脑蛋白水解物。连续3次的中试生产表明,本工艺稳定可控,可以用于脑蛋白水解物的生产。
与采用超滤工艺的常规脑蛋白水解物的生产工艺相比,本研究在超滤工艺的基础上增加了层析工艺。层析工艺一般多用于基因工程产品,如蛋白质及多肽、疫苗等的纯化,用于去除杂质、内毒素、病毒等,具有操作条件温和、效率高、重现性好的特点。常用的层析工艺包括离子离子交换色谱(IEC)、反相液相色谱、亲和色谱(Affinity chromatography)、凝胶过滤色谱(Gel filtration chromatography)等。生化药大多来源于新鲜的动物脏器,有效成分复杂。根据生化药的这个特点,结合脑蛋白注射液的质量研究标准征求意见稿,本研究优选采用反相液相色谱和凝胶过滤色谱。根据多肽、氨基酸等的疏水性,以C8(250 mm×21.2 mm,10 μm)制备色谱柱首先纯化出具有生物活性的脑蛋白产品,然后进一步采用G25进行凝胶层析,不但可以去除反相液相色谱中引入的有机试剂,同时也去除了原料及前述操作过程中可能引入的内毒素等物质,进一步提升了产品的安全性。相比生化药生产常用的超滤过程,本操作虽然具有使用成本高的缺点,但其生产的产品具有均一性好、各成分相对恒定的特点,为脑蛋白水解物的质量控制及有效性的进一步研究打下了坚实基础,为规范脑蛋白水解物注射液的生产工艺奠定了基础。
[1]于秀军,楯林義孝,郭力.脑蛋白水解物注射液对NG2蛋白聚糖阳性神经祖细胞分化的影响[J].脑与神经疾病杂志,2010,18(1):21.
[2]邓锋,梁蔚阳.氨基酸分析法测定脑蛋白水解物注射液中肽的含量[J].药物分析杂志,2010,30(10):2001.
[3]国家药典委员会.关于注射用脑蛋白水解物国家标准的公示[ED/OL].(2015-11-26)[2016-01-04].http://www. chp.org.cn/view/ff80808150c920700151427525de75ef?a= BZHXYP.
[4] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:59-61,88-89.
[5]Ubhi K,Rockenstein E,Vazquez-roque R,et al.Cerebrolysin modulates pronerve growth factor/nerve growth factor ratio and ameliorates the cholinergic deficit in a transgenic model of Alzheimer’s disease[J].J Neurosci Res,2013,91(2):167.
[6]Panisset M,Gauthie RS,Moessle RH,et al.Cerebrolysin in Alzheimer’s disease:a randomized,double-blind,placebocontrolled trial with a neurotrophic agent[J].J Neural Transm,2002,109(7/8):1089.
[7]国家食品药品监督管理局.关于加强脑蛋白水解物注射液监督检查的通知[S].2008-12.
[8]杨彦彪,张志叶,魏春华.脑蛋白水解物制剂的质量标准及不良反应[J].中国药房,2012,23(1):82.
(编辑:邹丽娟)
Optimization of the Extraction Technology of Cerebroprotein Hydrolyzate
HUANG Jie1,WANG Xiaogong2,SHAN Min1,TIAN Fuyuan3(1.Xi’an Institute for Food and Drug Control,Xi’an 710054,China;2.Xi’an Disai Biological Pharmaceutical Co.,Ltd.,Xi’an 710016,China;3.Shaanxi Wanxin Medicine Procurement and Supply Station,Shaanxi Xianyang 710065,China)
OBJECTIVE:To optimize the extraction technology of cerebroprotein hydrolyzate.METHODS:It was extracted by alkaline extraction solution with pH approximately 9;using the comprehensive score of similarities of total nitrogen content and peptide map of cerebroprotein hydrolyzate(cerebrolisin)as index,L9(34)orthogonal test was conducted to optimize the addition amounts of trypsin and pepsin,and hydrolysis time in pig brain(1 kg)hydrolysis technology,and the optimized technology was verified.RESULTS:Optimized extraction technology was as follows as trypsin adding 8 g,pepsin adding 5 g,hydrolysis time 12 h;the total nitrogen contents of obtained cerebroprotein hydrolyzate were 5.20,5.18,5.20 mg/ml(RSD=2.22%,n=3),peptide figure similarities were 93%,94%,96%(RSD=1.62%,n=3),comprehensive scores were 0.911,0.917,0.932(RSD=1.18%,n=3),respectively.CONCLUSIONS:The optimized technology is rational with high extraction rate and peptide map similarity.
Cerebroprotein hydrolyzate;Extraction technology;Orthogonal test;Total nitrogen content;Peptide map similarity
R977.4;R943
A
1001-0408(2016)28-3985-03
10.6039/j.issn.1001-0408.2016.28.30
*主管药师,硕士。研究方向:化学药物分析。电话:029-85533639。E-mail:hj810726@126.com
(2016-02-06
2016-05-20)

