二十五味珊瑚丸的微生物限度检查方法验证
王 玮 古桑德吉 德吉卓嘎
西藏自治区食品药品检验所药理室,西藏 拉萨 850000
二十五味珊瑚丸的微生物限度检查方法验证
王 玮 古桑德吉 德吉卓嘎
西藏自治区食品药品检验所药理室,西藏 拉萨 850000
目的:建立二十五味珊瑚丸微生物检查方法。 方法:分别采用倾注法和薄膜过滤法对4种阳性菌株进行回收率实验。结果:二十五味珊瑚丸有较强的抑菌作用,采用薄膜过滤法才能彻底消除其抑菌作用,3种菌株回收率均能达到50%。结论:采用薄膜过滤法测定二十五味珊瑚丸中的需氧菌,霉菌和酵母菌可按倾注法测定,控制菌可按常规法测定。
二十五味珊瑚丸;倾注法;薄膜过滤法
藏药二十五味珊瑚丸(藏药名:球玛尔尼阿日布)由公元18世纪著名藏医药学家帝玛尔·丹增彭措研制,转载于公元19世纪藏医药学家迷旁·朗杰加措编撰的《集药利乐库》,该书记载了二十五味珊瑚丸的配方及功能主治,并沿用至今[1],现收载于1995年版中华人民共和国卫生部药品标准(藏药第1册)中。该藏药由珊瑚、珍珠、诃子、木香、青金石、麝香、红花等25味藏药材组成的复方制剂,具有开窍、通络、止痛等功效。用于“白脉病”神志不清、身体麻木、头昏目眩、脑部疼痛、血压不调、头痛、癫痫及各种神经性疼痛。此标准中没有规定具体的微生物限度检查方法,为确保微生物检查方法的科学性和结果的准确性,研究按照《中国药典》2015年版第四部的规定对其微生物限度检查进行方法验证试验。
1仪器与材料
1.1 样品 二十五味珊瑚丸(A企业,批号141104;B企业,批号20150506;C企业,批号20150407;D企业,批号150401)。
1.2 试验用培养基 胰酪大豆胨液体培养基(TSB,批号:151228)、胰酪大豆胨琼脂培养基(TSA,批号:151230)、沙氏葡萄糖液体培养基(批号:151219)、沙氏葡萄糖琼脂培养基(批号:151219)、RV沙门菌增菌液体培养基(批号:150916)、木糖赖氨酸脱氧胆酸盐琼脂培养基(批号:151210)、麦康凯液体培养基(批号:151204)、麦康凯琼脂培养基(批号:141016)均为北京陆桥技术股份有限公司产品。 1.3 试验菌株 大肠埃希菌(CMCC(B)44 102)、金黄色葡萄球菌(CMCC(B)26 003)、枯草芽孢杆菌(CMCC(B)63 501)、白色念珠菌(CMCC(F)98 001)、乙型副伤寒沙门菌(CMCC(B)50 094)均由中国食品药品检定研究院提供。
1.4 仪器 BPG-9200BH型高温鼓风干燥箱(上海-恒科技有限公司);SPX-250B型生化培养箱(上海跃进医疗器械厂);PYX-PHS-60×75-BS-Ⅱ型隔水式电热恒温培养箱(上海跃进医疗器械厂);1300系列Ⅱ级A2型生物安全柜(美国热电公司);HTV-200型集菌仪(杭州泰林医疗器械厂);2H-2型自动漩涡混合器(天津药典标准仪器厂);PL202-S电子天平(梅特勒-托多仪器(上海)有限公司);YXQ-LS-50S11型立式压力蒸汽灭菌器(上海博迅实业有限公司医疗设备厂)。
2 方法与结果
2.1 菌液的制备 按照《中华人民共和国药典》(2015版)四部非无菌产品微生物限度检查[2]。2.1.1 菌液制备 接种大肠埃希菌、枯草芽孢杆菌、乙型副伤寒沙门菌和金黄色葡萄球新鲜培养物至胰酪大豆胨琼脂培养液中,30~35℃培养36h;接种白色念珠菌的新鲜培养物至沙氏葡萄糖液体培养基中,23~28℃培养36h。乙型副伤寒沙门菌为控制菌检查用菌,不用于菌株回收率测定。
2.1.2 供试液制备 称取样品10g,加入pH7.0氯化钠-蛋白胨缓冲液至100mL,制成1∶10供试液;吸取1∶10供试液1mL,加入pH7.0氯化钠-蛋白胨缓冲液至10mL,制成1∶100供试液。
2.1.3 试验组 取上述制备好的供试液,加入制备好的菌液,混匀,分别制成每1mL含菌数为10~100CFU的试验菌液。
2.1.4 供试液对照组 取“2.1.2”制备好的供试液,以稀释液代替菌液其他同试验组。
2.1.5 菌液对照组 取pH7.0氯化钠-蛋白胨缓冲液替代供试液,按试验组操作加入菌液来进行微生物回收试验。
2.2 倾注法
2.2.1 试验组 取1∶10试验菌液1mL注入平皿中,含白色念珠球菌组倾注沙氏葡萄糖琼脂培养基15~20mL,除含白色念珠球菌组外倾注胰酪大豆胨琼脂培养基15~20mL,待凝固后,含白色念珠菌组置于25~28℃培养5d,除白色念珠菌组外置于30~35℃培养72h,观察结果测定菌落数,每组实验菌株平行制作2个平皿。
2.2.2 供试品对照组 取“2.1.4”试液1mL注入平皿中,按倾注法测定供试品本底菌数。
2.2.3 菌液对照组 取“2.1.5”试液1mL注入平皿中,其他同试验组。
2.2.4 稀释剂对照组 取稀释液1mL注入平皿中,其他同试验组。
2.2.5 结果 经试验,表1中选取的4个厂家样品均对白色念珠球菌无明显抑制作用,回收率在50%以上,采用倾注法即可满足对样品中霉菌及酵母菌的检查。样品对大肠埃希菌及金黄色葡萄球菌无明显抑制作用,回收率在50%以上,但对枯草芽孢杆菌有明显抑制作用,回收率大部分在50%以下。表2采用1∶100供试液测定了菌株的回收率,回收率大部分在50%以下。结果表明采用倾注法可能无法满足对样品中需氧菌的检查,故接下来采用薄膜过滤法法对谷草芽孢杆菌回收率进行测定。表3为稀释剂试验用菌回收率。
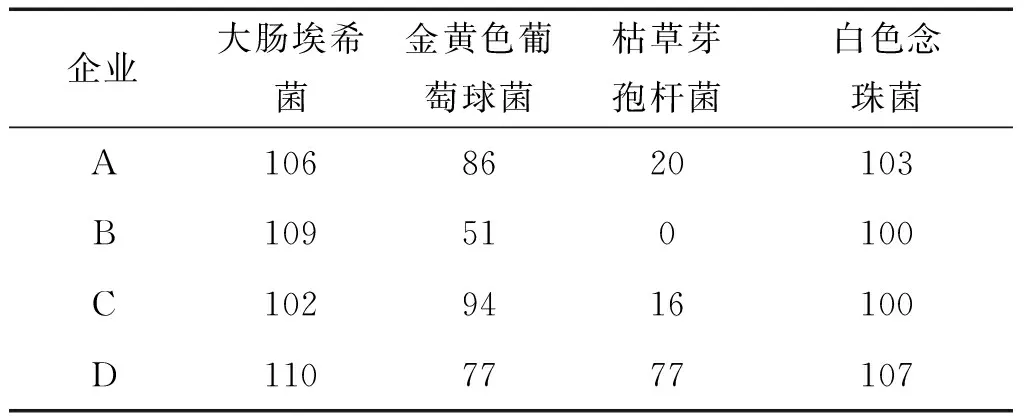
表1 倾注法测定各实验菌株的回收率 (%)

表2 倾注法测定实验菌株的回收率 (%)

表3 稀释液对照组实验菌株的回收率 (%)
2.3 薄膜过滤法
2.3.1 试验组 取1∶10试验菌液2mL注入薄膜过滤器中,用100mL pH7.0氯化钠-蛋白胨缓冲液冲洗,使分散均匀,全量过滤,再以pH7.0氯化钠-蛋白胨缓冲液冲洗,每次100mL冲洗4次,全量滤过,转帖至胰酪大豆胨琼脂培养基上。由表1中看出样品对于枯草芽孢杆菌的抑制作用比较强,先进行枯草芽孢杆菌回收率的测定。
2.3.2 供试品对照组 取“2.1.4”制备的试液2mL加入薄膜过滤器中,不加试验菌液,其它同试品验组。
2.3.3 菌液对照组 取“2.1.5”制备的试验液2mL加入薄膜过滤其中,用100mL pH7.0氯化钠-蛋白胨缓冲液冲洗,使分散均匀,全量过滤,转帖至胰酪大豆胨琼脂培养基上。
2.3.4 稀释剂对照组 取稀释液2mL薄膜过滤器中,用100mL pH7.0氯化钠-蛋白胨缓冲液冲洗,使分散均匀,全量过滤,转帖至胰酪大豆胨琼脂培养基上。
2.3.5 结果 表4中,1∶10供试液任对试验菌有一定的抑制作用。表5为稀释液对照组实验菌株的回收率。表6中,用同样薄膜过滤法法取1∶100供试液测定了菌株的回收率,结果表明,各试验菌株回收率均大于50%,故采用1∶100供试品溶液进行薄膜过滤法,适用于二十五味珊瑚丸的细菌的微生物限度测定试验。

表4 薄膜过滤法测定实验菌株的回收率 (%)

表5 稀释液对照组实验菌株的回收率 (%)
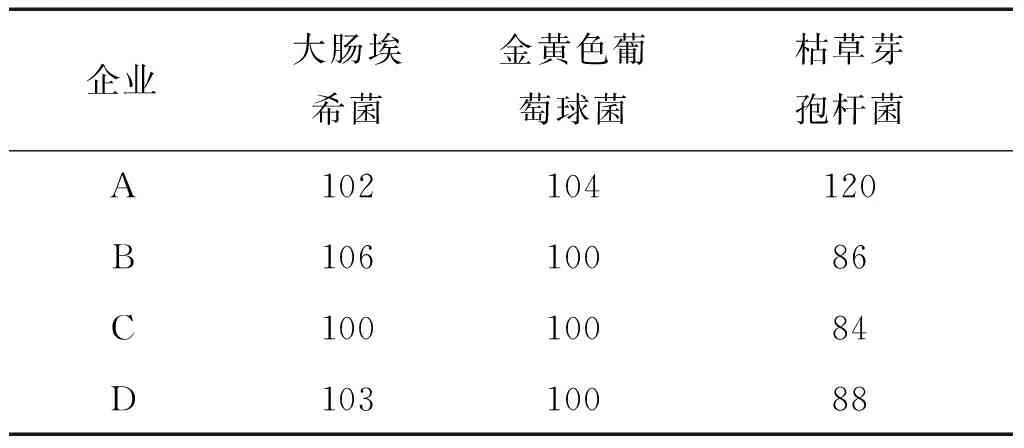
表6 薄膜过滤法测定各实验菌株的回收率 (%)
2.4 控制菌检查法的验证 本品为含药材原粉的固体口服药,因此以大肠埃希菌和沙门菌为控制菌进行验证。
2.4.1 试验组 取1∶10供试液10mL及大肠埃希试验菌液1mL加入100mL胰酪大豆胨液体培养基中;直接称取供试品10g及乙型副伤寒沙门菌液1mL加入200mL胰酪大豆胨琼脂培养液中,依相应控制菌检查法进行检查。试验菌液溶度均在10~100CFU。
2.4.2 供试品对照组 其他同供试品组但不加入试验菌液。
2.4.3 稀释剂对照组 取pH7.0氯化钠-蛋白胨缓冲液1mL加入10mL胰酪大豆胨液体培养基中。
2.4.4 结果 采用常规控制菌检查法,均能检出试验菌,表明此法可适用于二十五珊瑚丸的控制菌检查。结果见表7。
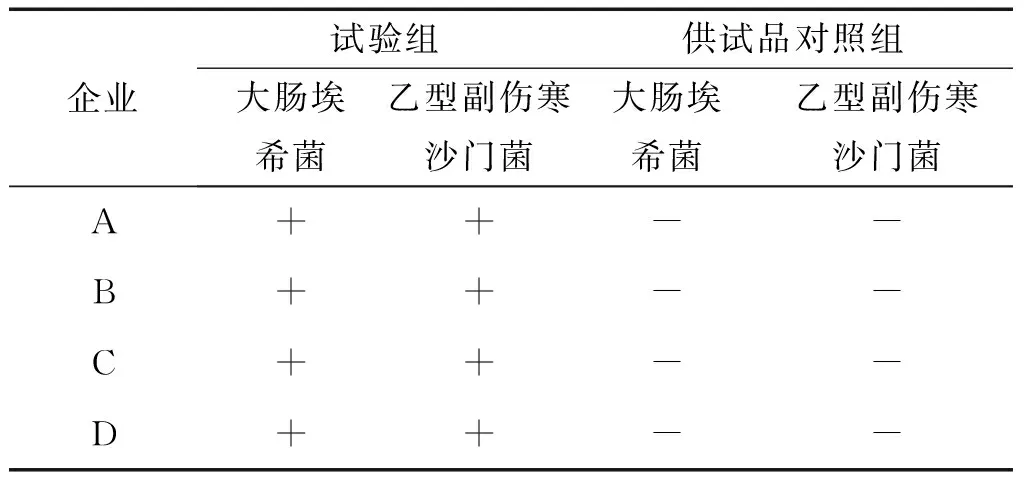
表7 控制菌验证结果
3 讨论
二十五味珊瑚丸是含有多种成分的复合制剂,通过倾注法不难发现二十五味珊瑚丸是一种抑菌作用较强的药品,在本次验证过程中首先考虑增加稀释液和薄膜过滤法联用来去除药品中的抗菌活性。薄膜过滤法能很好的把外界影响和操作者的主观因素减少到最低,所以该方法更为客观,能够全面反映药品的染菌情况[3]。
由于西藏自然环境特殊,海拔高,含氧量仅为平原地区的60%左右,在制备金黄色葡萄球菌和其他试验用菌时,需将培养时间由《中国药典》2015年版第四部中规定的18~24h延长至36h,才能良好生长,故将试验用菌培养时间延长至36h。
[1] 杜文兵,黄福开,罗远带,等. 二十五味珊瑚丸药理及临床研究进展[J].世界中西医结合杂志,2013,8(5):537-540.
[2]国家药典委员会. 中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:1105-1106.
[3]王亚婷. 薄膜过滤法在药品微生物限度检查中的应用[J].河北化工,2013,36(4):8-9.
(编辑:程鹏飞)
Validation Method for Microbial Limit of Ershiwuwei Shanhu Wan
WANG wei GU Sangdeji DEJi zhuoga
Pharmacological Room,Tibet Institute for Food and Drug Control,Lhasa 850000,China
Objective Set up Ershiwuwei shanhu wan microbiological examination method. Methods Pouring method and membrane filtration method were used respectively for four kind of positive strain rate experiments. Result Ershiwuwei shanhu wan strong bacteriostasis, finally USES the membrane filtration method can eliminate the bacteriostatic action, Three strains of recovery rate can reach 50%.Conclusion Using the membrane filter method for determination of aerobe in Ershiwuwei shanhu wan,Mold and yeast can press pour method,Control bacteria can according to the conventional method.
Ershiwuwei Shanhu Wan;Pour Method;Membrane Filtration Method
2016-07-21
王玮(1985-),女,汉族,本科,研究方向为药品微生物限度。E-mail:67597683@qq.com
R284
A
1007-8517(2016)20-0027-03

