一种新的机械混合法制备Ag(I)@β吸附剂及其吸附CO性能
岳盈溢,朱保昆,黄艳,肖静,廖头根
1 云南中烟工业有限责任公司技术中心,云南昆明 650231;2华南理工大学化学与化工学院,广东广州510640
一种新的机械混合法制备Ag(I)@β吸附剂及其吸附CO性能
岳盈溢2,朱保昆1,黄艳2,肖静2,廖头根1
1 云南中烟工业有限责任公司技术中心,云南昆明 650231;2华南理工大学化学与化工学院,广东广州510640
CO是卷烟主流烟气中的主要有害物质之一,长期接触低浓度CO可造成慢性中毒。本文提出一种新的机械混合法制备吸附CO的Ag(I)@β吸附剂,采用N2吸附法和X射线衍射分别表征了Ag(I)@β吸附剂的孔隙结构和晶体结构;采用固定床吸附技术模拟吸烟过程,研究其吸附CO性能,并考察了制备条件对其性能的影响。结果表明:使用新的机械混合法制备负载AgNO3的吸附剂,可避免银盐的分解,制得高分散性的负载型AgNO3吸附剂,其对CO的吸附性能优于传统正己烷混合法得到的。Ag(I)@β吸附剂的焙烧时间对其性能有影响,AgNO3负载量较高时,所需要的最佳焙烧时间也较长;当AgNO3和β分子筛质量比为0.10g/g时,其对CO吸附容量达到最佳值,是原始β分子筛的4.76倍,其抗水蒸气吸附性能也得到提高。
卷烟;Ag(I)@β;吸附剂;CO吸附;抗水蒸气
CO是卷烟主流烟气中的主要有害成分之一,研究表明,长期接触低浓度CO可能造成慢性中毒,对人体神经系统、心血管系统及血液生化成分均有不利的影响[1]。鉴于CO对人体健康的严重危害,有效的治理卷烟主流烟气中的CO迫在眉睫。因此,世界各国相继出台政策控制卷烟烟气中的CO含量。2004年,欧盟明确规定:市售卷烟的烟气CO含量必须低于10 mg/支[2],我国在卷烟国标中也规定了烟气中CO含量的限制。
吸附技术去除CO具有经济有效,工艺简单,操作方便,无腐蚀和环境污染等优点。吸附分离法通过在卷烟滤嘴处添加适当的选择性吸附材料,可有效的过滤掉主流烟气中的CO,而吸附剂性能是该技术的关键。物理吸附剂利用微弱的范德华力吸附CO,它对CO的吸附容量和选择性都很低[3]。BuddaV Reddy等[4]发现:把氮化过渡金属氧化物纳米颗粒如Fe2O2N2、氮化氧化铁等加入卷烟滤嘴中,可降低主流烟气中CO和NO的含量,但减少量仅为10%左右。Zhang Youjin[5]制备了多孔材料负载的CuO/Mn3O4,该材料不仅能够拦截主流烟气中的CO,还能减少大量的苯并[a]芘,N-亚硝胺。然而,该材料在高温下的CO吸附量并不高。此外,JorgDe Haeck等[6]发现掺杂银的金纳米粒子簇对CO有着较高的催化氧化活性,从而可以提升对CO的吸附量。JiWoong Yoon等[7]发现MOF MIL-100(Fe)中的一部分Fe3+转化为Fe2+后,对含有π键的CO有着较强的吸附作用力。
β分子筛是唯一一种大孔三维十二元环交叉通道体系结构的高硅分子筛,具有适度的酸性,良好的热稳定性和化学稳定性,广泛应用于吸附和催化领域。然而,针对CO吸附的基于β分子筛的л络合吸附剂的研究尚未见报道。
为了克服Cu(I)类CO吸附剂在空气中极易氧化,卤化银类吸附剂焙烧温度高、见光易分解等缺点,制备具有高CO吸附性能、且易应用于卷烟滤嘴中的吸附剂,本文探讨采用无溶剂机械混合法制备Ag(I)@β吸附剂。采用N2吸附法表征了Ag(I)@β吸附剂的空隙结构,采用X射线衍射分析不同Ag(I)@β吸附剂的晶体结构,采用固定床吸附技术模拟吸烟过程,测定其对CO的动态吸附性能,并与采用传统浸渍法[8]制备的л络合吸附剂进行比较。此外,还用静态法测定了Ag(I)@β吸附剂的抗水蒸气吸附性能,讨论了制备条件对 Ag(I)@β的结构和CO吸附性能的影响关系。
1 材料与方法
1.1 原料
β分子筛(天津南化催化剂有限公司);硝酸银(AgNO3,分析纯,国际集团化学试剂有限公司);正己烷(C6H14,分析纯,广东省光华科技股份有限公司);氢气(H2,99.99%,广州市卓正气体有限公司);氮气(N2,99.99%,广州市卓正气体有限公司);一氧化碳(CO,99.99%);一氧化碳氢气标准混合气体(CO浓度5%,广州市卓正气体有限公司);干空气(广州市科名气体有限公司);卷烟样品A,卷烟样品B(均为某卷烟厂的市售产品)。
1.2 试验方法
1.2.1 机械混合法制备吸附剂
制备步骤:(1)首先将β分子筛置于马弗炉中在300℃下焙烧2 h,然后冷却至室温;(2)分别以0.05 g/g、0.10 g/g、0.20 g/g、0.30 g/g的比例将AgNO3粉末与β分子筛置于玛瑙球磨罐中,保持干燥并将球磨罐放入行星式球磨机内,以160 r/min机械混合4 h;(3)将干燥的AgNO3/β分子筛混合物置于管式炉中,在Ar气氛下加热至195 ℃并保持3 h;(4)冷却至室温后,放置干燥器中备用。
1.2.2 正己烷混合法制备吸附剂
为比较不同Ag(I)@β吸附剂的制备方法对CO吸附性能的影响,本文也采用传统的正己烷混合法[8]制备了Ag(I)@β吸附剂。制备步骤:(1)以不同的比例将AgNO3粉末与β分子筛混合后,将其置入正己烷溶液中,充分搅拌10 min以上。(2)将混合物进行干燥,得到AgNO3/β分子筛混合物。(3)将混合物置于真空干燥箱中50 ℃真空干燥12 h。(4)将干燥的AgNO3/β分子筛混合物置于管式炉中,在Ar气氛下加热至195 ℃并保持3 h。(5)冷却至室温。
1.3 吸附材料表征
1.3.1 吸附材料比表面积和孔径分析
采用美国ASAP2020M快速比表面积和孔径分布分析仪测定样品的比表面积和孔径分布。
1.3.2 X射线衍射(XRD)分析
采用德国Bruker公司生产的D8-ADVANCE型号X射线衍射仪对试验样品进行检测。实验条件为:光源采用辐射源Cu靶Kα辐射,管压40 kV,管流40 mA,扫描范围2θ= 5°-50°,扫描速度为0.1秒/步;使用X射线衍射卡进行定性分析。
1.4 固定床吸附CO透过曲线测定方法
为了模拟实际吸烟过程,采用固定床吸附技术测定CO动态工作吸附量。图1为固定床吸附实验流程图。实验过程中,首先将吸附剂烘干,然后装填于固定床填充柱中;用H2吹扫填充柱30 min,当在线色谱分析仪的基线稳定后通入CO/ H2混合气体,从固定床出口端的流出气体经色谱检测,得到出口气体中CO浓度随时间变化的曲线,也被称为固定床吸附CO的透过曲线。

图1 固定床吸附技术实验流程图Fig.1 The fl ow diagram of fi xed bed adsorption technology
本实验固定床吸附柱的长度为25 cm,直径为0.6 cm。CO为目标吸附质,采用CO/H2混合气体。其中混合气体的流量V0为5 mL/min,根据实际主流烟气中CO的浓度,设定CO浓度为5%。通常一支烟能够产生400~500 mg的主流烟气,在实际情况中,国内外卷烟的CO含量为6~16 mg/cig,CO的浓度接近5%。此时动态工作吸附容量的计算方法为:
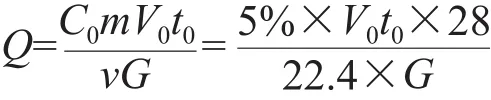
式中Q为工作吸附容量(mg/g),C0为CO的进料浓度,t0为CO在固定床上的吸附透过时间(min),t0越大,表明吸附剂的CO吸附性能越好。V0为混合气体的流量(mL/min),m为CO的分子量,v为每摩尔CO的气体体积,G为吸附柱内吸附剂的质量(g)。
1.5 吸附剂的水蒸气吸附性能测试
采用美国Micromeritics公司生产的水蒸气吸附仪测试样品水蒸气的吸附等温线,测试温度为25℃。
1.6 吸烟机抽吸测定
按照《GB/T 23356-2009 卷烟 烟气气相中一氧化碳的测定 非散射红外法》的方法进行抽吸,吸烟机型号: Borgwaldt RM20H转盘式吸烟机。
2 实验结果与讨论
2.1 机械混合法制备Ag(I)@β吸附剂的孔隙结构表征

表1 β分子筛和机械混合法制备的4种Ag(I)@β的孔隙结构Tab.1 Pore structure parameters of four Ag(I)@β adsorbents
表1列出四种AgNO3改性β分子筛(Ag(I)@β)的孔隙结构。从表1改性前后的孔隙结构数据看出:β分子筛表面经AgNO3改性后,Ag(I)@β吸附剂的比表面积随着AgNO3负载量的增加而减小。可见AgNO3成功的负载到了β分子筛的孔道表面。此外我们还注意到,当β分子筛表面负载AgNO3的比例增加时,孔容和孔径的下降的幅度也很小,说明AgNO3在β分子筛表面并未出现明显的堵孔现象,表面分散性好。
2.2 机械混合法制备Ag(I)@β吸附剂的XRD表征
图2示出Ag(I)@β的XRD谱图。由图可见:当AgNO3负载量为0.05 g/g、0.10 g/g时,Ag(I)@β的XRD谱图与初始β分子筛相同,并未出现明显的AgNO3特征峰(2θ= 28.97°,32.80°,35.47°)。这是由于AgNO3在β分子筛表面分散较好,其颗粒尺寸低于XRD的检测限[9]。当AgNO3的负载量为0.20 g/g时,Ag(I)@β谱图中出现了极为微弱的AgNO3特征峰,说明此时AgNO3的颗粒尺寸刚刚进入XRD的检测范围,达到了原子水平分散;当AgNO3的负载量为0.30 g/g时,Ag(I)@β谱图中有较为明显的AgNO3的特征峰(2θ= 28.97°,32.80°,35.47°),意味着负载在β分子筛上的AgNO3颗粒变大,可能以一定颗粒大小的晶相堆叠起来。值得注意的是,此时的Ag(I)@β的XRD谱图始终未出现Ag单质(Ag0)的特征峰(2θ= 38.11°,44.23°),说明AgNO3并未发生分解反应而生成单质Ag。

图2 Ag(I)@β的XRD谱图Fig.2 XRD spectra of Ag(I)@β

图3 正己烷混合法制备Ag/β吸附剂的XRD谱图Fig. 3 XRD spectra of Ag/β adsorbents made through n-hexane
与此形成对照的是:应用正己烷混合法制备Ag/β吸附剂,其XRD谱图(图3)显示,与原始β分子筛相比,Ag/β吸附剂在2θ为38.11°和44.23°的位置上出现了两个新峰,其对应为Ag0的特征峰。这说明部分负载的AgNO3分解生成了Ag单质。这可能是由于AgNO3在有机溶剂(正己烷)存在下易发生分解反应:2AgNO3= 2Ag+2NO2↑+O2↑。而不同于Ag(I), Ag0并不能与CO发生π络合,这会导致Ag/β吸附剂的CO吸附效率变低。而机械混合法制备的Ag(I)@β吸附剂可克服此缺点,避免Ag单质的产生。因此,正己烷混合法制备Ag/β吸附剂对CO的吸附性能低于机械混合法制备的Ag(I)@β吸附剂。
2.3 机械法制备Ag(I)@β吸附剂对CO的吸附透过曲线

图4 CO在β分子筛和机械法制备的4种Ag(I)@β上的吸附透过曲线Fig. 4 CO breakthrough curves of four Ag(I)@β adsorbents
应用固定床吸附技术测定改性β分子筛吸附CO的性能。图4示出了CO在机械法制备的4种Ag(I)@β上的吸附透过曲线。从图中可看出:与初始β分子筛相比,CO在Ag(I)@β上的吸附透过时间明显增长,表明β分子筛在表面负载Ag(I)后,其对CO的工作吸附容量增大。负载量为0.10 g/g的Ag(I)@β其对CO的工作吸附容量比是原始β分子筛的4.76倍。我们注意到:在负载量为0.05~0.10 g/g的范围,Ag(I)@β对CO的工作吸附容量随着AgNO3负载量的增加而增加;但当AgNO3负载量超过了0.10 g/g,Ag(I)@β对CO的工作吸附容量随AgNO3负载量的增加而逐步减少。出现这一现象的可能主要原因是:
(1)CO分子是一种存在反馈π键的弱极性分子,CO与Ag+结合时,二者之间既有σ键,又有反馈π键,从而可形成牢固的羰基化合物而发生强吸附;CO与Ag(I)结合形成羰基化合物时,一般存在两种形式:侧基络合和端基络合,它们一共对应着如下3种反应形式:
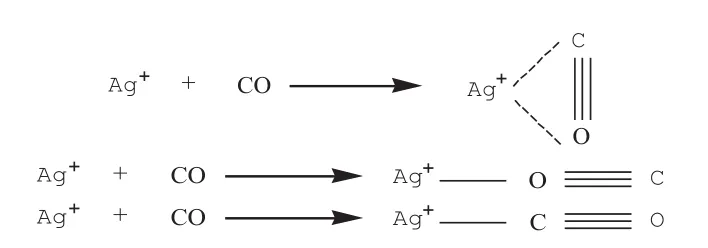
(2)当β分子筛表面负载适量的Ag(I)后,其表面可提供更多的л络合吸附位,因而其对CO的吸附容量增大,其最大吸附容量在0.10 g/g时获得。应用以下公式可以求出金属盐在多孔材料表面的理论分散阈值[10]:

上式中,n0为理论分散阈值,s为一个AgNO3分子在β分子筛上的截面积,经过分子模拟计算,s为1.52×10-18m2,M为AgNO3的摩尔质量,NA为阿伏伽德罗常数,A为β分子筛的截面积,为573.65 m2/g。将以上数据代入公式中计算,可得n0为0.11 g/g。而在我们的实验中,0.10 g/g Ag(I)@β对CO的工作吸附容量最大,与理论计算的结果吻合;
(3)然而,当进一步增大Ag(I)的负载量时,所负载的超过分散阈值的Ag(I)会以晶体的形式堆积起来,即可能会堵塞β分子筛的孔道,降低β分子筛的比表面积,因而Ag(I)@β吸附剂表面的л络合吸附位减少,其对CO的吸附容量逐步下降。
值得强调的是:根据自发单层分散原理,晶体自发单层分散所需要的温度与其自身熔点有关[11]。而AgNO3的熔点(212℃)远低于AgCl的熔点(455℃),因此与此前报导的AgCl负载活性炭材料相比[10],负载AgNO3所需要的焙烧温度大幅降低,由400℃降低为195℃。此外,AgNO3克服了卤化银见光易分解的缺点,显示出更好光稳定性和安全性,更有利于制备和应用于卷烟滤嘴中。
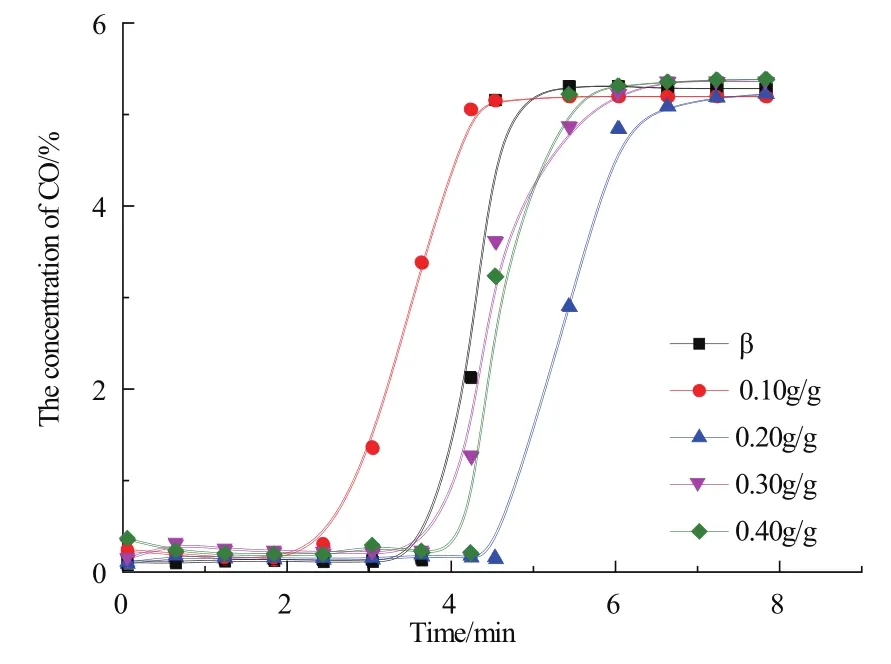
图5 CO在正己烷混合法制备Ag/β吸附剂上的吸附透过曲线Fig. 5 CO breakthrough curves of Ag/β adsorbents made through n-hexane
图5示出CO在传统正己烷混合法制备的四种比例Ag/β上的吸附透过曲线。从图中可看出:与原始β分子筛相比,CO在正己烷混合法制备Ag/β吸附剂上的吸附透过时间并没有大幅度增长,有的甚至低于原始β分子筛,吸附效果并不理想。
2.4 焙烧时间对Ag(I)@β吸附CO性能的影响

图6a CO在四种0.05 g/g Ag(I)@β的吸附透过曲线Fig. 6a CO breakthrough curves of four 0.05 g/g Ag(I)@β adsorbents

图6b CO在四种0.10 g/g Ag(I)@β的吸附透过曲线Fig. 6b CO breakthrough curves of four 0.10 g/g Ag(I)@β adsorbents
在实验过程中发现:以相同的实验条件同时焙烧负载量分别为0.05 g/g和0.10 g/g的Ag(I)@β吸附剂时,0.05 g/g Ag(I)@β吸附剂部分变为黑色,而0.10 g/g的Ag(I)@β吸附剂没有变色。这些现象显示,在0.05 g/g Ag(I)@β吸附剂可能出现AgNO3分解,析出的Ag单质呈黑色。通常,当固体物质颗粒的粒径小到一定程度后(比如纳米级),其粒径越小,则其分解温度就越低,越易分解。当AgNO3负载量比较低时,它不仅较好地分散在载体上,而且其粒子尺寸也相对较小,因此其分解温度就会降低或更容易分解[12]。由此我们推测:不同AgNO3负载量的Ag(I)@β吸附剂所需要的最佳焙烧时间是不同的。因此以机械混合法制备的Ag(I)@β吸附剂为例子,进一步考察了焙烧时间对所制备Ag(I)@β的CO吸附性能的影响。图6a和6b分别示出不同焙烧时间制备的0.05 g/g 和0.10 g/g Ag(I)@β对CO的吸附透过曲线。由图可见:对于0.05 g/g Ag(I)@β吸附剂,焙烧时间为1.5 h制备的材料其对CO吸附量达到最大值(10.52 mg/g);对于0.10 g/g Ag(I)@β吸附剂,焙烧时间为2 h制备的材料其对CO吸附量达到最大值(12.52 mg/g)。这也说明AgNO3负载量越大,所需的最佳焙烧时间越长。

图7不同焙烧时间制备的0.10g/g Ag(I)@β的XRD谱图 (a-3小时;b-2小时)Fig. 7 XRD spectra of two 0.10g/g Ag/β adsorbents baked at different time
图7示出不同焙烧时间制备的0.10 g/g Ag(I)@β的XRD谱图。由图可见,对于一定AgNO3负载量的Ag(I)@β,当其制备过程中焙烧时间过长时,会有一定量的Ag单质析出(XRD谱图的特征峰为 2θ=38.11°,44.23°),因而可导致л络合吸附位减少。因此,焙烧时间是决定所制备Ag(I)@β吸附剂对CO吸附性能优劣的一个重要参数。
2.5 Ag(I)@β的抗水蒸气吸附性能

图8 β分子筛和Ag(I)@β的水蒸气吸附等温线Fig. 8 Adsorption isotherms of water vapor on β and Ag(I)@β adsorbent
图8示出β分子筛和机械混合法制备的Ag(I)@β在25 ℃的水蒸气吸附等温线。该吸附等温线属于Ⅱ型吸附等温线,说明水分子在β分子筛和Ag(I)@β上的吸附为多层吸附。通过β分子筛负载前后的水蒸气等温线比较,发现:Ag(I)@β对水蒸气的吸附量低于初始β分子筛,说明相比β分子筛,Ag(I)@β吸附剂具有更好的抗水汽吸附性能。在实际工况条件下,CO混合气中往往含一定量的水蒸气,在吸附剂吸附CO的过程中,水蒸气分子也会占据一定的吸附位点,和CO形成竞争吸附,从而降低材料对CO的吸附能力。由于改性后Ag(I)@β吸附剂具有更好的抗水汽吸附性能,这将有利于其在实际工况条件下对CO吸附。
2.6 吸烟机抽吸测定Ag(I)@β对CO吸附

表2 在卷烟滤嘴中添加Ag(I)@β对CO及TPM(焦油、水、尼古丁)的吸附效果Tab. 2 CO and TPM adsorption of cigarettes fi lter with Ag(I)@β adsorbents
实验数据表明,滤嘴中添加Ag(I)@β对主流烟气中的TPM(焦油、水、尼古丁)含量影响很小,变化率在2%范围内,表明此材料对于焦油、水和尼古丁的吸附量很小,另一方面,可以看出,两类卷烟滤嘴中添加Ag(I)@β后,均对CO有较为明显的吸附效果,这是由于Ag(I)@β吸附剂可以和CO进行π络合,形成羰基化合物,从而发生化学吸附,因此对CO具有良好选择性。这些实验也证明了:添加Ag(I)@β对CO有较好的吸附效果,但并不会影响卷烟的口味和劲头。
3 结论
(1)采用机械混合法成功制备了高分散性的Ag(I)@β分子筛吸附剂,其对CO吸附性能优于正己烷混合法制备的载Ag(I)@β分子筛吸附剂;
(2)β分子筛表面负载AgNO3后,其对CO的工作吸附容量大幅提升。随着AgNO3负载量的增多,Ag(I)@β吸附剂对CO的工作吸附量呈先增大后减小的规律,负载量为0.10 g/g的Ag(I)@β分子筛吸附剂对CO吸附达到最高值12.52 mg/g,比初始β分子筛增大约4.76倍;
(3)焙烧时间对所制备Ag(I)@β吸附性能有明显影响,不同AgNO3负载量的Ag(I)@β吸附剂所需要的最佳焙烧时间不同;AgNO3负载量越大,所需的焙烧时间越长;
(4)与原始的β分子筛相比,Ag(I)@β分子筛吸附剂对水蒸气的平衡吸附容量下降,表明β分子筛表面负载AgNO3后,其抗水蒸气吸附性能提高。
[1] Mizobuchi, Manabu, Kinugawa,et al. Catalyst for removing carbon monoxide in hydrogen rich gas and production method therefor [P].US Pat: 6713032:2004-03-30.
[2] 吕功煊,聂聪,赵明月等. 应用含纳米贵金属催化材料降低卷烟烟气中CO技术研究[J].中国烟草学报,2003,9(3):18-27.Lu Gongxuan, Nie Cong, Zhao Mingyue, et al. Studies on technologies of removal of harmful components in cigarette smoke[J]. acta tabacaria sinica,2003,9(3):18-27. (in Chinese)
[3] Sato H, Kosaka, W; Matsuda R, Hori A, Hijikata Y,Belosludov R V, Sakaki S, Takata M, Kitagawa S, Self-Accelerating CO Sorption in a Soft Nanoporous Crystal [J].Science 2014, 343, (6167):167-170.
[4] Budda V.Reddy, Firooz Rasouli. Reduction of carbon monoxide and nitric oxide in smoking articles using nanoscale particles and/or clusters of nitrided transition metal oxides:US20050109356 A1 [P]. 2005-05-26.
[5] Zhang You-jin, Hu Qi-xiu, Hu Biao, et al. Preparation,characterization and application of a new kind of mesoporous composite [J]. Materials Chemistry and Phycics,2006,96:16-21.
[6] JorgDe Haeck, Nele Veldeman, et al. Carbon Monoxide Adsorption on Silver Doped Gold Clusters, American Chemical Society, 2011, 115:2103-2109.
[7] Yoon J W, Seo Y K, Hwang Y K, et al. Controlled reducibility of a metal organic framework with coordinatively unsaturated sites for preferential gassorption[J]. Angew Chem Int Ed 2010, 49: 5949-5952.
[8] 谢有畅,张佳平,童显忠等.一氧化碳高效吸附剂CuCl/分子筛[J].高等学校化学学报,1997,18(07):1159-1165.XIE Youchang, ZHANG Jiaping, TONG Xianzhong, et al.High Efficiency CO Adsorbent CuCl/Zeolite[J]. Chemical Journal of Chinese Universities, 1997,18(07):1159-1165.(in Chinese)
[9] Xiao Jing, Wang Xiao-xing, Chen Yong-sheng, et al.Ultra-Deep Adsorptive Desulfurization of Light-Irradiated Diesel Fuel over Supported TiO2-CeO2 Adsorbents[J].IndEngChem Res 2013, 52, 15746-15755.
[10] 黄丽娜,改性一氧化碳吸附剂的几个问题研究(硕士学位论文) [D].南京工业大学,2005.HUANG Lina, Study on Some Problems about the Improving of Carbon Monoxide Adsorbents [D]. Nanjing University of Technology,2005. (in Chinese)
[11] 段琼,自发单层分散的研究进展[J].四川化工, 2008,6(11):13-16.Duan Qiong, Advances in the Studies of Spontaneous Monolayer Dispersion [J].Sichuan Chemical Industry,2008,6(11):13-16. (in Chinese)
[12] 唐艳军,李友明,宋晶等. 纳米/微米碳酸钙的结构表征和热分解行为[J].物理化学学报, 2007, 23(5): 717- 722.TANG Yanjun, LI Youming, SONG Jing , et al. Structural Characterization and Thermal Decomposition Behavior of Microsized and Nanosized CaCO3[J].Wuli Huaxue Xuebao,2007,23(5):717-722. (in Chinese)
Ag(I)@β prepared by a novel mechanical mixing method and its CO adsorption ability
YUE Yingyi2, ZHU Baokun1, HUANG Yan1, XIAO Jing2, LIAO Tougen1
1 Technology Center, China Tobacco Yunnan Industrial Co. Ltd., Kunming 650231, China;2 School of Chemistry and Chemical Engineering, South China University of Technology, Guangzhou 510640, China
A series of Ag(I)@β adsorbents were prepared by a novel mechanical mixing method for CO adsorption. Textural properties and crystalline structures of the Ag(I)@β adsorbents were characterized by N2adsorption test and X-ray diffraction. CO adsorption performance of Ag(I)@β was examined by fi xed bed experiments. E ff ects of preparation conditions on its CO adsorption performance were discussed. Results showed that (1) Applying the mechanical mixing method to prepare Ag(I)@β can avoid decomposition of AgNO3to Ag0to get well-dispersion of AgNO3over β zeolite, and thus CO adsorption capacity of the prepared Ag(I)@β adsorbents were much higher than that of Ag(I)@β synthesized by traditional impregnation of silver chloride-cyclohexane solution; (2) Calcination time for preparing adsorbents had impact on CO adsorption performance of the adsorbents. Ag(I)@β with higher loading of AgNO3had longer optimal calcination time so that the Ag(I)@β with optimal CO adsorption performance can be obtained; (3) At weight ratio 0.1 g/g of AgNO3to β zeolite, CO adsorption capacity of Ag(I)@β reached maximum of 12.52 mg/g, 4.76 times that of original β zeolite. Its water vapor resistance became better than the original β zeolite.
cigarette, Ag(I)@β, adsorbent, π-complexation, water vapor resistance
岳盈溢,朱保昆,黄艳,等. 一种新的机械混合法制备Ag(I)@β吸附剂及其吸附CO性能[J]. 中国烟草学报,2016,22(2)
中国烟草总公司科技重大专项基金资助项目(110201101028);云南中烟工业有限责任公司科技项目基金资助项目(2012FL03)
岳盈溢(1990—),在读硕士研究生,从事吸附分离研究,Email:yueyingyi@126.com
廖头根(1980—),理学博士,从事材料工程研究,Email:wmlitto@163.com
2014-12-15
: YUE Yingyi, ZHU Baokun, HUANG Yan, et al. Ag(I)@β prepared by a novel mechanical mixing method and its CO adsorption ability [J]. Acta Tabacaria Sinica, 2016, 22(2)

