常见临床标本的病原菌谱变化及耐药趋势分析
王淑玉,姚姗姗
(菏泽市立医院 检验科,山东 菏泽274031)
常见临床标本的病原菌谱变化及耐药趋势分析
王淑玉,姚姗姗
(菏泽市立医院 检验科,山东 菏泽274031)
由于抗生素易于获取且适用广泛,在院内及院外都存在着过度使用及频繁更换的情况,从而导致引起感染的细菌谱明显改变,对各种抗生素耐药的菌株也逐年增多。为了应对耐药菌的大量出现,临床近年来开始逐步重视抗生素的规范使用。本研究将对本院近两年临床标本的病原菌分布及耐药情况进行回顾性分析,从而及时监控抗生素逐步合理使用后本地区病原菌谱的变化及耐药趋势,为临床治疗提供更合理的依据。
1 材料与方法
1.1 标本来源 2013年1月至2014年12月我院门诊及住院患者的各类标本共13576份,其中痰液6943份(51.14%),血液2296份(16.91%),尿液850份(6.26%),脑脊液775份(5.71%),脓液1745份(12.85%),胸水414份(3.05%),胆汁105份(0.73%),其他标本439份(3.23%)。
1.2 试剂与仪器 VITEK2全自动微生物鉴定系统、GPS-SH和GNS-NT专用药敏卡均购自法国生物梅里埃公司。标准菌株为:大肠埃希菌(ATCC25922)、铜绿假单胞菌(ATCC27853)、金黄色葡萄球菌(ATCC29213)、肺炎克雷伯菌(ATCC13883),购于卫生部临检中心。
1.3 细菌鉴定及药敏试验 按临床微生物操作规程接种标本,由VITEK2全自动微生物鉴定系统鉴定菌株。药敏采用VITEK系统的GPS-SH和GNS-NT专用药敏卡,少数细菌采用K-B纸片扩散法进行药敏试验,结果判读标准按2010年CLSI文件规定的判断标准[1,2]。
1.4 统计学方法 采用WHONET5.6和SPSS20.0软件进行数据统计分析。采用卡方检验进行统计分析,P<0.05有统计学意义。
2 结果
2.1 病原菌的检出及分布情况
两年共收到阳性细菌标本4304份,其中2013年分离阳性细菌标本1692份,革兰阳性菌391株(23.11%),革兰阴性杆菌1237株(73.11%),真菌64株(3.78%)。2014年分离阳性细菌标本2612份,其中革兰阳性菌663株(25.38%),革兰阴性菌1803株(69.03%),真菌146株(5.59%)。各年病原菌的检出及分布情况见表1。
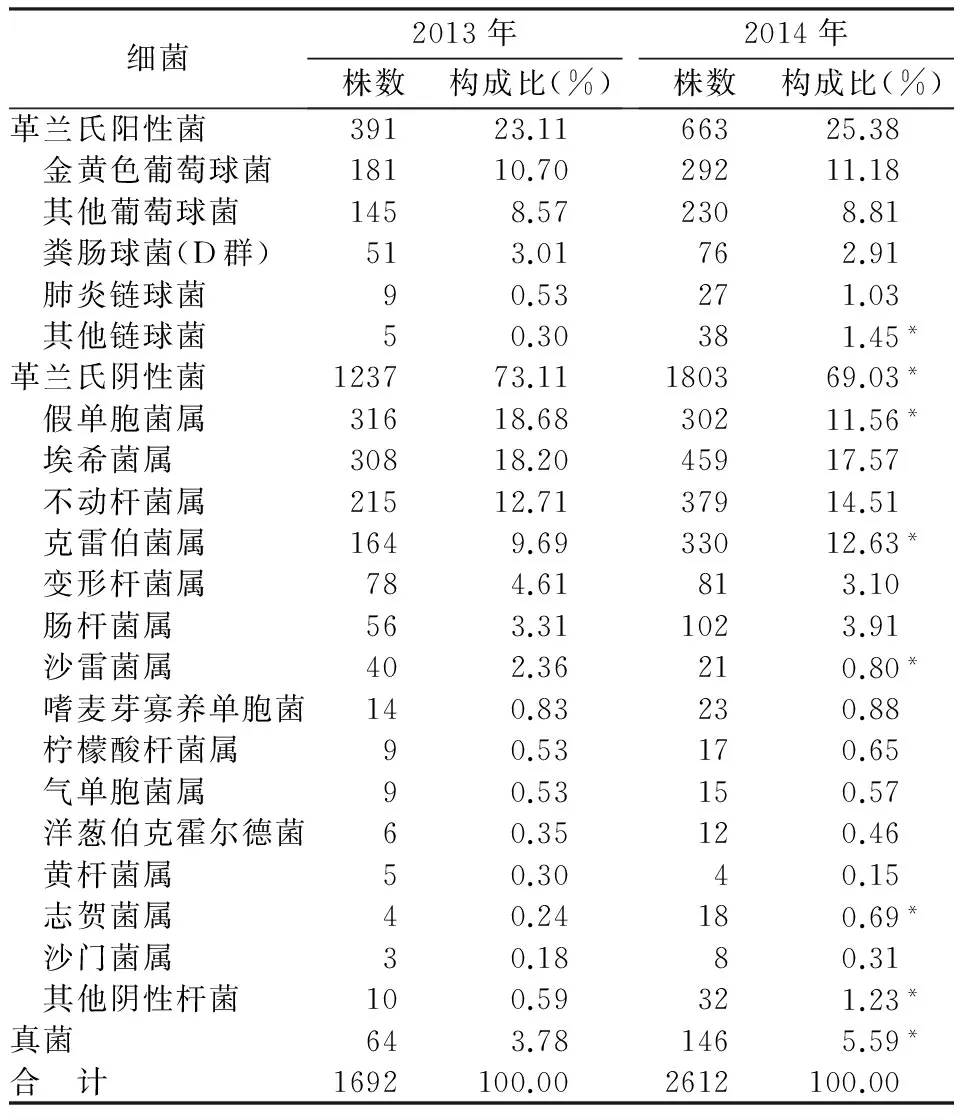
表1 各年病原菌分布及其构成比
*:与2013年相比,P<0.05,具有统计学意义。
2.2 检出率在前五位的细菌及其耐药情况
近两年检出率在前五位的细菌共2946株,占检出总数的68.24%,分别为假单胞菌属、埃希菌属、不动杆菌属、金黄色葡萄球菌、克雷伯菌属,五种菌的排名及耐药情况见表2、表3和表4。

表2 检出率前5位的细菌排名
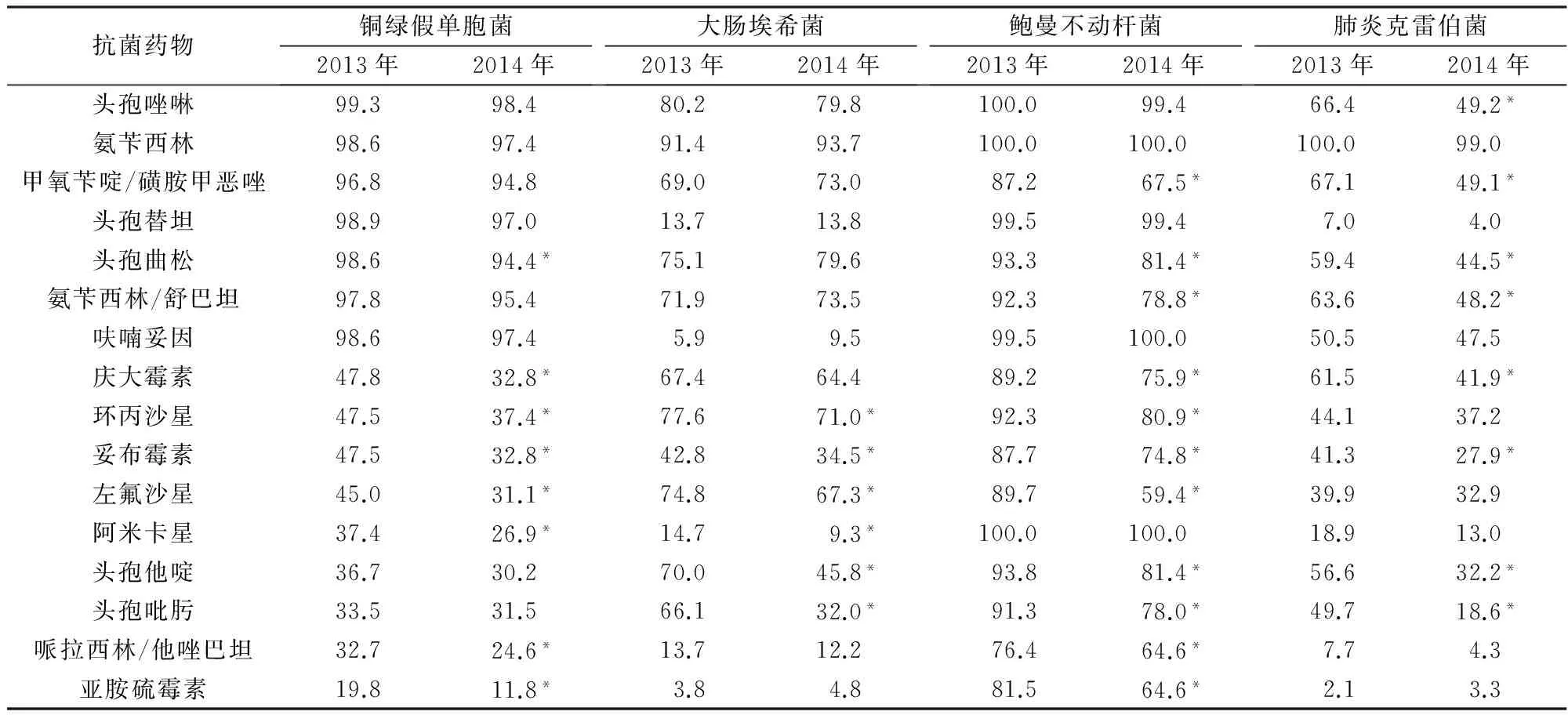
表3 不同年份主要革兰氏阴性细菌的耐药率(%)比较
*:与2013年相比,P<0.05,具有统计学意义。
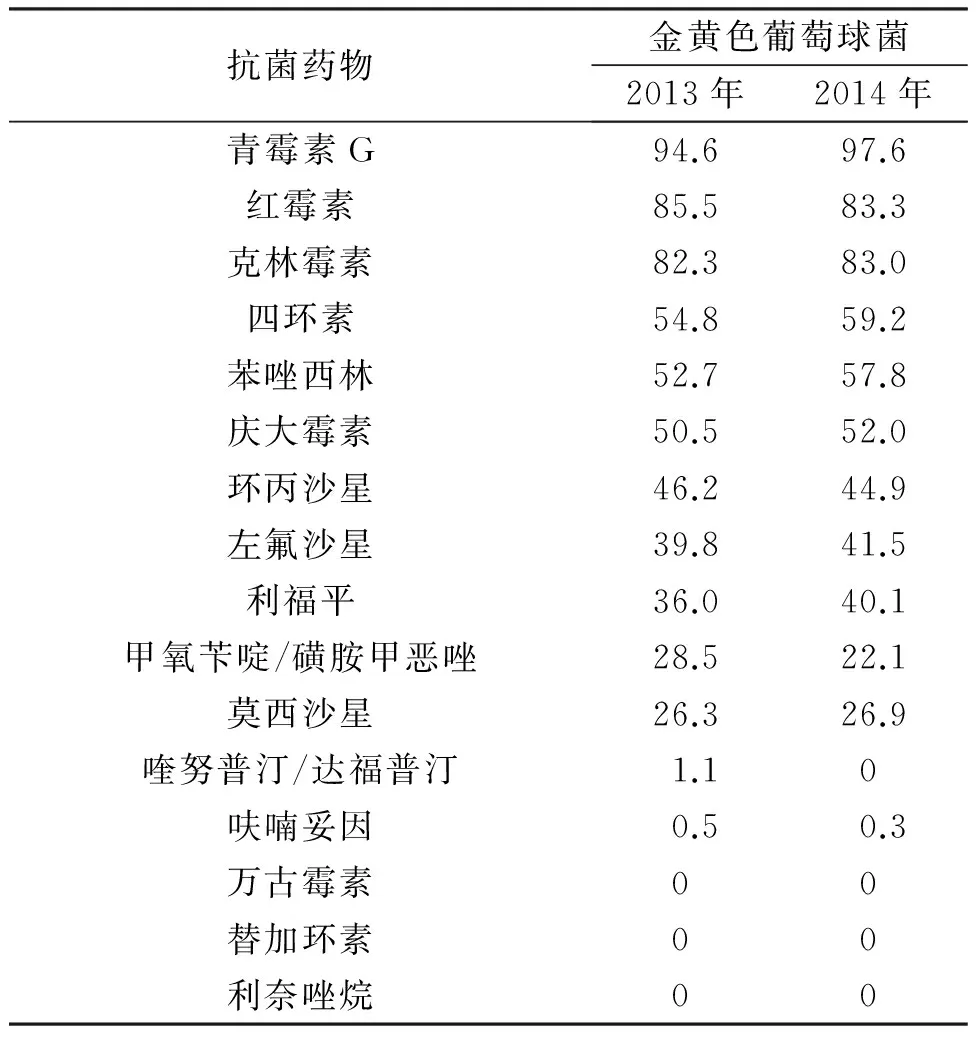
表4 不同年份主要革兰氏阳性细菌的耐药率(%)比较
注:与2013年相比,P>0.05。
2.3 多重耐药菌的检出情况
多重耐药菌,广义上也包括广泛耐药菌或超级细菌,其产生和发展给临床诊治带来巨大挑战[3]。经统计,我院多重耐药菌也逐年增多,具体检出情况见表5。
3 讨论
从本文细菌分离结果看,两年来痰液标本送检率最高,达51.14%,胆汁标本送检率最低,占送检标本总数的0.73%,但其病原菌分离率最高,达75.7%。
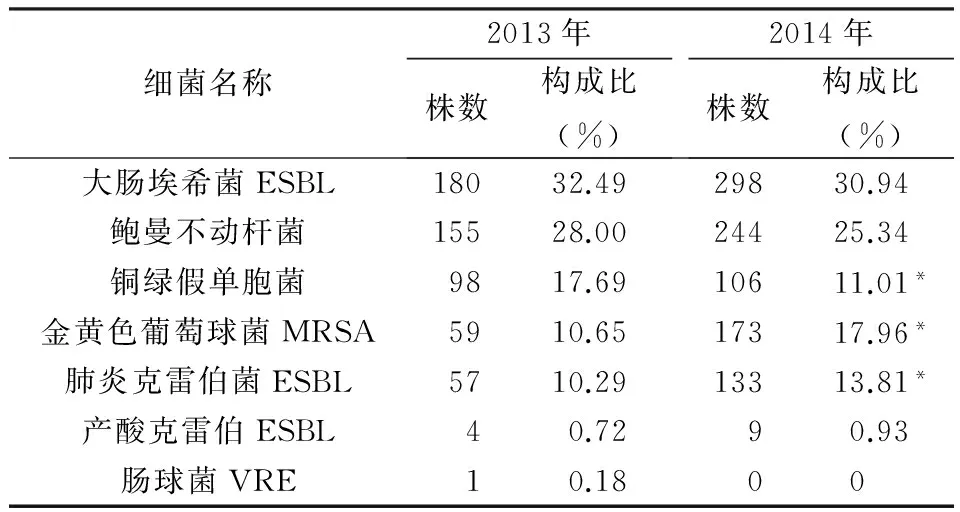
表5 多重耐药菌的分布及构成比
*:与2013年相比,P<0.05,具有统计学意义。
在各种临床标本中,分离出的病原菌主要为革兰氏阴性杆菌,占70.4%,高于周云松等[4]报道的61%,其次为革兰氏阳性菌,占24.4%,真菌占5.2%,与相关报道基本相符[5]。
根据数据统计结果显示,自我院严格控制抗生素使用以来,引起感染的病原菌谱开始出现变化,由表1可见,革兰氏阴性菌的检出呈减少趋势,与2013年相比有显著性差异(P<0.05),其中假单胞菌属和沙雷菌属的检出率减少,而克雷伯菌属及志贺菌属的检出呈上升趋势,这些菌株的变化与2013年相比都有显著性差异(P<0.05)。与2013年相比,革兰氏阳性菌的检出无显著性变化(P>0.05)。同时,由表2也可看出,近两年检出率在前五位的病原菌无变化,分别为假单胞菌属、埃希菌属、不动杆菌属、金黄色葡萄球菌、克雷伯菌属,与徐韫健等[5]报道的嗜麦芽窄食单胞菌位于前五位的研究结果有细微差别,但两年来病原菌的构成有所不同,与2013年相比,2014年假单胞菌属明显减少,其检出率2013年排名第一,2014年排名第四。
两年间除了病原菌谱发生了部分变化,病原菌对抗菌药物的敏感性也发生了改变。由表3可见,革兰氏阴性菌对抗菌药物的耐药率高,其中铜绿假单胞菌对头孢唑啉、复方新诺明、头孢替坦、头孢曲松、氨苄西林/舒巴坦、呋喃妥因的耐药率在95%以上,对阿米卡星、哌拉西林/他唑巴坦、亚胺硫霉素相对敏感,与2013年相比,2014年检出的铜绿假单胞菌对多种抗生素的耐药率出现了下降,其中对头孢曲松、庆大霉素、环丙沙星、妥布霉素、左氟沙星、阿米卡星、哌拉西林/他唑巴坦、亚胺硫霉素等抗菌药物的耐药率下降明显(P<0.05)。
大肠埃希菌对哌拉西林的耐药率高,达93.33%,对头孢唑啉、头孢曲松、左氟沙星的耐药率在75%以上,低于梁剑等[6]的报道。对呋喃妥因、阿米卡星、哌拉西林/他唑巴坦、亚胺硫霉素较为敏感,与2013年相比,2014年检出的大肠埃希菌对环丙沙星、妥布霉素、左氟沙星、阿卡米星、头孢他啶、头孢吡肟等抗菌药物的耐受率下降明显(P<0.05)。
鲍曼不动杆菌耐药性强,对绝大多数抗菌药物不敏感,其中对头孢唑啉、氨苄西林、阿卡米星的耐药率达100%,对头孢替坦、呋喃妥因的耐药率达99%以上,对头孢他啶、头孢曲松、氨苄西林/舒巴坦、环丙沙星、头孢吡肟的耐药率在90%以上,明显高于相关报道[7]。据统计结果显示,2014年该菌对抗菌药物的敏感性有所升高,其中对甲氧苄啶/磺胺甲恶唑、头孢曲松、氨苄西林/舒巴坦、庆大霉素、环丙沙星、妥布霉素、左氟沙星、头孢他啶、头孢吡肟、哌拉西林/他唑巴坦、亚胺硫霉素升高明显(P<0.05)。
肺炎克雷伯菌对哌拉西林、氨苄西林的耐药率达100%,对头孢替坦、阿米卡星、哌拉西林/他唑巴坦、亚胺硫霉素较为敏感,与2013年相比,2014年检出的肺炎克雷伯菌对抗菌药物的敏感性升高,其中对头孢唑啉、甲氧苄啶/磺胺甲恶唑、头孢曲松、氨苄西林/舒巴坦、庆大霉素、妥布霉素、头孢他啶、头孢吡肟的敏感性增高明显(P<0.05)。
金黄色葡萄球对青霉素G的耐药率高达90%以上,明显高于王晓旭等[8]报道,而对喹努普汀/达福普汀、呋喃妥因、万古霉素、替加环素、利奈唑烷极为敏感,与陆静兰等[9]的报道一致。另外统计结果显示,与2013年相比,2014年检出的金黄色葡萄球菌对各类抗菌药物的耐药性无明显变化(P>0.05)。
由常见病原菌的耐药结果可见,随着抗菌药物应用逐渐规范,病原菌对部分抗菌药物的耐药性有降低趋势,但是多重耐药菌仍大量存在,两年间我院共分离多重耐药细菌1491 株,占检出细菌的34.5%,其中金黄色葡萄球菌232株,肺炎克雷伯菌190株,2014年两种细菌的检出量较2013年增长明显(P<0.05),铜绿假单胞菌204株,其检出率呈下降趋势(P<0.05),大肠埃希菌、产酸克雷伯、鲍曼不动杆菌、肠球菌无明显变化。
由此可见,随着临床对抗菌药物的规范使用加大重视,病原菌谱及耐药趋势发生了部分变化,这种变化是否有积极意义,需要继续对病原菌及其耐药情况进行监测。另外,临床细菌耐药性强仍是临床面临的严峻问题,临床医生应严格控制抗菌药物的用量及适用指征,重视住院病人的病原菌标本培养,加强与微生物实验室的沟通,及时根据病原菌的耐药情况调整用药。
[1]Clinical and Laboratory Standards Institute.Performance Standards for Antimicrobial Susceptibility Testing[S].Fifteenth Informational Supplement,2010,M100-S20,Vol 30 No.1.
[2]Clinical and Laboratory Standards Institute.Performance Standards for Antimicrobial Susceptibility Testing[S].Fifteenth Informational Supplement,2010,M100-S20-U,Vol 30 No.15.
[3]董 梅,匡铁吉.临床细菌多重耐药机制研究进展及对策[J].解放军医学院学报,2013,34(2):101.
[4]周云松,夏光琴,贺 梅,等.2012年医院感染病原菌分布与药敏分析[J].中华医院感染学杂志,2014(22):5495-5496,5505.
[5]徐韫健,易建云,范慎薇,等.2009-2011年我院优势细菌的药敏分析[J].国外医药抗生素分册,2013,34(1):21.
[6]梁 剑,曾 玲,李江,等.208例尿路感染大肠埃希菌耐药性分析[J].医学临床研究,2014,31(3):489.
[7]吴 琳,吴至成,翟英超,等.海南医学院附属医院鲍曼不动杆菌的感染分布及耐药性分析[J].南昌大学学报(医学版),2012,52(3):21.
[8]王晓旭,李秀成,王 禹,等.对2451份临床标本中病原菌感染分布及耐药性分析[J].航空航天医学杂志,2012,23(9):1109.
[9]陆静兰,廖 彬.311株金黄色葡萄球菌的耐药性分析[J].广西医学,2013,35(10):1392.
1007-4287(2016)10-1760-03
王淑玉,女,34岁,硕士,主管技师,研究方向:微生物检验。
2015-04-25)

