硅酸锂粉体的微波水热法制备及其表征
郭志峰(神华准能资源综合开发有限公司,内蒙古 鄂尔多斯 010300)
硅酸锂粉体的微波水热法制备及其表征
郭志峰(神华准能资源综合开发有限公司,内蒙古鄂尔多斯010300)
以氢氧化锂和硅酸乙酯为原料,采用微波水热法在80~150℃下成功地制备出高纯硅酸锂粉体,并利用场发射扫描电镜(FE-SEM)、X-射线能谱仪(EDS)、X射线多晶粉末衍射仪(XRD)、比表面积(BET)及孔径测试仪对所制备的硅酸锂粉体的微观形貌、元素和物相组成、吸附性能进行了表征研究,结果表明,微波水热法使硅酸锂的结晶温度降低到80℃,极大地降低了硅酸锂粉体的合成能耗,在80℃下水热反应40min可以得到结晶良好、疏松多孔、具有较大比表面积和微孔结构的纯相硅酸锂粉体,采用谢乐公式计算出其晶粒平均尺寸为70.65nm。
硅酸锂粉体;微波水热法;孔径结构
1 实验
1.1原料
正硅酸乙酯(TEOS),分析纯,阿拉丁试剂;氢氧化锂(LiOH. H2O),分析纯,国药集团化学试剂有限公司;盐酸(HCl),分析纯,国药集团化学试剂有限公司;氟化钠(NaF),分析纯,国药集团化学试剂有限公司。
1.2粉体的制备
配制0.1mol/L的LiOH溶液200ml,按n(F):n(Li)=1将矿化剂氟化钠加入LiOH溶液中,搅拌混合均匀。将TEOS按照n(Si):n(Li)=1:2滴加至LiOH溶液中,同时滴加氨水使TEOS完全水解形成硅酸溶胶,然后将该溶胶体系调至pH值为9,按一定比例加入矿化剂NaF,继续搅拌2h,然后将该溶液陈化10h。将陈化后的溶液加入罐体材料为聚四氟乙烯的微波消解罐中,放入微波消解仪中,程序升温至60~150℃,在最高温度下保持40min。反应结束后自然空气冷却,倒出产物,用乙醇洗涤产物数次后再用蒸馏水洗涤,除去其表面覆着的杂质离子,再在60℃下干燥3h。

图1 分别在150℃、120℃、100℃、80℃下所合成的硅酸锂粉体的FE-SEM形貌
2 测试与表征
2.1粉体物相表征
德国BrukerD8-Advance型X-射线多晶粉末衍射仪,采用Cu靶Kα1射线,工作电压和电流分别为40kV、40mA,扫描角度范围5°~95°,步长0.01°,每步0.1s,扫描完成后采用DIFFRAC EvaluationPackage数据分析软件进行物相的检索分析,采用Scherrer公式计算产物的晶粒尺寸。
2.2粉体微观结构表征
采用德国ZEISS-SUPRA55型高分辨率场发射扫描电子显微镜观察粉体的微观形貌结构及颗粒大小,并采用Oxford-AztecX-Max80型X-射线能谱仪对粉体进行了微区元素分析。
2.3比表面积及孔径分布表征
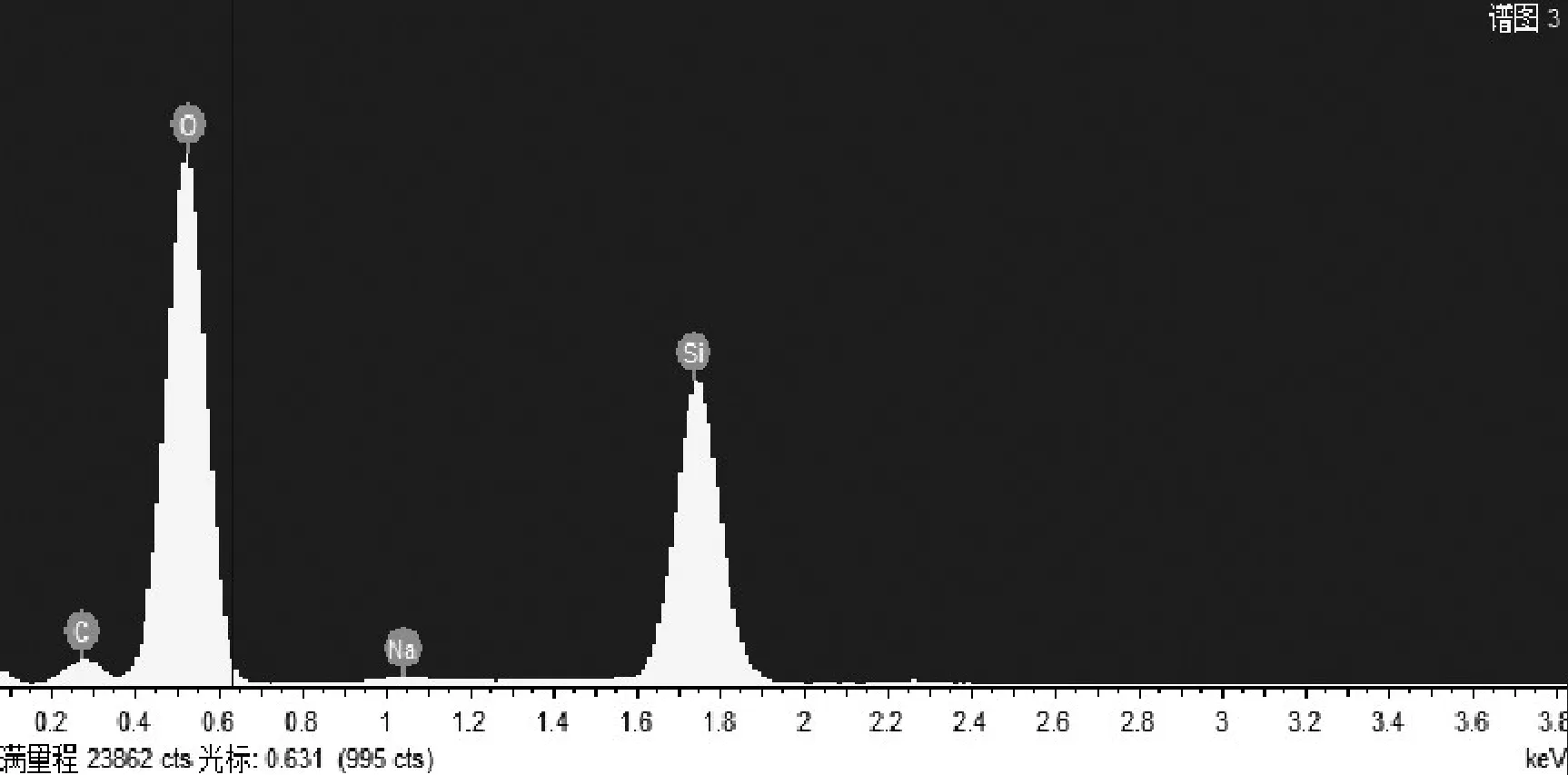
图2.80℃下所合成硅酸锂粉体颗粒的EDS谱图

图3.150℃下所合成的硅酸锂粉体的等温线

图4.120℃下所合成的硅酸锂粉体的等温线
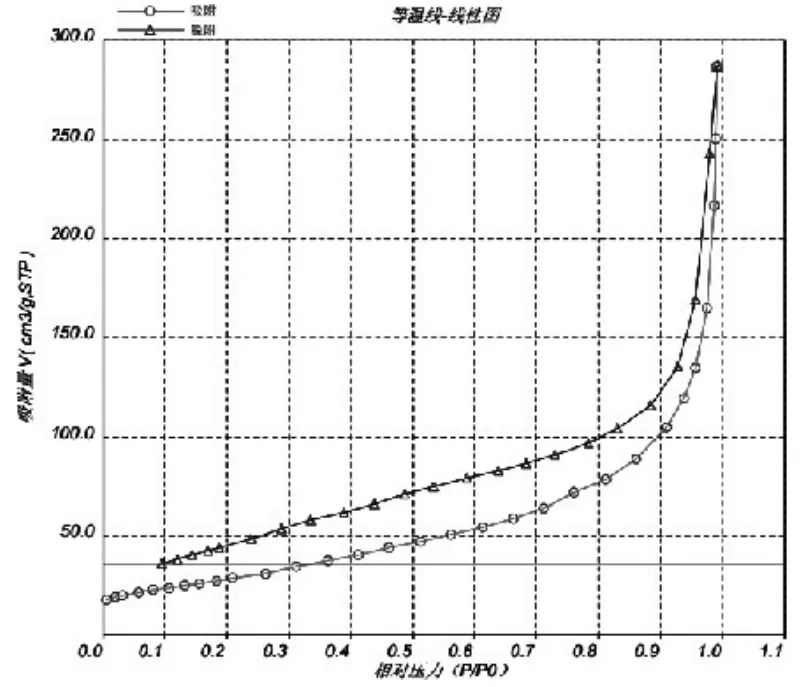
图5.100℃下所合成的硅酸锂粉体的等温线

图6.80℃下所合成的硅酸锂粉体的等温线

表2 几种硅酸锂材料的孔径分布Table2 The pore size distribution o f the Li2SiO4
北京金埃谱科技有限公司V-Sorb 2800TP比表面积及孔径分析仪,静态容量法测定,氦气做载气,氮气做吸附气,测定吸附-脱附等温线,由吸附数据通过多点线性拟合求得BET比表面积,用单凝聚点(P/Po=0.9963)法求得孔容积,由吸附等温线确定孔结构,利用公式4V/A(V为孔容积,A为吸附BET比表面积)计算平均孔径。
3 结果与讨论
3.1产物的FE-SEM分析
图1中A、B、C、D分别为采用微波水热法在150℃、120℃、100℃、80℃下合成的硅酸锂粉体的SEM图像。从图中可以看出,在150℃下所合成的硅酸锂粉体的晶粒尺寸较小且团聚严重,这可能是由于较高的反应温度使得形成了过多的晶核,但是又没有足够的时间或条件长大,就会造成晶粒尺寸变小,团聚正是尺寸小造成的,体系倾向于表面能的降低。随着温度的降低,体系内晶核减少,反应和扩散速度变慢,使得硅酸锂晶粒可以逐渐长大,团聚减弱,所合成的硅酸锂粉体的晶粒尺寸比在150℃条件下所合成的晶粒尺寸大且晶粒分散性好,从图中可以看到在120℃和100℃条件下所合成的硅酸锂晶体晶粒尺寸皆比较大,基本上没有团聚现象产生,但随着反应温度逐渐降低到80℃后,所合成的粉体呈疏松多孔状,这可能是由于反应温度继续降低时,所合成的硅酸锂晶体由于热力学的原因不能紧密结合所造成得。
3.2产物的EDS分析
为了进一步验证在80℃的低温下所合成的粉体为Li2SiO4晶体,对采用微波水热法在80℃下所合成粉体中的晶体颗粒进行了EDS点扫描,图1为EDS谱图,从图中可以看到粉体中主要含有的元素为Si和O两种元素,由于EDS可以检出的元素范围为4-92号元素,Li元素不在此范围内,因而EDS谱图中没有Li元素的谱峰,EDS定量结果显示Si和O两种元素的原子百分比接近于1:4,从以上结论进一步可以验证所合成的粉体为Li2SiO4粉体。(图2所示)
但其孔结构为非微孔型;在120℃和100℃下所合成的硅酸锂粉体的氮气吸附等温线皆为Ⅲ型,可知此温度下所合成的硅酸锂粉体与氮气分子具有弱的相互作用力,这可以解释为在此温度范围内所合成的硅酸锂粉体由于晶粒比较大,同时其又不具有微孔结构,所以对氮气分子的吸附能力比较弱,这也可从这两种粉体具有较小的比表面积而得到验证。在80℃下所合成的硅酸锂粉体的氮气吸附等温线为Ⅰ型,低压端偏Y轴则说明此温度下所合成的硅酸锂粉体与氮气分子具有非常强的相互作用力,这是由于存在许多微孔,微孔内的强吸附势所造成得。(如图3-图6所示)
表2为采用微波水热法分别在150℃、120℃、100℃、80℃下所合成的硅酸锂粉体的孔径分布表,从表中中孔和微孔的孔径分布数据皆可以看到,在80℃下所合成的硅酸锂粉体的孔径最小,可理解为其具有微孔结构;在120℃和100℃下所合成的硅酸锂粉体的孔径严重偏大,可理解为其具有中孔结构。80℃下所合成的硅酸锂粉体具有微孔结构这也可从SEM图1(D)中所具有的疏松多孔的结构而得到验证。
4 结语
采用微波水热法在低温条件下(80~150℃)成功合成了结晶良好、纯度较高且具有较小的晶粒尺寸和较大的比表面积的硅酸锂粉体,微波水热法将硅酸锂的合成温度降低到了80℃,与传统水热法相比显著提高了反应效率,降低了反应能耗,且在此温度下所合成的硅酸锂粉体具有微孔结构,表现出非常强的吸附能力。
[1]Pfeiffer H,Bosch P,Bulbulian S.Synthesisof lithium silicates[J].JournalofNuclearMaterials,1998,257(3):309-317.
[2]Tang Tao,Zhang Zhi,Meng Jianbo,et al.Synthesis and characterization of lithium silicate powders[J].Fusion Engineering and Design,2009,84(12):2124-2130.
[3]Cruz D,Bulbulian S,Lima E,et al,Kinetic analysis of the thermal stability of lithium silicates[J].Journal of Solid State Chemistry,2006,179(3):909-916.
[4]Morales A A,Preiffer H,Delfin A,et al.Phase transformations on lithium silicates under irradiation[J].Materials Letters,2001,50(1):36-40.
[5]Zhang Bo,Easteal Allan J.Effect of HNO3on crystalline phaseevolution in lithium silicate powders prepared by sol-gelprocesses[J].JournalofMaterials Science,2008,43(15):5139-5142.

