碳点-荧光素荧光共振能量转移体系在阿司匹林测定中的研究与应用
金文英 ,廖秀芬 ,陶慧林* ,赵 颖 ,刘绍州 ,梁永敏
(1.广西高校食品安全与检测重点实验室,桂林理工大学 化学与生物工程学院,广西 桂林 541004;2.广西产品质量检验研究院,广西 南宁 530007)
碳点-荧光素荧光共振能量转移体系在阿司匹林测定中的研究与应用
金文英1,廖秀芬2,陶慧林1*,赵颖2,刘绍州2,梁永敏1
(1.广西高校食品安全与检测重点实验室,桂林理工大学化学与生物工程学院,广西桂林541004;2.广西产品质量检验研究院,广西南宁530007)
研究了经L-y半胱氨酸修饰后的碳点(CDs)-荧光素(FAM)荧光共振能量转移体系,并利用该体系建立了测定阿司匹林(ASP)的新方法。结果表明:在λex=330 nm下,于pH 7.0的Tris-HCl缓冲液中,CDs与FAM反应5 min后能发生有效的荧光共振能量转移,能量供体CDs将能量转移到受体FAM,使FAM的荧光显著增强,而ASP的加入可有效猝灭FAM的荧光,且ASP浓度在1.0~150.0 μg/mL范围内与体系的荧光猝灭值ΔIF呈良好的线性关系(r=0.999 6),基于此建立了测定ASP的新方法。在最佳实验条件下,方法的检出限达0.33 μg/mL(3δ/k,n=11),回收率为 97.1%~105.3%,相对标准偏差(RSD)不大于4.6%(n=6)。常见的无机离子以及与ASP同类型的药物对测定影响较小,方法的选择性较好。
碳点;荧光素;荧光共振能量转移(FRET);阿司匹林
阿司匹林(Aspirin,ASP)是从柳树皮和柳叶中提取的传统解热镇痛药,现已广泛用于解热镇痛、抗风湿、预防暂时性脑缺血及中风,治疗脑血栓,预防心绞痛、心肌梗死[1]。同时,ASP可治疗女性痛经,治疗腹泻、胆道蛔虫,也具有抗肿瘤转移作用,针对不同的疾病,其用量各不相同。因此寻找阿司匹林含量测定的方法具有重要意义。目前测定ASP含量的方法主要有高效液相色谱法[2-3]、光度法[4-5]、电化学分析法[6-7]、荧光光谱法[8-9]等。
荧光共振能量转移(Fluorescence resonance energy transfer,FRET)是两个荧光基团间的距离小于10 nm时荧光能量由供体向受体转移的现象[10-11]。由于FRET方法简单、灵敏度高,在分析检测领域得到了很大的发展[12-13]。碳点(Carbon dots,CDs)是一种新型的纳米材料,具有发光性质稳定、荧光寿命长等特点,且与其他荧光材料相比具有更好的生物安全性,是一种优良的光学材料[14-15]。CDs被引入FRET中,使其应用领域不断扩大。本文选用CDs 为能量供体,荧光素(Fluorescein,FAM)作为能量受体,构建了一个新型的能量转移体系,并将所建立的FRET体系应用于阿司匹林肠溶片中阿司匹林含量的测定。
1 实验部分
1.1仪器与试剂
RF-5301PC 荧光光度计(日本岛津公司),TU-1901 双光束紫外可见分光光度计(北京普析通用仪器有限公司),FA1104电子分析天平(中国江苏泰兴市电子仪器厂),pHS-3C精密pH计(上海雷磁仪器厂),JEM-2010透射电子显微镜(日本电子株式会社)。
ASP标准液(250.0 μg/mL):使用时稀释至所需浓度;FAM(10 μg/L,广州化学试剂厂);三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl,pH 7.0):配制0.10 mol/L的Tris母液,然后用0.10 mol/L HCl溶液调至相应的pH值。实验所用试剂均为分析纯,实验用水为二次蒸馏水。
1.2实验方法
1.2.1水溶性CDs的合成按文献[16]稍作修改:在反应釜中加入0.2 g柠檬酸钠、1.5 g碳酸氢铵固体、10 mL水及50 μL 0.1 mol/L的L-y半胱氨酸在 180 ℃下反应 4 h左右,冷却装置后,定容至100 mL,于4 ℃冰箱中保存,备用。
1.2.2测定方法于一系列 5 mL 比色管中加入一定量的 CDs,FAM和ASP,用 pH 7.0的Tris-HCl缓冲液定容至刻度,反应 5 min 后,于λex=330 nm处测定相应荧光强度IF。仪器的激发和发射狭缝宽度均为 5 nm。
2 结果与讨论
2.1碳点(CDs)的表征
透射电子显微镜(TEM)、紫外光谱法、荧光光谱法是对 CDs 进行表征的常见手段。用TEM可对CDs进行直观的形貌观察,以获得其形状、粒径大小及分散性等信息。通过CDs的TEM图(图1A)可以看出所合成的 CDs 分散性较好,粒子尺寸分布较为集中。CDs的紫外吸收光谱和荧光光谱见图1B,其最大吸收峰在343 nm,荧光发射峰在443 nm,Stokes位移100 nm。根据参考文献,用硫酸奎宁作为标准物质(Φs=0.55)[17],计算得CDs的量子产率Φu为0.65。由此可见,本文所合成的CDs具有分散性好、粒度均匀、荧光量子产率高、峰形窄而对称等特点。

图1 CDs的TEM图(A)以及吸收光谱和荧光光谱(B)Fig.1 TEM image(A),absorption and fluorescence spectra of CDs(B)a.absorption spectrum;b.fluorescence spectrum
2.2FRET体系的构建
供体的荧光发射光谱和受体紫外吸收光谱有相当程度的光谱重叠是分子间发生能量转移的必要条件之一。对CDs的荧光光谱和FAM的吸收光谱进行分析可知,CDs的荧光峰在443 nm处,FAM的吸收峰在491 nm处,两者差为48 nm。此外,根据参考文献[18],计算得光谱重叠面积J=2.8×10-14J/(cm3·L·mol-1)。说明供体CDs的荧光光谱与受体FAM的紫外吸收有较好的重叠,为二者之间发生能量转移提供了前提条件。

图2 CDs(a)、FAM(b)和CDs-FAM(c)的荧光光谱Fig.2 Fluorescence spectra of CDs(a),FAM(b)and CDs-FAM mixture(c)ρCDs=4.0 μg/mL,ρFAM=2.0 μg/mL

图3 ASP对 CDs-FAM能量转移体系的影响Fig.3 Effects of ASP on the FRET of CDs-FAMρASP:(a-j):0.0,1.0,4.0,8.0, 16.0,40.0,60.0,80.0,120.0,150.0 μg/mL;ρCDs=4.0 μg/mL;ρFAM=2.0 μg/mL
为了获得理想的能量转移效果,用330 nm激发混合体系。同一物质在相同的浓度下分别绘制CDs、FAM和两者混合物的荧光光谱,结果如图2所示。由图2可知,体系中供体CDs发生荧光猝灭,将能量有效地转移给受体FAM,使FAM的荧光显著增强,说明在CDs-FAM之间发生了有效的荧光共振能量转移。
根据 Förster 非辐射能量转移机制,影响能量转移效率的主要因素是供体-受体之间的距离(r)和临界能量转移距离(R0)。供体与受体之间的能量转移效率E为[19]:
式中,F为加入能量给受体后给体的荧光强度;F0为未加入受体时给体的荧光强度;k2为偶极空间取向因子(取k2=2/3),N为水和有机溶剂的平均折射率(取1.37),Φ为供体的荧光量子产率,J为光谱重叠程度。根据前文计算结果Φ= 0.55,J=2.8×10-14J/(cm3·L·mol-1)。根据上式计算得E=0.66,R0=3.62 nm,r=3.25 nm,说明CDs与FAM间发生了有效的能量转移。

图4 CDs(a)及加入ASP前(b)、后(c)CDs-FAM的紫外吸收图谱Fig.4 Absorption spectra of CDs(a),and CDs-FAM system before(b)and after(c)addition of ASP ρCDs=4.0 μg/mL,ρFAM=2.0 μg/mL;ρASP=16.0 μg/mL
2.3ASP对CDs-FAM体系的作用
考察了不同浓度ASP对CDs-FAM能量转移体系的影响,结果如图3所示。ASP能有效猝灭CDs-FAM体系中FAM的荧光强度,且随着ASP浓度的增大,FAM的荧光猝灭程度增强。据此可以建立能量转移荧光猝灭体系体系测定ASP的新方法。

2.4实验条件的优化
按实验方法,考察了pH值、反应介质、反应温度和反应时间等条件对 CDs-FAM-ASP体系的影响。实验表明,pH 7.0时,ASP对体系的荧光猝灭最灵敏。因此考察了pH 7.0的不同缓冲介质及其用量对体系的影响,发现加入4 mL Tris-HCl 缓冲液时可获得最佳的猝灭效果。此外,体系在35 ℃下反应5 min可达稳定,并且可稳定1 h以上。
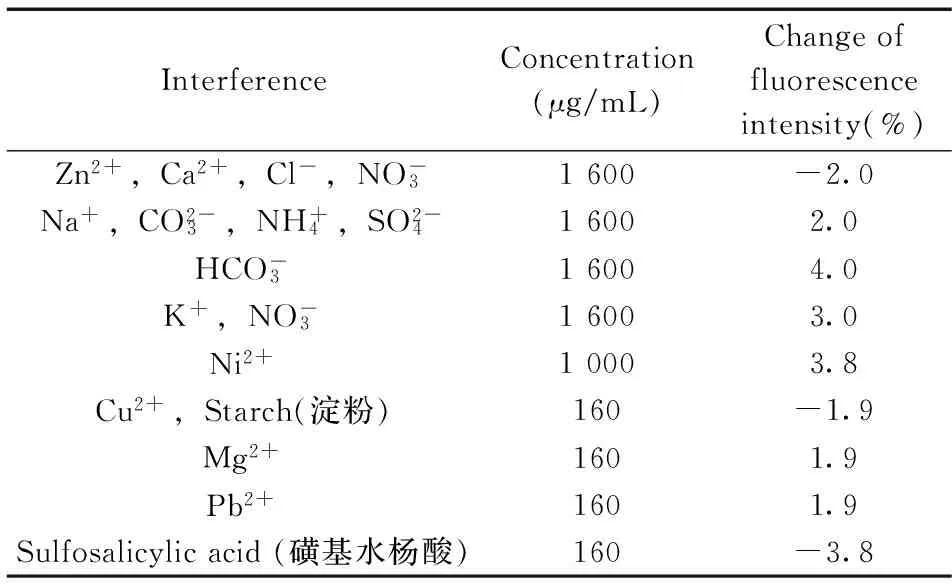
表1 干扰物质对体系的影响Table 1 Effect on the measurement result by interference
2.5工作曲线
按照“1.2.2”方法对不同浓度ASP进行检测,并绘制工作曲线,结果显示,体系的荧光猝灭值(ΔIF)与ASP 的浓度(ρ,μg/mL)在 1.0~150.0 μg/mL范围内呈良好的线性关系,线性方程为ΔIF=11.74ρ+4.34,相关系数(r)为 0.999 6,检出限(3δ/k)为0.33 μg/mL。
2.6干扰实验
ASP浓度为16 μg/mL 时,在最优实验条件下考察了部分共存物质对体系的影响,结果如表1所示。由表1可知,当相对误差控制在±5%以内时,常见阳离子、阴离子及小分子物质对体系基本没有影响,说明该体系对ASP具有较高的选择性。
2.7样品分析
考察了该 FRET 体系测定ASP的可行性和实用性,对ASP肠溶片(100 mg/粒)中ASP含量进行了检测。参考文献[20]进行样品前处理:取阿司匹林肠溶片1 粒,研碎,加入 3~5 mL乙醇,待溶解后将溶液转入100 mL容量瓶中,强烈振摇使阿司匹林溶解,再用乙醇定容至刻度。取50 μL 母液,按照实验方法,定容至5 mL进行检测,同时进行加标回收实验。结果测得ASP肠溶片中ASP的含量分别为96.8,98.0,102.1 mg/粒,方法回收率为97.1%~105.3%,相对标准偏差(RSD)不大于4.6%(见表2)。
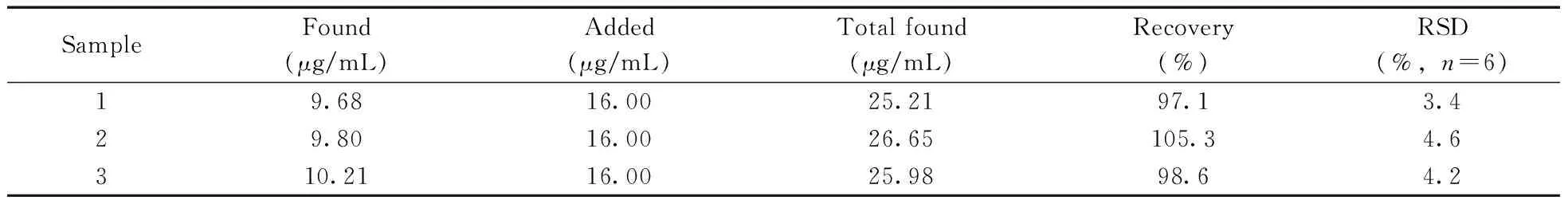
表2 样品的分析结果Table 2 Analytical results of samples
3 结 论
本文以CDs作为能量给体,FAM作为能量受体构建了CDs-FAM FRET体系,对 CDs-FAM体系进行探讨,计算了能量转移体系的相关参数,并利用 CDs-FAM体系建立了测定ASP的新方法。在最佳实验条件下,该方法对ASP的检测范围为1.0~150.0 μg/mL,相关系数(r)为 0.999 6,检出限达 0.33 μg/mL。将方法应用于阿司匹林肠溶片中ASP含量的测定,回收率为97.1%~105.3%,RSD不大于4.6%。该方法灵敏度高、选择性好、操作简单、线性范围宽,同时具有较高的准确度和精密度,具有推广应用价值。
[1]Pan Z A,Sun X F.PharmacopoeiaofChina.Beijing:Chemical Industry Press(潘正安,孙小芳.中华人民共和国药典.北京:化学工业出版社),2005.
[2]Kumaraswamy G,Ravindra N,Jyothsna B.AsianJ.Pharm.,2014,4(3):116-120.
[3]Mullangi R,Sharma K,Srinivas N R.Biomed.Chromatogr.,2012,26(8):906-941.
[4]Zhang X L,Su H,Yao Z X,Lan Y L.Chin.J.Spectrosc.Lab.(张小玲,粟晖,姚志湘,兰月来.光谱实验室),2011,28(4):1911-1915.
[5]Wang C X,Shu Y Q.GuangdongChem.Ind.(王晨霞,舒余琪.广东化工),2014,41(23):200-201.
[6]Kruanetr S,Prabhu R,Pollard P,Fernandez C.Surf.Eng.Appl.Electrochem.,2015,51(3):283-289.
[7]Zhou G Z,Lu D,Sun Y X.J.HunanUniv.ArtsSci.:Nat.Sci.Ed.(周谷珍,鲁丹,孙元喜.湖南文理学院学报:自然科学版),2012,24(2):28-30.
[8]Wei X,Zhou Z P,Hao T F,Xu Y Q,Li H J,Lu K,Dai J D,Zheng X D,Gao L,Wang J X,Yan Y S,Zhu Y Z.Microchim.Acta,2015,182(7):1527-1534.
[9]El-Din M S,Eid M,Zeid A.Luminescence,2013,28(3):332-338.
[10]Clegg R M.Curr.Opin.Biotechnol.,1995,6(1):103-110.
[11]Ha T,Enderle T,Ogletree D F,Chemla D S,Selvin P R,Weiss S.Proc.Nat.Acad.Sci.,1996,93(13):6264-6268.
[12]Chen G W,Song F L, Xiong X Q,Peng X J.Ind.Eng.Chem.Fundam.,2013,52(33):11228-11245.
[13]Sahoo H J.Photochem.Photobiol.C,2011,12(1):20-30.
[14]Xu Y,Wu M,Feng X Z,Yin X B,He X W,Zhang Y K.Chem.Eur.J.,2013,19(20):6282-6288.
[15]Liu L Q,Li Y F,Zhan L,Liu Y,Huang C Z.Sci.Chin.Chem.,2011,54(8):1342-1347.
[16]Guo Y M,Wang Z,Shao H W,Jiang X Y.Carbon,2013,52:583-589.
[17]Tao H L,Liao X F,Zhou S L,Zhong F X,Yi Z S,Chen J.J.Instrum.Anal.(陶慧林,廖秀芬,周素莲,钟福新,易忠胜,陈俊.分析测试学报),2014,33(7):820-824.
[18]Tao H L,Zhu S Y,Shou H J,Li S H.Chin.J.Anal.Chem.(陶慧林,朱仕毅,寿红娟,黎舒怀.分析化学),2011,39(3):372-376.
[19]Gao G Y,Liu L,Fu X,Yang R,Qu L B.Chin.J.Lumin.(高桂园,刘璐,付璇,杨冉,屈凌波.发光学报),2012,33(8):911-915.
[20]Li K Q.Chin.Pharm.(李克庆.中国药师),2006,9(10):925-927.
Study on Carbon Dots-Fluorescein Fluorescence Resonance Energy Transfer System and Its Application in Aspirin Analysis
JIN Wen-ying1,LIAO Xiu-fen2,TAO Hui-lin1*,ZHAO Ying2,LIU Shao-zhou2,LIANG Yong-min1
(1.Guangxi Colleges and Universities Key Laboratory of Food Safety and Detection,College of Chemistry and Bioengineering,Guilin University of Technology,Guilin541004,China;2.Guangxi Zhuang Autonomous Region Testing Institute of Product Quality,Nanning530007,China)
A fluorescence resonance energy transfer(FRET)system between fluorescence carbon dots(CDs,donor)and fluorescein(FAM,acceptor)was constructed,and a novel method for the sensitive and selective determination of aspirin(ASP)was accordingly proposed.It was found that in pH 7.0 Tris-HCl buffer,effective energy transfer from CDs to FAM occurred,which resulted in a great enhancement of the fluorescence intensity of FAM.Upon the addition of ASP,fluorescence quenching of FAM occurred,and the change of FAM fluorescence intensity was in a good linearity(r=0.999 6)with ASP in the concentration range of 1.0-150.0 μg/mL.A novel fluorescence quenching platform for the determination of ASP was constructed.Under the optimum conditions,the detection limit of ASP for this method was 0.33 μg/mL(3δ/k,n=11),and the spiked recoveries ranged from 97.1%to 105.3%with RSD(n=6)not more than 4.6%.The result showed that common relevant substance,cations and anions did not interfere with the detection of ASP.
carbon dots;fluorescein;fluorescence resonance energy transfer(FRET);aspirin
2016-03-14;
2016-04-09
国家自然科学基金资助项目(61264007);广西高校食品安全与检测重点实验室资助项目
陶慧林,教授,研究方向:光谱分析,Tel:0773-5898551,E-mail:thl@glut.edu.cn
10.3969/j.issn.1004-4957.2016.09.013
O657.3;TQ460.72
A
1004-4957(2016)09-1147-05

