在线中和富集-离子色谱法测定高纯氢氧化钠中痕量阴离子
凌小芳,郑洪国,谭诗珂,唐 聪,吴 宇
(1.成都产品质量检验研究院有限责任公司,四川 成都 610100;2.赛默飞世尔科技有限公司,四川 成都 610011)
在线中和富集-离子色谱法测定高纯氢氧化钠中痕量阴离子
凌小芳1*,郑洪国2,谭诗珂1,唐聪2,吴宇1
(1.成都产品质量检验研究院有限责任公司,四川成都610100;2.赛默飞世尔科技有限公司,四川成都610011)
建立了在线中和、富集待测离子后用离子色谱对高纯氢氧化钠中痕量阴离子进行检测的分析方法。样品经超纯水溶解、稀释后直接进样。试样经外接纯水输送至In Guard H消除OH-基体干扰,然后经过富集柱浓缩待测阴离子,再经阀切换技术进入离子色谱系统,以淋洗液发生器产生的KOH为淋洗液,流速为1.0 mL/min,采用IonPac AS11-HC分析柱分离后,电导检测器检测。结果表明,在0.1~10.0 mg/L的线性范围内,氯离子、硫酸根、氯酸根的线性相关系数分别为0.999 8,0.999 6和0.999 2。方法对于氯离子、硫酸根、氯酸根的检出限分别为0.03,0.07,0.06 mg/kg,加标回收率分别为92%~104%,91%~111% 和 92%~106%,相对标准偏差(n=7)均小于2.0%。
高纯氢氧化钠;氯离子;硫酸盐;氯酸盐;在线中和富集;离子色谱
随着我国合成纤维生产的蓬勃发展,化纤工业生产的基础原料高纯氢氧化钠的需求量日益增加,每年约需40万吨[1]。GB/T 11199-2006《高纯氢氧化钠》中所规定的氢氧化钠是指用氯化钠水溶液电解产生的氢氧化钠[2],其中对不同类型高纯氢氧化钠中氯化物(以氯化钠计)、硫酸盐(以硫酸钠计)、氯酸盐(以氯酸钠计)的最低限量要求分别为0.004%,0.001%和0.001%,均为痕量限定。目前,针对氯离子、硫酸根、氯酸根3种阴离子的经典分析方法有比浊法、沉淀法、滴定法、分光光度法。这些方法大多针对不同离子分别进行纯手工操作或结合小型仪器测定,操作繁琐且易受实验条件、人员因素的干扰[3-5],并且所用硫氰酸汞、邻联甲苯胺等试剂对人体及环境有毒害性。因此,建立一种操作简便、准确、环境友好的方法对此3种痕量阴离子进行检测很有必要。
离子色谱法在无机阴离子分析领域是一种成熟的技术,具有操作简单、成本低等优点,是同时测定多种阴离子的理想方法[6]。目前,该方法在氯离子、硫酸根、氯酸根测定方面已有很多报道[7-12]。但运用离子色谱测定浓碱时,样品基体会干扰分析,待测组分的分离情况也会发生很大改变[6,13]。Petersen等[13]运用离子色谱法测定了50%氢氧化钠溶液中的硝酸盐和硫酸盐含量,曾文芳等[14]运用离子色谱法测定了浓碱中痕量阴离子,此两种方法在对浓碱中的痕量阴离子进行测定前,均采用离线中和小柱或离子交换树脂进行手动离线中和。但由于离线小柱的容量较小,导致样品中和不完全,且手动离线中和易对痕量离子造成污染,导致测定结果重复性差。有研究提出使用在线中和器对浓碱中的氢氧根进行在线中和[6],但此方法成本高、仪器复杂,不适合在实验室推广。贺伟等[15]利用柱在线中和富集离子色谱法测定大气吸收液中的痕量阴离子,采用在线中和柱取代在线中和器对氢氧根离子进行在线中和。本文在借鉴前人研究经验的基础上,尝试用柱在线中和、富集离子色谱法经过一次处理,同时测定了高纯氢氧化钠中的氯离子、硫酸盐、氯酸盐3种阴离子。此方法操作便捷、重复性好、易实现自动化,且降低了成本和仪器的复杂程度,大大提高了方法的适用性。
1 实验部分
1.1仪器与试剂
ICS2000离子色谱仪(Thermo Fisher),配置电导检测器。ASRS500,4 mm抑制器。阴离子分析柱AS11-HC+AG11-HC。在线中和富集系统见图1。
实验用水为超纯水(电导率18.2 MΩ·cm),由Milli-Q纯水机产生。氯化钠标准品(纯度≥99%,Sigma公司);无水硫酸钠标准品(Sigma公司);氯酸钾标准品(Sigma-Aldrich公司)。
1.2试剂的配制
氯离子、硫酸根、氯酸根标准储备液(1 000 mg/L):分别称取1.648 4 g氯化钠、1.478 7 g无水硫酸钠和1.468 8 g氯酸钾标准品溶于水中,用水稀释至1 L,贮于聚丙烯或高密度聚乙烯瓶中,4 ℃冷藏存放。氯离子、硫酸根、氯酸根离子混合标准溶液(100 mg/L):分别移取10 mL氯离子、硫酸根、氯酸根标准储备液至100 mL容量瓶,用水定容至100 mL。再生液:称取192.2 g(精确至0.001 g)甲磺酸,用水定容至1 L,即为2 mol/L的甲磺酸溶液。淋洗液:由淋洗液发生器产生的KOH溶液。
1.3色谱条件
色谱柱:阴离子分析柱AS11-HC+AG11-HC;抑制器:ASRS500,4 mm;柱温:30 ℃;进样体积25 μL;淋洗液及六通阀切换时间程序见表1。

表1 淋洗液及阀切换时间程序Table 1 Time program for eluent and valve-switching
*valve 1 and valve 2 are neither in the loading state nor in the injection state,it is the running time of program after sample injected
1.4样品前处理
称取试样11.208 g(精确至0.000 1 g),以水溶解并定容至100 mL,充分振荡混匀后作为试样溶液待测。空白样品除不加试样外,其他处理步骤同上。
2 结果与讨论
2.1样品预处理条件的选择
AS11-HC阴离子分离柱采用高交联度(55%)、小直径(9 μm)的乙基-乙烯基苯-二乙烯基苯多孔基球为基质,基球表面涂覆直径70 nm的MicroBeadTM阴离子交换涂层,使其柱容量为290 μeq(250×4 mm)。AS11-HC分离柱具有以下优点:进行高浓度样品分析时不会出现过载和峰拖尾现象;通过大体积直接进样可检测痕量有机酸和无机阴离子;允许使用更高浓度的淋洗液,从而扩大梯度淋洗的范围。因此,该柱适于采用NaOH溶液进行梯度淋洗分析复杂基体中的阴离子。
由于高纯氢氧化钠中的氯离子、硫酸根、氯酸根浓度很低,而氢氧化钠自身的OH-基体浓度很高,所以OH-对分析的准确性影响较大。故样品经溶解稀释后直接进样的方法受到限制。本文采用在线样品前处理装置对样品进行在线处理后再进样检测,其原理是利用阀切换使强碱性样品通过在线中和柱后变成中性样品,再完全进入大定量环或浓缩柱中从而实现自动在线前处理,实验装置如图1所示。其中,阀1和阀2为电磁六通阀。IonPac ATC-HC(9×75 mm)为超纯水纯化柱,In Guard H(9×24 mm)为在线基体消除柱,IonPac TAC-ULP1(23 mm×5 mm)为富集柱,IonPac AG11-HC和IonPac AS11-HC分别为保护住和分析柱。在线样品前处理柱通过外接的超纯水进行平衡,每进80针样品后用20 mL 2 mol/L甲磺酸溶液进行冲洗再生。如图1所示,管路走实线状态时六通阀1状态为Load,六通阀2状态为Inject,反之相反。实验过程为:①进样。阀1处于Load状态,阀2处于Inject状态,在线基体消除柱与超纯水源外接泵相连,富集柱与分析柱相连;②在线基体消除。以超纯水将25 μL定量环中样品转移至基体消除柱上,待测组分被持续转移富集到富集柱上,持续时间为1 min。阀1处于Inject状态,阀2处于Load状态;③ 待测组分分析。以KOH淋洗液将富集柱上的待测组分转移至分析柱上后,进行分离测定,基体消除柱持续不断地以水进行冲洗。阀1处于Load状态,阀2处于Inject状态。
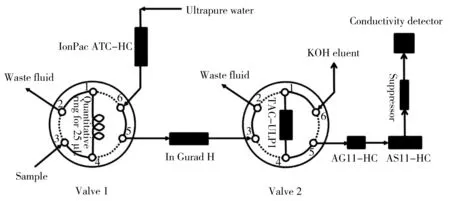
图1 在线中和富集系统装置图Fig.1 Drawing of online neutralization and enrichment system
2.2超痕量组分的在线浓缩切换时间选择

表2 不同浓缩切换时间的峰面积Table 2 Peak area of different enrichment switch time
基于本方法运用阀切换对样品进行在线浓缩,考察了同一样品在1,2,3 min不同浓缩时间下检测的峰面积结果(表2)。由检测结果可知,在1.0 mL/min水的载动下,样品从定量环经In Guard H柱去除基体,再将待测组分富集到浓缩柱TAC-ULP1上仅需1 min。考虑到In Guard H柱及连接管路死体积的影响,不建议将收集时间进一步缩短,以确保不同实验室之间检测结果的良好重现性,所以最终选择超痕量组分的在线浓缩切换时间为1 min。
2.3方法的线性
在最佳色谱条件下,对浓度为0.1,0.5,1.0,5.0,10.0 mg/L的氯离子、硫酸根、氯酸根系列浓度标准溶液进样分析。以阴离子的浓度(mg/L)为横坐标,对应峰面积为纵坐标,绘制标准曲线。结果显示,在0.1~10.0 mg/L范围内,3种阴离子的线性关系良好,相关系数分别为0.999 8,0.999 6,0.999 2,可满足现代分析方法的要求。
2.4方法的准确度
为表征该方法对不同样品、不同加标浓度的检测结果,选择对编号为1,4,4-1,7,10的样品进行不同浓度的加标试验(其中4-1样品和4样品为同一厂家生产的同一批次样品),并对同一样品进行不同加标浓度的检测以考察此方法的准确性。试样的检测结果及加标回收率见表3。该方法对3种阴离子的回收率为91%~111%,回收率满足分析要求。
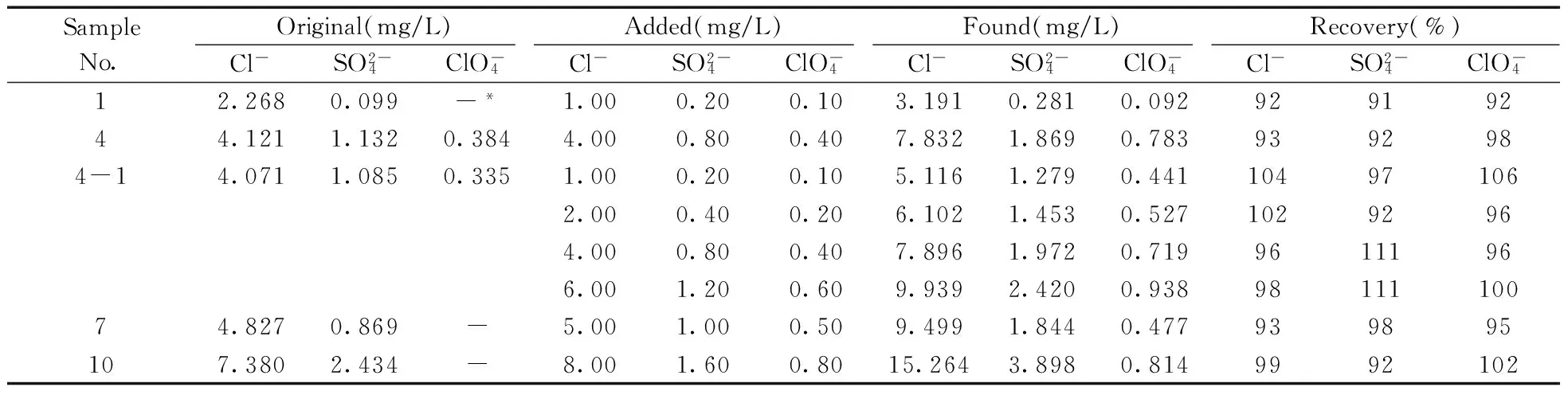
表3 样品的检测结果及加标回收率Table 3 Determination results of sample and its spiked recoveries
*:no data
2.5方法的重复性、检出限及定量下限
采用本方法对样品溶液连续进样测定7次,7次进样测定的平均结果见表4,并计算测定结果的标准差(S)和相对标准偏差(RSD)。根据MDL=3.14SV/m(mg/kg) (其中V为样品的定容体积,m为此样品在该体积下的称样量)计算3种阴离子的检出限,根据MQDL=4MDL计算方法的定量下限。结果显示,该方法对氯离子、硫酸根、氯酸根检测的RSD分别为0.12%, 1.0%, 1.1%, 说明方法的重复性较好。对氯离子、硫酸根、氯酸根的检出限分别为0.03, 0.07, 0.03 mg/kg,定量下限分别为0.12, 0.29, 0.26 mg/kg。结果表明此方法满足分析要求,具有可行性。

表4 方法的重复性、检出限及定量下限Table 4 Repeatiblity, detection limit and quantitative limit of the method
3 结 论
本文基于离子色谱法,利用在线中和柱和阀切换技术实现了待测样品的在线中和、富集,进而对高纯氢氧化钠中的氯离子、硫酸根、氯酸根进行检测。该方法能有效解决检测中前处理操作复杂、繁琐的问题,降低人为因素的干扰。此外,柱在线中和处理方法的运用中和了高纯氢氧化钠溶液中高浓度的OH-,去除了样品中的碳酸盐,有效消除了检测过程中的基体干扰,降低了背景电导。在线浓缩富集技术的应用实现了痕量阴离子待测物的浓缩富集,从而降低了该方法的检出限并使实验结果更精确。该方法对3种痕量阴离子检测的回收率为91%~111%,RSD为0.12%~1.1%,检出限等指标均满足现代仪器分析的要求。
[1]GB/T 11212-2013.Sodium Hydroxide for Chemical Fiber Use.National Standards of the People’s Republic of China(化纤用氢氧化钠.中华人民共和国国家标准).
[2]GB/T 11199-2006.High-purity Sodium Hydroxide.National Standards of the People’s Republic of China(高纯氢氧化钠.中华人民共和国国家标准).
[3]GB/T 11213.2-2007.Sodium Hydroxide for Chemical Fiber Use-Determination of Sodium Chloride Content——Spectrometric Method.National Standards of the People’s Republic of China(化纤用氢氧化钠 氯化钠含量的测定 分光光度法.中华人民共和国国家标准).
[4]GB/T 11213.5-2006.Sodium Hydroxide for Chemical Fiber Use——Determination of Sulphate Content.National Standards of the People’s Republic of China(化纤用氢氧化钠 硫酸盐含量的测定.中华人民共和国国家标准).
[5]GB/T 11200.1-2006.Sodium Hydroxide for Industrial Use-Determination of Sodium Chlorate Content——o-Tolidinespectrometric Method.National Standards of the People’s Republic of China(工业用氢氧化钠 氯酸钠含量的测定 邻-联甲苯胺分光光度法.中华人民共和国国家标准).
[6]Mou S F,Liu K N,Ding X J.MethodandApplicationofIonChromatography.2nd ed.Beijing:Chemical Industry Press(牟世芬,刘克纳,丁晓静.离子色谱方法及应用.2版.北京:化学工业出版社),2005:17-225.
[7]Wang M Y,Wang M J,Li P C,Li Y H,Du X R.RockMiner.Anal.(王梅英,王敏捷,李鹏程,李艳华,杜晓冉.岩矿测试),2013,32(4):586-589.
[8]Wu K Y,Ren W X,Xue P C,Lei T R.Mod.Instrum.(武开业,任文祥,薛鹏程,雷涛瑞.现代仪器),2009,15(1):70-71.
[9]Tai H X.ChinaChlor-Alka(台红霞.中国氯碱),2009,3:37-39.
[10]Yao C Y,Chen M L.J.ZhejiangUniv.:Sci.Ed.(姚超英,陈梅兰.浙江大学学报:理学版),2009,36(5):575-580.
[11]Hu Z Y,Ye M L,Pan G W,Zhang T T.J.Instrum.Anal.(胡忠阳,叶明立,潘广文,张婷婷.分析测试学报),2012,31(5):580-583.
[12]Tian F,Xie J L.Chin.J.Anal.Chem.(田芳,谢家理.分析化学),2004,32(4):522-524.
[13]Pettersen J M,Johnsen H G,Lund W.Talanta,1988,(3):245-247.
[14]Zeng W F,Ye M L,Zhu Y.J.Instrum.Anal.(曾文芳,叶明立,朱岩.分析测试学报),2006,25(2):112-114.
[15]He W,Ding H,Shi C O,Yang L,Wang W J.Chin.J.Chromatogr.(贺伟,丁卉,施超欧,杨柳,王文佳.色谱),2012,30(4):340-344.
Determination of Trace Anions in High Purity Sodium Hydroxide by Ion Chromatography with On-line Sample Neutralization and Column Concentration
LING Xiao-fang1*,ZHENG Hong-guo2,TAN Shi-ke1,TANG Cong2,WU Yu1
(1.Chengdu Institute of Product Quality Inspection Co.Ltd.,Chengdu610100,China;2.Thermo Fisher Scientific Corporation,Chengdu610011,China)
An ion chromatographic(IC) method was developed for the determination of trace anions in high purity sodium hydroxide after sample neutralization and column concentration.Samples were dissolved and diluted with de-ionized water,and then injected into the IC system directly without any further pretreatment.The sample solution was delivered with de-ionized water,firstly on-line filtrated with In Guard H column for pre-removing OH-,and then concentrated with IonPac TAC-ULP column.The anions under test in the enrichment column were delivered in the IC system when the valve was switched.With the eluent KOH produced by eluent generator at a flow rate of 1.0 mL/min,the anions were separated on an IonPac AS11-HC column and detected with conductivity detector,then quantitively analyzed by the external standard method.The results indicated that the correlation coefficients of chloride,sulfate,chlorate were 0.999 8,0.999 6 and 0.999 2,respectively,in the linear range of 0.1-10.0 mg/L.The detection limits for chloride,sulfate,chlorate were 0.03,0.07,0.06 mg/kg,respectively,and their spiked recoveries were 92%-104%,91%-111% and 92%-106%,respectively,with their relative standard deviations (n=7) not less than 2.0%.The method was applied in the determination of anions in high purity sodium hydroxide samples with satisfactory results.
high purity sodium hydroxide;chloride;sulfate;chlorate;on-line sample neutralization and column concentration;ion chromatography(IC)
2016-01-28;
2016-03-07
凌小芳,硕士,工程师,研究方向:化学工程,Tel:028-84843082,E-mail:lingfang11111@sina.cn
10.3969/j.issn.1004-4957.2016.09.014
O657.75;TQ425.222
A
1004-4957(2016)09-1152-05

