SDS影响下煤层气水合物储气特性的Raman光谱分析
吴 强, 赵子琪, 刘传海
(1.黑龙江科技大学 安全工程学院, 哈尔滨 150022;2.黑龙江科技大学 瓦斯等烃气输运管网安全基础研究国家级专业中心实验室, 哈尔滨 150022)
SDS影响下煤层气水合物储气特性的Raman光谱分析
吴强1,2,赵子琪1,2,刘传海1,2
(1.黑龙江科技大学 安全工程学院, 哈尔滨 150022;2.黑龙江科技大学 瓦斯等烃气输运管网安全基础研究国家级专业中心实验室, 哈尔滨 150022)
煤层气储运是影响其综合利用的主要因素。利用自主搭建煤层气水合反应Raman原位测试平台,在2.0 ℃、4.0 MPa条件下开展四种浓度SDS溶液体系煤层气水合实验,获得不同时刻气相及反应结束时刻水合物相Raman光谱图。基于Raman谱带面积比、van der Waals-Platteeuw模型,计算出各体系水合物孔穴占有率、水合指数等结构参数,进而确定出水合物含气率。结果表明:水合过程气相Raman谱峰强度呈显著梯度变化,反映了煤层气水合反应存在微观物质传递;水合指数随SDS浓度增大而呈递减趋势,当SDS浓度为5.2 mmol/L时,含气率达最大值。
煤层气水合物; 拉曼光谱; SDS; 水合指数; 含气率
0 引 言
煤层气作为一种非常规能源,其安全、资源、环境效应逐渐被重视[1-3]。煤层气(CH4>90%)储运是影响其综合利用的主要因素。目前,主要储运方法有高压压缩、低温液化、管道运输等。鉴于煤层气水合物具有固化温度压力条件温和、储气率高(1 m3水合物可储存164 m3CH4)、储存安全稳定(常压、-10~-15 ℃不易分解),课题组提出水合物法储存与运输煤层气的技术思路。但是,煤层气固化速度慢、生成量小,难以满足连续化工业应用要求,制约了该技术的发展。
煤层气与水络合固化过程,是物质传递与热量传递过程。研究发现,机械法、试剂与介质添加法是促进气体水合物快速生成的两种有效措施。Lv等[4]利用大型鼓泡塔反应器研究CP流速、CH4操作压力及温度对CP-CH4水合物生成的影响;Yang等[5]研究TBAB-CH4体系在0~5 ℃、2.01~7.07 MPa条件下,CH4的储气能力与压力和TBAB浓度的关系;Tsimpanogiannis等[6]利用鼓泡塔反应装置研究多孔介质内CP-CH4体系的反应特征。
已有研究多为宏观层面,通过温度、压力变化确定反应体系水合物生成过程变化规律,很难观测到水合物形成过程的微观细节。国外学者利用Raman光谱技术开展含热力学促进剂体系水合物特征研究。Hashimoto等[7]利用Raman光谱技术证实,在THF-H2体系和TBAB-H2体系中由于少量的THF或TBAB能够形成半笼型水合物,使得体系中的H2会占据水合物笼的小孔穴,而THF或TBAB则进入大孔穴。Trueba等[8,9]为了阐明水合物潜在储H2能力,运用Raman光谱技术对TBAB-H2和TBAF-H2半笼型水合物的生成动力学开展了一系列实验;Moryama等[10]运用Raman光谱技术测试出,体系CH4+THF形成的是II型甲烷水合物,当压力高于3 MPa时,CH4+THF体系中水合物小孔穴中CH4分子逐渐增多,并且在5~60 MPa的压力下,小孔穴中的CH4分子几乎被占满。
上述实验主要基于Raman光谱法研究热力学添加剂对CH4、H2等一元气体水合物的影响,关于动力学添加剂对气体水合物微观特性变化鲜见报道。
笔者基于Raman光谱测试技术对不同浓度SDS(十二烷基硫酸钠)溶液影响下煤层气水合物含气率进行研究。通过开展对水合反应产物的Raman光谱原位检测及定量分析,从水合物结构类型、孔穴占有率和水合指数等微观指标探讨不同浓度SDS对煤层气水合物含气率的影响。
1 实 验
1.1仪器与材料
图1为煤层气水合物Raman原位测试系统。LabRAM HR800可见显微共焦Raman光谱仪由法国Jobin Yvon公司生产,配备开放式显微系统、高精度自动平台、532 nm激光器及50倍长焦物镜。实验扫谱范围为2 800~3 600 Raman Shift。自主设计的夹套制冷型高压可视原位反应釜采用蓝宝石视窗,有效容积3 mL,有效承压20 MPa。低温恒温槽由上海比朗仪器有限公司生产,控温范围-10~95 ℃。数据采集器、工控机分别记录原位反应釜压力/温度、Raman光谱数据。实验用纯CH4气样(体积分数为99.99%)模拟煤层气,由哈尔滨通达气体有限公司配制;SDS由天津博迪化工股份有限公司生产;实验用水为自制蒸馏水。
Sun等[11,12]用悬滴法在273.2~278.8 K和0.4~9.5 MPa范围内测定了CH4和SDS溶液两相界面张力进而确定了临界胶束浓度(CMC值),发现当SDS的浓度达到1.7 mmol/L左右时,达到了在CH4-H2O系统中的临界胶束浓度。SDS溶液的浓度为CMC时能够有效地降低水合反应物的两相界面张力,有利于促进水合物生成,基于此,确定了实验SDS浓度,实验方案见表1。
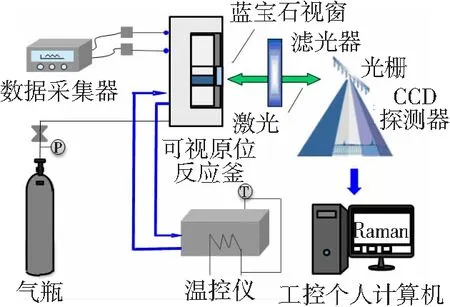
图1 煤层气水合反应Raman原位测试平台
Fig. 1In-situ Raman spectrascopy test platform for coalbed methane hydrate

表1 水合体系的初始条件
1.2实验方法
首先,利用单晶硅样品对Raman光谱仪进行校正。利用蒸馏水清洗反应釜2~3次后,注入1.5 mL反应溶液。然后,将低温恒温槽设定为2.0 ℃并开始制冷循环,直至反应釜内的温度达到并保持在2.0 ℃。向釜内充入煤层气置换2次,随后充入煤层气至4.0 MPa,并立即对气相进行Raman测试,每隔20 min测试一次,直至反应釜内压力不再变化时,对最终水合产物进行Raman测试。
2 结果与讨论
2.1水合过程煤层气气相Raman光谱分析
由于Raman谱线强度与入射光强度和样品分子的浓度成正比[13],故气相谱峰强度变化可反映气相CH4浓度变化,进而可定性推断出CH4分子在气相与水合物相之间的物质传递量的规律。
图2为四组煤层气气相Raman光谱,图2中显示,2 919 cm-1处为CH4气相峰。每组实验进行六次气相测试,分别自第0 min开始,每间隔20 min测试一次,图中谱峰为气相CH4的C—H键伸缩振动特征峰。图2a~d分别为0、1.7、3.4和5.2 mmol/L SDS+CH4体系气相Raman光谱与各组每个最高峰点值随时间变化的曲线,由图2可见,峰强随时间的增长而降低。
图2a所示,清水体系在前时间100 min内无生成水合物,故选择从0 min开始每间隔200 min测试一次。继续观察后发现,当水合物反应进行至400 min时,反应釜内开始出现颗粒状水合物晶体,在0~400 min内CH4气相峰强度下降不明显,说明在此阶段内从气相到水合物相发生了较慢且少量的物质传递,400~600 minCH4气相峰强的下降幅度变得明显,说明在此阶段CH4分子继续转移到水合物相中。600~800 min峰强下降幅度小,800~1 000 min峰强无明显变化,说明物质传递过程结束。
由图2可以较为直观地看出气相谱峰强度逐渐减弱,说明CH4分子在气相和水合物相之间发生了物质传递,并且SDS浓度分别为1.7、3.4和5.2 mmol/L时,均在短时间内发生了较大量的物质传递,物质传递速率均较0 mmol/L时大,说明SDS可以加快CH4分子在气相和水合物相之间的物质传递速率。
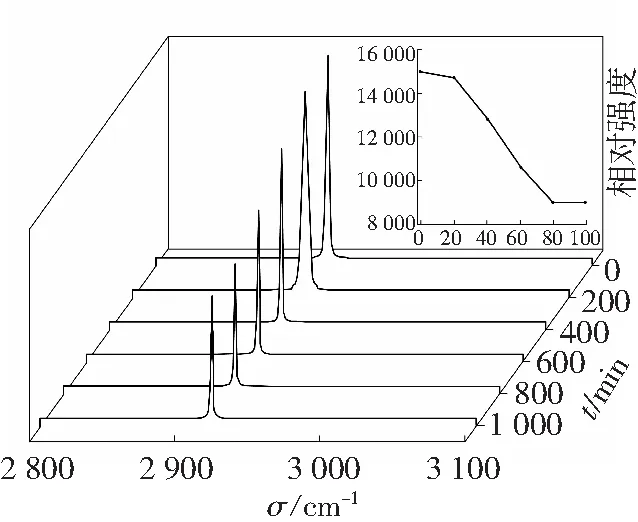
a
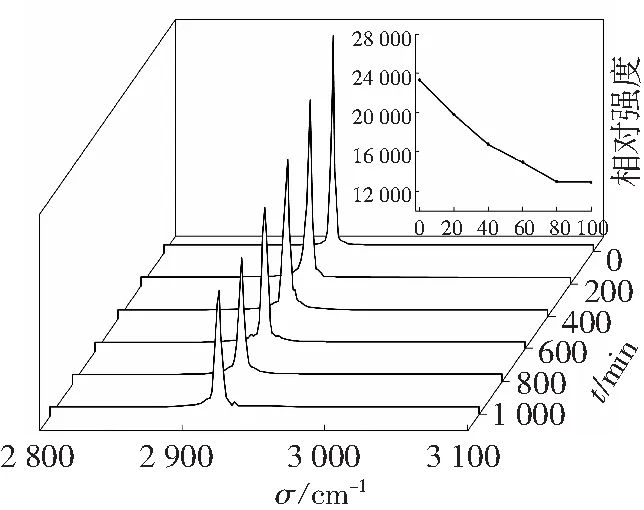
b

c
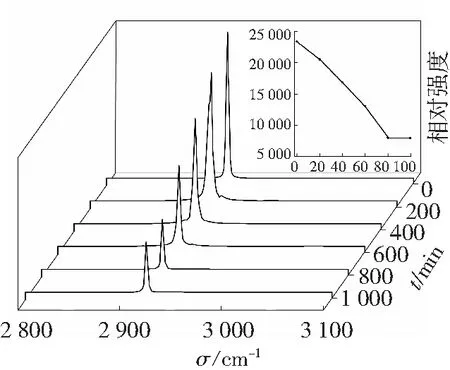
d
Fig. 2C—H stretching band of CH4vapor phase in four systems
2.2水合物相Raman光谱分析
图3是实验体系1~4水合物相Raman光谱。以图3a谱图为例说明水合物相Raman光谱特征,图中显示CH4分子水合物相Raman峰相对气相峰发生偏移,分别向低波数和高波数迁移,2 904 cm-1处为大孔穴中CH4分子的特征峰,2 919 cm-1处为小孔穴的特征峰。 CH4分子特征峰之所以发生偏移,是因为CH4分子分别进入水合物大、小孔穴,化学环境不同导致。据文献[14,15]所知,实验体系1~4中生成的CH4水合物均为I型。在3 000~3 500 cm-1处的宽峰是水合物中水分子O—H键振动峰。由图中实验照片可以看出,水合物生成位置具有一定的随机性。
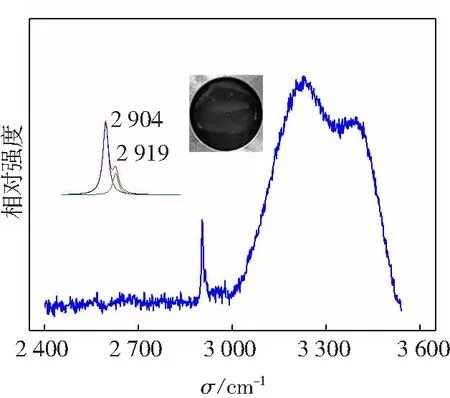
a cSDS=0 mmo1/L
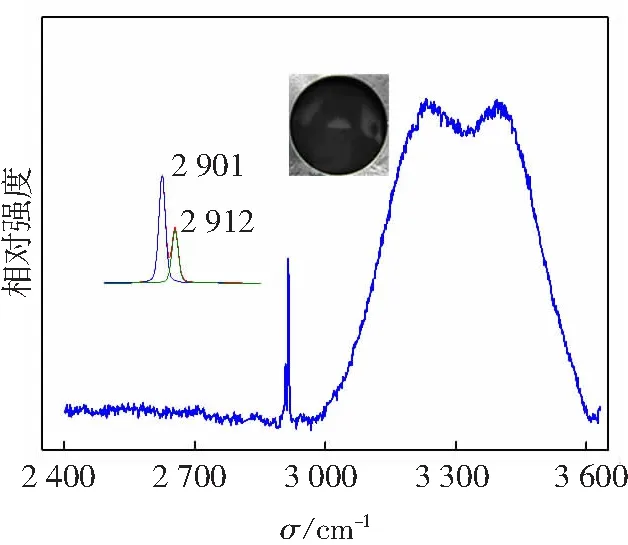
b cSDS=1.7 mmo1/L
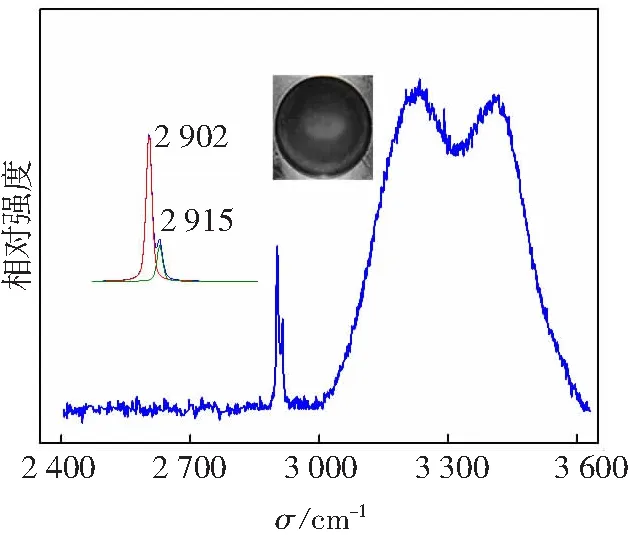
c cSDS=3.4 mmo1/L
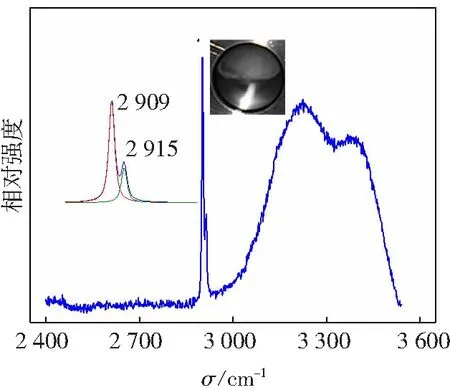
d cSDS=5.2 mmo1/L
Fig. 3C—H stretching band and O—H stretching band of CH4hydrate
2.3水合物含气率的计算
理论上,CH4分子I型结构水合物可以表示为8 CH4·46 H2O,即CH4·5.75 H2O,5.75为理论水合指数,一般用n表示[16]。
运用Labspec5.0对Raman谱图数据进行分析,再利用谱峰拟合软件PeakFit对四个体系的水合物Raman谱带进行褶积,最终混合Gauss+Lorenz谱带面积比等于大、小孔穴中CH4分子的数量比,结果如表2所示。
运用van der Waals-Platteeuw模型及谱带面积比确定大孔穴与小孔穴中CH4的绝对占有率[17]。I型结构水合物中大孔穴的数量是小孔穴的三倍,故有CH4分子大、小孔穴占有率与谱带面积之间关系满足式(1)[18]:
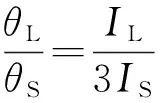
(1)
式中:θL、θS——大孔穴和小孔穴的绝对占有率;
IL、IS——大孔穴和小孔穴Raman峰面积。
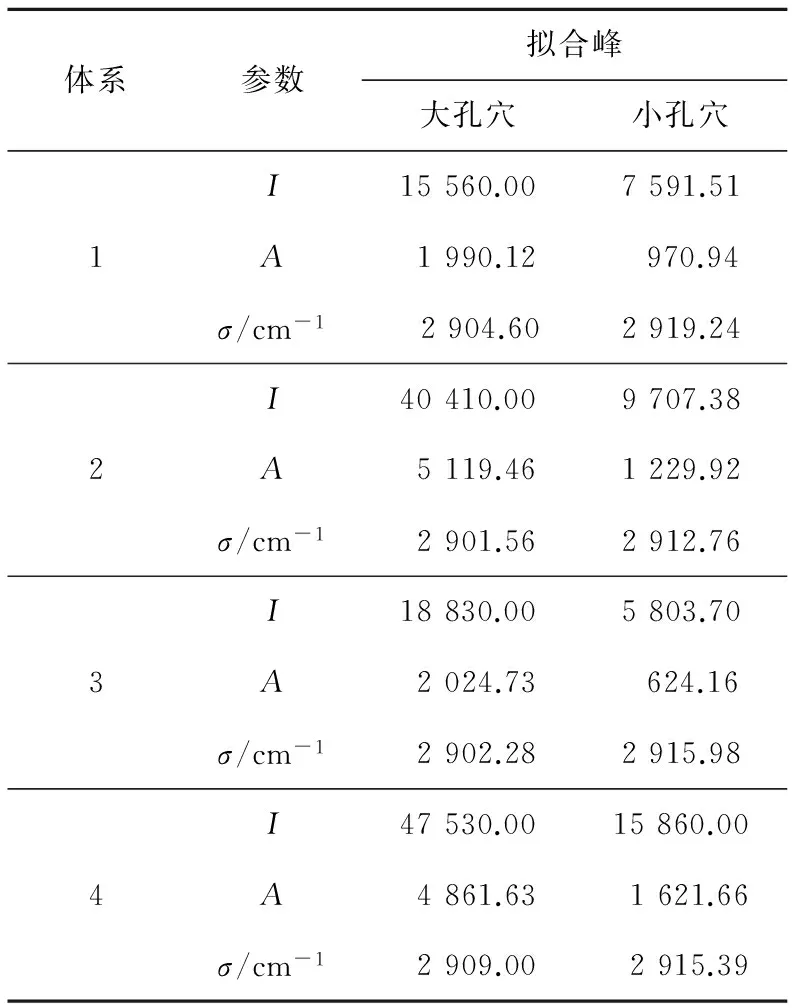
表2 谱峰拟合参数值
由van der Waals-Platteeuw模型可知I型水合物晶格化学势计算式:
Δμw,H=Δμ(h)-Δμ(h0),
(2)
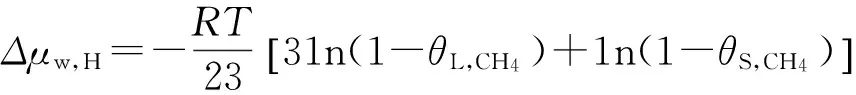
(3)
式中:Δμw,H——水分子在水合物晶格与自由水中的化学位之差。据文献[19]所知,I型水合物取1 297 J /mol。由式(1)~(3),可计算得到θL和θS的值,结果如图4所示。
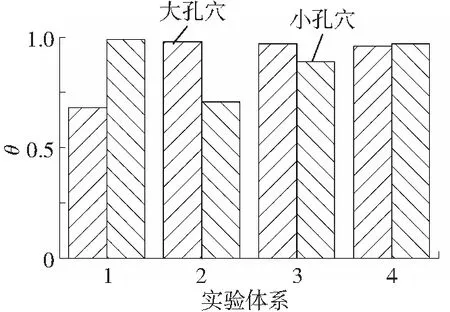
图4 各体系水合物孔穴占有率
图4显示,实验体系1~4水合物的大孔穴占有率变化比较明显(68%~98%),在SDS浓度分别为0、1.7、3.4和5.2 mmol/L的SDS-CH4体系水合物中小孔穴占有率均较高(70%~99%),而纯水体系中小孔穴占有率最小。
由θL和θS值结合式(4)计算水合指数:
(4)
实验体系1~4的水合指数分别为7.62、6.31、6.03、5.98,呈递减趋势,根据以上数据可计算得出煤层气水合物含气率分别为75.45%、91.07%、95.35%、96.15%,可以看出,在实验中,SDS增大了水合物的含气率,并在浓度为5.2 mmol/L时水合物含气率达到最大。
3 结 论
(1)SDS显著影响了不同时刻Raman气相峰强度,使之呈梯度变化,说明SDS能够加快煤层气水合过程微观物质传递速度,且SDS体系较纯水体系的物质传递速率大,即SDS溶液能够加快煤层气水合过程物质传递,有利于加速煤层气水合物的生成。
(2)在实验体系中,SDS对煤层气水合物大孔穴占有率影响不大,但增大了小孔穴占有率,且浓度越大,增强效果越明显。
(3)实验中SDS显著降低了煤层气水合物的水合指数,增大了水合物含气率,因此,认为在一定浓度范围内,SDS可提高水合物的含气率。
[1] MOORE T A. Coalbed methane:a review[J]. International Journal of Coal Geology, 2012, 101(6): 36-81.
[2]孟召平, 刘翠丽, 纪懿明. 煤层气/页岩气开发地质条件及其对比分析[J]. 煤炭学报, 2013, 38(5): 728-736.
[3]琚宜文, 李清光, 颜志丰, 等. 煤层气成因类型及其地球化学研究进展[J]. 煤炭学报, 2014, 39(5): 806-815.
[4]LV NANQIU, LI XIAOSHEN, XU CHUNGANG, et al. Experimental investigation of the formation of cyclopentane-methane hydrate in a novel and large-size bubble column reactor[J].Industrial & Engineering Chemistry Research,2012,51(17): 5967-5975.
[5]YANG L, FAN S S, LANG X M, et al.Component of Clathrate Hydrates Formed in CH4-TBAB-H2O System[C]//Advanced Materials Research. International Conference on Manufacturing Science and Technology, 2012: 2883-2888.
[6]TSIMPANOGIANNIS I N, LICHTNER P C . Gas saturation rseulting form methane hydrate dissociation in a porous medium:comparison between analytical and pore-network results[J]. The Journal of Physics Chemistry, 2013, 117(21): 11104-11116.
[7]HASHIMOTO S, SHU M, SUGAHARA T, et al. Thermodynamic and Raman spectroscopic studies on H2+tetrahydrofuran+water and H2+tetra-n-butyl ammonium bromide+water mixtures containing gas hydrates[J].Chemical Engineering Science, 2006, 61(24): 7884-7888.
[8]TRUEBA A T, RADOVIC I R, ZEVENBERGEN J F, et al.Kinetics measurements and in situ Raman spectroscopy of formation of hydrogen-terabutylammonium bromide semi-hydrates[J].International Journal of Hydrogen Energy, 2012, 37(7): 5790-5797.
[9]TRUEBA A T, RADOVIC I R, ZEVENBERGEN J F, et al.Kinetic measurements and in situ Raman spectroscopy study of the formation of TBAF semi-hydrates with hydrogen and carbon dioxide[J].International Journal of Hydrogen Energy, 2013, 38(18):7326-7334.
[10]MORYAMA C T, SUGAHARA T, FRANCO D Y Y, et al. In situ raman spectroscopic studies on small-cage qccupancy of methane in the simple methane and methane+deuterated tetrahydrofuran mixed hydrates[J].Journal of Chemical & Engineering Data, 2015, 60(12): 3581-3587.
[11]SUN C Y, CHEN G J, YANG L Y. Interfacial tension of methane-water with surfactant near the hydrate formation conditions[J]. Journal of Chemical and Engineering Data, 2004, 49(4): 1023-1025.
[12]张艳霞, 吴兆亮, 武增江, 等. 温度对高浓度SDS水溶液泡沫稳定性及分离的影响[J].高校化学工程学报, 2012, 26(3): 536-540.
[13]QIN J, KUHS W F. Calibration of Raman quantification factors of guest molecules in gas hydrates and their application to gas exchange processes involving N2[J].Journal of Chemical & Engineering Data, 2014, 60(2): 369-375.
[14]LINGAP, DARABOINA N, RIPMEESTER J A, et al.Enhanced rate of gas hydrate formation in a fixed bed column filled with sand compared to a stirred vessel[J].Chemical Engineering Science, 2012, 68(1): 617-623.
[15]SCHICKS J M, RIPMEESTER J A. The coexistence of two different methane hydrate phases under moderate pressure and temperature conditions:kinetic versus thermodynamic products[J].Angewandte Chemie International Edition, 2004, 43(25): 3310-3313.
[16]PICQUART M, LABORDE M. Vibrational mode behavior of SDS aqueous solutions studied by Raman scattering[J].The Journal of Physics Chemistry, 1986, 90(2): 243-250.
[17]张保勇, 刘传海, 吴强, 等. CO2—CH4—N2瓦斯混合气水合分离产物Raman光谱特征[J].光谱学与光谱分析, 2014, 34(6): 1560-1565.
[18]LEE H H, AHN S H, NAM B U, et al. Thermodynamic stability,spectroscopic identification,and gas storage capacity of CO2-CH4-N2mixture gas hydrates:implications for landfill gas htdrates[J].Environmental Science & Technology, 2012, 46(7): 4184-4190.
[19]HANDA Y P, TSE J S. Thermodynamic properties of empty lattices of structure I and structure II clathrate hydrates[J].The Journal of Physics Chemistry, 1986, 90(22): 5917-5921
(编辑徐岩)
Study on SDS effect on characteristic of gas storage for CMM hydrate via Raman spectroscopy
WUQiang1,2,ZHAOZiqi1,2,LIUChuanhai1,2
(1.School of Safety Engineering, Heilongjiang University of Science & Technology, Harbin 150022, China 2.National Central Laboratory of Hydrocarbon Gas Transportation Pipeline Safety,Heilongjiang University of Science & Technology, Harbin 150022, China)
This paper gives weight to the storage and transportation of coal mine gas-a main factor influencing its comprehensive utilization. The research building on the experiments on hydration reactions of coalbed methane with four kinds of concentration of SDS solutions, performed at 2.0 ℃ and 4.0 MPa using in-situ Raman spectroscopy test platform for coalbed methane hydration reaction gives the Raman spectra of the vapor phase in different times and the hydrate phase in the last time and calculates the cavity occupancy and hydration numbers,based on the object molecular various vibrational mode and the Raman bands area ratio,combined with the model of van der Waals-Platteeuw. The results show that a remarkable gradient change occurs in the Raman spectra intensity of gas phase in the hydration reaction,reflecting the occurrence of microcosmic mass transmission in the process; and the hydration numbers show downtrend due to the rise of the SDS concentration,and,the gas volume fraction reaches to the maximum when the SDS concentration is 5.2 mmol/L.
CMM hydrate; Raman spectra; SDS; hydration numbers; gas volume fraction
2015-12-27
国家自然科学基金重点项目(51334005);国家自然科学基金项目(51274267, 51404102);黑龙江省研究生创新科研资金项目(YJSCX2015-101HKD)
吴强(1959-),男,山东省临沭人,教授,博士生导师,研究方向:安全科学与工程,E-mail:wq0160@sina.com。
10.3969/j.issn.2095-7262.2016.01.007
TD712.1;O657.3
2095-7262(2016)01-0025-06
A

