聚乳酸基热固性聚氨酯及其形状记忆性能
石朔,顾林,杨义浒,余海斌,陈锐,肖湘莲,邱军
1 中国科学院宁波材料技术与工程研究所,浙江 宁波 315201
2 中国科学技术大学 纳米科学技术学院,江苏 苏州 215123
3 深圳光华伟业股份有限公司,广东 深圳 518057
4 孝感市易生新材料有限公司,湖北 孝感 432100
研究报告
聚乳酸基热固性聚氨酯及其形状记忆性能
石朔1,2,顾林1,杨义浒3,余海斌1,陈锐4,肖湘莲3,邱军3
1 中国科学院宁波材料技术与工程研究所,浙江 宁波315201
2 中国科学技术大学 纳米科学技术学院,江苏 苏州215123
3 深圳光华伟业股份有限公司,广东 深圳518057
4 孝感市易生新材料有限公司,湖北 孝感432100
石朔,顾林,杨义浒,等. 聚乳酸基热固性聚氨酯及其形状记忆性能. 生物工程学报,2016,32(6): 831-838.
Shi S,Gu L,Yang YH,et al. Synthesis and characterization of polylactide-based thermosetting polyurethanes with shape memory properties. Chin J Biotech,2016,32(6): 831-838.
通过聚乳酸二元醇和聚乳酸-聚己内酯共聚物二元醇与六亚甲基二异氰酸酯 (HDI)三聚体交联反应合成了一系列生物基热固性聚氨酯 (Bio-PUs)。利用傅里叶红外 (FTIR)、差示扫描量热分析 (DSC)、热失重分析 (TGA)、万能拉伸机和细胞毒性等测试方法对获得的聚乳酸基聚氨酯进行了表征。结果表明,与聚乳酸二元醇相比,聚乳酸-聚己内酯共聚物二元醇降低了生物基热固性聚氨酯的玻璃化温度 (Tg),提高了热固性聚氨酯的热稳定性;且聚乳酸-聚己内酯型聚氨酯的力学性能和形状记忆性能更为优异。其中,聚乳酸-聚己内酯共聚物二元醇分子量为3 000时得到的热固性聚氨酯 (Bio-PU2-3000)的杨氏模量为277.7 MPa,伸长率为230%;聚乳酸-聚己内酯共聚物二元醇分子量为1 000得到的热固性聚氨酯 (Bio-PU2-1000)在人体体温下的形变回复时间仅为93 s。另外,通过显微镜观察到细胞在含聚乳酸基热固性聚氨酯的培养液中生长状态良好,表明制备得到的生物基聚氨酯无细胞毒性。
聚乳酸二元醇,聚乳酸-聚己内酯共聚物二元醇,热固性聚氨酯,形状记忆,细胞毒性
Chinese Journal of Biotechnology
http://journals.im.ac.cn/cjbcn
June 25,2016,32(6): 831-838
©2016 Chin J Biotech,All rights reserved
随着石油资源的日益减少以及人们环保意识的不断增强,用可再生的生物资源取代石油化学品来制备高分子材料已逐渐成为人们研究的热点[1-4]。淀粉、纤维素、半纤维素等生物质由于溶解性差很难被直接使用,但可以利用这些生物质发酵来制备生物基单体,生物基单体再通过聚合反应获得高分子材料[5-8]。其中,聚乳酸 (PLA)是以淀粉等发酵的乳酸为原料化学合成的一类高分子材料[9-12],其具有完全生物降解、良好生物相容性、可再生等特点,在自然界的微生物等作用下可完全分解、最终分解为CO2和水,能够实现生态平衡循环[13-18]。
在全球范围内,调研了其中80个生产可降解塑料或者共混物的单位,这80家单位中大约有20%的公司正在生产PLA相关的塑料材料。然而,高分子量的PLA仍存在一些局限性:1)PLA合成要求单体纯度高、工艺复杂、反应过程控制精度高,导致其高成本[19-20];2)PLA抗冲性差、柔性差、耐热性差、易水解[21-24];3)PLA品种单一,产品变化小,限制了其应用领域。基于上述原因,我们开发了低酸值、低残留的PLA及其共聚多元醇,并实现了工业化中试生产。获得的PLA及其共聚多元醇,可以作为下游聚氨酯行业的生物基多元醇原料,运用灵活的化学反应,能够获得一系列高性能聚乳酸基聚氨酯材料[25-26]。
本文利用中试产品聚乳酸二元醇和聚乳酸-聚己内酯共聚物二元醇与HDI三聚体反应制备聚乳酸基热固性聚氨酯,系统地研究聚乳酸二元醇与聚乳酸-聚己内酯共聚物二元醇的结构对获得的热固性聚氨酯热性能、力学性能、形状记忆性能和生物性能的影响。由于所获得的聚乳酸基热固性聚氨酯是无毒、可降解的生物基材料,因此这些研究将为其在生物医学上的应用打下基础。
1 材料与方法
1.1原料
实验原料见表1。其中,聚乳酸基二元醇包括聚乳酸二元醇 (PLA1000)和聚乳酸聚己内酯共聚二元醇 (co-PLA1000,2000,3000)。
1.2形状记忆聚乳酸基热固性聚氨酯的制备
准确称量5 g聚乳酸基二元醇和30 g THF于烧杯中,适当加热搅拌促进二元醇的溶解,待溶解完全呈透明状后,加入一定量的HDI三聚体 (NCO/OH摩尔比为1.05∶1,具体见表2)和少量SnOct2,搅拌2 min后将溶液缓慢倒入事先放置水平的聚四氟乙烯模具内,在室温下放置48 h,然后在80 ℃下放置2 d,进行进一步的固化交联。

表1 实验原料Table 1 Reagents of the experiment

图1 聚乳酸基热固性聚氨酯制备反应示意图Fig. 1 Reaction scheme for preparing Bio-PUs.
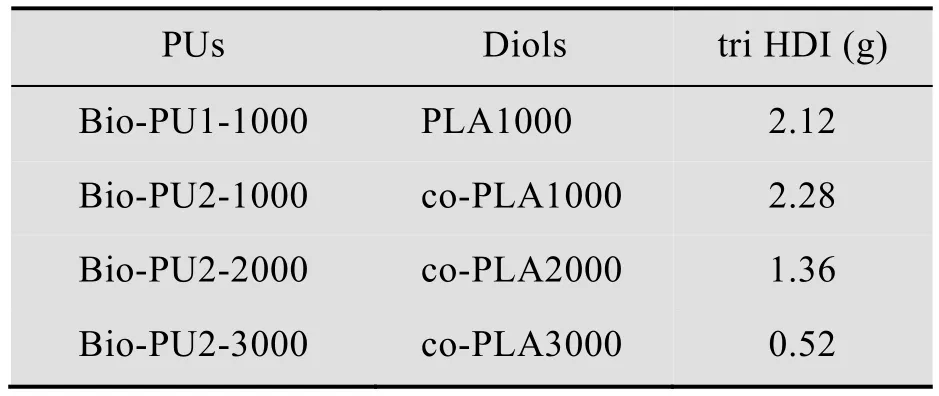
表2 聚乳酸基热固性聚氨酯原料配比Table 2 The proportion of raw materials
1.3测试与表征
1.3.1FTIR分析
采用Nicolet 6700 傅里叶变换红外光谱仪(Thermo Fisher Scientific)。利用全反射红外进行测试。
1.3.2DSC分析
采用Diamond差示扫描量热仪(PerkinElmer)。在氮气氛围下,从-30 ℃升到180 ℃,升温速率10 ℃/min,再以50 ℃/min降至-30 ℃,然后以10 ℃/min升至180 ℃。
1.3.3TGA分析
采用Diamond热重仪 (PerkinElmer)。在氮气氛围下,以20 ℃/min从室温升至600 ℃。
1.3.4力学性能测试
采用Instron5567万能拉伸机 (Instron)。在25 ℃下,以100 mm/min的拉伸速率进行测试。
1.3.5细胞毒性测试
将聚乳酸基热固性聚氨酯分别放入去离子水和75%的乙醇中超声消毒30 min后,将样品浸没在EMEM培养基 (含10%胎牛血清、1%青霉素和1%链霉素的α-MEM)中,然后在95%湿度、5%CO2、20%O2、37 ℃的细胞培养条件下培育72 h。将2×105个人骨髓间充质干细胞(hMSCs)种植在24 孔板的每个孔中。在提取物中培养一段时间 (1 d、3 d)后通过细胞增殖来检测细胞活力,并与纯细胞培养液中细胞活力作比较。具体为:将50 μL的细胞增殖检测剂添加到培养板的每个孔中,在暗处培养4 h后测量在562 nm下的吸光度。每组实验进行4个独立样本测试。
2 结果与分析
2.1聚乳酸基热固性聚氨酯的合成及结构分析
形状记忆聚乳酸基热固性聚氨酯的制备如图1所示。对获得的聚乳酸基热固性聚氨酯进行了全反射傅里叶红外光谱表征,结果见图2。
在图2中,1 752 cm-1处强吸收峰为聚乳酸基二元醇中酯键C=O的特征吸收峰,1 093 cm-1和1 184 cm-1处较强的吸收峰为酯键结构中v(C(O)-O)和v(O-C)的伸缩振动峰。1 393 cm-1和1 360 cm-1处的峰为甲基的对称弯曲振动的吸收峰,1 452 cm-1处的峰为亚甲基和甲基的反对称弯曲振动的吸收峰,2 872 cm-1和2 948 cm-1处为甲基、亚甲基和次甲基的伸缩振动吸收峰。而在3 500 cm-1附近的-OH吸收峰基本消失。另外,3 345 cm-1附近较宽而弱的吸收峰为-N-H的特征伸缩振动吸收区域,1 534 cm-1较弱的吸收区域为-C-N的对称弯曲振动吸收区域。且1 690 cm-1处峰为氨基甲酸酯中C=O的吸收峰。这些结果表明聚乳酸基二元醇中的羟基与HDI三聚体发生了反应,最终形成了具有交联结构的热固性聚氨酯。

图2 聚乳酸基热固性聚氨酯的FTIR光谱Fig. 2 FTIR spectra of Bio-PUs.
2.2热性能
DSC分析是研究聚合物的微观相分离、玻璃化转变、熔融转变和结晶转变等常见的手段。为此,我们对所合成的聚乳酸基热固性聚氨酯材料进行了DSC分析。图3为聚乳酸基热固性聚氨酯的DSC曲线,相应的玻璃化转变温度Tg归纳在表3中。

图3 聚乳酸基热固性聚氨酯的DSC曲线Fig. 3 DSC curves of Bio-Pus.

表3 聚乳酸基热固性聚氨酯的热性能Table 3 Thermal properties of Bio-PUs
由图3可知,所获得的聚乳酸基热固性聚氨酯材料有一个较为明显的Tg,但没有熔融峰或结晶峰。这表明所获得的聚乳酸基热固性聚氨酯材料为无定型非晶态结构。其中,Bio-PU2-1000、Bio-PU2-2000和Bio-PU2-3000的Tg分别为24.1 ℃、18.1 ℃和14.5 ℃,可以看出,随着聚乳酸-聚己内酯二元醇分子量的增加制备得到的聚氨酯的Tg降低。这主要是由于随着聚乳酸-聚己内酯二元醇含量的增加,制备得到的聚氨酯的交联密度减小,而相应的硬段含量减少。另外,由聚乳酸-聚己内酯型聚氨酯的Tg比聚乳酸聚氨酯的Tg要低的多,这主要是由于己内酯无规共聚到聚乳酸二元醇的分子链上,有效地降低了聚乳酸二元醇的Tg,从而也降低了所制备的聚氨酯的Tg。

图4 聚乳酸基热固性聚氨酯的TGA曲线Fig. 4 TGA curves of Bio-PUs.
图4是聚乳酸基热固性聚氨酯的TGA曲线,相关的结果见表3。聚乳酸基热固性聚氨酯的5%热失重温度 (T5%)在202.6-240 ℃之间。其中,Bio-PU1-1000的T5%的温度为202.6 ℃,而Bio-PU2-1000的T5%的温度为237.6 ℃。另外,这2个聚氨酯最快热失重温度Tmax相接近。可以看出,聚乳酸-聚己内酯型聚氨酯表现的热性能较之与聚乳酸型聚氨酯更为优异,这说明己内酯的引入提高了热固性聚乳酸基聚氨酯的热稳定性。
2.3力学性能
聚乳酸基聚氨酯作为一种潜在的医用材料,研究其力学性能对其在临床医学上的应用非常重要。采用万能拉伸机对制备得到的聚乳酸基热固性聚氨酯材料进行力学性能测试。图5为聚乳酸基热固性聚氨酯的应力-应变曲线,所有样品的拉伸强度 (σb)、杨氏模量 (E)以及断裂伸长率 (εb)归纳在表4中。
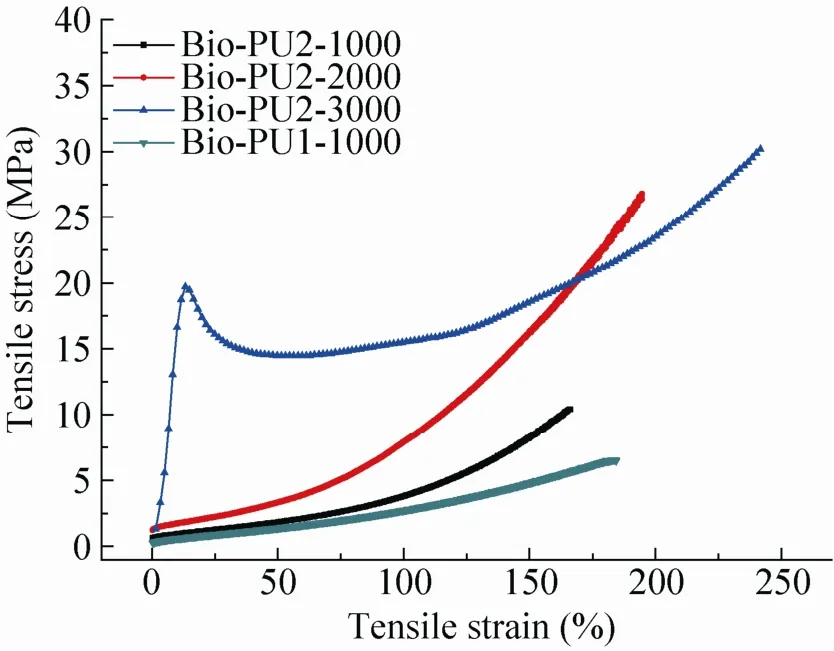
图5 聚乳酸基热固性聚氨酯的应力-应变曲线Fig. 5 Stress-strain curves of Bio-PUs.

表4 聚乳酸基热固性聚氨酯的机械性能Table 4 Mechanical Properties of Bio-PUs
由于聚乳酸基热固性聚氨酯材料均具有交联结构,因此其机械性能很好,都呈现出较高的杨氏模量、断裂强度和拉伸强度。由表4可以看出,随着聚氨酯链中聚乳酸-聚己内酯二元醇分子量的增加,材料的杨氏模量和断裂强度呈逐渐增大趋势,断裂伸长率也呈逐渐增加趋势,这主要是由于随着聚氨酯内聚乳酸-聚己内酯二元醇分子量的增加,降低了热固性聚氨酯的交联密度,同时由于聚酯链的刚性等综合因素造成。其中,Bio-PU2-3000力学性能最好,E、σb、εb分别为277.1 MPa、26.7 MPa和230.0%。
2.4形状记忆性能
为了测定聚乳酸基热固性聚氨酯材料的形变回复时间,利用摄像机连续拍摄材料在一定温度下的形状变化过程。
图6和7是聚乳酸基热固性聚氨酯材料在人体体温 (37 ℃)下由弯曲状态回复到初始状态的形变回复过程。Bio-PU1-1000在155 s内回复到了原来的形状,而Bio-PU2-1000回复到了原来的形状仅需93 s。这说明所获得的聚乳酸基热固性聚氨酯中引入柔性的聚己内酯链段能够缩短回复时间,从而具有更好的形状记忆性能。
2.5细胞毒性

图6 Bio-PU1-1000的形状记忆性能Fig. 6 The shape memory behavior of Bio-PU1-1000.

图7 Bio-PU2-1000的形状记忆性能Fig. 7 The shape memory behavior of Bio-PU2-1000.
细胞毒性结果见图8。从图8可以看出,Bio-PU1-1000和Bio-PU2-1000的OD值与空白相接近,表明它们之间的细胞活力基本一致。并且根据单因素方差分析,各组OD值直接无显著性差。同时通过显微镜观察到细胞在含聚乳酸基热固性聚氨酯的培养液中生长状态良好,这表明聚乳酸基热固性聚氨酯材料对人骨髓间充质干细胞未表现出毒性。

图8 聚乳酸基热固性聚氨酯的细胞毒性分析Fig. 8 Cytotoxicity of Bio-PUs examined.
3 结论
通过聚乳酸二元醇和聚乳酸-聚己内酯共聚物二元醇与HDI三聚体交联反应制备了一系列生物基热固性聚氨酯,这些聚乳酸基热固性聚氨酯具有优良的热性能、机械性能、形状记忆功能和生物性能。聚乳酸基热固性聚氨酯的Tg在14.5-37.7 ℃之间,耐热温度高于200 ℃,杨氏模量高达277.7 MPa,断裂伸长率达230%,在人体体温下形状回复时间可小于100 s,且无细胞毒性。另外,与聚乳酸型聚氨酯相比,聚乳酸-聚己内酯型聚氨酯的Tg更低,热稳定性更好,机械性能更良,形状记忆性更优。
REFERENCES
[1] Auras R,Harte B,Selke S. An overview of polylactides as packaging materials. Macromol Biosci,2004,4(9): 835-864.
[2] Lim LT,Auras R,Rubino M. Processing technologies for poly (lactic acid). Prog Polym Sci,2008,33(8): 820-852.
[3] Nampoothiri KM,Nair NR,John RP. An overview of the recent developments in polylactide(PLA)research. Bioresour Technol,2010,101(22): 8493-8501.
[4] IwataT. Biodegradable and bio-based polymers: future prospects of eco-friendly plastics. Angew Chem Int Ed,2015,54(11): 3210-3215.
[5] Elezi O,Kourkoutas Y,Koutinas AA,et al. Food additive lactic acid production by immobilized cells of Lactobacillus brevis on delignified cellulosic material. J Agric Food Chem,2003,51(18): 5285-5289.
[6] Rosenberg M,Rebroš M,Krištofíková L,et al. High temperature lactic acid production by Bacillus coagulansim mobilized in lentiKats. Biotechnol Lett,2005,27(23/24): 1943-1947.
[7] Gao MT,Hirata M,Koide M,et al. Production of L-lactic acid by electrodialysis fermentation (EDF). Proc Biochem,2004,39(12): 1903-1907.
[8] Choudhury B,Basha A,Swaminathan T. Study of lactic acid extraction with higher molecular weight aliphatic amines. J Chem Technol Biotechnol,1998,72(2): 111-116.
[9] Holted CH,Muller A,Rehbinder D. Lactic Acid. Copenhagen-Der: VerlagChemie,International Research Association,1971.
[10] Maharana T,Mohanty B,Negi YS. Melt-solid polycondensation of lactic acid and its biodegradability. Prog Polym Sci,2009,34(1): 99-124.
[11] Chen GX,Kim HS,Kim ES,et al. Synthesis of high-molecular-weight poly(L-lactic acid)through the direct condensation polymerization of L-lactic acid in bulk state. Eur Polym J,2006,42(2): 468-472.
[12] Feerzet A,Kenji Y,Shi Q,et al. Synthesis of polylactic acid by direct polycondensation undervacuum without catalyst,solvents and iniciators. Chem Eng J,2009,151(1-3): 342-350.
[13] Vink ETH,Rábago KR,Glassner DA,et al. Applications of life cycle assessment to NatureWorks™ polylactide (PLA)production. Polym Degrad Stabil,2003,80(3): 403-419.
[14] Prempeh N,Li JL,Liu DG,et al. Plasticizing effects of epoxidized sun flower oil on biodegradable polylactide films: a comparative study. Polym Sci,2014,56(6): 856-863.
[15] Auras R,Lim LT,Selke SEM,et al. Biodegradation//Poly(Lactic Acid): Synthesis,Structures,Properties,Processing,and Applications. Hoboken,NJ: John Wiley & Sons,Inc.,2010: 423-430.
[16] Lee SH,Kim SH,Han YK,et al. Synthesis and degradation of end-group-functionalized polylactide. J Polym Sci,Part A: Polym Chem,2001,39(7): 973-985.
[17] Reed AM,Gilding DK. Biodegradable polymers for use in surgery-poly(glycolic)/poly(lactic acid)homo and copolymers: 2. In vitro degradation. Polymer,1981,22(4): 494-498.
[18] Bendix D. Chemical synthesis of polylactide and its copolymers for medical applications. Polym Degrad Stab,1998,59(1): 129-135.
[19] Kricheldorf HR. Syntheses and application of polylactides. Chemosphere,2001,43(1): 49-54.
[20] Yanagase A,Fijimoto M,Shimoi Y,et al. Preparation of cyclic esters: JP 07309861,1995.
[21] Becker JM,Pounder RJ,Dove AP. Synthesis of poly(lactide)s with modified thermal and mechanical properties. Macromol Rapid Commun,2010,31(22): 1923-1937.
[22] Wang SG,Cui WJ,Bei JZ. Bulk and surface modifications of polylactide. Analyt Bioanalyt Chem,2005,381(3): 547-556.
[23] Rasal RM,Janorkar AV,Hirt DE. Poly(lactic acid)modifications. Prog Polym Sci,2010,35(3): 338-356.
[24] Jiang L,Wolcott MP,Zhang JW. Study of biodegradable polylactide/poly(butylene adipateco-terephthalate)blends. Biomacromolecules,2006,7(1): 199-207.
[25] Wang W,Peng P,Chen X,et al. Polylactide-based polyurethane and its shape-memory behavior. Eur Polym J,2006,42(42): 1240-1249.
[26] Wang W,Peng P,Chen X,et al. Shape memory effect of poly(L-lactide)-based polyurethanes with different hard segments. Polym Int,2007,56(7): 840-846.
(本文责编郝丽芳)
January 8,2016; Accepted: April 19,2016
s: Lin Gu. Tel: +86-574-87603879; E-mail: gulin@nimte.ac.cn
Synthesis and characterization of polylactide-based thermosetting polyurethanes with shape memory properties
Shuo Shi1,2, Lin Gu1, Yihu Yang3, Haibin Yu1, Rui Chen4, Xianglian Xiao3, and Jun Qiu3
1 Ningbo Institute of Materials Technology and Engineering,Chinese Academy of Sciences,Ningbo 315201,Zhejiang,China
2 School of Nano Science and Technology,University of Science and Technology of China,Suzhou 215123,Jiangsu,China
3 Shenzhen Esun Industrial Co.,LTD,Shenzhen 518057,Guangdong,China
4 Xiaogan Esun Industrial Co.,LTD,Xiaogan 432100,Hubei,China
A series of bio-based thermosetting polyurethanes (Bio-PUs)were synthesized by the crosslinking reaction of polylactide and its copolymers diols with hexamethylene diisocyanate (HDI)trimer. The obtained Bio-PUs were characterized by Fourier Transform Infrared Spectroscopy (FTIR),Differential Scanning Calorimetry (DSC),Thermal Gravimetric Analysis (TGA),universal tensile testing machine and cytotoxicity test. Results indicate that the PLA copolymer (P(LA-co-CL))diols reduced the glass transition temperature (Tg)of Bio-PUs and improved their thermal stability,compared with PLA diols. The Bio-PUs synthesized from P (LA-co-CL)diols exhibit better mechanical performance and shape memory properties. Especially,Young modulus and elongation at break of the obtained Bio-PUs were 277.7 MPa and 230% respectively; the shape recovery time of the obtained Bio-PUs at body temperature was only 93 s. Furthermore,alamar blue assay results showed that the obtained Bio-PUs had no cell toxicity.
polylactide,poly(lactide-co-caprolactone),polyurethane,shape memory,cytotoxicity
10.13345/j.cjb.160014
Supported by: National Natural Science Foundation of China (No. 21404112),Ningbo Natural Science Foundation (No. 2015A610016),and Ningbo Key Scientific and Technological Project (No. 2014B10023).
Yihu Yang. Tel: +86-755-26031978; E-mail: bright@brightcn.net
国家自然科学基金 (No. 21404112),宁波市自然科学基金 (No. 2015A610016),宁波市重点工业项目 (No. 2014B10023)资助。

