热应激对猪卵母细胞葡萄糖-6-磷酸脱氢酶活性及染色质构型的影响
刘 勇,张 领,吴晓庆,卫朝辉,王艳红,王启磾,高 迪,丁 彪,吴风瑞,王 荣,李文雍
(阜阳师范学院 胚胎发育与生殖调节安徽省重点实验室,安徽 阜阳 236037)
(Key Laboratory of Embryo Development and Reproductive Regulation of Anhui Province, Fuyang Teachers College, Fuyang 236037, China)
热应激对猪卵母细胞葡萄糖-6-磷酸脱氢酶活性及染色质构型的影响
刘 勇,张 领,吴晓庆,卫朝辉,王艳红,王启磾,高 迪,丁 彪,吴风瑞,王 荣,李文雍
(阜阳师范学院 胚胎发育与生殖调节安徽省重点实验室,安徽 阜阳 236037)
将屠宰场采集的猪卵巢分为热应激组和对照组,分别检测两组未成熟卵母细胞的各项指标。利用亮甲酚蓝染色法研究葡萄糖-6-磷酸脱氢酶活性,对比分析热应激对细胞代谢活性的影响;利用Hoechst33342标记DNA区分染色质构型,对比分析热应激对细胞染色质构型的影响。结果表明:热应激组卵母细胞BCB+比例显著低于对照组(P<0.05)。热应激组卵母细胞的各期染色质构型比例与对照组比例差异不显著(P>0.05)。BCB+和BCB-组卵母细胞GV1-GV3染色质构型差异不显著(P>0.05),但对照组BCB+卵母细胞的GV4构型比例明显高于BCB-(P<0.05),且GVBD差异不显著(P>0.05);而热应激组BCB+卵母细胞的GVBD比例明显低于BCB-(P>0.05),且GV4差异不显著(P>0.05)。综上,热应激对猪未成熟卵母细胞造成的损伤主要是影响了细胞的代谢活性,对细胞染色质构型的影响不大。
染色质构型;葡萄糖-6-磷酸脱氢酶;猪卵母细胞;热应激
(KeyLaboratoryofEmbryoDevelopmentandReproductiveRegulationofAnhuiProvince,FuyangTeachersCollege,Fuyang236037,China)
养猪业是我国畜牧业的重要支柱产业之一,养猪业的健康发展越来受到国家的重视。各种环境因素对猪的养殖造成的影响也越来越受到人们关注。热应激会给猪带来应激反应,使猪机体代谢紊乱,内分泌异常,繁殖机能降低,给养猪业造成巨大的经济损失[1],这是我国中部和南部养猪生产普遍面临的一个问题。已有研究表明,热应激影响母猪的内分泌活动、酶的活性改变、代谢过程发生紊乱,从而直接或间接地对卵子的发育产生不良影响,降低了母猪的生产和繁殖能力[2],但热应激损伤未成熟卵母细胞的机理仍不清楚。
影响未成熟卵母细胞质量的因素很多。葡萄糖-6-磷酸脱氢酶(Glucose-6-phosphatedehydrogenase, G6PD)是一种主要作用于机体新陈代谢和生长发育必不可少的酶,是戊糖磷酸途径中的首个限速酶,主要作用是将葡萄糖转变为戊糖,为后来的生物反应提供原材料[3],对维持胞质中NADPH和细胞氧化还原平衡具有重要意义[4]。用亮甲酚蓝(BCB)染色法可以筛选出更具有发育潜能高质量的卵母细胞。乔利敏等[5]研究表明,用BCB法可以有效地筛选出发育活力高的牛卵母细胞。染色质构型是代表染色质凝集程度和空间分布的指标,卵母细胞染色质构型可以反映未成熟卵母细胞成熟的能力[6]和支持胚胎发育的能力[7]。目前,已经开展了关于人[8],马[9],牛[10],猪[11],小鼠[12]等动物的GV染色质构型研究,尤其是小鼠相关研究,已经证实小鼠染色质构型与基因转录表达相关[13]。Liu等[14]研究表明,猪未成熟卵母细胞染色质构型与DNA甲基化程度高度相关。Guo等[15]具体阐述了DNA甲基转移酶3A(DNA-methyltransferase3A, DNMT3A)的自抑制作用以及组蛋白H3诱导DNMT3A激活的机制。
综上所述,G6PD和染色质构型是反映未成熟卵母细胞质量的重要指标。本试验通过研究热应激对猪卵母细胞G6PD活性和染色质构型的影响,探讨热应激对猪卵母细胞造成损伤的机理,为家畜繁殖等领域的研究和应用提供新的思路和基础数据。
1 材料与方法
1.1 主要仪器与试剂
1.1.1 主要仪器Leica DMI3000B倒置荧光显微镜,Nikon SMZ745体式显微镜,Leica DFC420C冷光CCD图像采集系统,Thermo3111 CO2培养箱。
1.1.2 主要试剂10×D-PBS(Sigma, P5493),Hoechst 33342(Sigma, B2261),亮甲酚蓝(Solarbio, B8820),青霉素(哈药集团),硫酸链霉素(华北制药),生理盐水(湖北科伦)。
1.2 研究对象及处理
本试验采用的猪卵巢取自雨润集团安徽省福润肉类加工有限公司屠宰场,将卵巢放入盛有25 ℃灭菌生理盐水(添加100 IU·mL-1青霉素和0.05 mg·mL-1硫酸链霉素)的保温瓶中,2 h内送至实验室。清洗后的卵巢分为2组:将卵巢处于25 ℃含青霉素和硫酸链霉素的生理盐水中常温处理,记为25 ℃组(对照组);将卵巢处于42 ℃含青霉素和硫酸链霉素的生理盐水中热应激处理,记为42 ℃组(热应激组)。2组各处理1 h[16-17]。
1.3 卵母细胞的收集和分组
各处理1 h后,以游标卡尺测量卵泡直径,选取直径为2~6 mm卵泡的卵细胞,用10 mL注射器、18号针头抽取卵泡内容物,并集中于保温的15 mL离心管内暂存。200g离心2 min后,弃去上清,用D-PBS重悬沉淀并转入35 mm培养皿,用自制口吸管在Nikon SMZ745体式显微镜下拣卵,分别记为25 ℃组和42 ℃组。
1.4 亮甲酚蓝(BCB)染色卵母细胞
将收集到的两组卵母细胞分别置于含有26 μmol·L-1BCB染液的24孔培养板中, 覆盖液状石蜡后放入5%CO2,100%湿度,38.5 ℃培养箱染色1 h,在Nikon SMZ745体式显微镜下,将细胞质呈蓝色的卵母细胞记为BCB+组,细胞质不呈蓝色的记为BCB-组(图1)。由此可以分别得到:25 ℃组BCB+组、25 ℃组BCB-组、42 ℃组BCB+组和42 ℃组BCB-组。并用冷光CCD图像采集系统采集图像用于统计分析。
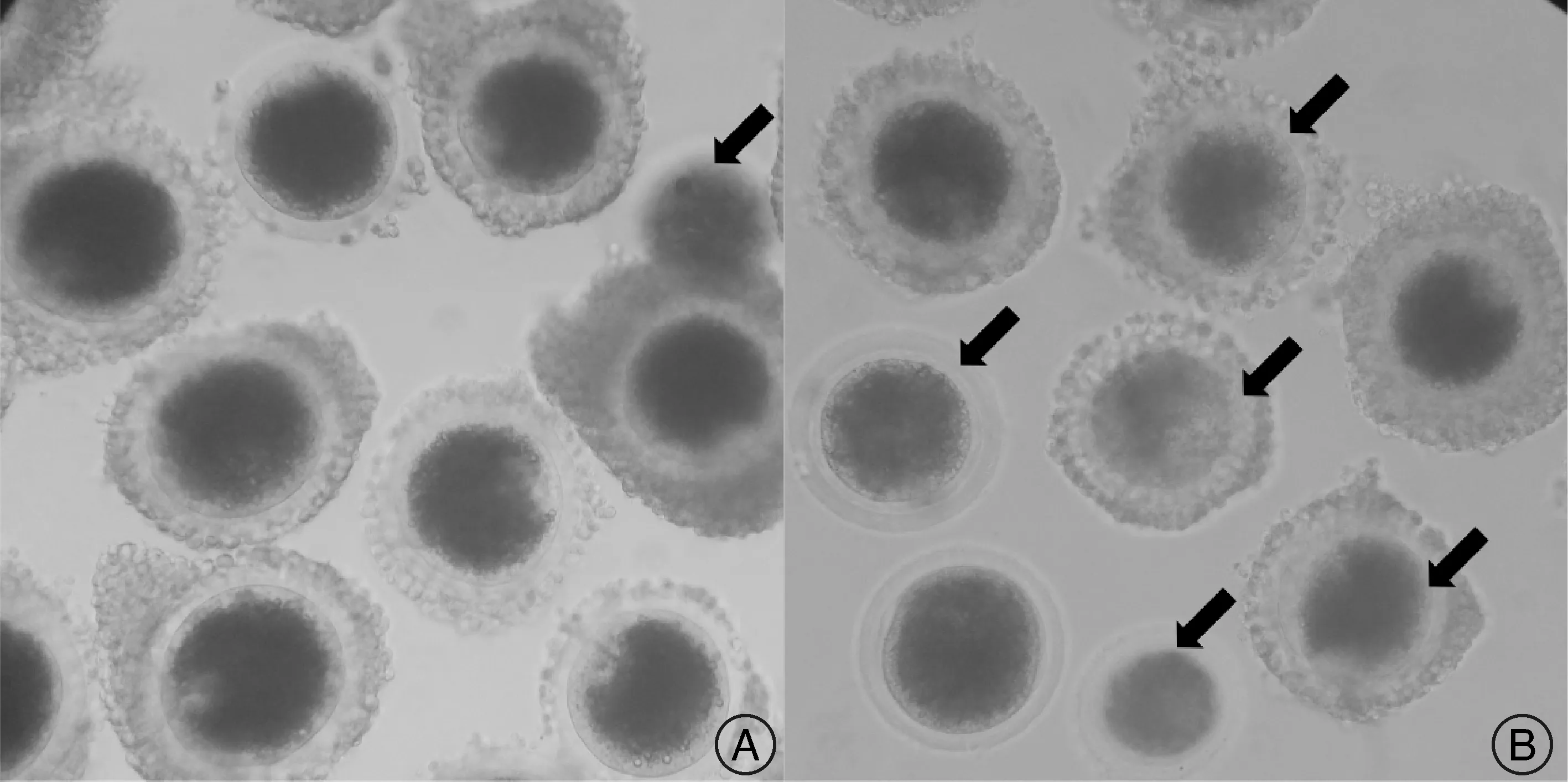
热应激前后BCB染色结果; A: 25 ℃组处理后染色结果; B: 42 ℃组处理后染色结果。 箭头所指为BCB-, 其余为BCB+。 图像放大倍数200×。图1 猪卵母细胞热应激前后BCB染色结果Fig.1 Pig oocyte dyed by BCB before and after heat stress
1.5 卵母细胞染色质构型分组
将收集到经过亮甲酚蓝染色的4组卵母细胞,分别脱卵丘后置于含10 μg·mL-1Hoechst 33342的D-PBS中避光孵育10 min,然后,移到载玻片上,用盖玻片轻压。先在相差显微镜下观察核仁和核膜的状态,再用荧光显微镜,在紫外激发波长为220~360 nm下,观察生发泡内染色质的分布。根据Sun等[18]对猪卵母细胞GV染色质构型的研究,将染色质构型分为:(1)GV1期,核膜完整,核仁完整,核仁由染色质包围,呈环状或马蹄型,有时核仁的一侧附着一块凝集的染色质;(2)GV2期,构型与GV1期相似,但是在生发泡内有1~8个凝集的染色质,主要分布在核膜附近;(3)GV3期,核膜和核仁依然明显,但染色质呈团块状或丝网状,分布在整个生发泡内;(4)GV4期,核膜模糊,核仁消失,在核仁处有凝集的染色质或不规则的网状染色质;(5)GVBD期,核膜破裂,核仁消失,染色质高度凝集。分别记录各组卵母细胞染色质构型的分类情况。
1.6 数据统计
每组试验至少重复3次,每组不少于15枚卵母细胞,数据采用SPSS软件进行卡方检验和成对t检验(P<0.05认为差异显著)。
2 结果与分析
2.1 热应激与葡萄糖-6-磷酸脱氢酶活性的相关性
用SPSS卡方检验统计25 ℃组和42 ℃组中BCB染色的数据,结果表明,25 ℃组BCB+的比例为(85.51±2.54)%,42 ℃组BCB+的比例为(17.62±1.55)%,结果中Pearson卡方sig值小于0.05,说明差异显著。说明热应激前后,猪卵母细胞G6PD活性发生了变化。具体结果见图2。
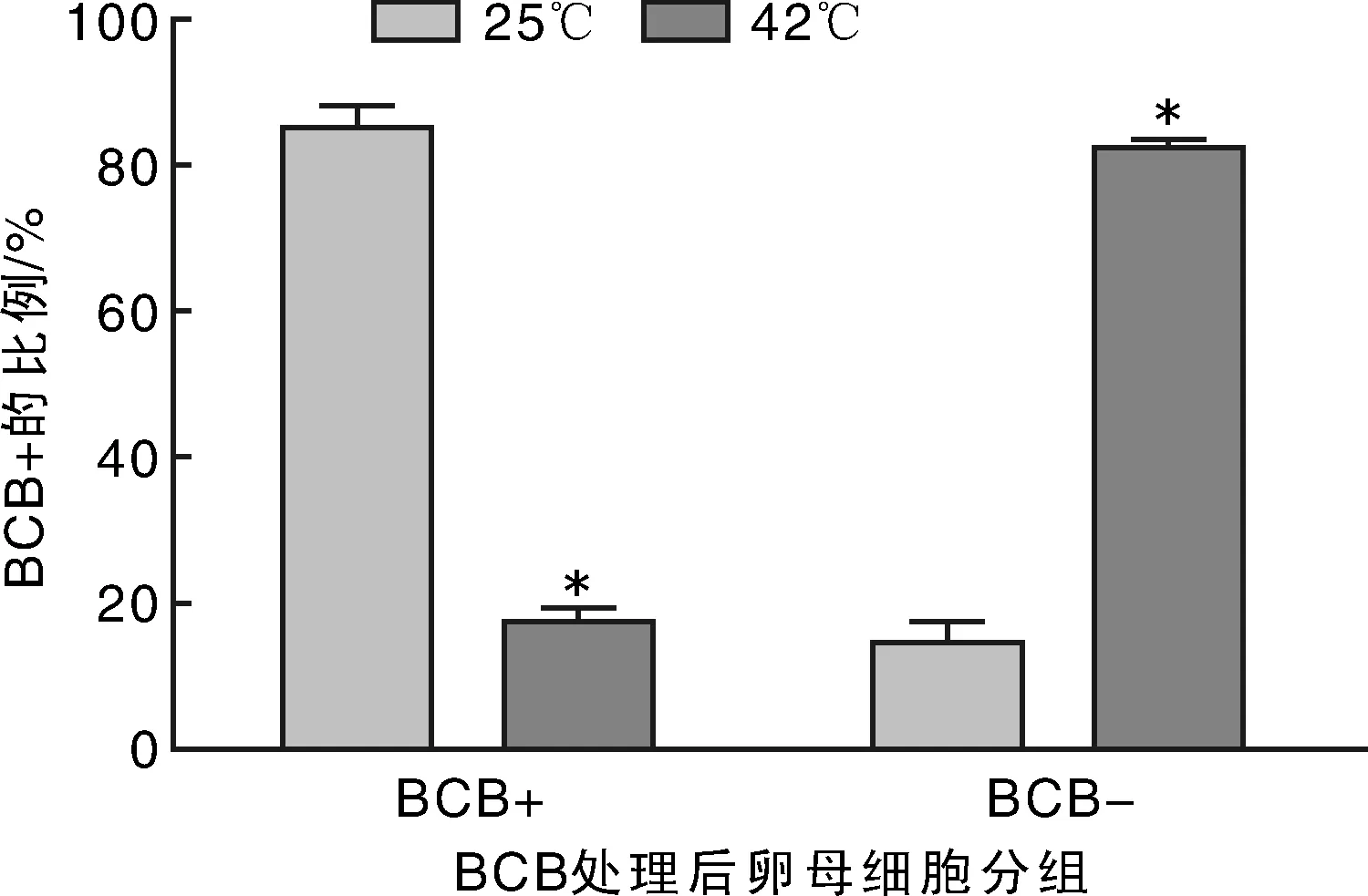
*表示25 ℃组和42 ℃组BCB染色结果差异显著(P<0.05)。图2 不同处理组BCB染色结果Fig.2 BCB dyeing results of different treatment groups
2.2 热应激与猪卵母细胞染色体构型的相关性
对25和42 ℃下猪卵母细胞染色质构型变化的数据采用SPSS软件进行卡方检验。结果表明, GV1在25和42 ℃处理组中所占比例均较高[(48.8±5.44)% VS. (47.51±7.62)%,P>0.05)],而GV2,GV3和GV4在25和42 ℃处理组中所占比例比较低,均不满20%。卡方检验结果显示,各组的P值均大于0.05,说明各组数据没有显著性差异,表明热应激对猪卵母细胞染
色体构型没有影响。如图3,在25和42 ℃下,呈现的是不同染色体构型的卵数占总卵数的比例差异。
因为各组BCB处理差异显著,但是各组染色质构型之间均没有差异显著性,因此我们分析了这两个指标的相关性。
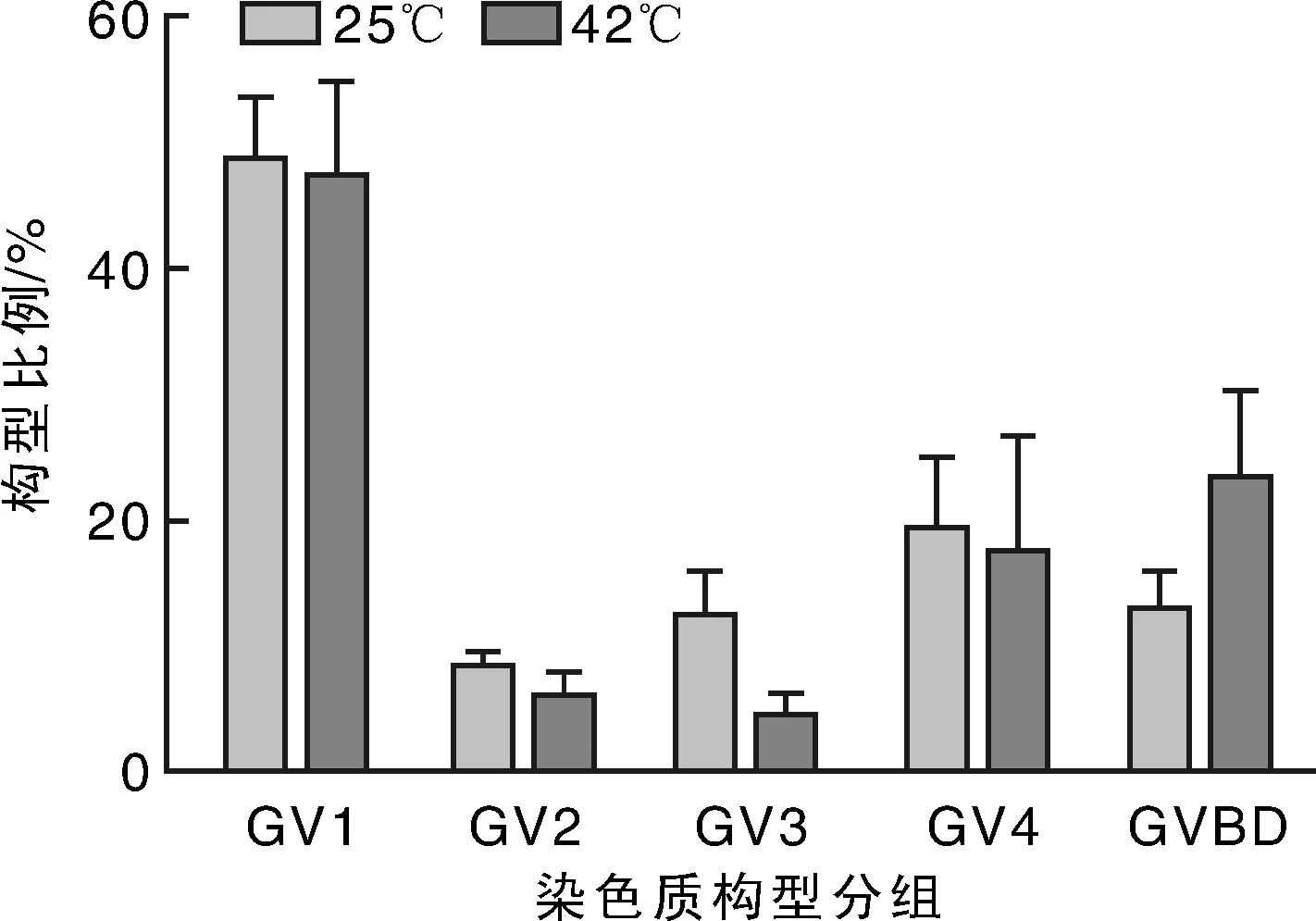
图3 不同处理染色质构型的结果Fig.3 Chromatin configuration under different treatments
表1 25和42 ℃处理后不同BCB染色结果后住卵母细胞染色质构型比例
Table 1 Chromatin configuration proportion of oocyte processed at 25 or 42 ℃
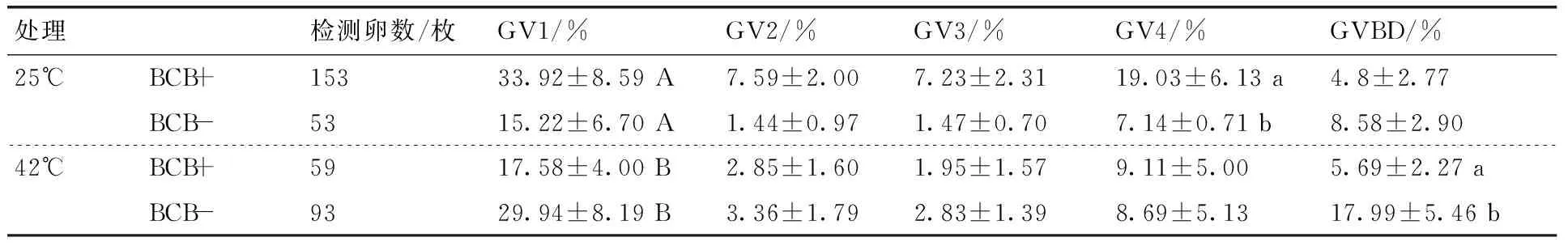
处理检测卵数/枚GV1/%GV2/%GV3/%GV4/%GVBD/%25℃BCB+15333.92±8.59A7.59±2.007.23±2.3119.03±6.13a4.8±2.77BCB-5315.22±6.70A1.44±0.971.47±0.707.14±0.71b8.58±2.9042℃BCB+5917.58±4.00B2.85±1.601.95±1.579.11±5.005.69±2.27aBCB-9329.94±8.19B3.36±1.792.83±1.398.69±5.1317.99±5.46b
注:同列数据后没有相同小写字母表示相同温度处理后BCB+与BCB-构型比例差异显著,无相同大写字母表示不同温度处理后的BCB+或BCB-之间差异显著(P<0.05)。
25和42 ℃处理后BCB染色不同结果,利用成对t检验方法进行数据处理,结果如表1所示。热应激处理前后GV1构型卵中BCB+的比例由(33.92±8.59)%显著降低至(17.58±4.00)%,BCB-的比例由(15.22±6.70)%显著升高至(29.94±8.19)%。在25 ℃下,BCB+组卵母细胞的GV4比例显著高于BCB-组(P<0.05),其他各组染色质构型比例差异不显著。在45 ℃下,BCB+和BCB-组卵母细胞的GV4比例差异不再显著,而两组GVBD比例差异显著(P<0.05)。
综上所述,热应激对葡萄糖-6-磷酸脱氢酶活性造成较大影响,而对GV染色质构型影响不大。处于GV1和GV4染色质构型的卵母细胞更容易受到热应激的影响而发生GVBD。
3 讨论
本文通过对比热应激组和对照组卵母细胞的G6PD活性和染色质构型的变化,研究热应激对猪未成熟卵母细胞的主要影响是改变G6PD活性及染色质构型的比例,为应激对生殖健康的影响提供了新的思路。把从屠宰场取回的卵巢,分别在42和25 ℃处理1 h,然后进行BCB染色1 h。结果表明,热应激组卵母细胞的BCB+比例达到(85.51±2.54)%,而25℃对照组未成熟卵细胞的BCB+比例仅有(17.62±1.55)%,差异显著(P<0.05)。为什么热应激会对卵母细胞葡萄糖-6-磷酸脱氢酶活性造成差异呢?已有研究表明,G6PD可以调节NADPH,对细胞的生长具有重要作用[19]。而且缺乏G6PD的细胞对于氧化应激非常敏感[20],在代谢中产生和来源于外界的活性氧会对细胞产生伤害。Pandolfi 等[21]用G6PD基因敲除小鼠研究发现,其缺失会影响胚胎发育,产生的胚胎干细胞具有高度敏感的氧化应激反应。综上,可以得出热应激可能通过降低G6PD活性的途径,影响细胞内新陈代谢平衡以及耐活性氧的能力。这些细胞质内酶类的损伤,可能是未成熟卵母细胞受到热应激伤害的主要原因。
试验中观察到猪的未成熟卵的染色质构型主要有4种表现形态,即GV1, GV2, GV3 ,GV4。实验结果表明,热应激前后,猪卵母细胞的染色质构型比例并没有发生显著变化。大多数卵母细胞染色质构型仍处于GV1期。这可能是由于未成熟卵的状态处于GV1的时候是处于生理的最佳状态[21]。GV期未成熟卵母细胞染色质的重构主要受到DNA甲基化和组蛋白乙酰化的调控。经刘勇等[22]和Endo等[23]的研究,在这个过程中染色质发生凝集,经过DNA甲基化和组蛋白乙酰化使某些基因转录活性降低,所以染色质构型的改变需要DNA去甲基化或者组蛋白去乙酰化。目前没有研究表明,热应激会影响DNA甲基化或组蛋白乙酰化程度,也没有研究表明短时间的处理对染色质构型有显著影响。本研究短时间热应激处理结果表明,染色质构型没有受到影响,这可能是由于短时间热应激不足以改变表观遗传模式和染色质构型。这说明短时间热应激对细胞核的功能没有明显影响。
从表1可以看出,GV1,GV2和GV3染色质构型在不同BCB染色分组卵母细胞中,所占比例也比较稳定,这可能是由于他们染色质凝集,细胞核状态相对稳定[24]。但对GV1染色质构型的卵母细胞,热应激以后,BCB+比例显著减少,BCB-比例显著增加,因此认为热应激损伤了卵母细胞的G6PD酶活力。GV4处于GV向成熟或GV向凋亡转换的过渡时期,各方面的生理状态并不稳定[25],可能过渡时期细胞的生理状态更容易受到热应激影响,导致了GV4构型卵母细胞更容易受到热应激影响。
综上所述,猪卵巢42 ℃热应激处理1 h,主要对猪未成熟卵母细胞的代谢活性产生影响,而对细胞的染色质构型没有显著影响。GV1和GV4染色质构型的猪未成熟卵母细胞,葡萄糖-6-磷酸脱氢酶活性更容易受到热应激的影响。
[1] 郭勇,冯尚连,黄仁华,等. 不同气温对母猪繁殖性能的影响[J]. 浙江农业学报,2007,19(4):317-320.
[2] 占今舜,张彬. 热应激对母猪繁殖性能的影响及应对措施[J]. 养猪,2013 (3):45-48.
[3] ZHANG H S, WANG S Q. Nrf2 is involved in the effect of tanshinone IIA on intracellular redox status in human aortic smooth muscle cells[J].BiochemicalPharmacology, 2007, 73(9):1358-1366.
[4] CEJUDO F J, FERRNDEZ J, CANO B, et al. The function of the NADPH thioredoxin reductase C-2-Cys peroxiredoxin system in plastid redox regulation and signalling[J].FEBSLetters, 2012, 586(18):2974-2980.
[5] 乔利敏,黄成定,马月辉. 亮甲酚蓝染色对牛卵母细胞体外成熟的影响[J]. 中国畜牧兽医,2009,36(2):82-85.
[6] 孙兴参,岳奎忠,马所峰. 前培养对猪卵母细胞生发泡染色质构型和体外成熟的影响[J]. 动物学报,2003,49(1):86-90.
[7] FUNAHASHI H, CANTLY T C, DAY B N. Synchronization of meiosis in porcine oocytes by exposure to dibutyl cyclic adenosine monophosphate improves developmental competence followinginvitrofertilization[J].BiologyofReproduction,1997, 57(1):49-53.
[8] PARFENOV V, POTCHUKALINA G, DUDINA L, et al. Human antral follicles: oocyte nucleus and the karyosphere formation (electron microscopic and autoradiographic data)[J].GameteResearch, 1989, 22(2):219-231.
[9] HINRICHS K, SCHMIDT A L, FRIEDMAN P P, et al.Invitromaturation of horse oocytes: characterization of chromatin configuration using fluorescence microscopy[J].BiologyofReproduction, 1993, 48(2):363-370.
[10] 郑海英,杨春燕,张秀芳,等. 亚麻酸对水牛卵母细胞体外成熟与早期胚胎体外发育的影响[J]. 浙江农业学报,2015, 27(2):165-170.
[11] SUN X S, LIU Y, YUE K Z, et al. Changes in Germinal Vesicle (GV) Chromatin Configurations During Growth and Maturation of Porcine Oocytes[J].MolecularReproductionandDevelopment, 2004, 69(2):228-234.
[12] LIU Y, SUI H S, WANG H L, et al. Germinal vesicle chromatin configurations of bovine oocytes[J].MicroscopyResearchandTechnique,2006,69(10):799-807.
[13] ZUCCOTTI M, PONCE R H, BOIANI M, et al. The analysis of chromatin organisation allows selection of mouse antral oocytes competent for development to blastocyst[J].Zygote,2002, 10(1):73-78.
[14] LIU Y, DING B, YANG X X, et al. Dynamic Transformation of DNA Methylation and Chromatin Configuration in Porcine Oocyte during Follicular Growth[J].AsianJournalofAnimalandVeterinaryAdvances, 2012, 11(10):1739-1744.
[15] GUO X, WANG L, LI J, et al. Structural insight into autoinhibition and histone H3-induced activation of DNMT3A[J].Nature,2015, 517(7536):640-644.
[16] 李莉,华再东,郭帅,等. 猪卵巢采集月份、保存温度及时间对其卵母细胞体外成熟的影响[J]. 湖北农业科学,2013,52(23):5085-5087.
[17] 张弛, 曹俊伟, 张涌. 热应激对牛卵母细胞克隆胚体外发育的影响[J]. 西北农林科技大学学报, 2007, 35(12):6-10.
[18] SUN X S,LIU Y,YUE K Z,et al.Changes in germinal vesicle (GV) chromatin configurations during growth and maturation of porcine oocytes[J].MolecularReproductionandDevelopment, 2004, 69(2):228-234.
[19] 安选,刘良忠. 葡萄糖-6-磷酸脱氢酶的研究进展[J]. 中国生物制品学杂志,2011, 24(6):745-748.
[20] AKIDE-NDUNGE O B, TAMBINI E, GIRIBALDI G, et al. Co-ordinated stage-dependent enhancement of Plasmodium falciparum antioxidant enzymes and heat shock protein expression in parasites growing in oxidatively stressed or G6PD-deficient red blood cells[J].MalariaJournal, 2009, 8(6):113.
[21] PANDOLFI P P,SANATI F,RIVI R,et al.Targeted disruption of the housekeeping gene encoding glucose 6-phosphate dehydrogenase(G6PD):G6PD is dispensable for pentose synthesis but essential for defense against oxidative stress[J].TheEMBOJournal,1995, 14(21):5209-5215.
[22] 刘勇,张领,贾二腾,等. 未成熟卵母细胞的形态与成熟能力、染色质构型和H3K27三甲基化水平的相关性研究[J]. 中国细胞生物学学报,2014, 36(11):1484-1490.
[23] ENDO T, NAITO K, AOKI F, et al.Changes in histone modifications duringinvitromaturation of porcine oocytes[J].MolecularReproductionandDevelopment, 2005, 71(1):123-128.
[24] TAN J H, WANG H L, SUN X S,et al.Chromatin configurations in the germinal vesicle of mammalian oocytes[J].MolecularHumanReproduction, 2009, 15(1):1-9.
[25] HINRICHS K, CHOI Y H, LOVE L B, et al.Chromatin configuration within the germinal vesicle of horse oocytes: changes post mortemand relationship to meiotic and developmental competence[J].BiologyofReproduction, 2005, 72(5):1142-1150.
(责任编辑 卢福庄)
Effects of heat stress on glucose-6-phosphate dehydrogenase activity and the chromatin configuration in pig oocytes
LIU Yong, ZHANG Ling, WU Xiao-qing, WEI Zhao-hui, WANG Yan-hong, WANG Qi-di, GAO Di, DING Biao, WU Feng-rui, WANG Rong, LI Wen-yong*
Pig ovaries collected from the slaughterhouse were divided into heat stress group and control group. Immature oocytes were taken from ovaries in each group. Brilliant cresol blue staining method was used to study glucose-6-phosphate dehydrogenase (G6PD) activity of immature oocytes in each group. Hoechst 33342 was used to label DNA and distinguish the chromatin configuration. It was shown that the percentage of BCB+oocyte in heat stress group was significantly lower than that in control group(P<0.05). The proportions of chromatin configuration exhibited no significant differences between heat stress group and control group(P>0.05). The proportions of GV1 to GV3 had no significant difference between BCB+and BCB-oocytes(P>0.05). In the control group, the proportion of GV4 chromatin configuration was obviously higher in BCB+oocytes than that in BCB-ones(P<0.05), but the proportion of GVBD had no significant difference(P>0.05). The proportion of GV4 chromatin configuration had no significant difference between BCB+and BCB-in the heat stress group(P>0.05), but the proportion of GVBD was obviously lower in BCB+oocytes than that in BCB-(P<0.05). In conclusion, the heat stress affected the metabolic activity of porcine immature oocytes, but had little effects on chromatin configuration.
chromatin configuration; glucose-6-phosphate dehydrogenase (G6PD); pig oocyte; heat stress
http://www.zjnyxb.cn
10.3969/j.issn.1004-1524.2016.01.04
2015-05-18
国家自然科学基金(31201789,31372273);安徽省自然科学基金项目(1508085QC59,1408085QC65);安徽省省级学科建设重大项目(皖教秘科[2014]28号);安徽省大学生创新创业训练计划项目(AH201410371031);省级科研机构校级委托专项(2014PTFY04ZD);阜阳师范学院学生科研立项资助的课题(fsyxsc201431)
刘勇(1980—),男,黑龙江大庆人,博士,副教授,主要从事胚胎工程相关研究。E-mail:drliuyong@gmail.com
*通信作者,李文雍,E-mail:liwenyong@aliyun.com
S811.2
A
1004-1524(2016)01-0022-06
浙江农业学报ActaAgriculturaeZhejiangensis, 2016,28(1):22-27
刘勇,张领,吴晓庆,等. 热应激对猪卵母细胞葡萄糖-6-磷酸脱氢酶活性及染色质构型的影响[J].浙江农业学报,2016,28(1):22-27.

