基于水溶性浸出物及HPLC指纹图谱评价不同贮存年限半夏的品质*
王朋展,巩丽丽,容蓉,姜立国
(1.山东中医药大学药学院,济南 250355; 2.山东中医药大学实验中心,济南 250355; 3.山东健坤药业有限公司,济南 250106)
基于水溶性浸出物及HPLC指纹图谱评价不同贮存年限半夏的品质*
王朋展1,巩丽丽2,容蓉1,姜立国3
(1.山东中医药大学药学院,济南 250355; 2.山东中医药大学实验中心,济南 250355; 3.山东健坤药业有限公司,济南 250106)
研究不同贮存年限半夏药材的浸出物,建立浸出物的HPLC特征指纹图谱,为半夏药材品质评控提供参考。浸出物测定方法采用药典法;HPLC指纹图谱的色谱条件:采用C18色谱柱(150 mm ×4.6 mm,5 μm),以水-甲醇为流动相,梯度洗脱,流量为0.8 mL/min,检测波长为260 nm,柱温为25℃,进样体积为50 μL。采用相似度评价及聚类分析技术揭示14批样品的相似性及差异性。14批半夏浸出物有12批合格,2批不合格。建立14批半夏浸出物样品的高效液相指纹图谱,确定了3个共有峰,共有峰保留时间的相对标准偏差小于2%,峰面积的相对标准偏差差异较大。1#~7#半夏样品有12个共有峰,共有峰保留时间的相对标准偏差小于1.5%,峰面积的相对标准偏差差异较大。各批次药材化学成分组成及含量均存在一定差异。以半夏浸出物数据与其高效液相色谱指纹图谱数据为基础,将指纹图谱相似度评价与聚类分析结合起来,用浸出物含量及评价软件测评结果对半夏品质进行综合评估,可以更精确地对半夏药材进行质量控制。
半夏;浸出物;高效液相色谱指纹图谱;聚类分析;相似度分析
半夏来源于天南星科植物半夏的块茎,始载于《神农本草经》,具有燥湿化痰、降逆止呕、消痞散结的功效[1]。现代药理研究表明半夏具有抗肿瘤、免疫调节、抗血小板凝集、抗心律失常和抗早孕等多种生物活性[2-5]。作为一种传统临床用药,半夏用量较大,但野生资源匮乏,而且栽培品种得不到很好的质量保证,以致使临床药效达不到预期效果[6-7]。一般对半夏等传统药材的鉴别还停留在形态、显微以及简单的理化鉴别阶段[8-11],随着中药现代化发展,这些传统鉴别方法的局限性凸显。因此,寻找一种对半夏药材简单快速而又科学有效的鉴别方法迫在眉睫。除了市场上出现的伪品半夏会对患者的治疗产生一定不良影响外,不同采收时间、年限对半夏中有效物质含量也会产生影响,相应的亦会对疗效产生影响[12-14]。中国药典2015年版对半夏浸出物指标作了相应规定,即按水溶性浸出物采用冷浸法测定[1],浸出物含量不得少于9.0%。笔者在此方法的基础上首次结合水溶性浸出物的高效液相色谱指纹图谱[15]对不同采收年限的半夏药材进行综合鉴别,以期对半夏药材的质量评价提供参考。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱系统:Agilent 1200型,附带自动进样器、在线脱气机、四元梯度泵、柱温箱和DAD检测器,美国Agilent公司;
超纯水器:PURELAB型,英国ELGA公司;
数控超声波清洗器:KQ-250DE型,昆山市超声仪器有限公司;
台式低速离心机:TD5A型,盐城市凯特实验仪器有限公司;
气浴恒温振荡器:TS-100C型,匡贝实业(上海)有限公司;
分析天平:Mettler AE240型,十万分之一,瑞士梅特勒-托利多公司;
核苷对照品:尿嘧啶(批号:N-024-150730)、尿苷(批号:N-025-150730)、腺嘌呤(批号:X-060-150801)、腺苷(批号:X-022-141027)、黄嘌呤(批号:H-069-150729 )次黄嘌呤(批号:C-069-150728)、次黄嘌呤核苷(批号:J-059-150730)、胸苷(批号:X-074-150715)、胞苷(批号:B-109-150715)和鸟苷(批号:N-021-150730),标示含量均≥98%,成都瑞芬思生物科技有限公司。
甲醇:色谱纯;
实验用水为超纯水;
半夏药材:共14批,经山东中医药大学生药教研室徐凌川教授鉴定为天南星科植物半夏属半夏的干燥块茎,以上药材凭证标本存于本实验室,样品来源见表1。
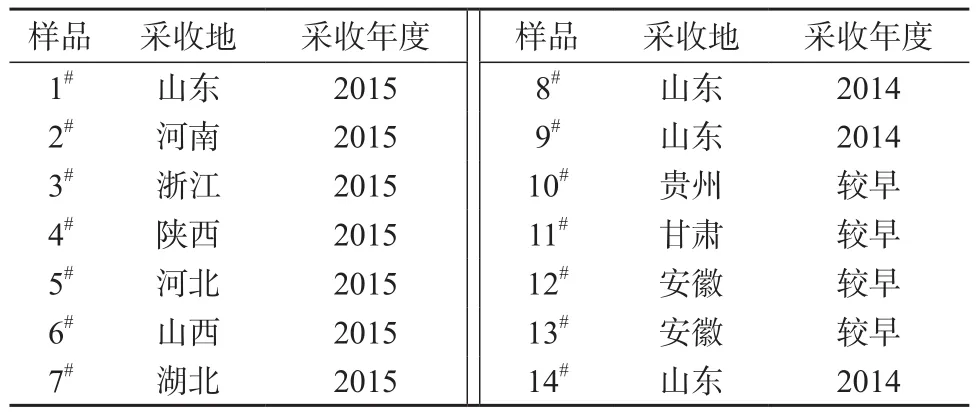
表1 半夏样品来源及采收年度
1.2 样品处理
1.2.1 水溶性浸出物的制备
水溶性浸出物采用《中国药典》2015版规定的浸出物测定法中的冷浸法进行测定。将上述药材粉末过4号筛,分别取约4 g,精密称定,置于250 mL具塞锥形瓶中,精密加水100 mL,密塞,冷浸,前6 h置于振荡器中振荡冷浸,后静置18 h,离心,用干燥的过滤器快速滤过,精密移取滤液20 mL,置于干燥至恒重的蒸发皿中,水浴蒸干后再于105℃干燥3 h,转移至干燥器中冷却30 min。
1.2.2 浸出率计算
取上述干燥浸出物,迅速精密称定重量,计算浸出率。
1.3 指纹图谱研究
1.3.1 色谱条件
色谱柱:Diamonsil C18色谱柱(150 mm×4.6 mm,5 μm,北京迪马欧泰科技发展中心);流动相:水-甲醇,梯度洗脱程序中甲醇占比0~7.0 min为 2%,7.0~7.1 min为 2%~3%,7.1~27.0 min为3%~30%,27.0~43.0 min为30%~99%,43.0~55.0 min为99%~100%;流动相流量:0.8 mL/min;柱温:25℃;检测器:DAD检测器;检测波长:260 nm;进样体积:50 μL。
1.3.2 混合对照品溶液制备
分别准确称取各核苷对照品适量,加水溶解配制成尿嘧啶、胞苷、次黄嘌呤、黄嘌呤、尿苷、腺嘌呤、次黄嘌呤核苷、鸟苷、胸苷和腺苷含量分别为 1.05,1.10,1.02,0.98,1.04,0.92,0.96,1.08,1.06,0.94 mg/mL的对照品储备液。精密移取上述各对照品储备液适量,加水配成尿嘧啶、胞苷、次黄嘌呤、黄嘌呤、尿苷、腺嘌呤、次黄嘌呤核苷、鸟苷、胸苷和腺苷含量分别为52.5,55,51,49,52,46,48,54,53,47 μg/mL的混合对照品储备液,备用。
1.3.3 供试品溶液制备
取1.2.1中续滤液,以0.22 μm微孔滤膜滤过,即得。
1.4 方法学考察
1.4.1 稳定性考察
取6#供试品溶液,分别于制备后0,2,4,8,12,24 h按1.3.1色谱条件进样,测定10种核苷成分(尿嘧啶、胞苷、次黄嘌呤、黄嘌呤、尿苷、腺嘌呤、次黄嘌呤核苷、鸟苷、胸苷、腺苷)的含量及主要色谱峰的保留时间及色谱峰面积。保留时间的相对标准偏差小于2.0%(n=6),色谱峰面积的相对标准偏差小于1.5%(n=6),表明供试品溶液提取后24 h内稳定性良好。
1.4.2 精密度考察
取同一份混合对照品溶液,同一天连续进样6次,考察色谱峰保留时间和色谱峰面积的一致性,各色谱峰保留时间的相对标准偏差小于1.5%,色谱峰面积的相对标准偏差小于1.0%,表明仪器精密度良好。
1.4.3 重现性考察
取供试品6号粉末6份,分别按照1.3.3方法制备供试品溶液,按照1.3.1色谱条件进样测定,考察各主要色谱峰保留时间和色谱峰面积的一致性,保留时间的相对标准偏差小于1.0%,色谱峰面积的相对标准偏差小于1.5%,表明此法重复性良好,符合指纹图谱技术要求。
2 结果与讨论
2.1 指纹图谱检测波长的选择
从以往的半夏指纹图谱研究文献可以发现,大多采用254 nm 或者其它单一波长作为其成分的检测波长。本实验用DAD 检测器对样品进行190~400 nm 全波长扫描,并对各波长下的色谱图进行分析比较。结果发现其在260 nm处色谱峰最丰富,故选择最佳检测波长为260 nm,各峰分离良好,特征峰明显且峰形较好。
2.2 对照品的选择
查阅文献[16]得知,半夏水溶性浸出物水溶性成分主要有鸟苷、腺苷等,故选择核苷类物质作为本实验的对照品。
2.3 浸出物测定结果分析
按实验方法测定供试品溶液,测定结果如表2。表2结果表明,水溶性浸出物的测定结果浸出率在6.57%~19.25%之间,平均为12.99%;其中有8#,11#不合格,低于药典规定9.0%。另外,非2015年采收半夏的浸出物浸出率平均值为10.00%,2015年采收半夏的浸出物平均值为15.99%。
2.4 HPLC指纹图谱
取各样品续滤液按照1.3.1色谱条件进样测定,得到各样品的HPLC指纹图谱。利用2004A 版《中药色谱指纹图谱相似度评价系统》计算软件,设置6#号药材为参照指纹图谱,时间窗宽度为0.5,剪切了前2 min溶剂峰,采用多点校正后进行自动匹配,确定了不同采收时间的样品共有峰。同时精密吸取混合对照品溶液适量,按1.3.1色谱条件进样50 μL,参照对照品的色谱行为及其DAD检测紫外光谱图,在样品色谱图上对其峰进行指认,确认了6个成分,结果见图1。
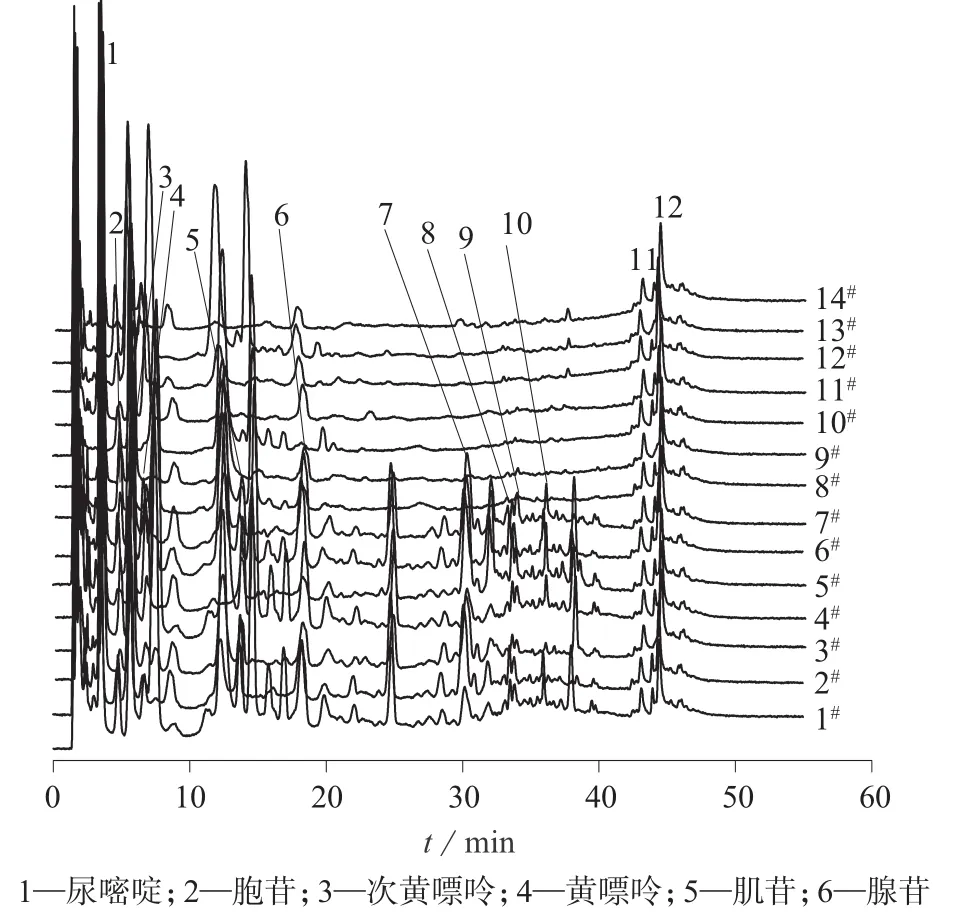
图1 半夏药材共有模式色谱图
2.5 HPLC指纹图谱相似度计算
利用国家药典委员会“中药色谱指纹图谱相似度评价系统(2004A)”设置6#号药材为参照指纹图谱,时间窗宽度为0.5,剪切前3 min 溶剂峰后,采用多点校正后进行自动匹配,得到14批半夏药材在260 nm 下的共有指纹图谱(图1)和指纹图谱相似度结果。根据软件计算结果确认14批样品中有3个共有峰(见图1中1,11,12峰),共有峰保留时间的相对标准偏差小于2.0%,峰面积的相对标准偏差差异较大,样品相似度结果见表3。1#~7#为2015年采收半夏样品,有12个共有峰(见图1,其中7~12峰未确认),共有峰保留时间的相对标准偏差小于1.5%,同样峰面积相对标准偏差的差异亦较大。各批次药材化学成分组成及含量均存在一定差异。1#~7#号样品260 nm图谱相对于对照图谱的相似度(6#为参照指纹图谱)除2#为78.8%外,其余均大于90%;8#~14#号相似度(13#为参照指纹图谱)除14#为48.6%外,其余均大于73%但小于86%。数据表明半夏药材的化学成分组成较为相似,但各批次药材相同成分含量差异较大。其中2015年采收半夏的化学成分种类含量明显高于采收时间较久的药材,说明采收年限对半夏品质产生较大的影响,如要更为客观地反映半夏药材的内在品质需要进一步分析。
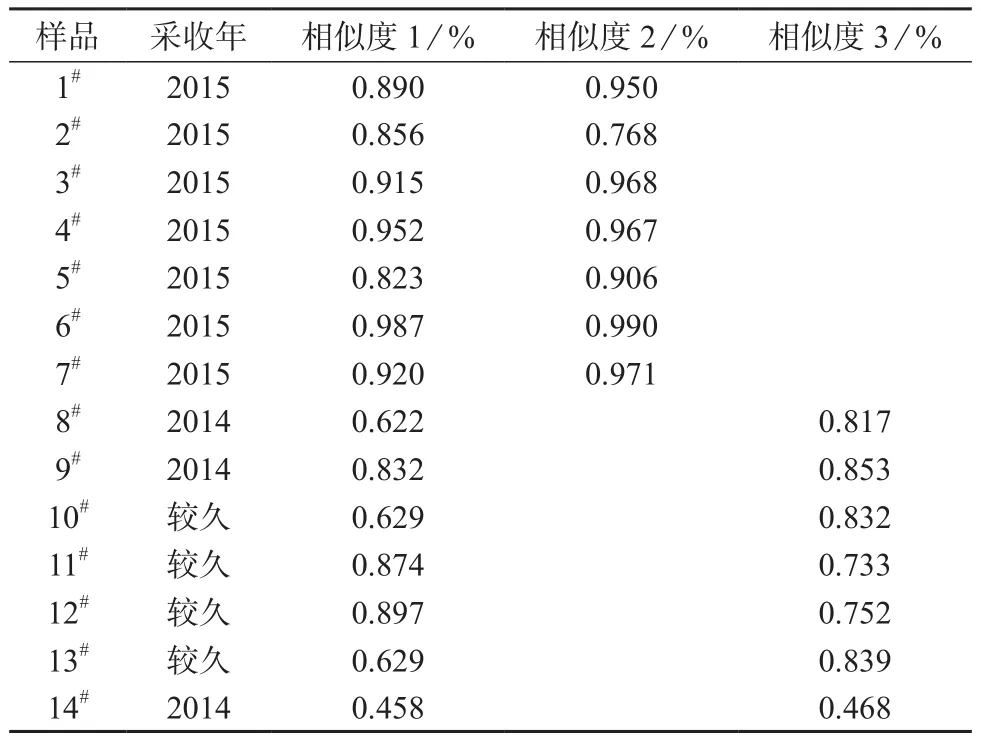
表3 半夏样品相似度结果
2.6 聚类结果分析
将14批指纹图谱实验数据导入SPSS17.0,定义样品之间的距离为欧式距离的平方,类与类之间的距离为组间距离,系统聚类结果如图2。从图2可以看出,可将半夏分为1#~7#,8#~14#两类,而1#~7#均为2015年采收,其余年代较久者归为一类。
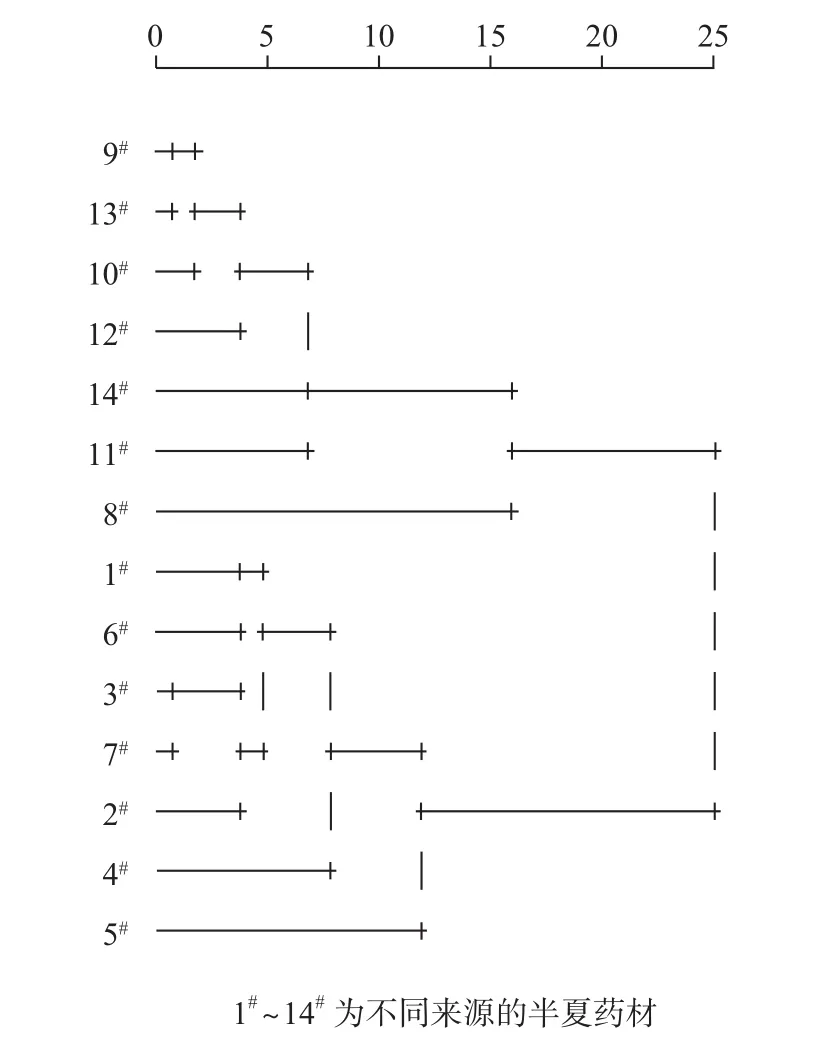
图2 半夏药材聚类分析结果
2.7 指纹图谱结果讨论
相似度评价、聚类分析方法的结果不完全相同。原因可能是中药本身是多成分复杂体系,在进行中药指纹相似度评价计算时,可能会由于人工的多点矫正,出现特征峰矫正不完全,从而导致信息缺失。从指纹图谱相似度结果可以看出,1#~7#样品图谱相对于对照图谱的相似度除个别外相似度均较高,而8#~14#样品差别则较大;而聚类分析结果将14批药材归为不同的2类,结果表明不同采收年限的半夏的化学成分组成差异明显。其原因可能是随着贮存时间延长,半夏药材中的一些化学成分发生了分解或者转化,使其含量与种类产生变化,导致不同贮存年限半夏化学成分组成的差异。相同采收年限半夏药材的化学成分组成则较为相似,但各批次药材仍存在差异,表现为不同批次药材化学成分种类差异以及同一成分不同批次之间量的差异。原因可能是不同地区的土壤、气候、水分、矿物质分布情况以及药材种源等影响了中药材的质量。实验中还发现不同产地的半夏样品仍能部分聚成一类,这说明半夏药材具有一定的产地适应性。
2.8 指纹图谱联合浸出率结果分析
综合浸出率结果以及浸出物指纹图谱的相似度结果,可以发现:浸出率与指纹图谱均不能单一反映半夏药材品质。数据表明,浸出率大小顺序为6#>2#>1#>5#>4#>3#>7#>13#>14#>9#>12#>10#>8#>11#,而相似度结果顺序为6#>4#>7#>3#>1#>12#>11#>2#>9#>5#>10#=13#>8#>14#。由浸出率结果中8#,11#样品低于9.0%,判定为不合格。而相似度评价结果中11#样品与其它样品相似度相比居中,可见二者的结果不完全一致。浸出物结果能直接反映半夏采收年限的大小,采收年限小的浸出率高,采收时间长则反之。而指纹图谱评价结果显示,半夏采收年限较小的样品化学成分种类丰富,贮存年限久的则反之。分析原因:随着贮存年限增长有些成分转化或分解导致其含量下降。也有些产地的半夏样品不容易发生转化,从而保持了原药材的品质,比如11#甘肃样品。古籍记载半夏陈者为佳,认为其久放可使刺激人咽喉,引人失音的毒性成分含量下降,但现代研究表明此类有毒成分并不具水溶性也不具挥发性,久放并不能降低其毒性。故笔者认为半夏陈者为佳的观点还有待进一步商榷,需进行现代药理研究来进一步确定。从侧面反映了对于中药材的鉴别要从多方面入手,不能仅凭一次一类检测结果而决定药材品质。
3 结语
研究了不同贮存年限半夏药材的浸出物,并建立其浸出物的HPLC特征指纹图谱。采用指纹图谱相似度计算软件对14批半夏样品的HPLC指纹图谱进行分析,不同贮存年限半夏其相似度差别较大。同时,采用SPSS 17.0统计分析软件对14批半夏样品的HPLC指纹图谱进行聚类分析,结果表明,贮存年限对半夏药材质量稳定性有一定影响。本实验首次联合半夏水溶性浸出物浸出率和其指纹图谱相似度评价结果双重鉴定标准对不同采收年限的半夏药材进行鉴别,为半夏药材品质评控提供参考。本实验中还发现半夏水溶性浸出物除2.4中6类核苷类成分共有峰外,其它共有峰需在以后的研究中采用所对应的标准品或者利用LC-MS技术进一步验证。
[1] 国家药典委员会.中华人民共和国药典[M].一部.北京:化学工业出版社,2015: 119,1 494.
[2] 姚军强.半夏的药理作用及其临床配伍运用[J].中医研究,2013(2): 3-5.
[3] Moon B C,Kim W J,Ji Y,et al. Molecular identification of the traditional herbal medicines,Arisaematis Rhizoma and Pinelliae Tuber,and common adulterants via universal DNA barcode sequences[J/OL]. Genetics & Molecular Research Gmr,2016, 15(1): gmr.15017064[2016-02-19].http: //www.funpecrp.com.br/ gmr/year2016/vol15-1/pdf/gmr7064.pdf.
[4] Xie H H,Xu J Y,Xie T,et al. Effects of Pinellia ternata (Thunb.)Berit.on the metabolomic profiles of placenta and amniotic fluid in pregnant rats[J]. Journal of ethnopharmacology,2016,183:38-45.
[5] Yu H L,Zhao T F,Wu H,et al. Pinellia ternata lectin exerts a proinflammatory effect on macrophages by inducing the release of pro-inflammatory cytokines,the activation of the nuclear factorκB signaling pathway and the overproduction of reactive oxygen species[J]. International Journal of Molecular Medicine,2015,36(4): 1 127-1 135.
[6] 潘平,李伟平,熊明星,等.我国半夏产业现状及可持续发展策略[J].中国药房,2013(31): 2 881-2 884.
[7] 高景莘,张绿明,卢先明.野生与栽培半夏的镇咳祛痰作用对比研究[J].湖南中医药大学学报,2010(7): 25-27.
[8] 吴兵,李敏,黄博,等.市售大黄、半夏、红花、茯苓掺伪的快速鉴别方法[J].中国现代中药,2012(4): 18-21.
[9] 李江维,许润春,王鹏飞,等.半夏与掺伪半夏及水半夏的鉴别研究[J].亚太传统医药,2015,11(24): 23-26.
[10] 杨晓日,崔振华.半夏与水半夏性状鉴别及薄层色谱法与紫外谱线组法的鉴别价值[J].四川中医,2016(2): 104-106.
[11] 张婷,尹玉芳.半夏与水半夏的鉴别研究[J].中国中医基础医学杂志,2014(2): 250-251.
[12] 王孝华,梅艳,王海玲,等.不同采收期对半夏块茎产量和品质的影响[J].中国农学通报,2012,28(13): 285-289.
[13] 隋利强,吴水生. RP-HPLC法测定不同贮存年限半夏饮片中腺苷和鸟苷的含量[J].黔南民族医专学报,2012(3): 157-159.
[14] 邹积隆,丁国明,张少华,等.“六陈”的实验研究(Ⅰ)贮存时间对半夏药理作用的影响[J].山东中医学院学报,1992(1):54-55.
[15] 王甫成,孟祥松,蒋磊,等. HPLC指纹图谱法鉴别半夏及其伪品[J].辽宁中医药大学学报,2016(4): 56-58.
[16] 周欣,汤洪波,龚小见,等.半夏药材水溶性成分的HPLC指纹图谱研究[J].中华中医药杂志,2009(12): 1 635-1 637.
国家休闲食品检测中心实验室筹建
国家质检总局下发通知,批准筹建国家质检总局休闲食品检测区域性中心实验室(泉州),成为继国家质检总局福建石油化工检测中心实验室、国家质检总局福建陶瓷及矿产品检测中心实验室之后,泉州检验检疫局获批建设的第3个区域性中心实验室,将为泉州及至福建休闲食品产业发展提供强有力的技术支撑。
泉州已成为我国重要的休闲食品出口基地,2015年全市出口值达1.65亿美元,由44家糖果、调味紫菜、蜜饯、果冻、糕点饼干类等出口休闲食品生产企业组成的产业集群已初具规模,产品热销东盟、欧美、中东、非洲、南美洲等50多个国家和地区。
在休闲食品产业快速发展的同时,检测实验室建设尚不能与之匹配,建设高水平、高层次的休闲食品检测中心实验室十分必要和紧迫。泉州检验检疫局相关负责人表示,此次获准筹建国家质检总局休闲食品检测区域性中心实验室(泉州),检测范围覆盖干果、膨化食品、糖果、酒类、饮料、罐头、果脯蜜饯、粮油、乳及乳制品、肉及肉制品、水产品、调味品等,经中国合格评定国家认可委员会(CNAS)认可的检测项目有217项。新建休闲食品检测中心实验室,将缩短检测周期,为泉州及至福建休闲食品产业的行政执法、企业产品自控、应对国外技术性贸易壁垒促进扩大出口等提供强技术支持和保障。
(泉州晚报)
Quality Evaluation of Pinellia Ternata of Different Reserve Time Based on Water-Soluble Extract and HPLC Fingerprint
Wang Pengzhan1, Gong Lili2, Rong Rong1, Jiang Liguo3
(1. School of Pharmaceutical Sciences, Shandong University of Traditional Chinese Medicine, Jinan 250355, China;2. Experience Center of Shandong University of Traditional Chinese Medicine, Jinan 250355, China;3. Shandong Jiankun Pharmaceutical Co., Ltd., Jinan 250106, China)
HPLC fingerprint of Pinellia Ternata was established which were derived from different harvest time and provided reliable method and scientific basis for their quality control. The contents of water-soluble extract was determined by Chinese Pharmacopoeia. The HPLC fingerprint chromatographic separation was achieved on a C18column (150 mm×4.6 mm, 5 μm), water and methanol solution was used as mobile phase in gradient elution program with the flow rate of 0.8 mL/min, the column temperature of 25℃, the injection volume of 50 μL and the detection wavelength of 260 nm. The similarity evaluation and clustering analysis were used to reveal similarities and differences in 14 batches of samples. The extract of 12 batches in 14 batches Pinelliae Rhizoma were qualified and 2 batches failed. The HPLC fingerprint of 14 batches of Pinelliae Rhizoma extract were set up and 3 common peaks were obtained, the RSD of the relative retention time of the common peaks was below 2%, the RSD of the relative peak area was difference. 1#-7#samples had 12 common peaks, the RSD of the relative retention time of the common peaks was below 1.5%, the RSD of the relative peak area was difference. 14 batches of medicinal in chemical composition and content were difference. Based on water-soluble extract data and HPLC fingerprint data and combined the fingerprint similarity evaluation system and cluster analysis, this comprehensive evaluation can be more precise for the Pinelliae Rhizoma quality control.
Pinelliae Rhizoma; water-soluble extract; HPLC fingerprint; clustering analysis; similarity analysis
O657.7
A
1008-6145(2016)05-0019-05
10.3969/j.issn.1008-6145.2016.05.005
*科技部科技重大专项(2014ZX09509001-001);山东省高校中医药抗病毒协同创新中心项目(XTCX2014C01-02)
联系人:容蓉;E-mail:rong_sdutcm@hotmail.com
2016-07-12

