依达拉奉注射液与3种晶体液配伍稳定性考察
马 静,贾燕花,王晓青,郭代红*
依达拉奉注射液与3种晶体液配伍稳定性考察
马静1,贾燕花2,王晓青2,郭代红1*
目的考察依达拉奉注射液与转化糖电解质注射液、钠钾镁钙葡萄糖注射液、复方电解质注射液3种晶体液配伍使用的稳定性。方法考察配伍液的外观、pH值和不溶性微粒,同时采用高效液相色谱法测定配伍液中依达拉奉的含量。结果室温下,依达拉奉注射液与3种晶体液在6 h内,外观、pH值和不溶性微粒无明显变化,依达拉奉含量稳定。结论依达拉奉注射液分别与转化糖电解质注射液、钠钾镁钙葡萄糖注射液、复方电解质注射液3种晶体液配伍使用6 h内稳定,但是在使用过程中仍需谨慎。
依达拉奉;晶体液;配伍;稳定性
0 引言
脑血管疾病是目前致残和致死率都较高的常见疾病和多发疾病,且不受年龄限制[1]。依达拉奉是强效的自由基清除剂,是目前新型的中枢神经系统药物,对于急性脑梗死和脑出血患者起到神经保护的作用[2-3]。然而对于急性颅脑损伤的患者,其脑脊液和血液中的离子和微量元素含量均下降[4],晶体液对于补充丢失的细胞外液是非常适当和有效的,大量输注晶体液不仅可以维持内环境的稳定,还有降低颅内压和脑水含量的作用[5]。在临床医疗工作中,为增强药物疗效、减少临床液体用量以及提高患者治疗顺应性,常将晶体液与其他药物联合应用,然而药物之间可能存在配伍禁忌,尤其一些添加了离子和糖的复合电解质和平衡液等,使得部分遇离子不稳定的药物的使用安全性受到影响,药物配伍后出现浑浊、沉淀甚至增强毒副反应等禁忌反应和严重不良反应[6],同时,由于说明书不完善,缺乏明确指导,从而造成临床盲用、乱用现象严重,危害用药安全。本文根据依达拉奉注射液的临床用量,选取转化糖电解质注射液、钠钾镁钙葡萄糖注射液、复方电解质注射液3种晶体液进行配伍,考察配伍液的外观、pH值、不溶性微粒和含量,以期为临床安全用药提供实验性依据。
1 仪器与试药
1.1仪器Waters 2695-2487高效液相色谱仪;InerSustain®C18柱(4.6 mm×250 mm,5 μm);赛多利斯BT125D电子天平;赛多利斯PB-10酸度计;天津天河仪器有限公司GWJ-8JD型微粒检测仪。
1.2试药与试剂依达拉奉对照品(中检院,批号:100620-201202);依达拉奉杂质Ⅰ对照品(中检院,批号:101256-201201);依达拉奉注射液(吉林省博大制药有限责任公司,规格:20 mL∶30 mg,批号:01-140810);转化糖电解质注射液(扬子江药业集团-上海海尼药业有限公司,规格:500 mL,批号:1509074);钠钾镁钙葡萄糖注射液(江苏恒瑞医药股份有限公司,规格:500 mL,批号:14110948);复方电解质注射液(山西振东泰盛制药有限公司,规格:500 mL,批号:1408301);磷酸二氢铵、磷酸均为分析纯;甲醇为色谱纯。
2 方法与结果
2.1配伍溶液的配制在室温避光条件下,模拟临床依达拉奉用量,将30 mg依达拉奉分别与250 mL转化糖电解质注射液、钠钾镁钙葡萄糖注射液、复方电解质注射液进行配伍,得到配伍液A、B、C。
2.2外观及pH值考察将“2.1”项下配伍液室温避光下放置,分别于0、1、2、4、6 h对外观性状、pH值进行考察。依达拉奉与以上3种晶体液配伍后,在6 h内,外观性状均为无色澄明液体,未见显著性变化;pH值在6 h内比较稳定,未见显著性变化,具体结果见表1。
2.3不溶性微粒考察参照《中国药典》2015年版四部通则0903不溶性微粒检查法第一法,规定标示装量为100 mL以下的静脉用注射液、静脉注射用无菌粉末、注射用浓溶液及供注射用无菌原料药除另有规定外,每个供试品容器(份)中含10 μm及10 μm以上的微粒数不得过6 000粒,含25 μm及25 μm以上的微粒数不得过600粒。研究结果表明,依达拉奉与3种晶体液配伍后,不溶性微粒6 h内测定结果均符合规定。对“2.1”项下各配伍液进行不溶性微粒数考察,结果见表2。

表1 依达拉奉与3种晶体液配伍后的pH值

表2 依达拉奉与3种晶体液配伍后的不溶性微粒数
2.4含量测定
2.4.1色谱条件[7]色谱柱为InerSustain®C18柱(4.6 mm×250 mm,5 μm);以0.05 mol/L磷酸二氢铵溶液(用20%磷酸溶液调节pH值至3.5)-甲醇(50∶50)为流动相;检测波长为245 nm,进样量10 μL。
2.4.2溶液的制备供试品溶液的制备:取“2.1”项下配伍溶液作为供试品溶液。对照品溶液的制备:精密称取依达拉奉对照品适量,加流动相溶解并定量稀释制成每1 mL中约含1.2 mg的溶液,作为对照品储备液;精密量取对照品储备液1 mL至10 mL容量瓶中,用流动相稀释至刻度,混匀,作为对照品溶液。
2.4.3系统适用性实验分别取依达拉奉与杂质Ⅰ对照品适量,加甲醇溶解并稀释制成每1 mL中各约含1.2 μg的混合溶液,取10 μL注入液相色谱仪,记录色谱图,依达拉奉与杂质Ⅰ峰的分离度>8.0,系统适用性良好,且转化糖电解质注射液、钠钾镁钙葡萄糖注射液、复方电解质注射液在检测波长处均无干扰,见图1。
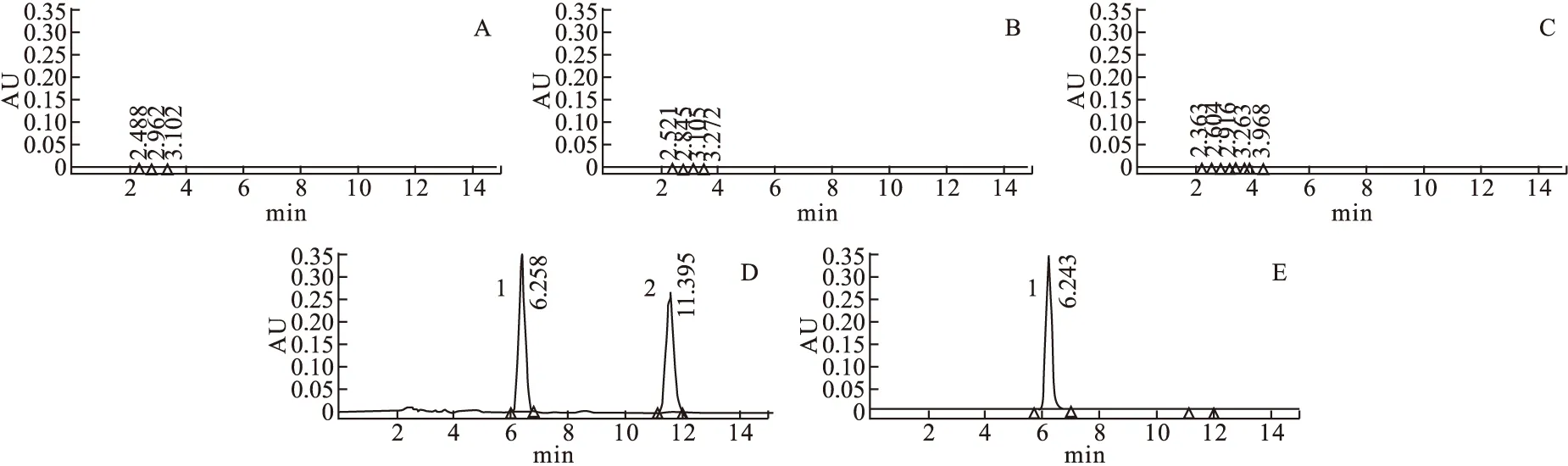
图1 依达拉奉高效液相色谱图
2.4.4线性关系考察分别精密量取依达拉奉对照品储备液0.6、0.8、1、1.2、1.4 mL置10 mL量瓶中,加流动相稀释至刻度,摇匀。分别精密量取10 μL注入高效液相色谱仪,按“2.4.1”项下色谱条件测定,记录色谱图。以浓度C(mg/mL)为横坐标,峰面积A为纵坐标进行线性回归,计算回归方程为:A=41 991 625.0 C+5 845.4(r=0.999 9,n=5)。结果表明,依达拉奉在0.072~0.168 mg/mL范围内线性关系良好。
2.4.5精密度试验取依达拉奉对照品溶液,重复进样5次,每次10 μL,测得峰面积,结果显示,RSD为0.59%(n=5),试验结果表明精密度良好。
2.4.6稳定性实验取依达拉奉对照品溶液,按照“2.4.1”项下色谱条件分析,分别在0、2、4、6、8 h测定依达拉奉峰面积结果显示,RSD值为0.53%(n=5),说明依达拉奉在8 h内稳定。
2.4.7回收率试验分别精密量取依达拉奉对照品约24、30、36 mg至25 mL容量瓶中,用转化糖电解质注射液定容至刻度,混匀,分别精密量取1 mL至10 mL容量瓶中,用转化糖电解质注射液定容至刻度,混匀,即得供试液,每个浓度制备3份。同法,制备钠钾镁钙葡萄糖注射液、复方电解质注射液的回收率供试液。精密量取供试液10 μL注入液相色谱仪分析测定,记录色谱图,结果见表3~表5。

表3 转化糖电解质注射液回收率试验结果
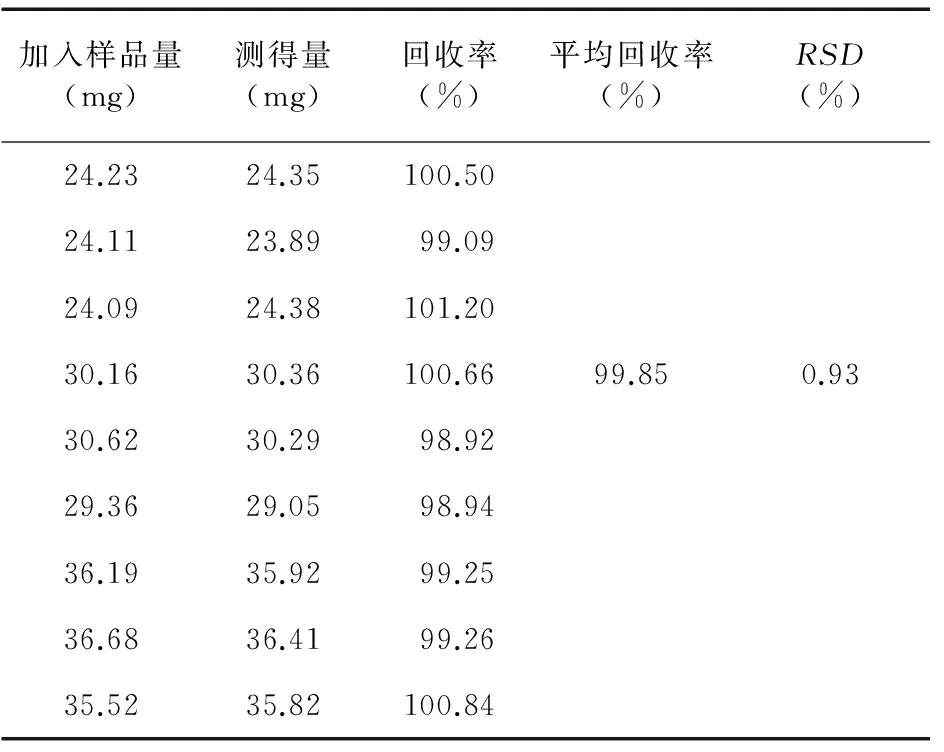
表4 钠钾镁钙葡萄糖注射液回收率试验结果
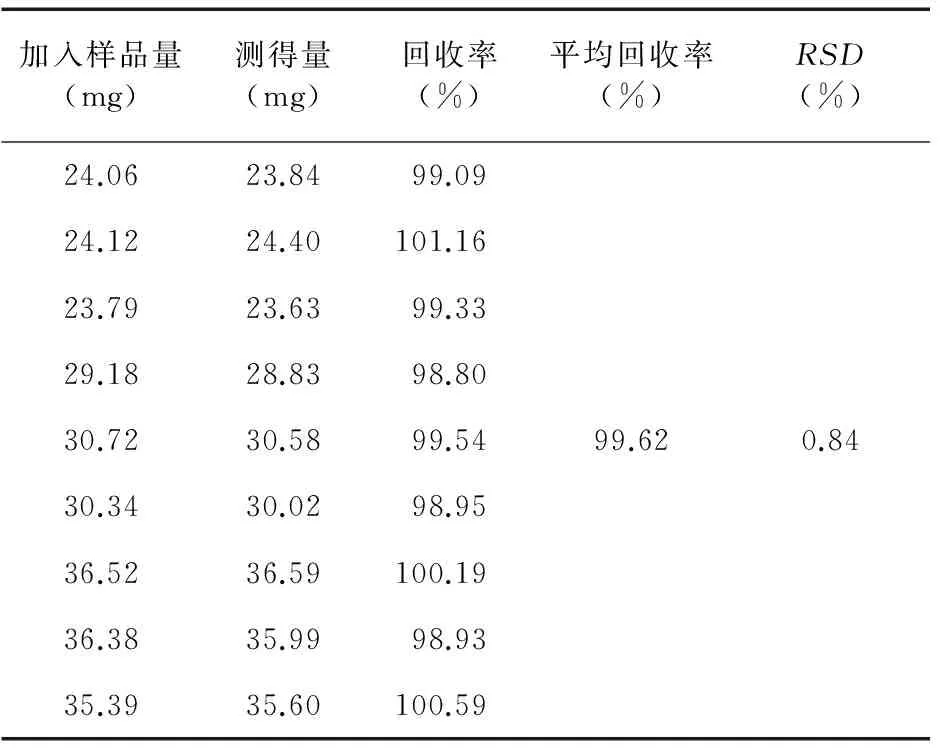
表5 复方电解质注射液回收率试验结果
2.4.8配伍液的含量测定依达拉奉与3种晶体液配伍后0~6 h内的含量测定结果见表6,依达拉奉与以上3种晶体液配伍,在6 h内含量均未见明显变化,试验结果中依达拉奉含量值RSD均小于2.0%,配伍稳定性良好。
3 讨论
转化糖电解质注射液、钠钾镁钙葡萄糖注射液和复方电解质注射液是3种复方晶体液,在临床上主要用于治疗一些伴有水和电解质紊乱的疾病,从而维持患者体液平衡。这3种复方晶体液的临床应用丰富了糖类和电解质类输液产品的种类,为临床提供了更多的选择,而且在临床上作为溶媒应用。将治疗药物与功能性的晶体液配伍是目前临床常见的治疗疾病的给药方式,但是对于一些要求稀释溶媒不含电解质或糖类的药物,这些复方制剂就不能作为溶媒使用[8-9]。依达拉奉注射液说明书中标示依达拉奉与各种含有糖分的输液混合时,可使依达拉奉的浓度降低。本文初步考察了依达拉奉注射液与三种含糖的复方晶体液的配伍稳定性,研究结果表明,依达拉奉在室温条件下6 h内稳定性良好,为依达拉奉在临床上与转化糖电解质注射液、钠钾镁钙葡萄糖注射液和复方电解质注射液配伍应用提供初步的实验依据。根据参考文献报道的依达拉奉不良反应情况[10],临床在使用时需慎重。
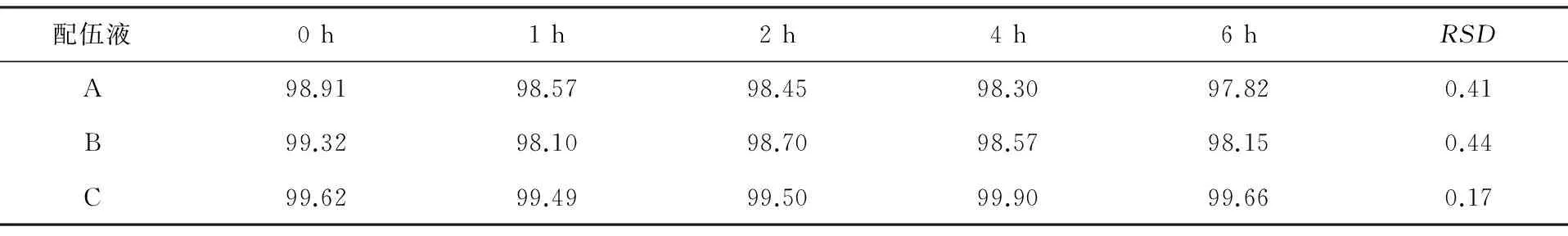
表6 依达拉奉与3种晶体液配伍后的含量考察
[1]王艳红,李立明.1990-2010年我国城乡成年人群脑血管疾病死亡率的流行趋势[J].中华疾病控制杂志,2013,17(3):185-189.
[2]王一沙,赵丽巍,郭婉姝.依达拉奉对急性脑梗死患者神经功能及血清超敏C反应蛋白水平的影响[J].实用药物与临床,2012,15(9):541-543.
[3]贾春红,张鸿.依达拉奉对急性脑梗死神经功能的保护作用[J].实用药物与临床,2009,12(1):11-12.
[4]王守军,阎庆华,朱美丽,等.颅脑损伤后脑脊液、血液中碳酸氢根、糖、电解质、微量元素含量的研究[J].中华神经医学杂志,2004,3(1):31-34.
[5]张志捷,杨建军,艾青,等.不同晶体液对脑损伤兔血清电解质、酸碱平衡和脑水肿的影响[J].临床麻醉学杂志,2008,24(4):325-327.
[6]石夏莹.简述药物配伍禁忌[J].海峡药学,2007,19(8):28-30.
[7]国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2015.
[8]王欧明.含果糖制剂的临床合理应用[J].中国医院药学杂志,2009,29(4):330-331.
[9]蒋莹,艾厚喜,孙芳玲,等.复方电解质注射液的配伍禁忌[J].中国新药杂志,2013,22(16):1978-1980.
[10]王淑洁,张建华,李俊英,等.依达拉奉不良反应的文献分析[J].实用药物与临床,2009,12(6):446-447.
Stability of edaravone injection used together with three kinds of crystalloid solution
MA Jing1,JIA Yan-hua2,WANG Xiao-qing2,GUO Dai-hong1*
(1.Chinese PLA Medical School,Beijing 100853,China;2.Department of Pharmacy,First Affiliated Hospital of PLA General Hospital,Beijing 100048,China)
ObjectiveTo determine the stability of edaravone injection used together with invert sugar electrolyte injection,sodium potassium,magnesium and calcium dextrose injection,and compound electrolyte injection.MethodsThe appearance,pH and insoluble particles of the mixed solution were observed,and the edaravone content of the three kinds of mixed solutions was determined by high performance liquid chromatography.ResultsAt room temperature,the appearance,pH value and insoluble particles had no significant change in 6 h,and the content of edaravone injection of the three kinds of crystalloid solution were stable.ConclusionEdaravone injection used together with invert sugar electrolyte injection,sodium potassium,magnesium and calcium dextrose injection,and compound electrolyte injection are stable within 6 h,but we still need to be cautious in the clinical application.
Edaravone;Crystalloid solution;Compatibility;Stability
2016-02-24
1.解放军医学院,北京 100853;2.解放军总医院第一附属医院药剂药理科,北京 100048
10.14053/j.cnki.ppcr.201609027

