柱前衍生HPLC-UV法测定人工牛黄中猪去氧胆酸含量
杨欢,丁月珠,段天璇,扶宇,王雄飞,王昭懿,袁瑞娟
北京中医药大学中药学院,北京 100102
柱前衍生HPLC-UV法测定人工牛黄中猪去氧胆酸含量
杨欢,丁月珠,段天璇,扶宇,王雄飞,王昭懿,袁瑞娟
北京中医药大学中药学院,北京 100102
目的建立柱前衍生HPLC-UV法测定人工牛黄中猪去氧胆酸含量的方法。方法以2-萘基溴甲基酮为衍生试剂、三乙胺为催化剂、60 ℃水浴条件下对猪去氧胆酸进行衍生,采用HPLC-UV法测定人工牛黄中猪去氧胆酸含量。结果当衍生试剂与猪去氧胆酸的摩尔比>20∶1,催化剂与猪去氧胆酸的摩尔比>15∶1,在60 ℃水浴条件下反应50 min时,衍生反应完全。猪去氧胆酸在0.1~2 μg范围内线性关系良好(r=0.999 7),平均回收率为97.85%(RSD=1.6%)。人工牛黄样品中猪去氧胆酸的含量为4.12%。结论本方法灵敏度高、准确可靠、稳定性和重复性好,可用于测定人工牛黄中猪去氧胆酸的含量。
人工牛黄;猪去氧胆酸;柱前衍生;高效液相色谱法;紫外检测
人工牛黄由牛胆粉、胆酸、猪去氧胆酸、牛磺酸、胆红素、胆固醇、微量元素等加工制成,是天然牛黄的代用品之一[1],其在中药制剂中的使用可有效缓解天然牛黄资源短缺。猪去氧胆酸为人工牛黄的特征成分之一,测定其含量可在一定程度上控制人工牛黄的质量,同时猪去氧胆酸也是区别人工牛黄和天然牛黄的指标性成分。由于猪去氧胆酸为末端吸收,无法采用高效液相紫外检测器进行检测。目前多采用高效液相蒸发光散射检测法[2-3]和薄层扫描法[4]测定其含量,但灵敏度较低。虽然采用质谱法测定有非常高的灵敏度,但存在仪器价格昂贵、重复性差等缺点。采用柱前衍生HPLC-UV法可以提高灵敏度,同时普适性强。故本试验采用柱前衍生后高效液相紫外检测器检测,对人工牛黄中猪去氧胆酸的含量进行测定。
1 仪器与试药
岛津高效液相色谱仪(LC-20AT),DF-101S集热式恒温加热磁力搅拌器(河南予华仪器有限公司),电子天平(CPA225D,北京赛多利斯仪器系统有限公司),KQ-300B型超声波清洗器(昆山市超声仪器有限公司),MTN-2800D型氮气吹干仪(天津奥特赛恩斯仪器有限公司)
猪去氧胆酸对照品(纯度98%,成都曼斯特生物科技有限公司,中国科学院成都生物研究所,批号MUST-15032804),人工牛黄(产地安徽,批号20110116,购自北京同仁堂),三乙胺(纯度为99.0%,天津市福晨化学试剂厂),2-萘基溴甲基酮(纯度98%,上海晶纯生化科技股份有限公司),水为去离子水,甲醇、乙腈均为色谱纯。其他试剂均为分析纯。
2 方法
2.1色谱条件
色谱柱:Agilent TC-C18(4.6 mm×150 mm,5 μm);流动相:甲醇-1%磷酸(83∶17,V∶V);流速:1.0 mL/min;检测波长:238 nm;进样量:20 μL。
2.2溶液的制备
2.2.1猪去氧胆酸标准溶液精密称取猪去氧胆酸对照品1 mg置1mL容量瓶中,用甲醇溶解并稀释定容至刻度。
2.2.2人工牛黄提取液精密称取人工牛黄 20 mg 于10 mL容量瓶中,用甲醇定容到刻度,称定质量,超声30 min(功率300 W,工作频率40 kHz),冷却至室温,再次称定质量,补足减失的质量,即得。
2.2.3衍生试剂溶液精密称取 2-萘基溴甲基酮63.5 mg于25 mL容量瓶中,用乙腈定容至刻度。
2.2.4催化剂溶液取三乙胺35.5 μL于10 mL容量瓶中,用乙腈定容至刻度。
2.3衍生化反应
取人工牛黄提取液,定容于1 mL容量瓶中,氮气吹干。加入催化剂溶液 0.1 mL、衍生试剂溶液0.75 mL,用甲醇定容至刻度,60 ℃水浴反应50 min后冷却到室温,加甲醇至刻度,按“2.1”项下色谱条件测定反应产物的峰面积。
2.4方法学考察
2.4.1专属性试验取催化剂溶液0.1 mL、衍生试剂溶液0.75 mL于1 mL容量瓶中后用甲醇定容到刻度,按“2.1”项下色谱条件记录色谱图与人工牛黄衍生化反应后的色谱图进行对比,见图1、图2。衍生试剂及催化剂对衍生产物无干扰,专属性良好。

图1 衍生试剂与催化剂HPLC图
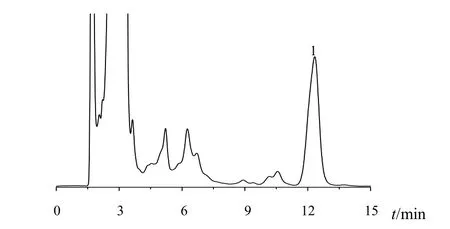
图2 人工牛黄经衍生后的HPLC图
2.4.2线性关系考察分别取猪去氧胆酸标准溶液0.005、0.01、0.02、0.05、0.07、0.1 mL于1 mL容量瓶中。按“2.3”项下条件进行衍生化反应,按“2.1”项下色谱条件测定反应产物峰面积。以峰面积对猪去氧胆酸质量作图,结果猪去氧胆酸在0.1~2 μg范围内线性关系良好,回归方程为Y=1.0×108X-9551 9,r=0.999 7。
2.4.3精密度试验将人工牛黄提取液按“2.3”项下条件进行衍生化反应后,按“2.1”项下色谱条件连续进样6次,记录峰面积,RSD=2.7%。
2.4.4重复性试验按照人工牛黄提取液的提取方法制备6份提取液,按“2.3”项下条件进行衍生化反应。按“2.1”项下色谱条件分别进样,记录峰面积,RSD=2.3%。
2.4.5稳定性试验将人工牛黄提取液分别于0、2、4、6、8、12、24 h进行HPLC测定,记录产物峰面积,RSD=2.4%,表明样品在24 h内稳定。
2.4.6加样回收率试验精密称取人工牛黄约10 mg,按人工牛黄提取液的方法提取6份提取液,取提取液定容于 1mL容量瓶中,氮气吹干。分别加入猪去氧胆酸标准溶液33、33、41、41、49、49 μL后按“2.3”项下条件进行衍生化反应,按“2.1”项下色谱条件测定反应产物的峰面积并计算回收率,结果见表1。

表1 猪去氧胆酸加样回收率试验
2.5样品含量测定
取人工牛黄样品,按上述提取方法和衍生条件反应后,测定猪去氧胆酸衍生产物峰面积,根据回归方程计算猪去氧胆酸含量,结果表明样品中猪去氧胆酸的含量为4.12%。
3 讨论
3.1衍生反应条件的确定
3.1.1衍生时间取猪去氧胆酸标准溶液0.1 mL于1 mL容量瓶中,加催化剂溶液0.1 mL、衍生试剂溶液0.5 mL,用甲醇定容至刻度,平行操作7份,分别于60 ℃水浴中反应10、20、30、40、50、60、70 min后冷却到室温,加甲醇至刻度,按“2.1”项下色谱条件测定反应产物的峰面积,结果见图3。反应产物的峰面积随反应时间而增大,反应50 min时达到最大。
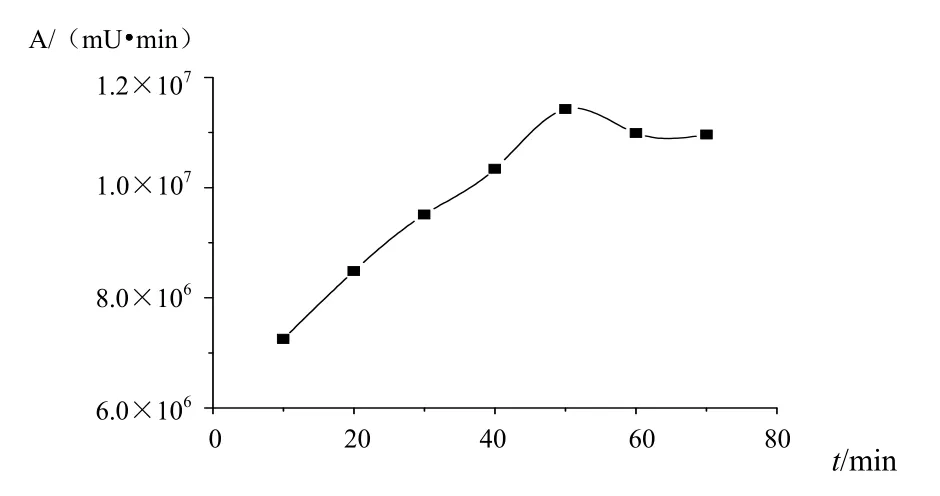
图3 猪去氧胆酸衍生产物峰面积与反应时间的关系
3.1.2催化剂用量取猪去氧胆酸标准溶液0.1 mL 于1 mL容量瓶中,加入衍生试剂溶液0.5 mL后分别加入2~30倍反应物摩尔量的催化剂溶液,用甲醇定容至刻度,60 ℃水浴反应50 min后冷却到室温,加甲醇至刻度,按“2.1”项下色谱条件测定反应产物的峰面积,结果见图4。反应产物的峰面积随加入催化剂溶液的增大而增大,当催化剂的摩尔量为反应物的10倍后反应产物的峰面积没有明显增加。

图4 猪去氧胆酸衍生产物峰面积与催化剂用量的关系
3.1.3衍生试剂用量取猪去氧胆酸标准溶液0.1 mL 于1 mL容量瓶中,加催化剂溶液0.05 mL后分别加入2~100倍反应物摩尔量的衍生试剂溶液,用甲醇定容至刻度,60 ℃水浴反应50 min后冷却到室温,加甲醇至刻度,按“2.1”项下色谱条件测定反应产物的峰面积,结果见图5。反应产物的峰面积随加入衍生试剂溶液的增大而增大,当催化剂的摩尔量为反应物的20倍后反应产物的峰面积没有明显增加。
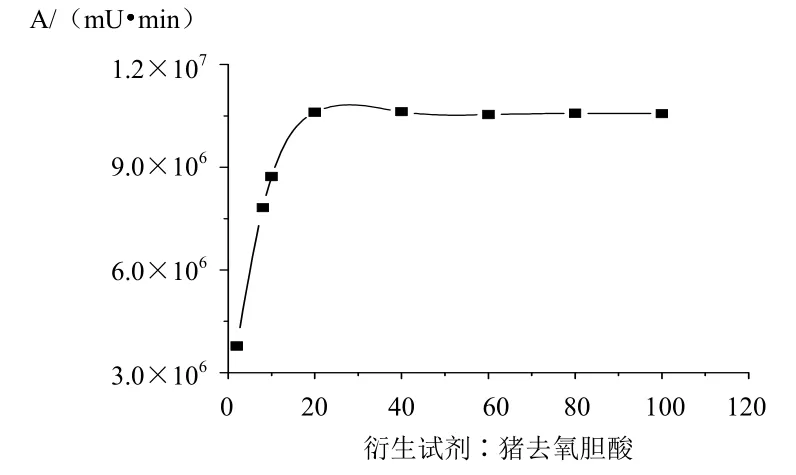
图5 猪去氧胆酸衍生反应产物与衍生试剂用量的关系
3.2高效液相色谱条件确定
衍生化反应后,将衍生产物在200~400 nm波长范围内紫外扫描,其最大吸收波长为238 nm,故选择238 nm作为检测波长。采用甲醇和1%磷酸溶液为流动相,衍生产物的峰形较好。同时,流动相的用量比为甲醇-1%磷酸(83∶17,V∶V)、流速为1.0 mL/min时,可以使衍生产物与杂质峰获得最佳分离。
4 小结
采用本法测定人工牛黄中猪去氧胆酸含量的结果与其他方法[4-5]相差不大。与其他文献报道的衍生方法[6-7]相比,本法以价格低廉的溴乙酰化试剂为衍生试剂、三乙胺为催化剂,提供碱性环境,降低了衍生反应的成本。本试验考察了衍生试剂用量、催化剂用量、反应时间对衍生产物的影响,确定了衍生反应进行完全所需的条件。整个衍生反应可在1 h内完成,利用HPLC-UV法对其进行分离,可在15 min内完成;方法学考察结果显示本法稳定可靠,可作为人工牛黄中猪去氧胆酸的含量测定的方法。本研究可为其他甾体类等无紫外吸收物质的分析提供依据,是一种灵敏度高、价格低廉、重复性好、快速简便的分析方法。
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015:5-8.
[2] 唐元军.HPLC-ELSD法同时测定猪胆粉中猪去氧胆酸和鹅去氧胆酸的含量[J].中药新药与临床药理,2010,21(6):651-653.
[3] 熊靖.人工牛黄甲硝唑胶囊中主要胆汁酸类成分的 HPLC-ELSD法测定研究[J].药物分析杂志,2015,35(6):1067-1071.
[4] 叶蓓蓓.薄层扫描法同时测定人工牛黄中胆酸及猪去氧胆酸的含量[J].药物分析杂志,2010,30(4):706-709.
[5] 冯芳.反相高效液相色谱-蒸发光散射检测法同时测定人工牛黄中多组分含量[J].药学学报,2000,35(3):216-219.
[6] 暴梅佳.柱前衍生化高效液相色谱法测定清开消炎片中猪去氧胆酸的含量[J].中药新药与临床药理,2010,21(2):186-188.
[7] 倪坤仪.反相高效液相色谱法测定牛黄类中成药中胆汁酸的含量[J].药学学报,1994,29(8):629-633.
Content Determination of Hyodeoxycholic Acid in Artificial Calculus Bovis by Pre-Column Derivatization HPLC-UV Method
YANG Huan, DING Yue-zhu, DUAN Tian-xuan, FU Yu, WANG Xiong-fei,WANG Zhao-yi, YUAN Rui-juan
(School of Chinese Materia Medica, Beijing University of Chinese Medicine,Beijing 100102, China)
Objective To establish a pre-column derivation HPLC-UV method for the content determination of hyodeoxycholic acid in artificial calculus bovis. Methods The hyodeoxycholic acid was derived by 2-bromo-2’-acetonaphthoneat using triethylamine as the catalyst in 60 ℃ water bath. After that, a HPLC-UV method was established to determine the content of hyodeoxycholic acid in artificial calculus bovis. Results When the derivatising time at 60 ℃ water bath was 50 min, the radio of the molar amount of derived reagents and hyodeoxycholic was over 20∶1 and the radio of catalyst and hyodeoxycholic was over 15∶1; the reaction was completed. The calibration curve was linear within the range of 0.1-2 μg for hyodeoxycholic acid (r=0.999 7), and the average recovery was 97.85% (RSD=1.6%). In this sample, the content of hyodeoxycholic is 4.12%. Conclusion The method is with high sensitivity, highly reproducible, reliable and accurate for the content determination of hyodeoxycholic acid in artificial calculus bovis.
artificial calculus bovis; hyodeoxycholic acid; pre-column derivation; HPLC; UV
R284.1
A
1005-5304(2016)10-0092-03
2015-11-07;编辑:陈静)
国家自然科学基金(81403071);国家级大学生创新训练计划项目(201410026033);北京中医药大学自主选题项目(2013-ZDXKKF-20、2013-YXJXTD-15)
袁瑞娟,E-mail:rjyuance@126.com
DOl:10.3969/j.issn.1005-5304.2016.10.021
——一个解释欧姆表刻度不均匀的好方法

