氧化石墨烯色谱固定相的制备及其在食品中三聚氰胺分析中的应用
张瑶琴,艾连峰,王曼曼,王学生*,刘 珊,侯 宁
(1.华北理工大学 公共卫生学院,河北 唐山 063000;2.河北出入境检验检疫局,河北 石家庄 050000)
氧化石墨烯色谱固定相的制备及其在食品中三聚氰胺分析中的应用
张瑶琴1,艾连峰2,王曼曼1,王学生1*,刘珊1,侯宁1
(1.华北理工大学公共卫生学院,河北唐山063000;2.河北出入境检验检疫局,河北石家庄050000)
以N,N-二环己基碳二亚胺为偶联剂,利用氧化石墨烯表面的羧基与氨基化硅球表面的氨基反应合成了一种氧化石墨烯键合硅球色谱固定相,通过扫描电镜和拉曼光谱对其进行表征,并考察了极性小分子在柱上的色谱行为。与氨基化硅球固定相相比,在相同的色谱条件下,三聚氰胺、双氰胺等氨基化合物的保留因子明显提高,且该固定相在亲水模式下对氨基化合物具有良好的保留性能,将其作为分析柱用于鸡蛋和牛奶中三聚氰胺的分析。该方法在0.2~50 μg/mL范围内线性良好,相关系数(r)为0.999 9,定量下限为0.87 mg/kg。在1,2,10 mg/kg加标水平下的回收率为84.7%~93.9%,相对标准偏差为4.1%~6.3%。关键词:氧化石墨烯;固定相;三聚氰胺;牛奶;鸡蛋;高效液相色谱(HPLC)
石墨烯(Graphene)是由碳原子紧密堆积成单层二维蜂窝状晶格结构的一种碳质新材料,因具有独特的物理化学性质而受到广泛关注[1]。氧化石墨烯(Graphene oxide,GO)是石墨烯的重要衍生物,由于其在单层碳原子构成的二维空间无限延伸的表面含有大量可修饰的基团(如羟基、羧基、环氧基、羰基等),因此可在水和多种有机溶剂中较好地分散,亲水性佳,生物兼容性好[2]。另外,氧化石墨烯具有较大的比表面积(石墨烯单片层表面积的理论计算值为2 630 m2/g)、高热稳定性和机械稳定性,因此有望成为一种理想的分离材料[3-5]。
目前,石墨烯材料已成功用于毛细管电泳、毛细管电色谱、气相色谱以及液相色谱固定相的合成[6-9]。2012年,Wang等[10]在毛细管中通过酸引发作用合成一种新型的GO掺杂聚合物毛细管色谱柱,并成功用于苯系物和多环芳烃的分离;Chen课题组[11]以3-氨丙基甲基二乙氧基硅烷为偶联剂将GO修饰到毛细管柱的内壁上,并用于甲苯、乙苯和萘等有机物的分离分析;2013年,Zhang等[12]以N-羟基琥珀酰亚胺/N-羟基硫代琥珀酰亚胺(NHS/EDC)为偶联剂将GO键合到氨基硅胶表面得到一种新型液相色谱固定相,通过与C18柱对比,发现该固定相对于中性化合物和非极性化合物具有良好的分离性能;Liang等[13]通过层层自组装法将GO键合到氨基化硅球表面,在反相色谱模式下,将得到的固定相用于苯胺、苯酚、多环芳烃和不同取代基的苯混合物的分离分析。目前,GO修饰的液相色谱固定相主要作为反相色谱模式分离目标物;且GO修饰的气相色谱固定相和液相色谱固定相多用于具有π-π共轭结构的苯系物和多环芳烃类等中性或弱极性物质的分离,而用于极性化合物的分析较少,特别是用于实际样品中极性小分子分析的研究未见报道。极性物质由于自身的性质,在传统C18色谱柱上保留较弱或难以保留。因此,常用的色谱固定相为正相或亲水固定相。如三聚氰胺是一种三嗪类含氮杂环的小分子极性化合物,采用C18柱分析时需加入辛烷磺酸钠等离子对试剂来实现三聚氰胺的保留,但会造成色谱系统的平衡时间长,且会降低色谱柱的使用寿命。因此,目前三聚氰胺的色谱分离多采用亲水型色谱柱(HILIC柱)[14-15]。
本研究以N,N-二环己基碳二亚胺为偶联剂,通过GO表面的羧基与氨基化硅球表面的氨基反应,将GO键合到氨基化硅球表面得到GO@SiO2固定相。考察了三聚氰胺、4-氨基安替比林、三聚氰酸等极性化合物在GO@SiO2固定相的色谱行为。GO@SiO2固定相对三聚氰胺、4-氨基安替比林等极性化合物在亲水模式下具有良好的保留性能。基于该固定相对极性分子的保留特点,将其用于三聚氰胺的分离分析,并通过优化色谱条件建立了该固定相分析检测鸡蛋和牛奶中三聚氰胺的新方法。
1 实验部分
1.1仪器与试剂
Waters UPLC-H-class超高效液相色谱仪(UPLC,美国Waters公司);LC-2010高效液相色谱仪(日本岛津公司);MS-H-S10 10通道标准加热磁力搅拌器(大龙兴创实验仪器有限公司);VORTEX GENIE旋涡混合器(美国Scientific Industries公司);固相萃取装置(美国Agilent Technologies公司);TRABOVAP 氮气吹干装置(美国Caliper Life Sciences公司);Milli-Q纯化系统(美国Millipore公司);S-4800型扫描电子显微镜(日本日立公司);DXR激光拉曼光谱仪(美国Thermo公司)。
除特别说明外,所用试剂均为分析纯。氨基化硅球(5 μm,天津博瑞键合有限公司);氧化石墨烯(GO,中国科学院山西煤炭化学研究所);N,N-二甲基甲酰胺(DMF,天津光复精细化工研究所);N,N-二环己基碳二亚胺(DCC,北京百灵威科技有限公司);醋酸铵(NH4OAc,北京迪马科技);氨水(石家庄试剂厂);色谱纯甲醇和乙腈购自Fisher Scientific(赫尔,比利时)。
标准物质:水杨酸(美国Sigma公司),双氰胺(DICY,美国Agela公司),三聚氰酸(CYA)、三聚氰胺(MEL)、克伦特罗、4-氨基安替比林(AA)、4-甲氨基安替比林(MAA)(德国Dr.Ehrenstorfer公司)。
1.2GO@SiO2固定相的制备与表征
以DCC为偶联剂,通过GO表面的羧基与氨基化硅球表面的氨基反应合成GO@SiO2填料(图1)[16-17]:将75 mg GO分散至75 mL DMF溶液中,超声30 min得到GO分散液。加入75 mg DCC和0.6 g氨基化硅球,并于50 ℃下搅拌24 h。反应结束后以8 000 r/min离心10 min,并用水和甲醇多次洗涤以除去未反应的GO和杂质,80 ℃烘干。将得到的GO@SiO2填料进行扫描电镜和拉曼光谱表征。利用湿法装柱,将空白氨基化硅球填料和合成的GO@SiO2填料装入不锈钢柱管(100 mm ×2.1 mm i.d.)得到色谱分析柱。
实验考察了GO用量(7.5,37.5,75,150 mg)和包覆次数(1次、2次)对GO@SiO2填料性能的影响。以三聚氰胺、双氰胺、克伦特罗、4-氨基安替比林、4-甲氨基安替比林、水杨酸和三聚氰酸作为目标物,对GO@SiO2色谱柱的色谱行为进行考察,通过保留因子(k)评价色谱性能。
1.3基于构筑的GO@SiO2分析柱分析测定牛奶及鸡蛋中三聚氰胺
1.3.1样品处理牛奶:取2.0 g牛奶于50 mL离心管中,加入14 mL乙腈和6 mL 10 g/L三氯乙酸溶液,摇匀,超声20 min,振荡提取10 min,10 000 r/min离心10 min,取上清液置于另一干净离心管中。
鸡蛋:取鸡蛋1枚,将蛋液搅匀,称取5.0 g于50 mL离心管中,加入23 mL乙腈-三氯乙酸混合溶液(体积比7∶3)和2 mL 22 g/L的乙酸铅溶液,摇匀,超声20 min,振荡提取10 min,10 000 r/min离心10 min,取10 mL上清液,待净化。
净化:按照国家标准方法[18]利用混合型阳离子固相萃取柱(PXC)对提取液进行净化,得到的洗脱液用50 ℃氮气吹干,加入1 mL乙腈定容,涡旋振荡1 min,过0.22 μm滤膜,待测。
1.3.2液相色谱条件色谱柱为合成的GO@SiO2分析柱(100 mm×2.1 mm);流动相为乙腈-10 mmol/L乙酸铵缓冲溶液(体积比80∶20);流速为0.3 mL/min;柱温30 ℃;检测波长220 nm;进样量为5 μL。
回收率与精密度:在牛奶、鸡蛋的阴性样品中分别添加三聚氰胺标准溶液,制成1.0,2.0,10.0 mg/kg 3个水平的加标样品,按照前处理步骤进行提取和净化,平行测定6次,计算回收率和精密度。
2 结果与讨论
2.1GO@SiO2固定相的制备与表征
2.1.1GO用量固定DMF的用量为75 mL,GO与DCC的质量比为1∶1,选择GO的用量分别为7.5,37.5,75,150 mg进行填料的合成。通过目标物三聚氰胺在色谱柱上的峰形和保留因子k评价不同条件所得色谱柱的性能。结果显示,随着GO用量的增大,GO@SiO2色谱柱对三聚氰胺的保留增强,k值增大;但当GO用量为150 mg时,在实验条件下峰形展宽且拖尾严重,因此选择GO用量为75 mg。
2.1.2GO包覆次数选择GO用量为75 mg,固定反应条件,分别包覆1次和2次。相比于GO包覆1次的GO@SiO2色谱柱,包覆2次时,三聚氰胺的保留时间增长,k值明显增大。但过多的GO使三聚氰胺的色谱峰展宽且拖尾严重,因此实验选择GO包覆1次的GO@SiO2色谱柱。
2.1.3GO@SiO2的表征通过扫描电镜对氨基化硅球和GO@SiO2的表面形貌进行分析。如图2所示,氨基化硅球的表面粗糙,经过实验方法反应后得到的GO@SiO2可以明显看出其表面的GO褶皱结构,说明GO成功键合到氨基化硅球的表面。氨基化硅球和GO@SiO2的拉曼光谱见图3,与氨基化硅球相比,GO@SiO2在1 350 cm-1和1 580 cm-1处有明显的特征峰,分别为D带和G带,进一步说明GO已成功键合到氨基化硅球的表面。
图2氨基化硅球(A)和GO@SiO2(B)的扫描电镜图
Fig.2SEM images of NH2-SiO2(A) and GO@SiO2(B)
2.1.4GO@SiO2色谱柱对极性目标物的色谱性能考察将氨基化硅球色谱柱和GO@SiO2色谱柱分别接入高效液相色谱仪,选择极性氨基化合物(三聚氰胺、双氰胺、克伦特罗、4-氨基安替比林以及4-甲氨基安替比林)、酸性化合物(水杨酸和三聚氰酸)作为目标物,进行色谱行为的考察,通过保留因子k评价色谱性能。如表1所示,与氨基化硅球色谱柱相比,由于GO的引入,上述两类目标物在保留行为上产生了较大变化。在相同色谱条件下,酸性目标物三聚氰酸和水杨酸在氨基硅球色谱柱的k高于GO@SiO2色谱柱;极性氨基化合物在GO@SiO2色谱柱上的k均高于氨基化硅球色谱柱。结果表明,该填料具有一定的亲水性,在亲水模式下,对所考察的带有氨基的极性小分子具有较好的保留行为。这可能是由于GO@SiO2表面带有未被GO包覆的氨基硅球上的氨基、硅羟基,GO表面的羧基、羟基以及非极性作用的碳链、石墨碳片层等基团,这些基团使得该填料具有亲水色谱模式的氢键作用、偶极作用和静电作用等多种次级效应。
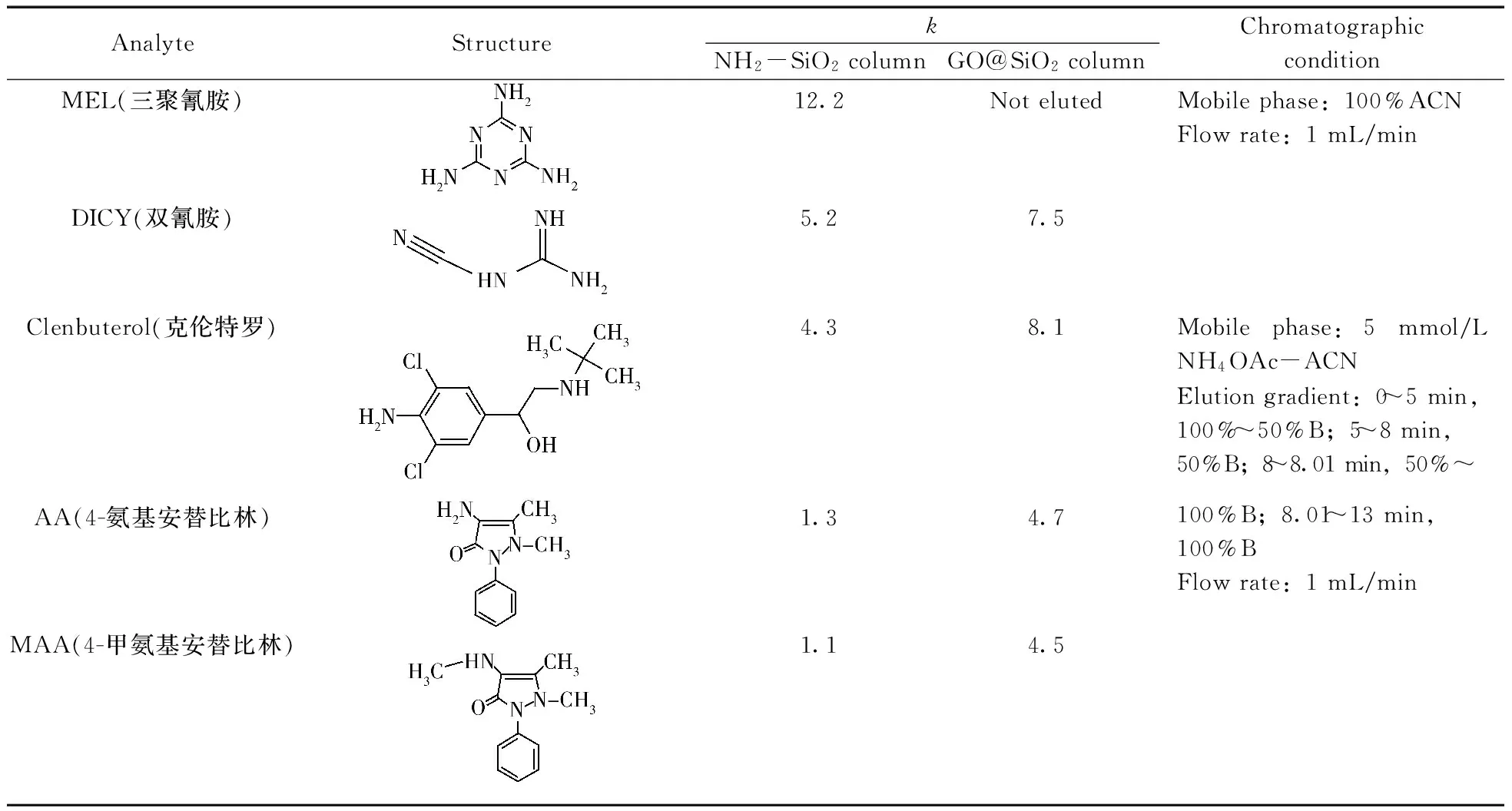
表1 不同物质在氨基化硅球色谱柱和GO@SiO2色谱柱上色谱行为的比较Table 1 Comparison of chromatographic behavior of different substances in the NH2-SiO2 column and GO@SiO2 column
(续表1)
2.2基于GO@SiO2柱测定牛奶、鸡蛋中的三聚氰胺
2.2.1流动相的选择固定有机溶剂与水相的体积比为8∶2,考察了乙腈-水、乙腈-0.1%甲酸水溶液、乙腈-10 mmol/L乙酸铵溶液以及乙腈-10 mmol/L乙酸铵溶液(含0.1%甲酸)作为流动相时对三聚氰胺分离分析的影响。结果显示,以乙腈-水、乙腈-0.1%甲酸水溶液和乙腈-10 mmol/L乙酸铵缓冲溶液(含0.1%甲酸)作为流动相时,峰展宽严重。而以乙腈-10 mmol/L乙酸铵溶液作为流动相时,峰形尖锐,响应值较高,因此选择乙腈-10 mmol/L乙酸铵溶液为最佳流动相。
2.2.2流动相配比的选择考察了不同配比的乙腈-10 mmol/L乙酸铵溶液流动相条件下,三聚氰胺标准溶液的保留时间和峰形。结果表明,随着流动相中乙腈含量的增加,三聚氰胺的保留时间增长,但峰展宽、拖尾严重,峰形变差。综合考虑,实验选择乙腈-10 mmol/L乙酸铵的比例为80∶20。
2.2.3线性范围用乙腈将三聚氰胺标准工作液稀释成0.2,0.5,1,2,5,10,20,50 μg/mL的系列浓度标准溶液,在优化色谱条件下进行测定,以三聚氰胺的浓度为横坐标(X,μg/mL),峰面积为纵坐标(Y)作图,得回归方程为Y=532.33X-66.06,相关系数(r)为0.999 9,说明三聚氰胺在0.2~50 μg/mL范围内线性关系良好。2.2.4回收率与精密度取空白牛奶、鸡蛋样品,在选定的色谱条件下进行加标回收实验,加标水平分别为1,2,10 mg/kg,按照样品处理方法进行提取净化,每个水平平行测定6次。得牛奶样品的加标回收率为84.7%~90.0%,相对标准偏差(RSD)为4.1%~6.0%;鸡蛋样品的加标回收率为89.2%~93.9%,RSD为4.1%~6.3%。图4为牛奶、鸡蛋的空白和加标样品的色谱图。
图4牛奶(A,B)和鸡蛋(C,D)的空白样品及加标后的色谱图
Fig.4Chromatograms of blank and fortified milk(A,B)and egg(C,D)samples A,C:blank samples;B,D:fortified samples
2.2.5检出限与定量下限在优化条件下,以基线噪声3倍峰面积(S/N=3)对应的三聚氰胺浓度计算得到检出限为0.25 mg/kg,以基线噪声10倍峰面积(S/N=10)对应的三聚氰胺浓度得定量下限为0.87 mg/kg,能够达到国家标准GB/T 22388-2008基于液相色谱对乳制品中三聚氰胺定量下限为2 mg/kg的分析要求。
3 结 论
本文合成了GO@SiO2固定相,并考察了极性化合物在该柱上的色谱行为,结果表明GO表面的含氧基团对氨基化合物具有良好的保留作用。将GO@SiO2固定相作为液相色谱固定相用于牛奶和鸡蛋中三聚氰胺的分析,能够满足国家标准对三聚氰胺的测定要求。该GO@SiO2色谱填料的制备,扩充了氧化石墨烯固定相的应用范围,同时也是商业化亲水柱的又一补充,GO@SiO2色谱柱具有成本低、色谱行为佳、实用价值高的特点。
[1]Rao C N R,Sood A K,Subrahmanyam K S,Govindaraj A.Angew.Chem.Int.Ed.,2009,48(42):7752-7777.
[2]Novoselov K S,Geim A K,Morozov S V,Jiang D,Zhang Y,Dubonos S V,Grigorieva I V,Firsov A A.Science,2004,306(5696):666-669.
[3]Wang X,Liu B,Lu Q,Qu Q.J.Chromatogr.A,2014,1362:1-15.
[4]Cui Y H,Yao W X,Zhang S L,Wang H D,Zhong F F.J.Instrum.Anal.(崔艳华,姚伟宣,张素玲,王海栋,钟芳芳.分析测试学报),2015,34(4):375-380.
[5]Wang X M,Wang H,Lu M X,Rao H H,Du X Z.J.Instrum.Anal.(王雪梅,王欢,鲁沐心,饶红红,杜新贞.分析测试学报),2015,34(12):1439-1445.
[6]Liu X L,Liu X,Liu X,Guo L P,Yang L,Wang S T.Electrophoresis,2013,34(6):1869-1876.
[7]Qu Q S,Gu C H,Gu Z L,Hu X Y.Anal.Chem.,2012,84:8880-8890.
[8]Liang R P,Liu C M,Meng X Y,Wang J W,Qiu J D.J.Chromatogr.A,2012,1266:95-102.
[9]Qu Q S,Shen Y Q,Gu C H,Gu Z L,Gu Q,Wang C Y,Hu X Y.Anal.Chim.Acta,2012,757:83-87.
[10]Wang M M,Yan X P.Anal.Chem.,2012,84(1):39-44.
[11]Xu Y Y,Niu X Y,Dong Y L,Zhang H G,Li X,Chen H L,Chen X Q.J.Chromatogr.A,2013,1284:180-187.[12]Zhang X Q,Chen S,Han Q,Ding M Y.J.Chromatogr.A,2013,1307:135-143.
[13]Liang X J,Liu S J,Song X W,Zhu Y W,Jiang S X.Analyst,2012,137(22):5237-5244.
[14]Zhu W X,Yuan P,Yang J Z,Liu Y F,Guo J F,Wei W,Zhang S S.J.Instrum.Anal.(祝伟霞,袁萍,杨冀州,刘亚风,郭俊峰,魏蔚,张书胜.分析测试学报),2008,27(12):1288-1292.
[15]Li Y Z,Hao W Q,Wang Y B,Chen Q,Li J C,Sun X L.Chin.J.Chromatogr.(李延昭,郝卫强,王余波,陈强,李锦春,孙晓丽.色谱),2012,30 (7):716-720.
[16]Liu Q,Shi J B,Sun J T,Wang T,Zeng L X,Jiang J B.Angew.Chem.Int.Ed.,2011,50(26):5913-5917.
[17]Sitko R,Zawisza B,Talik E,Janik P,Osoba G,Feist B,Malicka E.Anal.Chim.Acta,2014,834:22-29.
[18]GB/T 22388-2008.Determination of Memaline in Raw Milk and Dairy Products.National Standards of the People's Republic of China(原料乳及乳制品中三聚氰胺检测方法.中华人民共和国国家标准).
Fabrication of Graphene Oxide@SiO2as Stationary Phase and Its Application in Determination of Melamine in Food Samples
ZHANG Yao-qin1,AI Lian-feng2,WANG Man-man1,WANG Xue-sheng1*,LIU Shan1,HOU Ning1
(1.School of Public Health,North China University of Science and Technology,Tangshan063000,China;2.Hebei Entry-Exit Inspection and Quarantion Bureau,Shijiazhuang050000,China )
Graphene oxide(GO) has received great interest for its unique properties and potential applications in separation.Here,(GO)@SiO2composites-based stationary phase for high performance liquid chromatography(HPLC) were fabricated by covalently bonding GO onto aminosilica microspheres using N,N-dicyclohexylcarbodiimide as coupling agent.The reaction was achieved via coupling the amino groups of aminosilica and the carboxyl groups of GO.The prepared GO@SiO2was characterized by scanning electron microscopy and Raman spectroscopy.GO@SiO2composites were developed as stationary phase,and the chromatographic properties of bare SiO2and GO@SiO2were investigated by a series of polar compounds including melamine,cyanuric acid,clenbuterol,4-aminoantipyrine and 4-methylaminoantipyrine.Under the same conditions,GO@SiO2column obtained a better separation for polar analytes in hydrophilic mode and the column was used as an analytical column for the determination of melamine in egg and milk samples.The proposed method was linear over the range of 0.2-50.0 μg/mL with a correlation coefficient(r) of 0.999 9.The limit of quantitation for melamine was 0.87 mg/kg.The recoveries of melamine at three spiked levels of 1,2,10 mg/kg ranged from 84.7% to 93.9% with relative standard deviations (RSDs) of 4.1%-6.3%.
graphene oxide(GO);stationary phase;melamine;milk;egg;high performance liquid chomatography(HPLC)
2016-02-05;
2016-03-10
国家自然科学基金项目(21305028);河北省自然科学基金项目(B2013209238,H2016209018);河北省教育厅自然科学项目(Q2012155);国家质检总局项目(2013IK154,2014IK092)
王学生,硕士,教授,研究方向:卫生化学,Tel:0315-2592086,E-mail:xswang64@163.com
10.3969/j.issn.1004-4957.2016.08.009
O657.72;O623.732
A
1004-4957(2016)08-0981-06

