温度对香蕉不定芽生长及抗氧化酶活性的影响
丰 锋,叶银芳,叶春海(广东海洋大学农学院,广东 湛江 524088)
温度对香蕉不定芽生长及抗氧化酶活性的影响
丰 锋,叶银芳,叶春海
(广东海洋大学农学院,广东 湛江 524088)
为探明温度对香蕉不定芽生长及根系活力的影响,以巴西香蕉(Musa paradisiaca)为材料,在人工气候箱条件下研究温度对香蕉不定芽生长及抗氧化酶活性的影响。结果表明:SOD活性呈现上升-下降波动变化,POD活性先上升,培养15~20 d达到最高后下降,培养45 d后又缓慢上升,CAT活性整体先下降,培养45 d后上升;在30℃以内,随温度升高,根系活力逐渐增加,培养20 d后游离脯氨酸含量随温度升高而上升,培养50 d开始下降,MDA含量先逐渐下降后上升,培养20 d和45 d较低;30℃最适宜香蕉不定芽生长,此条件下培养25 d根系活力达最高(11.92 mg /g·h),游离脯氨酸(58.76 μg/g)和MDA含量(7.15 nmol/g)都较低,根茎叶生长旺盛(苗高5.02 cm、叶数3.64片、根数4.63条、根长4.91 cm),是最适宜移栽的时间;培养45 d根系活力为2.33 mg/g·h,游离脯氨酸(94.83 μg/g)和MDA含量(9.83 nmol/g)都较低,根茎叶生长旺盛(苗高6.15 cm、叶数4.97片、根数6.01条、根长6.06 cm),是次适宜移栽的时间。30℃最适宜香蕉不定芽的生长,培养25 d是最适宜移栽的时间。
香蕉试管苗;抗氧化酶;根系活力;游离脯氨酸;丙二醛
丰锋,叶银芳,叶春海. 温度对香蕉不定芽生长及抗氧化酶活性的影响[J].广东农业科学,2016,43(7):25-30.
香蕉是岭南四大佳果之一,也是世界上进出口贸易量最大的水果。在香蕉产业化生产中,种苗的生产至关重要,目前国内外大多采用组培快繁进行工厂化繁殖。与传统吸芽繁殖相比,香蕉组培快繁能迅速推广优良品种,繁殖系数高,周期短,生长整齐,收获一致,有利于集约化经营和商品化生产[1]。当前对香蕉试管苗的研究主要集中在培养基激素配比和环境因子上[1-3],生理生化和细胞组织结构方面的研究还很少。Andrea等[4]认为在生根培养中,根数、叶数和根长是衡量香蕉组培苗能否假植的3个重要指标。试管苗根的质量直接影响移栽成活率和试管苗移栽后的生长发育,而试管苗根的生长发育与培养基、培养条件等多种因素有关[5]。CAT活性、SOD活性、POD活性、根系活力、脯氨酸含量和丙二醛(MDA)含量等可间接反映根的质量[6-8]。本文研究了香蕉不定芽在不同温度下生根培养过程中CAT活性、SOD活性、POD活性、根系活力、脯氨酸含量、MDA含量的变化,以期找到香蕉不定芽的最佳培养条件和培养时间,培育优质壮苗,适时移栽或延长香蕉生根苗的货架期,为工厂化规范化生产提供依据。
1 材料与方法
1.1试验材料
供试品种为巴西蕉,香蕉第7代不定芽,由广东海洋大学农业生物技术研究所提供。试验于2012年1~10月在广东海洋大学植物细胞工程实验室进行。
1.2试验方法
1.2.1生根培养 将长势相对一致的不定芽(株高1.5~2 cm、茎粗0.2~0.3 cm)转入生根培养基(1/2MS+IBA 1.0 mg/L+NAA 0.2 mg/L+KT 0.5 mgL+少量活性碳+糖15 g/L+琼脂5.5 g/L)中,置于气候培养箱中,培养箱设置4个温度梯度(20、25、30、35℃),光照强度8.75 μmol/ m2·s,10 h/d。每个处理60瓶,每瓶6~8个不定芽。
1.2.2形态、生理指标及分析方法 每隔3 d观察1次,记录香蕉不定芽的形态变化;从培养10 d开始,每隔5 d随机取5瓶,共30株苗,分两组统计叶数和根数,用游标卡尺测量茎粗(距根茎交界部位5~6 mm处),用直尺测量根长、株高。取倒数1~3叶混匀,测定SOD、CAT、POD活性以及游离脯氨酸、MDA含量[9-12],取根尖(1 cm)部分测定根系活力(TTC法)[13]。采用邓肯氏新复极差法进行多重差异比较。
2 结果与分析
2.1温度对香蕉不定芽根系生长的影响
试验结果表明,25、30℃处理香蕉不定芽接种3 d开始生根,接种6 d后生根率达50%,接种10 d后生根率超过80%;20℃处理接种5 d开始生根,接种10 d生根率达50%;35℃处理不生根。20℃处理香蕉不定芽的根多为主根,根较短、少,伸长缓慢;25、30℃处理的根白色粗壮,伸长较快,主根和须根均较多,接种40 d后30℃处理的根大部分中间断开,近根尖部分变褐,25℃处理的根少部分易断,根尖变褐;20℃处理的根粗壮,呈白色。所有处理均开始长出根毛。
不同温度处理下不同培养时期的根数、根长变化见图1和图2,从图1、图2可见在20~30℃范围内,根数和根长在培养20 d内均直线上升,随着培养时间的延长,根数和根长缓慢增加;根长随温度升高而增加,30℃处理根长极显著高于其他处理;培养15~35 d内,25℃处理根长极显著高于20℃处理,培养40 d后25℃处理根长显著高于20℃处理;25℃处理香蕉不定芽根数最多,显著高于其他处理。

图1 温度对香蕉不定芽根数的影响

图2 温度对香蕉不定芽根长的影响
2.2温度对香蕉不定芽株高和叶数的影响
从图3、图4可以看出,温度过高(35℃)或过低(20℃)均不利于香蕉不定芽长高和长叶,25、30℃处理株高和叶数极显著高于20、35℃处理,35℃处理香蕉不定芽几乎不长高,多为莲座叶,培养25 d内30℃处理株高极显著高于25℃处理,培养30 d后差异不显著;30℃范围内,随着温度提高和培养时间延长,株高和叶数逐渐增加。30℃处理培养25 d内株高直线上升,培养20~35 d叶数增加最快;25℃处理培养30 d内株高直线上升,培养20~30 d叶数增加最快,之后均缓慢增加;20℃处理培养35 d前株高增加缓慢,之后才开始快速增加。

图3 温度对香蕉不定芽株高的影响

图4 温度对香蕉不定芽叶数的影响
2.3温度对香蕉不定芽抗氧化酶活性的影响
2.3.1SOD活性 所有处理的香蕉不定芽培养25 d SOD活性最强,之后除20℃处理SOD活性波动较小外,其他处理波峰波谷交替出现,活性呈“上升-下降-上升-下降-上升-下降”的变化趋势,培养10、20、25、45、60 d处理间差异均极显著(图5)。

图5 温度对香蕉不定芽SOD活性的影响
2.3.2POD活性 由图6可知,20、35℃处理的香蕉不定芽POD活性极显著高于25、30℃处理。从培养10 d起,所有处理的POD活性逐渐上升,20、25℃处理香蕉不定芽POD活性在培养20 d最高,30、35℃处理香蕉不定芽POD活性在培养15 d最高,之后均逐渐下降,培养45 d后又开始缓慢上升。
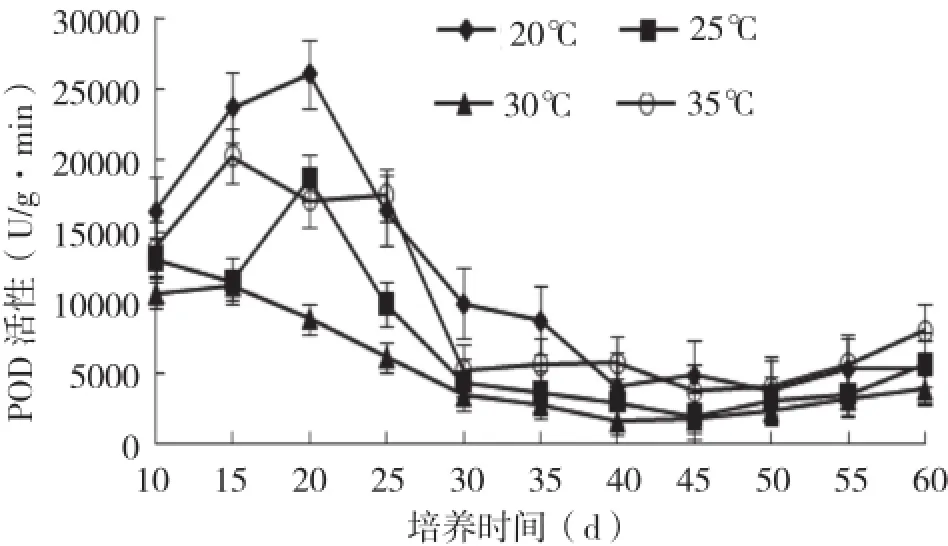
图6 温度对香蕉不定芽POD活性的影响
2.3.3CAT活性 图7显示,35℃处理香蕉不定芽CAT活性极显著低于其他处理,培养30 d后CAT活性随温度升高而下降,培养45 d后活性逐渐升高,30、35℃处理的CAT活性极显著低于20、25℃处理。20℃处理香蕉不定芽的CAT活性在培养15、30 d都出现高峰,随后下降;25℃处理的CAT活性在培养10~25 d稍微下降,在培养30 d出现高峰,随后下降;30℃处理的CAT活性在培养15 d出现高峰,随后下降;35℃处理的CAT活性在培养10~20 d稍微下降,在培养25 d出现高峰,随后下降。

图7 温度对香蕉不定芽CAT活性的影响
2.4温度对香蕉不定芽根系活力的影响
从图8可以看出,在30℃以内,随着温度升高,香蕉不定芽的根系活力逐渐增加;培养40 d内处理间差异极显著。20℃处理的根系活力逐渐上升,25℃处理的根系活力缓慢上升、至培养45 d后又逐渐下降,30℃处理的根系活力培养20 d急剧上升,培养25 d达到最大值,然后急剧下降,培养40 d后又逐渐上升。

图8 温度对香蕉不定芽根系活力的影响
2.5温度对香蕉不定芽游离脯氨酸含量的影响
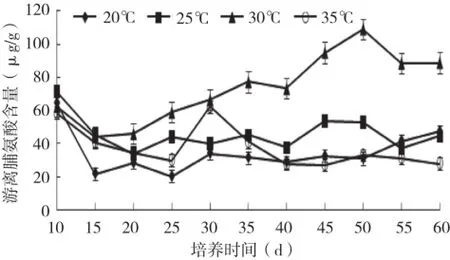
图9 温度对香蕉不定芽游离脯氨酸含量的影响
由图9可知,在30℃以内,香蕉不定芽培养20 d后游离脯氨酸含量随温度升高而上升,各处理间差异极显著;培养10 d起,所有温度处理的香蕉不定芽游离脯氨酸含量均下降,在培养15~60 d,20、25℃处理香蕉不定芽游离脯氨酸含量均平缓上下波动,35℃处理培养30 d达到高峰,随后平缓上下波动,直至培养50 d开始下降,趋于平缓。
2.6温度对香蕉不定芽MDA含量的影响
培养30 d后,所有处理间差异不显著。从培养10 d起,除35℃处理外,其他处理香蕉不定芽的MDA含量均下降,在培养20 d最低,之后逐渐上升,直到培养45 d MDA含量稍下降,培养50 d MDA含量上升,之后逐渐下降;35℃处理香蕉不定芽MDA含量在培养20 d达最高(图10)。

图10 温度对香蕉不定芽MDA含量的影响
3 结论与讨论
根系活力泛指根的吸收与合成能力,根的生长情况和活力水平直接影响地上部营养状况及产量水平,根系活力大小在一定程度上反映了作物吸收养分能力的强弱,一般情况下,根系活力越高,吸收养分能力越强,根系的生活力与定植成活率有相关关系,是反映容器苗质量的主要指标[13-14]。
本试验结果表明,香蕉不定芽的根数、根长在培养20 d内、株高在培养25 d内、叶数在培养30 d内均直线增加,之后增加缓慢。香蕉不定芽SOD活性在培养25 d出现波峰,培养50 d出现波谷;POD活性在培养25 d出现波峰,培养45 d最低,之后逐渐增加;CAT活性在培养15 d出现波峰,培养30 d后开始下降,培养45 d最低,之后快速增加。30℃处理香蕉不定芽根系活力在培养25 d最高,之后逐渐下降,其他处理根系活力在培养40 d后缓慢上升;30℃处理脯氨酸含量极显著高于其他处理;35℃处理MDA含量在培养20 d出现波峰,其他处理在培养20 d和45 d出现波谷,之后快速增加。可见,在转接后培养15 d内,香蕉不定芽的CAT活性不断增加,培养20 d内POD活性逐渐增加,MDA含量、脯氨酸含量逐渐下降,根数、根长直线增加,培养25 d内SOD活性逐渐增加,根系活力逐渐增加,株高直线增加,培养30 d内叶数直线增加。
SOD、POD、CAT等抗氧化酶类是植物中重要的抗氧化系统,对细胞的分化有促进作用[15]。SOD、POD、CAT可清除代谢过程中产生的活性氧,其中SOD是抗氧化防御体系的关键酶,可将歧化成H2O2和O2,而CAT和POD可以把H2O2转变成H2O[16]。SOD和CAT或POD共同作用可以清除植物体内具有潜在危险的和H2O2,从而最大程度减少活性氧的形成。MDA是膜脂过氧化的最终产物,其含量反映了细胞膜脂过氧化水平,反映植物遭受逆境伤害的程度[17]。游离脯氨酸的积累指数与植物的抗逆性有关,可作为植物抗逆性的一项生理生化指标[4]。
根据培养过程根数、根长、根系活力、株高、叶数等变化,可见光照强度没有显著影响,25~30℃是最适宜香蕉不定芽生根的温度。在此条件下,根据SOD、POD、CAT活性变化可见,培养初始阶段(25 d内)CAT活性最先上升(15 d),接着是POD活性上升(20 d),然后SOD活性上升(25 d),随之游离脯氨酸含量降低(15~20 d),MDA含量降低(15~20 d),有效地修复了切分损伤,根系活力增加并达到最高(25~30 d),根系数量和长度迅速增加(20 d内),株高(25 d内)和叶数(35 d内)迅速增加,培养25 d是最适宜香蕉试管苗移栽的时间;随叶数增加趋缓(30 d)、叶色逐渐变绿、光合作用逐渐增强,根毛出现,根系活力逐渐增加(40 d),但因环境密闭,CO2供应不足,叶片逐渐变黄衰老,培养后期(60 d内),SOD、CAT活性培养50 d最低、培养55 d最高,POD活性培养45 d最低,之后逐渐增加,游离脯氨酸、MDA含量培养50 d最高、培养55 d最低,根系活力培养40 d后开始逐渐增加。可见,培养后期阶段,培养55 d是较适宜的移栽时间。
综上可知,在香蕉试管苗生根培养过程中,30℃最适宜香蕉试管苗的生长,此条件下培养25 d时根系活力达到最高值11.92 mg /g·h,游离脯氨酸(58.76 μg/g)和MDA含量(7.15 nmol/g)均较低,根茎叶生长旺盛(苗高5.02 cm、叶数3.64 片、根数4.63 条、根长4.91 cm),是最适宜移栽的时间;培养45 d时根系活力(2.33 mg /g·h)较高,游离脯氨酸(94.83 μg/g)和MDA含量(9.83 nmol/g)均较低,根茎叶生长旺盛(苗高6.15 cm、叶数4.97 片、根数6.01 条、根长6.06 cm),是次适宜移栽的时间。
[1] 丰锋,叶春海,王耀辉. 香蕉增殖培养培养基配方的优化[J]. 果树学报,2007,24(3):397-399.
[2] 郑洪立,叶春海,王季槐. 温度和光照对香蕉组培苗生长和增殖的影响[J]. 热带作物学报,2008,29(4):455-459.
[3] 梁钾贤,陈彪,张志胜. 光温互作和培养基中的附加成分对香蕉试管苗生长的影响[J]. 植物生理学通讯,2006,42(3):401-405.
[4] Andrea K,Francisco J Z. Low-cost alterntives forthe micropropagtion of banana[J]. Plant Cell,Tissue and Organ Culture,2001,66(1):67-71. [5] 丰锋,叶春海. 香蕉生根培养基配方的优化研究[J]. 福建果树,2007(1):11-14.
[6] 刘金祥,谭杏婵,刘家琼. 高温胁迫对香根草含水量、膜透性、脯氨酸和叶绿素含量的影响[J]. 草原与草坪,2005(6):58-61.
[7] 许乃霞,杨益花. 抽穗后水稻根系活力与地上部叶片衰老及净光合速率相关性的研究[J].安微农业科学,2009,37(5):1919-1921.
[8] 牛蓓,傅华龙,卿人韦,等. 温度对组培金线莲生理生化影响的研究[J]. 四川大学学报(自然科学版),2004,41(4):842-844.
[9] Giannopolitis C N,Ries S K. Superoxide dismutase L occurrence in higher plants[J]. Plant Physiol,1977,59:309-314.
[10] Cakmak I,Marschner H. Magnesium defieieney and high light intensity enhance activities of superoxide dismutase ascorbate peroxidase,and glutathione reductase in bean leaves[J]. Plant Physiol,1991,98:1222-1227.
[11] 王爱国,罗广华. 植物的超氧物自由基与轻胺反应的定量关系[J]. 植物生理学通讯,1990,26 (2):55-57.
[12] 蒋德安,朱诚. 植物生理学实验指导[M]. 成都:成都科技大学出版社,1999:92-93.
[13] Popham P L,Novacky A. Use of dimethyl sulfoxide to detect hydroxyl radical during bacteria-induced hypersensitive reaction[J]. Plant Physiol,1991,96:1157-1160.
[14] 吴朝海,唐道城. 东方百合生长期根系的抗氧化酶活性及根系活力[J]. 贵州农业科学,2010,38(11):53-55.
[15] Yordanov Y,Yordavov E,Atanassov A. Plant regenera-tion from interspecific hybrid and backcross progeny of Helianthus eggertii× Helianthus annuis[J]. Plant Cell,Tissue and Organ Culture,2002,71(1):7-14.
[16] Mutasim M K,Kazumi H. Ethylene inhibitors enhance in vitro root formation on Faba bean shoots regenerated on medium containing thidiazuron[J]. Plant Growth Regulation,2000,32(1):59-63.
[17] Ekrem G,Songul G. Plant regeneration from unfertilized ovaries of sugar beet(Betavulgaris L.) cultured in vitro[J]. Turkish J of Botany,1998,22(4):233-238.
(责任编辑 张辉玲)
Effects of different temperatures on growth and root antioxidant enzyme activities of banana adventitious bud
FENG Feng,YE Yin-fang,YE Chun-hai
(College of Agriculture,Guangdong Ocean University,Zhanjiang 524088,China)
To clear the effects of temperature on the growth of banana adventitious bud and its root activity,taking ‘Brazil’ banana (Musa paradisiaca) as materials in the artificial climate chamber conditions. The results showed that SOD activity first increased and then decreased. POD activity first elevated and reached the highest in the 15-20 d,and then declined and slowly improved after 45 d. CAT activity first fell and increased after 45 d. At 30℃,with the increase of temperature,root activity gradually increased and the free proline content after 20 d rose and began to drop at the 50th d. MDA content decreased gradually and then increased,was lower at the 20th d and the 45th d. Banana adventitious bud grew best at 30℃. At the 25th day under this condition,the root activity reached the highest (11.92 mg /g·h),the contents of free praline (58.76 μg/g) and MDA (7.15 nmol/g) were low,and vigorous growing plantlets (height 5.02 cm,leaf numbers 3.64,root numbers 4.63±0.06,root length 4.91 cm) were most suitable for transplanting. At the 45th day under this condition,the root activity reached higher (2.33 mg /g·h),the contents of free praline (94.83 μg/g) and MDA (9.83 nmol/g) were low,and vigorous growing plantlets (height 6.15 cm,leaf numbers 4.97,root numbers 6.01,root length 6.06 cm) were suitable for transplanting. The results suggested that 30℃ was most suitable for the growth of banana adventitious bud and the most suitable time for transplanting was to train for 25 days.
banana plantlet; antioxidant enzyme; root activity; free proline; MDA
S668.1
A
1004-874X(2016)07-0025-06
2016-02-25
国家级大学生校外实践教学基地项目;广东省高等学校本科特色专业、专业综合改革、试点专业项目;广东省重大科技专项(2012A020200009,2013B020201004);广东省现代农业产业技术体系建设专项(0909354)
丰锋(1969-),男,教授,E-mail:ff1703@126.com

