维持性血液透析患者钙磷代谢现状的单中心横断面研究
唐莉,欧阳凌霞,姜继光,施翎,冯微微,吕敏,姚许平
维持性血液透析患者钙磷代谢现状的单中心横断面研究
唐莉,欧阳凌霞,姜继光,施翎,冯微微,吕敏,姚许平
目的探讨单中心维持性血液透析患者钙、磷和甲状旁腺激素等水平。方法选取透龄在3个月以上的维持性血液透析患者340例,于透析前检测电解质、肝功能及全段甲状旁腺激素(iPTH)等指标,参照KDIGO慢性肾脏病矿物质和骨异常临床实践指南及K/DOQI指南标准分析钙、磷及iPTH达标情况,并对患者性别、年龄、透龄及透析频率等进行分析。结果 (1)参照KDIGO慢性肾脏病矿物质和骨异常临床实践指南,患者血钙达标率59.7%(203/340),血磷达标率为18.8%(64/340),iPTH达标率为62.9%(214/340)。参照K/DOQI指南,患者血钙达标率41.5%(141/340),血磷达标率为29.7%(101/340),iPTH达标率为28.8%(98/340)。(2)多因素方差分析显示:患者年龄在45岁以下患者血磷达标率最低,透龄在37~60个月血磷达标率最低,血钙达标率最低分别为透龄3~12个月及60个月以上;透龄>60个月时iPTH达标率最低。每周3次透析频率患者血磷水平较每周2次患者显著降低,但达标率未见差异。结论按指南建议的钙磷达标标准,中心患者普遍存在钙磷代谢紊乱,尤其是血磷的水平。应加强患者的限磷饮食宣教及降磷药物治疗。
维持性血液透析;钙磷代谢
维持性血液透析患者血清钙、磷紊乱和全段甲状旁腺激素(iPTH)分泌异常均可增加终末期肾病患者心血管事件的危险性[1]。2009年改善全球肾脏病预后组织(KDIGO)颁布了适用于全球的慢性肾脏病-矿物质和骨异常(CKDMBD)的诊断、评估、预防和治疗的临床实践指南[2],在循证医学基础上,提出了不同的血钙、血磷和iPTH靶目标。这些目标与2003年发布的K/DOQI指南[3]存在一定的差异。笔者采用非随机横断面研究,对中心维持性血液透析患者钙、磷和甲状旁腺激素等按不同标准计算出的达标情况进行分析,了解患者 CKDMBD的现状及制定合理的管理目标。现将结果报道如下。
1 资料与方法
1.1一般资料入选标准:(1)2013年5月在宁波市泌尿肾病医院血液净化中心行规律血液透析3个月以上的维持性血液透析患者;(2)排除同期伴有肿瘤、严重感染等病患。共入选340例,其中男 188例,女 152例;平均年龄(54.7±15.65)岁;平均接受血液透析治疗时间为(42±36.77)个月。慢性肾功能衰竭原发病:慢性肾小球肾炎222例,糖尿病肾病51例,高血压肾损害23例,多囊肾22例,慢性移植肾肾病22例。
1.2研究方法所有患者于透析前空腹抽取外周血,检测血清白蛋白、碱性磷酸酶、钙、磷及iPTH等指标,根据公式计算血清白蛋白校正钙(Ac-Ca)水平。按照KDIGO指南建议[2],设定达标范围为血钙 8.4~ 10.5 mg/dl(2.10~ 2.55 mmol/L),血磷2.5~4.5 mg/dl(0.81~1.45 mmol/L),iPTH 130~600 pg/ml。参照2003年K/DOQI指南[3],设定达标范围为血钙8.4~9.5 mg/dl(2.10~2.37 mmol/L),血磷3.5~5.5 mg/dl(1.13~1.78 mmol/L),钙磷乘积≤4.52 mmol2/L2,血iPTH 150~300 pg/ml。分析患者血清钙、磷、iPTH水平和两种标准下达标情况,并对患者性别、年龄、透龄及透析频率差异等进行多因素方差分析,其中年龄分为<45岁、45~60岁及>60岁3组,透龄分为3~12个月、13~36个月、37~60个月及>60个月4组,透析频率分为2次/周及3次/周两组。
1.3统计方法使用 SPSS 19.0统计软件进行分析。计量资料用均数±标准差表示,两组比较采用 检验;计数资料比较用2检验。<0.05为差异有统计学意义。
2 结果
2.1血钙水平及达标分析患者平均校正血钙值为(2.21±0.26)mmol/L。参照KDIGO 标准血钙达标率为 59.7% (203/340),各透龄组患者血钙达标率差异有统计学意义(<0.05),透龄在12个月内患者血钙达标率最低,为47.6%。参照K/DOQI标准血钙达标率为41.5% (141/340),各透龄组患者血钙达标率差异无统计学意义(>0.05)。见表1。
2.2血磷水平及达标分析患者平均血磷值为(2.0±0.68)mmol/L。按KDIGO标准计算血磷达标率为18.8%(64/340);45岁以下患者血磷达标率低为8.0%(表2);透龄37~60个月患者血磷达标率最低为8.9%(表3);按K/DOQI标准计算血磷达标率为29.7%(101/340);45岁以下患者血磷达标率最低为20.0%,透龄37~60个月患者血磷达标率最低为22.8%。每周 3次透析患者平均血磷([1.86±0.57)mmol/L]显于每周 2次([2.13±0.71)mmol/L,=3.35,<0.05],每周3次透析患者血磷达标率为30.8%,每周2次为27.4%,达标率差异无统计学意义(2=0.695,=0.707)。
2.3iPTH水平及达标分析患者平均iPTH水平为(397.26±445.19)pg/ml。按KDIGO标准计算iPTH达标率为62.9% (214/340);按K/DOQI标准计算iPTH达标率为28.8%(98/340);各透龄组患者iPTH达标率差异显著,透龄>60个月患者iPTH达标率最低为16.9%,见表4。
iPTH在150~300 pg/ml与130~600 pg/ml范围时,血钙、血磷、钙磷乘积及碱性磷酸酶等差异无统计学意义(均>0.05),见表5。
3 讨论
在CKD维持性血液透析患者中,矿物质和骨代谢紊乱十分常见。目前国内外相关指南主要有KDIGO和K/DOQI两个指南。将这些指南应用并结合临床实践,帮助和改善CKD患者预后,是中国肾脏病学界的重要课题。2013年5月笔者对透析中心维持性血液透析患者进行钙磷等指标的横断面调查研究,分析患者钙磷代谢的现状及特点。
考虑透析患者严格控制血磷水平确实很难,KDIGO工作组允许适当灵活掌握透析前血清磷水平并声称推荐力度较差(2C)。2012年王海燕教授发布的中国参与透析预后与实践模式研究(DOPPS)研究数据显示我国血液透析(HD)患者中高磷血症的控制情况相当不理想,参照 K/DOQI指南血磷达标率为37.6%,其中年龄、地域及HD是高血磷的独立危险因素[4]。本文显示按K/DOQI指南血磷达标率为29.7%(101/340);而按 KDIGO指南标准血磷达标率仅为18.8%。统计分析年老患者血磷控制优于年轻患者,与Pelletier等[5]研究结论相似。饮食控制是控制高磷血症的首要措施,本透析中心缺乏专业营养师,提供的饮食建议仅限于宣教限制食用的高磷食物种类。宁波地处我国东部沿海,多数患者有食用海鲜的习惯,食物中含磷量明显高于内陆及北方。即使按每周3次血液透析清除血磷总量2400mg计算,仍远远小于患者磷每周5 600~9 600 mg摄入量。本中心透析频率为每周3次患者平均血磷水平显著低于每周2次及以下患者,但血磷达标率差异无统计学意义(>0.05)。因此透析清除磷的效果还要进一步增加,尤其需要增加高通量血液透析在患者中的应用。另外本文显示患者透龄在37~60个月时,透龄越大血磷水平越高,达标率越低;而在60个月以上时患者平均血磷水平出现下降,达标率上升。这可能是随着透龄的延长,患者矿物质及骨代谢异常的并发症逐步显现,透龄在60个月以上患者重视高磷的危害,治疗上更趋向积极,如限磷饮食及应用磷结合剂等。
iPTH既是甲状旁腺功能指标,也反映维持性血透患者骨代谢状态,多项指南均采用血iPTH作为重要的评价指标。KDIGO工作组对透析患者的PTH建议水平应该维持在正常上限的2~9倍。这一点与2003年K/DOQI的结果(即PTH水平维持在正常上限的3~6倍)相比是一个很重要的改变。Floege等[6]发布的一项前瞻性研究显示钙磷及iPTH水平在K/DOQI指南达标范围内的患者死亡率较低。KDIGO研究显示iPTH在150~300pg/ml的范围内时并不总能预测潜在的骨组织学或骨折,尤其在单独使用该指标时更是如此。本文显示在iPTH在150~300 pg/ml与130 ~600 pg/ml范围时,患者除了血钙差异有统计学意义外,患者血磷、钙磷乘积及碱性磷酸酶等水平差异均无统计学意义(均>0.05)。
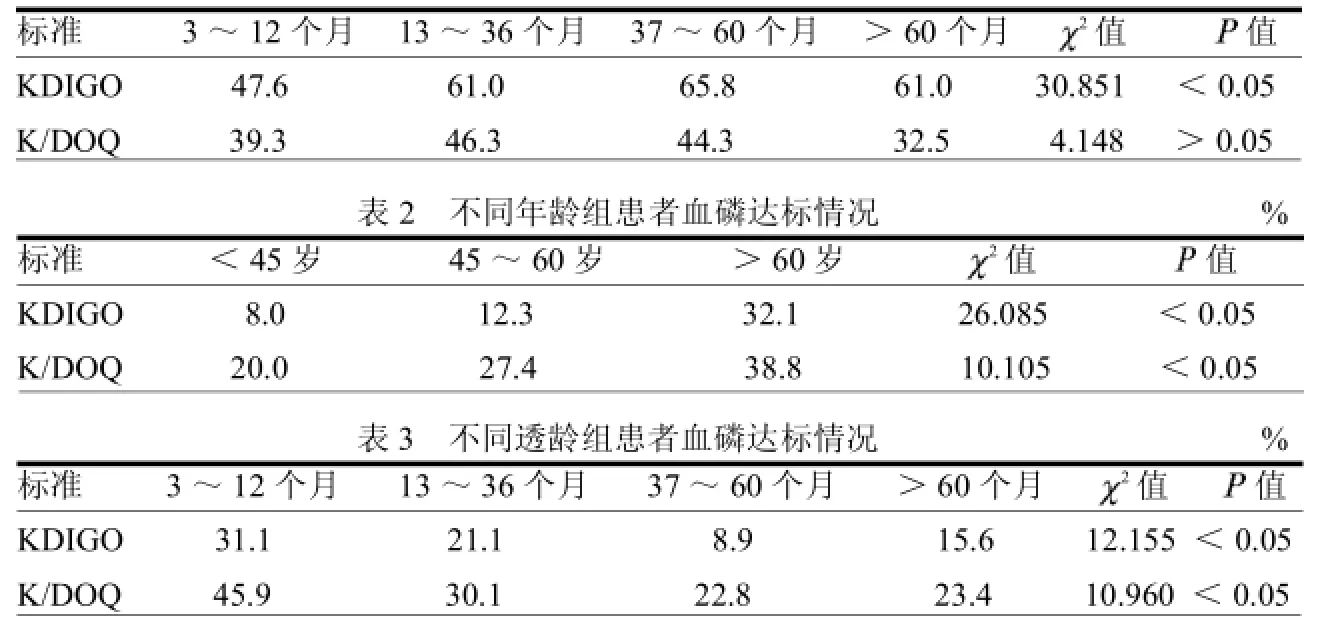
表1 不同透龄组患者血钙达标情况%
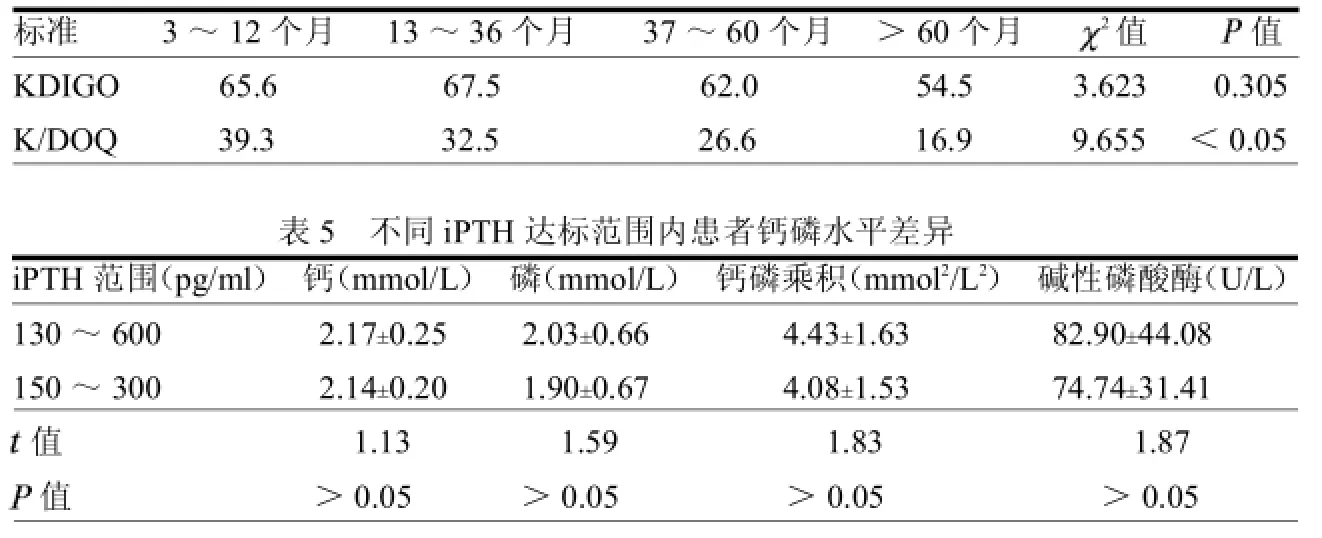
表4 不同透龄组患者iPTH水平达标情况%
[1]Slinin Y,Foley RN,Collins AJ.Calcium,phosphorus,parathyroid hormone,and cardiovascular disease in hemodialysis patients:theUSRDSwaves1,3and4study[J]. J AmSocNephrol,2005,16(6):1788-1793.
[2]KDIGO Clinical Practice Guideline for the Diagnosis,Evaluation,Prevention,and Treatment of Chronic Kidney Disease-Mineral and Bone Disorder(CKDMBD)[J].Kidney Int,2009,76(Suppl 113): S1-S130.
[3]K/DOQI clinical practice guidelines for bone metabolism and disease in chronic kidneydisease[J].Am J Kidney Dis,2003,
42(4 Suppl 3):S1-201.
[4]KongX,Zhang L,Zhang L,et al.Mineral and bone disorder in Chinese dialysis patients:a multicenter study[J].BMC Nephrol,2012,13(9):116.
[5]Pelletier S,Roth H,Bouchet JL,et al. Mineral and bone disease pattern in elderly haemodialysispatients[J].NephrolDial Transplant,2010,25(9):3062-3070.
[6]Floege J,Kim J,Ireland E,et al.Serum iPTH,calcium andphosphate,andthe risk of mortality in a European haemodialysis population[J].Nephrol Dial Transplant,2011,26(6):1948-1955.
10.3969/j.issn.1671-0800.2016.04.007
R459.5;R589
A
1671-0800(2016)04-0434-03
2015-10-10
(本文编辑:孙海儿)
315100宁波,宁波市泌尿肾病医院
欧阳凌霞,Email:oylx122@ aliyun.com

