传统锦州虾酱中产蛋白酶嗜盐菌的分离与鉴定
吕欣然,李 莹,马欢欢,缪璐欢,杜静芳,白凤翎,季广仁,励建荣
(1.渤海大学食品科学研究院,辽宁省食品安全重点实验室,生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013;2.锦州笔架山食品有限公司,辽宁锦州 121007)
传统锦州虾酱中产蛋白酶嗜盐菌的分离与鉴定
吕欣然,李莹,马欢欢,缪璐欢,杜静芳,白凤翎*,季广仁,励建荣
(1.渤海大学食品科学研究院,辽宁省食品安全重点实验室,生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013;2.锦州笔架山食品有限公司,辽宁锦州 121007)
目的:从传统锦州虾酱中分离产蛋白酶嗜盐菌,并对其进行鉴定。方法:应用1.0%脱脂乳Gibbons培养基分离产蛋白酶嗜盐菌,经形态学、生理生化和分子生物学对其鉴定。采用SDS-PAGE分析虾酱中可溶性蛋白的变化。结果:获得16株产蛋白酶嗜盐菌,菌株CW0-1、CW0-2、CW0-3和 CW0-4是弧菌属,菌株CW1-1、CW2-1和CW2-2是尼泊尔葡萄球菌,菌株CW2-3、CW5-1、CW5-2、CW5-3是马胃葡萄球菌,菌株CW3-1、CW3-2、CW4-1、CW4-2是枝芽孢杆菌,菌株CW4-3是独岛枝芽孢杆菌。弧菌属主要存在于原料虾中,嗜盐性葡萄球菌出现在发酵2个月和5个月,枝芽孢杆菌出现在发酵3~4个月。葡萄球菌和枝芽孢杆菌呈现交替演变,是虾酱发酵前期的优势产蛋白酶嗜盐菌。虾酱中的总可溶性蛋白随着发酵时间的延长逐渐下降。结论:葡萄球菌和枝芽孢杆菌是发酵前期虾酱中的优势产蛋白酶嗜盐菌,也是降解蛋白的主体微生物类群。
传统锦州虾酱,产蛋白酶嗜盐菌,发酵前期,分离与鉴定
传统锦州虾酱是以新鲜渤海出产的乌虾和白虾为原料,添加20%~30%高浓度的食盐,在自然条件下经1至2年长时间的发酵而成的地方海产调味品。嗜盐菌(halophilic bacteria)是一类生活在高盐度环境中的微生物,主要生长在盐湖、盐碱地、海水及腌制食品等高盐环境[1]。嗜盐菌中既包括芽孢杆菌属(Bacillus)、微球菌属(Micrococcus)、葡萄球菌属(Staphylococcus)、链球菌属(Streptococcus)、片球菌属(Pediococcus)中极度耐盐的细菌类群,还包括含有细菌视紫红质光合色素的红色极端嗜盐古细菌(extremely halophilic red archaea)和嗜盐乳酸菌(halophilic lactic acid bacteria)[2]。依据嗜盐浓度的不同,嗜盐菌可分为轻度嗜盐菌,盐浓度为0.2~0.5 mol/L;中度嗜盐菌盐浓度为0.5~2.0 mol/L;极端嗜盐菌盐浓度为大于3.0 mol/L[3]。嗜盐菌的发酵作用主要表现在海产调味品的发酵前期[4],在发酵前期一些菌群可产生蛋白酶降解虾体蛋白形成氨基酸等小分子代谢产物,赋予虾酱以特殊的风味和品质。黄紫燕等[5]从发酵半年的鱼露中分离获得一株嗜盐产蛋白酶乳酸菌T1,通过形态学初步鉴定菌株T1乳酸菌为芽孢杆菌属。来自海洋的产蛋白酶嗜盐菌主要包括芽孢杆菌、葡萄球菌和微球菌,其中芽孢杆菌是普遍关注的微生物类群,夏伟等[6]从海洋环境中分离获得一株产蛋白酶的海洋菌ZR-PW,通过形态学、生理生化和16S rRNA鉴定其为地衣芽孢杆菌,因其分解蛋白能力强,可应用于食品、酿造、医药和纺织等工业领域。Karbalaei-Heidari等[7]从伊朗各区域分离获得几株中度嗜盐菌,筛选出一株产蛋白酶的中度嗜盐菌盐湖菌属(Salinivibrio sp.)AF-2004。本文应用1.0%脱脂乳Gibbons培养基从发酵前期的传统锦州虾酱分离产蛋白酶嗜盐菌,通过形态学、生理生化和分子生物学方法对菌株进行鉴定,并利用SDS-PAGE技术对不同发酵时间虾酱中蛋白降解的过程进行分析,探究产蛋白酶菌株和虾酱蛋白演变的相关特征,为利用产蛋白酶嗜盐菌提升虾酱发酵进程奠定一定的基础。
1 材料与方法
1.1材料与仪器
虾酱样品自2014年4月25日原料投放第一天,每隔30 d从锦州笔架山食品有限公司进行采样。样品分别采自5个缸距离表面30 cm的中间部分,垂直采取200 g。采集后的样品保存于带盖玻璃瓶中,4℃冷藏。共采集5个月,样品按发酵时间记为0、1、2、3、4、5。分析前采用四等缩分法至25.0 g,备用。
SPX-250生化培养箱宁波海曙赛福实验仪器厂;GI54DWS立式压力蒸汽灭菌锅致微仪器有限公司;DL-CJ-2N超级洁净工作台北京东联哈尔仪器制造;BMM-480YS生物显微镜上海绘统光学仪器有限公司;PCR仪德国Eppendorf公司;PHSJ-3F pH计上海仪电科学仪器股份有限公司;Quantity one凝胶成像系统美国Bio-Rad公司;IKA Vortex GENIUS 3振荡器德国IKA公司;5804R高速冷冻离心机德国Eppendorf公司;移液器,德国Eppendorf公司。
Gibbons培养基:胰蛋白胨5.0 g,酵母粉10.0 g,柠檬酸钠3.0 g,氯化钾2.0 g,MgSO4·7H2O 20.0 g,氯化钠50.0 g,添加1000 mL蒸馏水,调pH7.2,121℃灭菌20 min;固体培养基需添加1.5%的琼脂粉。生化鉴定管杭州天和微生物试剂有限公司;细菌基因组DNA快速抽提试剂盒、DNA marker-D、Taq PCR Master mix上海生工生物工程有限公司;其他化学试剂北京奥博星生物技术有限公司。
1.2实验方法
1.2.1产蛋白酶嗜盐菌的富集及初步筛选取25.0 g虾酱样品置于225 mL灭菌水中振荡5 min,静置,取上层清液200 μL接种于10.0 mL Gibbons液体培养基中进行富集。取适量富集培养液接种于含1.0%脱脂乳的Gibbons固体培养基,30℃培养24~48 h。选取菌落周围产生透明水解圈即产蛋白酶嗜盐菌的菌落分离纯化。
1.2.2形态学分析将分离的产蛋白酶嗜盐菌单菌落划线接种于Gibbons固体培养基进行纯化,30℃培养48 h,挑取单个菌落进行革兰氏染色,镜检。
1.2.3生理生化鉴定参照《常见细菌系统鉴定手册》[8]和《伯杰氏细菌鉴定手册》[9]进行生理生化实验,包括半乳糖、蔗糖、乳糖、麦芽糖、葡萄糖、果糖、山梨醇和甘露醇等发酵糖醇实验,过氧化氢酶实验以及硫化氢实验。
1.2.4分子生物学鉴定菌株DNA采用细菌基因组试剂盒提取。PCR扩增引物为:27f:5′-AGAGTTT GATCCTGGCTCAG-3′,1492r:5′-TACGGYTACC TTTGTTACGACTT-3′。PCR扩增反应体系(25 μL):上下游引物各1.0 μL,DNA模板1.0 μL,Taq PCR Master mix 12.5 μL,ddH2O 9.5 μL。PCR扩增反应程序:94℃ 2 min,94℃ 1 min,60℃ 1 min,72℃ 90 s,循环30次,4℃保温。PCR纯化产物经1%琼脂糖凝胶电泳分析后送上海生工生物工程股份有限公司测序。测得序列登陆GenBank进行BLAST同源性比较,应用MEGA 5.0软件构建系统发育进化树。
1.2.5虾酱发酵液中总蛋白的提取和测定称取10.0 g虾酱样品置于50 mL离心管,加入30.0 mL超纯水,均匀混合后,11000 r/min离心15 min,取上层清液备用。
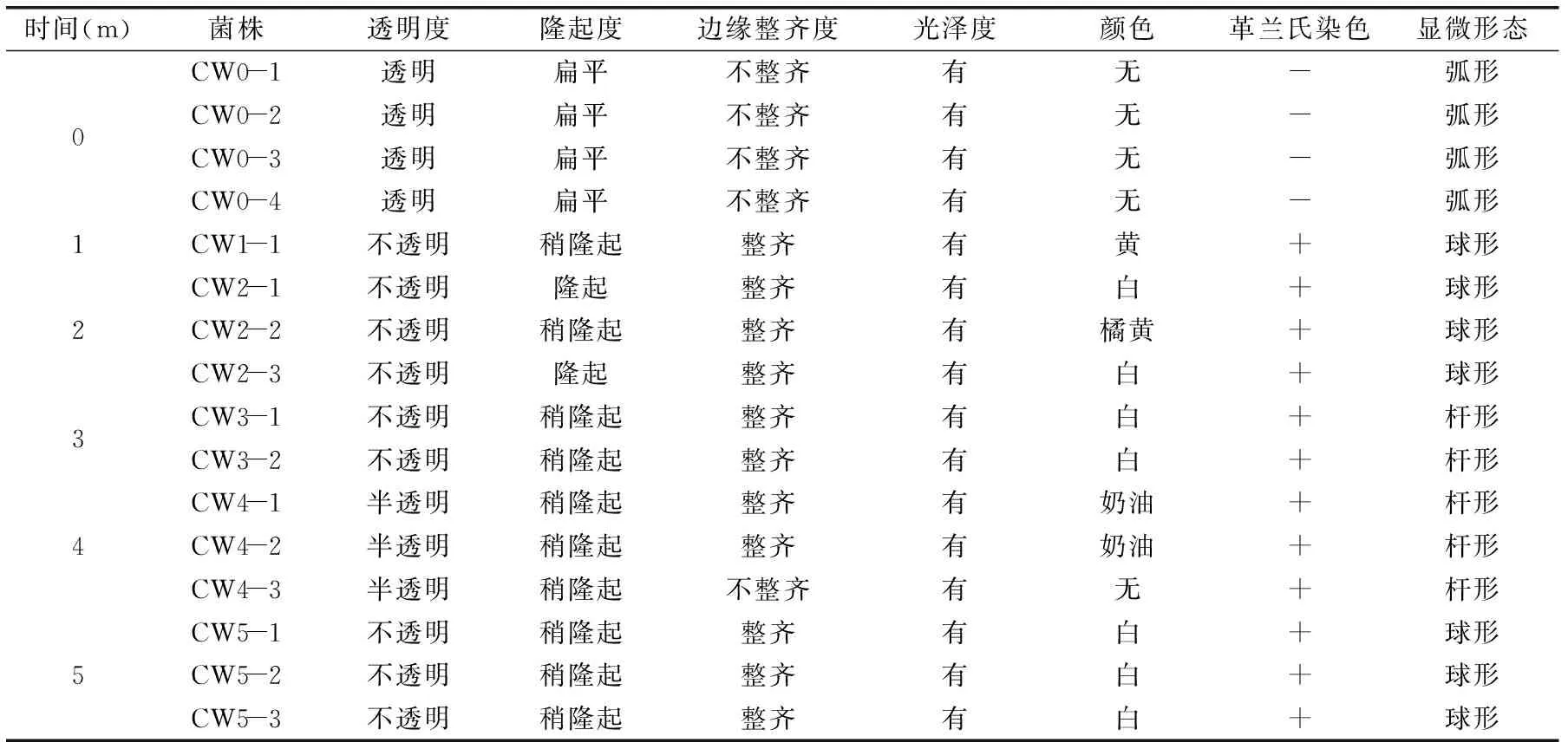
表1 虾酱中产蛋白酶嗜盐菌的形态学特征
取10 μL样品溶液加入适量的缓冲液将样品浓度调整为1.0 mg/mL,煮沸3 min。按参考文献[10]进行SDS-PAGE凝胶电泳,分离胶10%,浓缩胶5%,上样量10 μL,浓缩胶过程电压恒定为80 V,分离胶过程电压恒定为120 V。至溴酚蓝指示剂抵达胶片底部边沿时停止电泳。
电泳结束后将胶片转移至染色盒中,加入适量含0.1%考马斯亮蓝染色液(V异丙醇∶V冰醋酸∶V超纯水=25∶10∶65),在摇床上染色约1 h。倒掉染色液,加入适量脱色液(V冰醋酸∶V乙醇∶V超纯水=10∶5∶85),摇床上脱色,直至条带清晰无底色。采用Quantity One系统拍照。
2 结果与讨论
2.1产蛋白酶菌株的筛选
从1.0%脱脂乳的Gibbons固体培养基分离获得16株产蛋白酶嗜盐菌,图1是发酵3个月时分离的菌株CW3-1(左)和发酵4个月的菌株CW4-3(右)分解酪蛋白形成的透明圈,从图中可以看出两菌株产生的蛋白酶降解酪蛋白的比较明显。
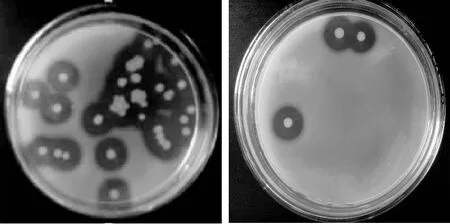
图1 虾酱中产蛋白酶嗜盐菌在脱脂乳平板上的菌落透明圈Fig.1 The transparent circles on skim-milk culture of protease-producing halophilic bacteria in shrimp paste
2.2产蛋白酶菌株形态特征和生理生化鉴定
2.2.1产蛋白酶菌株的形态特征对16株产蛋白酶菌株的形态学进行分析,从表1可以看出16株嗜盐菌可分为3种类型,即发酵开始时分离的4株革兰氏阴性弧菌CW0-1、CW0-2、CW0-3和CW0-4,发酵1、2、5个月分离的7株革兰氏阳性球菌CW1-1、CW2-1、CW2-2、CW2-3、CW5-1、CW5-2和CW5-3,发酵3、4个月分离的5株革兰氏阳性杆菌CW3-1、CW3-2、CW4-1、CW4-2和CW4-3。从菌落形态上看,革兰氏阴性弧菌呈扁平,表面光滑,光泽,透明,不产生色素;发酵前期的革兰氏阳性球菌菌落呈圆形,隆起,表面光滑湿润,不透明,多呈白色,少量的CW1-1及CW2-1菌株产生黄色和橙黄色色素;革兰氏阳性杆菌的菌落呈圆形,稍隆起,表面光滑有光泽,菌落的透明度、颜色都有所差异。
通过对1、2、3、4个月的4株嗜盐菌进行革兰氏染色,结果从图2中可以看出,发酵1个月的菌株CW1-1和2个月的菌株CW2-1的显微形态均为球形,前者呈单或双排列,后者呈葡萄状排列,CW1-1明显大于CW2-1;发酵3个月的菌株CW3-1和发酵4个月的菌株CW4-3皆呈杆状,多以成对出现,CW4-3的个体明显大于CW3-1。
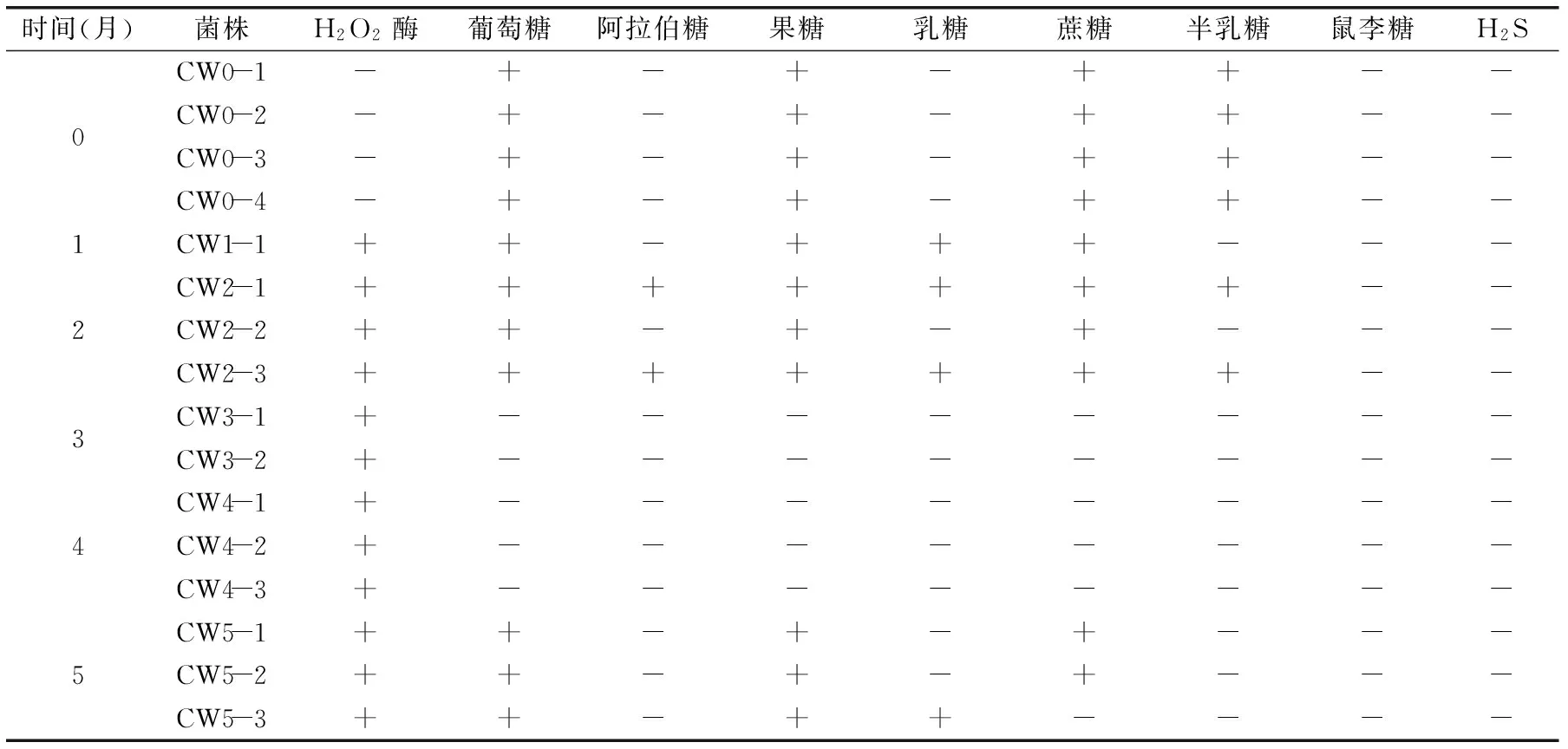
表2 虾酱中产蛋白酶嗜盐菌的生理生化鉴定结果

图2 产蛋白酶嗜盐菌菌株的显微形态(1000×)Fig.2 The micro-morphology of protease-producing halophilic bacteria strain in shrimp paste(1000×)注:A为菌株CW1-1;B为菌株CW2-1;C为菌株CW3-1;D为菌株CW4-3。
注:“-”表示阴性,“+” 表示阳性。
2.2.2产蛋白酶菌株的生理生化鉴定依据《常见细菌系统鉴定手册》和《伯杰氏细菌鉴定手册》对发酵0至5个月的16株嗜盐菌进行生理生化鉴定,结果如表2所示。由表2可知,初始虾酱样品中分离得到的4株革兰氏阴性弧菌CW0-1、CW0-2、CW0-3和CW0-4可以分解葡萄糖、果糖、蔗糖和半乳糖等糖类产酸,过氧化氢酶和产H2S实验均为阴性,初步判断这4株菌为弧菌属。7株革兰氏阳性球菌CW1-1、CW2-1、CW2-2、CW2-3、CW5-1、CW5-2和CW5-3能分解葡萄糖、果糖、蔗糖等糖类产酸,过氧化氢酶实验均为阳性,产H2S实验均为阴性,初步判断这7株菌为葡萄球菌属。5株革兰氏阳性杆菌CW3-1、CW3-2、CW4-1、CW4-2和CW4-3均不能发酵碳水化合物产酸,过氧化氢酶实验结果均为阳性,产H2S实验均为阴性,初步判断这5株菌为芽孢杆菌属。
2.2.3产蛋白酶菌株的分子生物学鉴定结果将产蛋白酶菌株的DNA提取后,经PCR扩增后的16S rRNA电泳图如图3所示,从图中可以看到16株在1500 bp处出现特异性亮带,表明目标片段被成功扩增。扩增产物送至生工生物工程(上海)股份有限公司测序,将菌株测序结果与NCBI数据库中已知序列进行BLAST比对,采用MEGA5.0软件建立系统发育树。结果见图4。

图3 虾酱中产蛋白酶嗜盐菌的PCR琼脂糖电泳图Fig.3 Agarose gel electrophoresis of PCR of protease-producing halophilic bacteria in shrimp paste注:1:菌株CW0-1;2:菌株CW0-2;3:菌株CW0-3;4:菌株CW0-4;5:菌株CW1-1;6:菌株CW2-1;7:菌株CW2-2;8:菌株CW2-3;9:菌株CW3-1;10:菌株CW3-2;11:菌株CW4-1;12:菌株CW4-2;13:菌株CW4-3;14:菌株CW5-1;15:菌株CW5-2;16:菌株CW5-3;M:maker。
图4是产蛋白酶嗜盐菌的系统发育树,由图可知,在初始虾酱样品中分离得到的4株产蛋白酶菌CW0-1、CW0-2、CW0-3和CW0-4,可初步判断属于弧菌属,弧菌广泛分布于水产品,是原料生存环境中存在的或原料自身携带的一类产蛋白酶菌。在1~5个月的发酵过程中,嗜盐性葡萄球菌和枝芽孢杆菌是产蛋白酶的优势菌,嗜盐性葡萄球菌包括菌株CW1-1、CW2-1、CW2-2、CW2-3、CW5-1、CW5-2、CW5-3,菌株CW1-1、CW2-1 和CW2-2与尼泊尔葡萄球菌(Staphylococcus nepalensis)F4同源性较近,可初步判定这4株菌是尼泊尔葡萄球菌,菌株CW2-3、CW5-1、CW5-2、CW5-3与马胃葡萄球菌(Staphylococcus equorum)Y15同源性较近,可初步判定菌株这4株菌是马胃葡萄球菌。枝芽孢杆菌包括菌株CW3-1、CW3-2、CW4-1、CW4-2和CW4-3,菌株CW3-1、CW3-2、CW4-1、CW4-2与枝芽孢杆菌(Virgibacillus sp.)SK37和KK-B1同源性较近,可初步判定这4株为枝芽孢杆菌,菌株CW4-3与独岛枝芽孢杆菌(Virgibacillus dokdonensis)JAN-2同源性较近,可初步判定其为独岛枝芽孢杆菌。
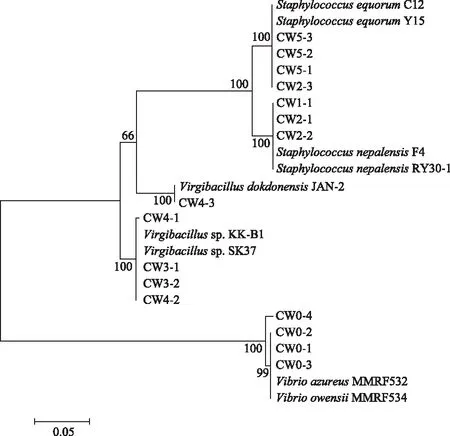
图4 虾酱中产蛋白酶嗜盐菌的系统发育树Fig.4 Phylogenetic tree of protease-producing halophilic bacteria in shrimp paste
2.3虾酱总可溶性蛋白的变化
虾酱发酵过程中蛋白质主要通过体系内微生物和酶的相互作用,使其降解为肽类、氨基酸和氨基态氮等小分子风味前体物质[11]。Udomsil等研究泰国鱼酱中4株嗜盐四联球菌M11、MS33、MRC5-5-2和MRC10-7-8在高盐浓度下对鱼肉蛋白的分解活性,研究表明4株四联球菌使蛋白分解形成风味物质的前体物质寡肽和低聚肽[12]。
图5是虾酱发酵前期的总可溶性蛋白的变化,由图可知,虾酱中总可溶性蛋白的条带主要分布在29.0~97.2 ku区间。前1个月,66.4~97.2 ku区间的大分子的蛋白质光密度较强,含量较高,随着发酵时间的延长其光密度逐渐减弱,到3个月时基本分解完全,表明大分子蛋白质可能是被芽孢杆菌和葡萄球菌产生的蛋白酶分解,使得含量逐渐降低[13]。前3个月,略小于66.4 ku的蛋白质分子的光密度有微量增加,可能是由于大分子蛋白质被降解转化成较小的蛋白质分子,3个月后,其光密度减弱,说明蛋白质在优势微生物枝芽孢杆菌和葡萄球菌的作用下逐渐被分解。前3个月,29.0 ku的蛋白质分子的含量逐渐上升,上升是由于大分子蛋白的降解形成小分子蛋白质,3个月后,29.0 ku的蛋白质分子的含量逐渐下降,下降是在活性较强的产蛋白酶的嗜盐性枝芽孢杆菌和葡萄球菌分解成更小的多肽和氨基酸[14]。总体来看,虾酱中的总可溶性蛋白随着发酵时间的延长逐渐被微生物降解,表明产蛋白酶的嗜盐性葡萄球菌和枝芽孢杆菌是导致产品中蛋白降解的主体微生物类群。
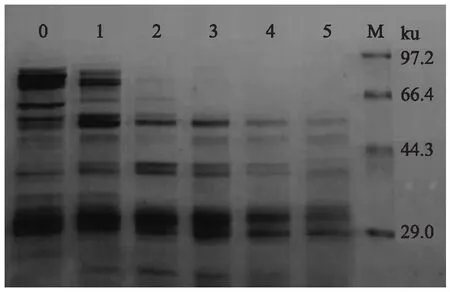
图5 虾酱发酵前期总可溶性蛋白的变化Fig.5 Change of total soluble protein extracted from shrimp paste in the fermentation prophase注:发酵时间0:0个月;1:1个月;2:2个月; 3:3个月;4:4个月;5:5个月;M:maker。
3 结论
应用1.0%脱脂乳Gibbons培养基从的传统锦州虾酱发酵前期样品中共分离获得16株产蛋白酶嗜盐菌,菌株CW0-1、CW0-2、CW0-3和CW0-4是弧菌属;菌株CW1-1、CW2-1和CW2-2是尼泊尔葡萄球菌;菌株CW2-3、CW5-1、CW5-2、CW5-3是马胃葡萄球菌;菌株CW4-3是独岛枝芽孢杆菌;菌株CW3-1、CW3-2、CW4-1、CW4-2是枝芽孢杆菌。弧菌属主要存在于原料虾中,嗜盐性葡萄球菌出现在发酵2个月和5个月虾酱,枝芽孢杆菌出现在发酵3~4个月。葡萄球菌和枝芽孢杆菌呈现交替演变,是虾酱发酵前期的优势产蛋白酶嗜盐菌。虾酱中的总可溶性蛋白随着发酵时间的延长逐渐降解,表明产蛋白酶嗜盐性葡萄球菌和枝芽孢杆菌是导致产品中蛋白降解的主体微生物类群。通过虾酱中产蛋白酶嗜盐菌菌株的分离鉴定及其对产品蛋白分解过程的分析,对探究产品品质形成具有潜在的研究价值。
[1]刘会强,张立丰,韩彬,等.嗜盐菌的研究新进展[J].新疆师范大学学报,2005,24(3):84-88.
[2]赵百锁,杨礼富,宋蕾,等.中度嗜盐菌在生物技术中的应用[J].微生物学通报,2007,34(2):359-362.
[3]Poli A,Esposito E,Orlando P,et al.Halomonas alkaliantarctica sp.nov.,isolated from saline lake Cape Russell in Antarctica,an alkalophilic moderately halophilic,exopolysaccharide-producing bacterium[J].Systematic and Applied Microbiology,2007,30(1):31-38.
[4]胡小喜,段彬,王香君,等.不同发酵温度下虾油中细菌的16S rDNA分子生态分析以及蛋白酶系和产品品质的变化研究[J].现代食品科技,2015,http://www.cnki.net/kcms/detail/44.1620.TS.20150811.1025.006.html.
[5]黄紫燕,刘春花,罗婷婷,等.鱼露发酵液中产蛋白酶乳酸菌的筛选及其添加应用[J].食品与发酵工业,2010,36(11):88-92.
[6]夏伟,闫志勇,朱绍辉,等.一株产蛋白酶海洋菌的筛选、鉴定及培养条件优化[J].中国农学通报,2012,28(20):154-158.
[7]Karbalaei-Heidari H R,Ziaee A A,Schaller J,et al.Purification and characterization of an extracellular haloalkaline protease produced by the moderately halophilic bacterium,Salinivibrio sp.strain AF-2004[J].Enzyme and Microbial Technology,2007,40(2):266-272.
[8]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001.
[9]布坎南,吉本斯.伯杰氏细菌鉴定手册(第八版)[M].北京:科学出版社,1984.
[10]Porzio M A,Pearson A M.Improved resolution of myofibrillar proteins with sodium dodecyl sulfate-polyacrylamide gel electrophoresis[J].Biochimica et Biophysica Acta(BBA)-Protein Structure,1977,490(1):27-34.
[11]Wang D,Zheng Z Y,Feng J,et al.A high salt tolerant neutral protease from Aspergillus Oryzae:Purification,characterization and kinetic properties[J].Applied Biochemistry and Microbiology,2013,49(4):378-385.
[12]Udomsil N,Rodtong S,Tanasupawat S,et al.Proteinase-producing halophilic lactic acid bacteria isolated from fish sauce fermentation and their ability to produce volatile compounds[J].International Journal of Food Microbiology,2010,141(3):186-194.
[13]Sun W,Zhou F,Sun D W,et al.Effect of oxidation on the emulsifying properties of myofibrillar proteins[J].Food and Bioprocess Technology,2013,6(7):1703-1712.
[14]Lin S,Zhang M,Liu J,et al.Construction and application of recombinant strain for the production of an alkaline protease from Bacillus licheniformis[J].Journal of Bioscience and Bioengineering,2015,119(3):284-288.
Isolation and identification of protease-producing halophilic bacteria in traditional Jinzhou shrimp paste
LV Xin-ran,LI Ying,MA Huan-huan,MIAO Lu-huan,DU Jing-fang, BAI Feng-ling*,JI Guang-ren,LI Jian-rong
(1.Research Institute of Food Science,Bohai University;Food Safety Key Lab of Liaoning Province; National & Local Joint Engineering Research Center of Storage,Processing and Safety Control Technology for Fresh Agricultural and Aquatic Products,Jinzhou,121013,China; 2.Bijia mountain food co.,Ltd,Jinzhou,121007,China)
Objective:To isolate and identify protease-producing halophilic bacteria from the fermentation prophase of traditional Jinzhou shrimp paste.Methods:Protease-producing halophilic bacteria were isolated by 1.0% skimmed milk Gibbons test.These strains were identified by morphology,biochemical characteristics and molecular biology.Total soluble protein was analyzed using SDS-PAGE test.Results:16 strains protease-producing halophilic bacteria were obtained.Strain CW0-1,CW0-2,CW0-3 and CW0-4 were identified as Vibro sp.,strain CW1-1,CW2-1 and CW2-2 were identified as Staphylococcus nepalensis,strain CW2-3,CW5-1,CW5-2 and CW5-3 were identified as Staphylococcus equorum,strain CW3-1,CW3-2,CW4-1 and CW4-2 were identified as Virgibacillus sp.,strain CW4-3 was identified as Virgibacillus dokdonensis.The Vibro sp.mainly existed in raw shrimp,halophilic Staphylococcus sp.were observed in fermentation second month and fifth month,Virgibacillus sp.were observed in fermentation third month to fourth month.Staphylococcus sp.and Virgibacillus sp.presented alternate successions,which were the dominant protease-producing halophilic bacteria in the fermentation prophase of shrimp paste.Total soluble protein was gradually decreased with the extension of fermentation time.Conclusion:Staphylococcus sp.and Virgibacillus sp.were the dominant protease-producing halophilic bacteria in the fermentation prophase of shrimp paste,and were considered as the dominant bacteria of degradation protein.
traditional Jinzhou shrimp paste;protease-producing halophilic bacteria;fermentation prophase;isolation and identification
2015-08-07
吕欣然(1990-),女,硕士研究生,研究方向:食品质量与安全控制,E-mail:lvxinran1990@163.com。
白凤翎(1964-)男,博士,教授,研究方向:食品质量与安全控制和食品微生物学,E-mail:baifling@163.com。
“十二五”国家科技支撑计划课题(2012BAD29B06);辽宁省高等学校创新团队课题(LT2014024)。
TS201.3
A
1002-0306(2016)07-0121-06
10.13386/j.issn1002-0306.2016.07.016

