组蛋白去乙酰化酶抑制剂对胶质瘤细胞增殖及E2F1表达的影响
袁忠民 梁琳 唐晓梅
·基础研究论著·
组蛋白去乙酰化酶抑制剂对胶质瘤细胞增殖及E2F1表达的影响
袁忠民梁琳唐晓梅
目的探讨组蛋白去乙酰化酶抑制剂(HDACIs)对胶质瘤细胞增殖及E2F1表达的影响。方法体外培养胶质瘤细胞U251,用2个E2F1干扰质粒she2f1a和she2f1b转染细胞,空载体BS/U6为对照,噻唑蓝比色法及核染色法检测细胞增殖率;TSA处理U251细胞2 h、4 h、8 h,及多种HDACIs包括曲古菌素A(TSA)TSA、伏立诺他(SAHA)、M344、丁酸钠(NaBu)NaBu、丙戊酸(VPA)、苯甲酰胺(M344)处理细胞8 h,二甲基亚砜(DMSO)处理为对照,蛋白免疫印迹法检测E2F1表达;用TSA处理8、12、24 h,DMSO处理为对照,噻唑蓝比色法分析细胞增殖率;采用多种HDACIs(TSA,SAHA, NaBu, VPA,M344)处理细胞24 h,噻唑蓝比色法分析细胞增殖率。结果与BS/U6比较,2个E2F1干扰质粒she2f1a和she2f1b都能沉默E2F1表达和抑制细胞增殖(P<0.05);与对照组比较,TSA处理细胞2 h和4 h未见抑制E2F1表达,处理8 h能抑制E2F1表达,其它HDACIs均能抑制E2F1表达;与对照组相比,TSA处理8 h未影响细胞增殖率(P>0.05),但TSA处理12 h能抑制细胞增殖(P<0.05),处理24 h抑制效应更强(P<0.05)。而且,其它HDACIs均能抑制细胞增殖(P<0.05)。 结论HDACIs能抑制胶质瘤细胞E2F1表达及其介导的细胞增殖。
神经胶质瘤;E2F1;组蛋白去乙酰化酶抑制剂
神经胶质瘤是中枢神经系统最常见的原发性肿瘤,恶性增殖是其主要特点之一,亦是造成高复发率的首要原因[1]。基于分子生物学和遗传学的研究表明,在高级别(WHO分级为Ⅲ和Ⅳ级)的胶质瘤样本中,调控细胞周期的关键蛋白的表达和功能出现明显异常[2]。如约25%的肿瘤样本中发现抑癌基因Rb缺失,约15%的样本中发现细胞周期素依赖性蛋白激酶 (CDKs)家族成员CDK4或CDK6活性异常增强,而抑癌基因p16在多达50%~70%的样本中缺失等[3-4]。这些信号的异常使得下游E2F蛋白家族(共有8个成员,E2F1~8)中关键分子转录因子E2F1的活性失去控制,失控的E2F1驱动细胞持续分裂,恶性增殖[5]。本研究采用小分子干扰、噻唑蓝比色法、蛋白免疫印迹法、转染等技术,检测多种组蛋白去乙酰化酶抑制剂(HDACIs)包括曲古柳菌素(TSA)、伏立诺他(SAHA)、丁酸钠(NaBu)、丙戊酸(VPA)、苯甲酰胺(M344)能否靶向影响E2F1表达及其功能。
材料与方法
一、U251细胞培养
神经胶质瘤细胞株U251的培养参考已发表文章进行[6]。U251细胞购自中科院上海细胞库。培养基为高糖DMEM(美国Invitrogen公司)加10%胎牛血清(美国Hyclone公司)。
二、U251细胞转染
转染参照Thermo公司的说明书,当U251细胞生长至融合度70%以上时,用Turbofect Transfection Reagent分别将质粒BS/U6、she2f1a、she2f1b转染到U251细胞内,于37℃恒温箱培养48 h。转染细胞分为3组,转染BS/U6作为对照组,2个E2F1干扰质粒为she2f1a组和she2f1b组(24孔板,每孔0.5 μg)。质粒BS/U6、she2f1a,she2f1b的靶序列参照已发表文章设计[5]。
三、细胞加药处理
参考已发表文章进行[6]。用胰酶消化U251细胞,种入24孔板,当细胞生长至融合度为50%~60%时,将细胞分为对照组[二甲基亚砜(DMSO, Sigma)处理]和组蛋白去乙酰化酶抑制剂组(分别用TSA、M344、NaBu、VPA处理),分别处理8、12、24 h后进行噻唑蓝比色法分析或Hoechst 33258核染色后计数细胞数。
四、蛋白免疫印迹
参考已发表文章进行[7]。为了检测曲古菌素A处理U251细胞后对E2F1的抑制作用是否发生在抑制细胞增殖之前,我们用曲古菌素A处理U251细胞2 h、4 h、8 h,用细胞裂解液(50 mmol/L Tris pH 7.4、150 mmol/L NaCl、2 mmol/L EGTA、1 mmol/L EDTA、1% Triton X-100、2.5 mmol/L Sodium pyrophosphate、1 mmol/L Glycerophosphate、1 mmol/L Na3VO4、1 mmol/L PMSF、1 μg/ml Leupeptin、5 μg/ml Aprotinin)裂解细胞检测E2F1的表达。同时,用多种HDACIs如0.5 μmol/L TSA、6 mmol/L NaBu、6 mmol/L VPA、1 μmol/L SAHA、1 μmol/L M344处理U251细胞8 h后裂解细胞检测E2F1表达。用针对E2F1的小分子干扰质粒转染U251细胞48 h后裂解细胞,检测E2F1表达。采用4%集成胶和10%分离胶,200 V电压电泳45 min,100 V电压转膜60 min。脱脂奶粉(5%)室温封闭1 h。一抗(anti-E2F1 1∶1 000,anti-GAPDH 1∶5 000,所有抗体均购自美国Cell Signaling Technology公司)孵育过夜(4℃),辣根过氧化物酶(HRP)标记的二抗(美国Jackson Immuno Research公司)室温孵育1 h。增强化学发光后曝光。
五、噻唑蓝比色法(MTT)分析
参考已发表文章进行[7]。用胰酶消化U251细胞,种入96孔板,每个处理为6个平行孔。只加培养液不加细胞作空白对照。为防止MTT分析时有边缘效应,板周边的孔不加细胞。当U251细胞生长至融合度为50%~60%时,转染质粒BS/U6、she2f1a、she2f1b共48 h,每孔加入MTT溶液(5 g/L)20 μl培养4 h,弃培养液,然后每孔加入DMSO 150 μl,振荡10 min,选择490 nm波长,在酶联免疫检测仪上测定全部孔包括平行孔的吸光度A值。
六、统计学处理
结 果
一、沉默E2F1抑制U251细胞增殖
与对照相比,2个E2F1干扰质粒she2f1a和she2f1b均能抑制E2F1表达和细胞增殖(BS/U6: 增殖率=100%; she2f1a:增殖率=78±6,n=3,P=0.02;she2f1b:增殖率=83±5, n=3, P=0.03)(图1 A, B)。核染色后统计细胞数,与对照组比较,干扰E2F1组的细胞减少(BS/U6: 100%; she2f1a:增殖率=79±2, n=3,P=0.007;she2f1b:增殖率=77±6,n=3, P=0.01)(图1 C)。
二、HDACIs抑制U251细胞E2F1表达
与对照组比较,TSA处理细胞8 h能抑制U251细胞E2F1表达(图2 A)。而且,与TSA一样,NaBu、VPA、SAHA和M344均能抑制E2F1表达(图2 B)。
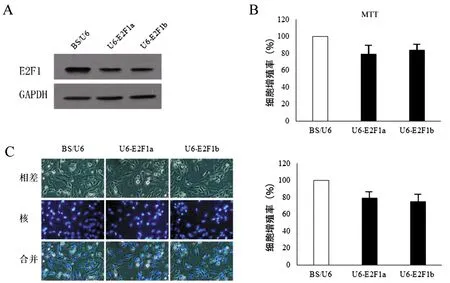
图1 沉默E2F1抑制U251细胞增殖
A:用BS/U6、she2f1a、she2f1b转染U251细胞48 h,蛋白免疫印迹法检查E2F1表达,GAPDH为标准化内参;B:BS/U6、she2f1a、she2f1b转染U251细胞48 h后MTT分析;C:BS/U6、she2f1a、she2f1b转染U251细胞48 h, Hoechst 33258染核后,荧光显微镜拍照(×200)
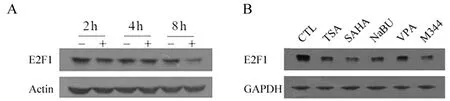
图2 HDACIss抑制U251细胞E2F1表达
A:0.5 μmol/L TSA处理U251细胞2 h、4 h和8 h,裂解细胞,蛋白免疫印迹法检测E2F1蛋白表达;B:用多种HDACIs包括0.5 μmol/L TSA、6 mmol/L NaBu、6 mmol/L VPA、1 μmol/L SAHA和1 μmol/L M344分别处理U251细胞12 h,DMSO作为溶剂对照(CTL),裂解细胞,蛋白免疫印迹法检测E2F1表达
三、HDACIs抑制U251细胞增殖
多组间比较差异有统计学意义(F=29.39,P=0.01)。与对照组比较,TSA处理细胞8 h不影响增殖率(P>0.05),但处理12 h抑制细胞增殖(P<0.05),处理24 h抑制效应更明显(P<0.05),见表1。
HDACIs包括NaBu、VPA、SAHA、M344处理U251细胞24 h均能抑制细胞增殖,各组与DMSO相比,差异均有统计学意义(P均<0.05),见表2。
讨 论
我们的研究显示,沉默E2F1抑制神经胶质瘤细胞株U251;TSA抑制E2F1表达发生在抑制细胞增殖之前;所使用的HDACIs均能抑制E2F1表达和肿瘤细胞增殖。笔者查阅文献发现,这是首次报道HDACIs能靶向抑制E2F1表达及其介导的胶质瘤细胞增殖。
表1 TSA处理细胞不同时间对U251细胞增殖的影响±s)
注:DMSO为对照组;增殖率=TSA处理组细胞数/DMSO组细胞数×100%(特定时间点)
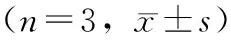
表2 HDACIs处理U251细胞24 h对细胞增殖的影响
注:aDMSO对照组与各个HDACIs处理组比较
E2F1是第一个被鉴定的具有转录活性的E2F家族成员,其活性受上游CDKs/Rb等分子精确调控,在调节细胞周期由G1期进入S期中发挥主导作用[8-9]。由于p16、Rb、p21等抑癌基因在高级别胶质瘤样本中发生高频缺失,E2F1对胶质瘤细胞增殖的作用在过去的研究中得到格外关注[10-11]。多家实验室包括我们均观察到利用小分子干扰RNA或反义核苷酸片段抑制E2F1表达抑制了胶质瘤细胞增殖。而且,多个微小RNA(miRNA)包括miRNA-329、miRNA-106a、miRNA-136、miRNA-138等均通过抑制E2F1表达抑制胶质瘤细胞增殖[12-15]。可见,在上游抑制信号缺失的情况下,E2F1的持续激活是造成胶质瘤细胞恶性增殖的关键原因之一,因而其是一个理想的分子靶点。
HDACIs的抗癌作用缘于其突出的促进肿瘤细胞凋亡或抑制细胞周期效应,而这些效应在正常细胞中的敏感性明显下降[16]。有文献报道HDACIs通过上调E2F1进而上调Bim等BH3-only蛋白促发线粒体依赖的细胞凋亡[17]。但在胶质瘤细胞株U251中,无论加大HDACIs浓度或是延长处理时间,我们都只检测到E2F1表达被抑制,而没有检测到E2F1被上调。可见,HDACIs抑制E2F1表达也是重要的抗癌机制之一。
总之,我们发现了HDACIs抑制E2F1表达进而抑制胶质瘤增殖的新机制。我们的研究一方面进一步支持了E2F1是治疗胶质瘤的理想靶点,另一方面提示HDACIs可能是的治疗胶质瘤的理想药物。未来我们的工作将进一步明确HDACIs调控E2F1表达的分子机制。
[1]陈正和,陈忠平. 脑胶质瘤的治疗进展. 新医学,2015,46(7):417-422.
[2]Lewis KM, Petritsch C. Asymmetric cell division: implication for glioma dvelopment and treatment. Transl Neurosi, 2013,4(4):484-503.
[3]Furnari FB, Fenton T, Bachoo RM, Mukasa A, Stommel JM, Stegh A, Hahn WC, Ligon KL, Louis DN, Brennan C, Chin L, DePinho RA, Cavenee WK. Malignant astrocytic glioma: genetics, biology, and paths to treatment. Gene Dev, 2007,21(21):2683-2710.
[4]Fischer M, Grossmann P, Padi M, DeCaprio JA. Integration of TP53, DREAM, MMB-FOXM1 and RB-E2F target gene analyses identifies cell cycle gene regulatory networks. Nucleic Acids Res, 2016 Jun 8. pii: gkw523. [Epub ahead of print].
[5]Johnson J, Thijssen B, McDermott U, Garnett M, Wessels LF, Bernards R. Targeting the RB-E2F pathway in breast cancer. Oncogene, 2016 Feb 29.[Epub ahead of print].
[6]袁忠民,曾敏灵,唐晓梅,伍燕娜,何国振. 组蛋白去乙酰化酶抑制剂对胶质瘤细胞增殖及MKK7表达的影响. 肿瘤防治研究, 2016, 43(1): 1-5.
[7]He W, Wu Y, Tang X, Xia Y, He G, Min Z, Li C, Xiong S, Shi Z, Lu Y, Yuan Z. HDAC inhibitors suppress c-Jun/Fra-1-mediated proliferation through transcriptionally downregulating MKK7 and Raf1 in neuroblastoma cell. Oncotarget,2016, 7(6):6727-6747,
[8]Udayakumar T, Shareef MM, Diaz DA, Ahmed MM, Pollack A. The E2F1/Rb and p53/MDM2 pathways in DNA repair and apoptosis: understanding the crosstalk to develop novel strategies for prostate cancer radiotherapy. Semin Radiat Oncol, 2010,20(4):258-266.
[9]Meng P, Ghosh R. Transcription addiction: can we garner the Yin and Yang functions of E2F1 for cancer therapy? Cell Death Dis, 2014,5:e1360.
[10]袁忠民,李明昌,杜汉强,陆永建. 肝癌缺失基因-1不同亚型在人神经胶质瘤组织中的表达及意义. 新医学,2010,41(2):98-10.
[11]Lladó V, López DJ, Ibarguren M, Alonso M, Soriano JB, Escribá PV, Busquets X Regulation of the cancer cell membrane lipid composition by NaCHOleate: effects on cell signaling and therapeutical relevance in glioma. Biochim Biophys Acta, 2014,1838(6):1619-1627.
[12]Xiao B, Tan L, He B, Liu Z, Xu R. MiRNA-329 targeting E2F1 inhibits cell proliferation in glioma cells. J Transl Me, 2013,11:172.
[13]Yang G, Zhang R, Chen X, Mu Y, Ai J, Shi C, Liu Y, Shi C, Sun L, Rainov NG, Li H, Yang B, Zhao S. MiR-106a inhibits glioma cell growth by targeting E2F1 independent of p53 status. J Mol Med, 2011,89(10):1037-1050.
[14]Chen W, Yang Y, Chen B, Lu P, Zhan L, Yu Q, Cao K, Li Q. MiR-136 targets E2F1 to reverse cisplatin chemosensitivity in glioma cells. J Neuro-Oncol, 2014,120(1):43-53.
[15]Qiu S, Huang D, Yin D, Li F, Li X, Kung HF, Peng Y. Suppression of tumorigenicity by microRNA-138 through inhibition of EZH2-CDK4/6-pRb-E2F1 signal loop in glioblastoma multiforme. Biochim Biophys Acta,2013,1832(10):1697-707.
[16]姚毅武, 姚和权, 蒋晟, 薛晓文. 组蛋白去乙酰化酶抑制剂抗肿瘤临床研究进展. 中国新药杂志, 2013,22(3):294-300.
[17]Gogada R, Yadav N, Liu J, Tang S, Zhang D, Schneider A, Seshadri A, Sun L, Aldaz CM, Tang DG, Chandra D. Bim, a proapoptotic protein, up-regulated via transcription factor E2F1-dependent mechanism, functions as a prosurvival molecule in cancer. J Biol Chem, 2013,288(1):368-381.
(本文编辑:洪悦民)
Effect of histone deacetylase inhibitor on the proliferation of glioma cells and expression of E2F1
Yuan Zhongmin,Liang Lin,Tang Xiaomei.
Department of Neurosurgery, the Second Affiliated Hospital of Guangzhou Medical University, Guangzhou 510260, China Corresponding author,Yuan Zhongmin,E-mail:yzm@gzhmu.edu.cn
ObjectiveTo investigate the proliferation effect of histone deacetylase inhibitors (HDACIs) on the proliferation of glioma cells and expression of E2F1. MethodsThe glioma cell line U251 were transfected with two plasmids of she2f1a or she2f1b, empty vector BS/U6 was regarded as a control, the cell proliferation rate was detected by tetrazoliumsalt (MTT) assays and nuclear staining method. U251 cells were treated with TSA for 2 h, 4 h and 8 h and treated with kinds of HDACIs including TAS, SAHA, M344, NaBu, VPA for 8 h. Dimethyl sulfoxide(DMSO) treatment was as control. Western blot was performed to test E2F1 expression. The glioma cell line U251 was treated with TSA for 8 h, 12 h and 24 h, DMSO treatment was regarded as control, and the cell proliferation rate was analyzed by MTT assays. U251 cells were treated with kinds of HDACIs including TSA, SAHA, M344, NaBu and VPA for 24 h, and then MTT assays were performed to determine cell proliferation rate. ResultsCompared with BS/U6, both she2f1a and she2f1b plasmids can silence E2F1 expression and inhibit cell proliferation (P<0.05). Compared with control, no significant inhibition of E2F1 expression was found in TSA treated cells at 2 h and 4 h, and the E2F1 expression was significantly inhibited at 8 h with TSA treatment, and the other HDACIs can significantly suppress E2F1 expression as well. MTT assays showed that TSA treatment 8 h samples did not remarkably affected cell proliferation rate (P>0.05), however, TSA treatment 12 h samples significantly inhibited cell proliferation. (P<0.05) and induced more suppression effects when lasting up to 24 h (P<0.05). Moreover, the other HDACIs can significantly inhibit cell proliferation (P<0.05). ConclusionHDACIs can suppress E2F1 expression of glioma cell and cell proliferation meditated by E2F1. Result
Glioma;E2F1;Histone deacetylase inhibitors

10.3969/j.issn.0253-9802.2016.08.003
广东省自然科学基金(2015A030313475);广州市科信局基金 (201510010180)
510260 广州,广州医科大学附属第二医院神经外科(袁忠民,唐晓梅);510515 广州,南方医科大学第一临床医学院(梁琳)
,袁忠民,E-mail: yzm@gzhmu.edu.cn
2016-05-25)

