Fe3O4/SiO2核壳结构复合纳米粒子的制备研究*
张慧勇
(洛阳理工学院材料科学与工程学院, 河南 洛阳 471023)
Fe3O4/SiO2核壳结构复合纳米粒子的制备研究*
张慧勇
(洛阳理工学院材料科学与工程学院, 河南洛阳471023)
首先通过共沉淀法、还原沉淀法和水热法制备Fe3O4纳米粒子,对其进行表面改性,防止粒子之间的团聚,然后采用溶胶-凝胶法,以Fe3O4纳米粒子为种子,在醇和水的混合体系中,碱性条件下催化正硅酸乙酯水解,生成物包覆在磁性纳米颗粒表面,制备小粒径核壳结构的二氧化硅磁性复合微球。利用X射线衍射仪对所制备的二氧化硅磁性复合微球的粒径和物相组成进行表征。实验结果表明二氧化硅磁性复合微球在室温下表现出良好的稳定性。
二氧化硅;四氧化三铁;纳米粒子;核壳结构;溶胶-凝胶
磁性纳米粒子以其独特的磁性能,在生物医学、信息技术领域具有广阔的应用前景,如磁流体、信息储存、固定化酶、核磁共振、靶向药物载体、核磁共振、免疫检测等生物医学领域有很大的应用潜力[1-2]。这些应用需要磁性粒子具有良好的化学稳定性、生物相容性和亲水性及良好的分散性[3-5],但是,磁性纳米粒子(如Fe、Co、Fe3O4、各种铁氧体化合物)具有比表面积大、比表面能高,由于尺寸效应、表面效应、磁偶极子引力等作用,磁性粒子易于发生团聚,降低了化学稳定性,并易于氧化,因此,很难直接应用。SiO2良好的生物相容性及抗分解能力的优点弥补了这一缺陷,Fe3O4是应用较多的无机磁性材料,用SiO2包覆Fe3O4制得的Fe3O4/SiO2在反复使用过程中,不易被氧化,磁性物质不易脱落,同时该物质还具有一定的生物相容性,对生物体不会造成严重的伤害。在Fe3O4表面包裹一层SiO2后,能大大地降低粒子的零电势点,从而屏蔽了磁偶极子的相互作用,使粒子具有良好的化学稳定性、生物相容性和分散性,加上SiO2表面存在大量的羟基,有利于复合粒子容易进一步的生物功能化[2, 6-8]。
本文通过共沉淀法、还原沉淀法和水热法制备出纳米级四氧化三铁磁性粒子,为了得到分散均匀的Fe3O4纳米粒子,采用柠檬酸钠对纳米粒子进行表面修饰,将正硅酸乙酯(TEOS)经水解形成溶胶,使溶质聚合凝胶化,再将凝胶干燥,最后得到核壳结构的二氧化硅复合粒子,并利用X射线衍射分析复合粒子的粒径和物相。对磁性纳米粒子的表面修饰可以有效的降低其表面能,增加粒子的抗氧化能力,获得的复合纳米粒子具有良好的分散性;而且适当的表面改性能够调节磁性纳米粒子与其他材料的相容性。通过SiO2的包被,可以屏蔽磁性粒子相互之间的偶极作用,避免粒子之间团聚现象的发生[7, 9-10],使其具有良好的稳定性、生物相容性和好的亲水性,为其在生物医学中的应用提供了重要保障。
1 实 验
1.1实验试剂
三氯化铁(FeCl3·6H2O,AR),中国·派尼化学试剂厂·郑州;硫酸亚铁(FeSO4·7H2O,AR),中国·派尼化学试剂厂·郑州;氨水(NH3·H2O,AR),洛阳市化学试剂厂;无水亚硫酸钠(NaSO3,AR),天津市德恩化学试剂有限公司;硫代硫酸钠(Na2S2O3,AR),天津市石英钟厂霸州市化工分厂;氢氧化钠(NaOH,AR),天津市联盟化工工贸有限公司;正硅酸乙酯(AR),天津市科密欧化学试剂有限公司;无水乙醇(AR),天津市凯通化学试剂有限公司;柠檬酸钠(AR),天津市德恩化学试剂有限公司。
1.2实验仪器
80-2离心机,常州市华普达教学仪器有限公司;CJJ78-1磁力加热搅拌器,金坛市大地自动化仪器厂;CS101-2EB真空干燥箱,湖南华德电子有限公司;AB204-S电子天平,常熟市佳衡天平仪器有限公司;DS5510DTH数控超声清洗器,合肥金尼克机械制造有限公司;HHS-1S电子恒温不锈钢水浴锅,上海市南阳仪器有限公司;高温反应釜(工作温度≤220 ℃),巩义市城区众合仪器供应站;D8 Focus X射线衍射仪,德国布鲁克公司。
1.3Fe3O4纳米粒子的制备
共沉淀法:称量3.929 g FeCl3·6H2O和2.6708 g FeSO4·7H2O(Fe3+:Fe2+=3:2),溶于盛有60 mL蒸馏水的三角瓶中,然后以6~8滴/分钟的速度向溶液中滴加浓氨水,将pH值调到10~11,置于磁力搅拌器上,用1000 r/min的速度加热搅拌30 min;接着,将三角瓶转移到70 ℃水浴中继续搅拌1 h;搅拌后,冷却到室温,用离心机将产物离心分离,并用去离子水和乙醇洗涤3~5次,将沉淀物放于烘干箱中,在60 ℃下真空干燥4 h,得到灰黑色Fe3O4纳米粒子。

水热法:称取2.7820 g FeSO4·7H2O和2.4785 g Na2S2O3溶于盛有28 mL蒸馏水的三角瓶中,置于磁力搅拌器上均匀搅拌;称取1.2 g NaOH,溶于盛有30 mL蒸馏水的三角瓶中,配制成1.0 mol/L的NaOH溶液;在不断搅拌下,向溶液中缓慢滴加NaOH溶液,调pH值至9~11,反应2 h后转移入高压釜中,置于烘箱中140 ℃反应5 h后取出,冷却至室温得到灰黑色沉淀;将产物离心分离,并用去离子水和乙醇洗涤3~5次,将沉淀在60 ℃下真空干燥4 h,得到灰黑色Fe3O4纳米粒子。
1.4Fe3O4纳米粒子表面改性及包被
采用柠檬酸钠对纳米粒子进行表面修饰,表面改性实验过程如下:称量柠檬酸钠7.4 g溶解于盛有50 mL蒸馏水的三角瓶中,浓度0.5 mol/L,均匀振荡;称取0.85 g Fe3O4粉末,超声分散在50 mL的柠檬酸钠溶液中,保持温度在60 ℃超声 4 h;反应完毕后,自然冷却到室温,将改性后的产物离心分离,加入适量乙醇絮凝,然后,重新分散在去离子水中,用于包被。
利用溶胶凝胶法对改性后的粒子进行包被,复合粒子Fe3O4/SiO2的制备过程如下:在三角瓶中配制60 mL的乙醇-水溶液(醇水比为5:1),将50 mL已改性分散的Fe3O4纳米粒子胶体与该乙醇-水溶液混合,置于磁力搅拌器上搅拌,搅拌速度为3000 r/min,30 min后加入2.8 mL的正硅酸乙酯,继续搅拌30 min;然后加入28 mL浓氨水,保证浓氨水与正硅酸乙酯的体积比为10:1,再搅拌2 h;最后,将产物离心分离,用无水乙醇和去离子水洗涤直至pH为7为止;将包被后的产物真空干燥过夜,即得到复合纳米粒子。
1.5样品的表征与测试
X射线衍射分析可给出材料物相组成和晶粒的尺寸等信息。测试条件为: 辐射源,Cu Kα射线;管电压,40 kV;管电流,30 mA;步长0.02°,扫描范围10°~70°。
2 结果与讨论
2.1共沉淀法制备Fe3O4纳米粒子及其包被
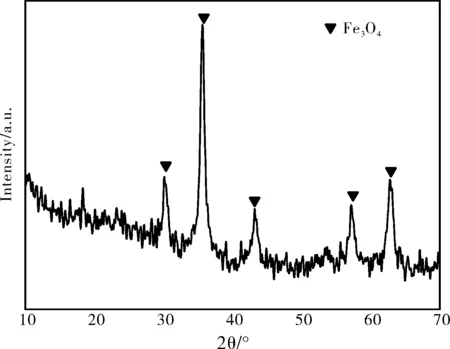
图1 共沉淀法制备Fe3O4纳米粒子包被后的XRD谱图
根据XRD表征结果,改性后粒子的表观粒子直径可以由Sherrer公式D=0.89λ/βcosθ(D为晶体粒子表观直径,λ为射线波长,β为衍射峰半高宽,θ为衍射角,0.89为比例常数),将λ=0.15406,β=0.615,θ=35.662/2,代入计算得到粒径D=24.36 nm。通过元素分析,与PDF卡片对比后发现,图形的最强峰和磁铁矿Fe3O4相吻合,通过物相分析,产物应为磁铁矿Fe3O4纳米粒子。在25°左右,没有出现明显的衍射峰。由此说明在合成Fe3O4/SiO2复合粒子时,只有少量或没有SiO2包被,原因可能有以下:(1)此方法得到的Fe3O4纳米粒子间可能存在非常严重的团聚现象,产品粒径分布范围较宽,影响了SiO2对其进行的包被;(2)这与条件控制有关,即Fe3O4纳米粒子改性的效果、包被过程中碱液的滴加速度和pH值测定的误差及最后对产物清洗程度等都可能有关。
2.2还原沉淀法制备Fe3O4纳米粒子及其包被
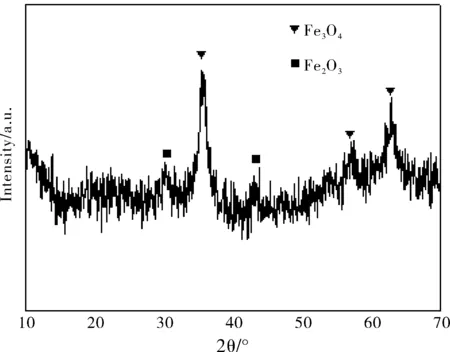
图2 还原沉淀法制备Fe3O4纳米粒子包被后的XRD谱图
根据XRD表征结果,将λ=0.15406,β=0.854,θ=35.642/2,代入由Sherrer公式D=0.89λ/βcosθ计算得到粒径D=17.83 nm。通过物相分析发现,含有大量的赤铁矿Fe2O3纳米粒子。而且由X射线衍射图谱可知,在30°以下,没有出现明显的衍射峰,即没有不定形SiO2的衍射峰出现。由于还原沉淀法的关键在于选择适当的还原剂,尽量少引入干扰离子,同时尽量减少副反应的发生。本实验用还原剂Na2SO3将1/3物质的量的Fe3+还原,保持Fe2+、Fe3+摩尔比为1:2,虽然密封条件下进行反应,但仍然避免不了反应容器中氧气的干扰,导致反应前Na2SO3发生部分被氧化和反应后制得的Fe3O4纳米粒子部分被氧化,比例的失衡导致赤铁矿Fe2O3纳米粒子的存在以及Fe3O4纳米粒子的团聚,影响了Fe3O4/SiO2复合纳米粒子的生成。
2.3水热法制备Fe3O4纳米粒子及其包被
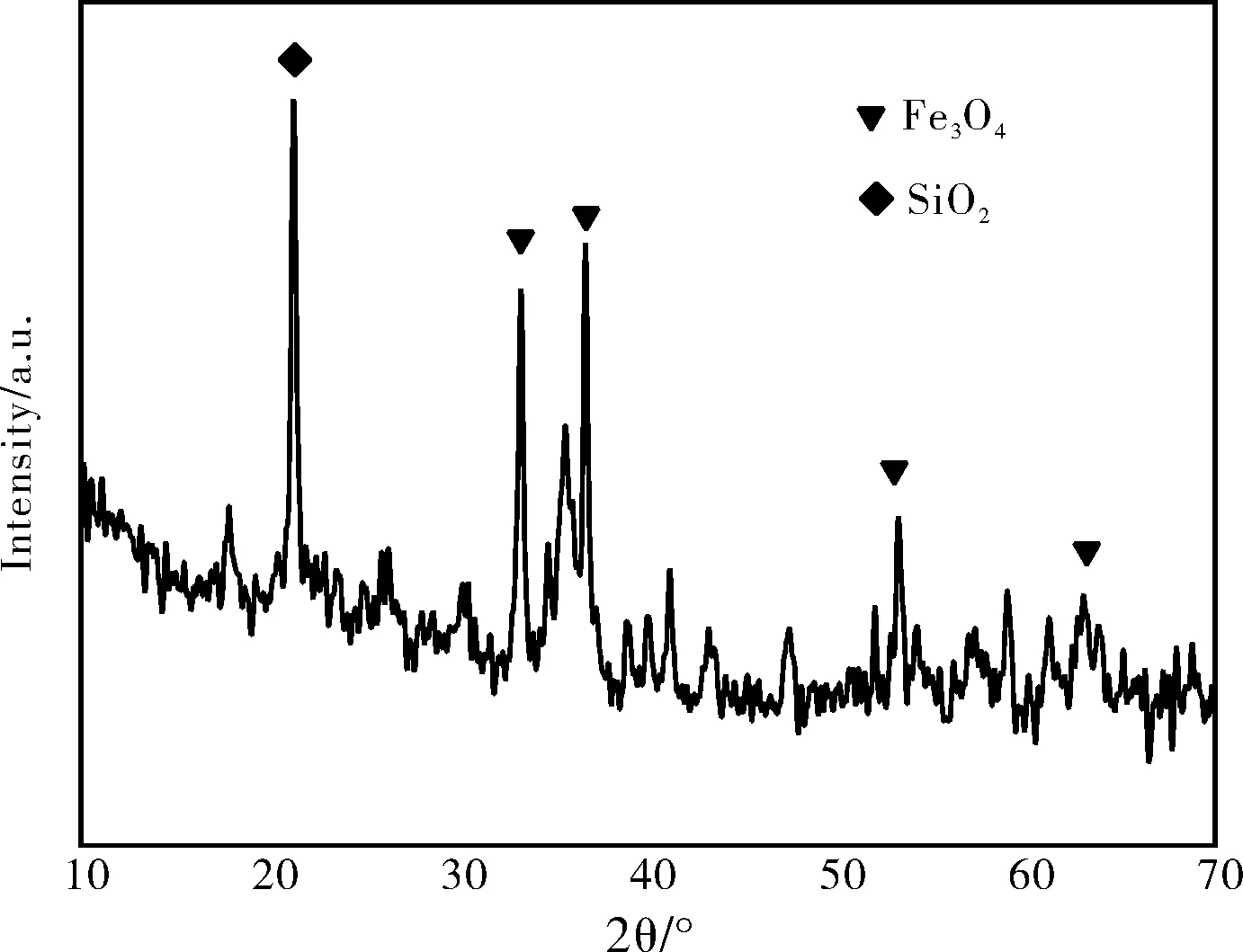
图3 水热法制备Fe3O4纳米粒子包被后的XRD谱图
根据XRD表征结果,将λ=0.15406,β=0.334,θ=36.700/2,代入Sherrer公式D=0.89λ/βcosθ计算得到粒径D=35.39 nm。从图3可以看出所得产物在21.244°处出现了一个衍射峰与文献中报道的无定型二氧化硅的衍射峰形相似[11],而且,由前面计算表明粒径明显增厚。上述结果表明在四氧化三铁纳米粒子的表面已经形成了二氧化硅包覆层,而Fe3O4纳米粒子的结构也几乎没有发生变化。实验表明:反应配比、反应温度和反应的pH值是制备的主要影响因素。水热法是在高温高压下进行的,故可以大大缩短反应时间;产物为晶态,无需晶化,可以避免发生团聚现象;而且反应过程中隔绝空气,减少了Fe3O4的氧化。
3 结 论
(1)本论文采用了共沉淀法、还原沉淀法和水热法合成Fe3O4粒子,制得粒径分别是24.36 nm、17.83 nm和35.39 nm。通过结果对比,共沉淀法制备的Fe3O4粒子最纯,但容易团聚
导致包被的效果不好;还原沉淀法制备的Fe3O4粒子粒径最小,但杂质过多;使用水热法制备Fe3O4粒子分散效果最佳,包被效果较好。原因是沉淀法和还原沉淀法制备条件非常苛刻,必须严格隔绝氧气,而实验过程中难免不遇到氧气,因此,合成产物容易团聚,而水热法制备时隔绝了空气,效果较好。
(2)通过溶胶凝胶法制备Fe3O4/SiO2核壳结构纳米粒子,操作简便,成本较低,易于规模化,包被后具有良好的稳定性。
[1]Jeon Y, Thangadurai D T, Piao L, et al. A facile one-step method to prepare size controlled Fe3O4submicro/nanoparticles[J]. Materials Letters, 2013, 96: 27-30.
[2]Sun L, Zhan L, Shi Y, et al. Microemulsion synthesis and electromagnetic wave absorption properties of monodispersed Fe3O4/polyaniline core-shell nanocomposites[J]. Synthetic Metals, 2014, 187: 102-107.
[3]段涛, 杨玉山,彭同江. 核壳型纳米复合材料的研究进展[J]. 材料导报, 2009, 23(2): 19-23.
[4]Ohulchanskyy T Y, Kopwitthaya A, Jeon M, et al. Phospholipid micelle-based magneto-plasmonic nanoformulation for magnetic field-directed, imaging-guided photo-induced cancer therapy[J]. Nanomedicine: Nanotechnology, Biology and Medicine, 2013, 9(8): 1192-1202.
[5]Qu J-B, Shao H-H, Jing G-L, et al. PEG-chitosan-coated iron oxide nanoparticles with high saturated magnetization as carriers of 10-hydroxycamptothecin: Preparation, characterization and cytotoxicity studies[J]. Colloids and Surfaces B: Biointerfaces, 2013, 102(0): 37-44.
[6]Ghaemy M,Naseri M. Synthesis of chitosan networks: Swelling, drug release, and magnetically assisted BSA separation using Fe3O4nanoparticles[J]. Carbohydrate Polymers, 2012, 90(3): 1265-1272.
[7]Jaber J,Mohsen E. Synthesis of Fe3O4@silica/poly(N-isopropylacrylamide) as a novel thermo-responsive system for controlled release of H3PMo12O40nano drug in AC magnetic field[J]. Colloids and Surfaces B: Biointerfaces, 2013, 102: 265-272.
[8]Jayarathne L, Ng W J, Bandara A, et al. Fabrication of succinic acid-Fe2O3nano core-shells[J]. Colloids and Surfaces A: Physicochem. Eng. Aspects, 2012, 403: 96-102.
[9]杨永林, 杨毅,程志鹏. 无机纳米粒子包覆研究进展[J]. 化工科技, 2006, 14(5): 28-32.
[10]庄叶凯,郑典模. 核壳型复合纳米粒子的研究现状及展望[J]. 江西化工, 2006, 8(1): 18-19.
[11]骆华锋. 二氧化硅包覆磁性纳米粒子的制备与表征[J]. 青岛科技大学学报(自然科学版), 2012, 33(3): 225-228.
Study on Preparation of Core-shell Fe3O4/SiO2Nanocomposite Particles*
ZHANGHui-yong
(School of Materials Science and Engineering, Luoyang Institute of Science and Technology, Henan Luoyang 471023, China)
Fe3O4nanoparticles were prepared by co-precipitation, reduction-precipitation and hydrothermal method, and then were modified to prevent the aggregation between particles. The Fe3O4nanoparticles were taken as seeds and the sol-gel method was carried out to prepare core-shell silica magnetic composite microspheres in the alcohol-water solution at room temperature by hydrolysising TEOS under alkaline condition. The particle size and phase composition of silica magnetic composite microspheres were characterized by X-ray diffraction. Experimental results showed that the magnetic composite microspheres had good stability at room temperature.
silica; iron oxide; nanoparticle; core-shell structure; sol-gel
国家自然科学基金(51302128);洛阳理工学院博士启动基金(No: 2011BZ02)。
张慧勇(1979-),女,讲师,主要从事纳米材料的教学与研究。
TQ139.2
A
1001-9677(2016)07-0052-03

