禽畜肉中金刚烷胺残留量测定的不确定度评定
尹丽丽
(上海天祥质量技术服务有限公司,上海 200233)
禽畜肉中金刚烷胺残留量测定的不确定度评定
尹丽丽
(上海天祥质量技术服务有限公司,上海200233)
建立LCMSMS方法测定禽畜肉中金刚烷胺残留量的方法,并进行了不确定度评定。本文中的不确定度评定数学模型是根据CNAS-GL06-2006《化学分析中不确定度的评估指南》和JJF1059.1-2012《测量不确定度评定与表示》建立的,并对主要影响因素进行了分析,得到了此测定方法的不确定度报告。结果表明:禽畜肉中的金刚烷胺残留量用LCMSMS方法测定,其不确定度主要来源于所用仪器,标准溶液的配制过程和校准曲线的拟合。
液相色谱-串联质谱;动物源性食品;金刚烷胺;不确定度
盐酸金刚烷胺为一种对称的三环状胺,在病毒进入宿主细胞过程中起到抑制作用,还对病毒的脱壳有影响,并对其繁殖进行抑制,因此用作治疗和预防病毒性感染,并对由于A型流感病毒引起的呼吸道症状有很好的治疗作用[1-2]。金刚烷胺是最早用于抑制流感病毒的抗病毒药,在抑制人流感病毒方面,金刚烷胺具有价格低廉,效果明显等特点。目前还曾在兽医临床上用于动物病毒病的预防和治疗,但并没被批准用作兽医,畜禽如果用人类的抗病毒药物,则很有可能引起病毒变异,进而影响人类用药的效果,并且可能导致动物病毒产生耐药性以及免疫抑制,如果不明确机理,还有可能导致药物在动物体内产生残留,间接影响人类健康[3-4]。我国农业部在2005年发布了第560号公告,其中明确禁止在兽药领域生产和销售金刚烷胺[5]。2006年美国FDA也明令禁止将金刚烷胺等人类抗病毒药物用于畜禽类[6]。
关于该类药物报道较多的是人血浆和药物中金刚烷胺类药物中金刚烷胺类药物的测定方法,主要包括气相色谱法[1]、液相色谱法[7-10]、毛细管电泳法[11]和液相色谱-串联质谱法[12-14]等。目前发布的金刚烷胺残留测定方法只有两个地方标准:DB32/T1163-2007 鸡肝中金刚烷胺残留量的测定液相色谱-串联质谱法,DB21/2394-2014 鸡肝和鸡肉中金刚烷胺 金刚乙胺的检测 超高效液相色谱串联质谱法(2015-6-29实施),参考标准及多次实验建立了我们实验室自己的测定方法,然而一切测量结果都不可避免地具有不确定度。本文依据法规CNAS-GL06-2006《化学分析中不确定度的评估指南》和JJF1059.1-2012《测量不确定度评定与表示》,分析了用LCMSMS方法测定金刚烷胺测量结果的不确定度,从而明确了测量结果准确性的影响因素,为得到更可靠准确的结果提供了理论基础和科学依据。
1 实 验
1.1材料与仪器
1.1.1材料与试剂
甲醇(色谱纯),美国天地;乙腈(色谱纯),美国天地;乙酸铵(优级纯),上海安谱;甲酸(优级纯),上海安谱;三氯乙酸(分析纯),国药集团;氨水(分析纯),国药集团;金刚烷胺标准品(纯度97.5%),上海安谱;金刚烷胺-D15标准品(纯度98%),TRC;实验用水均为Millipore系统产生的超纯水。
1.1.2仪器
THERMO液相色谱系统,赛默飞世尔科技公司;三重四极杆质谱分析仪(配有电喷雾离子源),赛默飞世尔科技公司;高速均质器,上海标本模型厂;涡旋混匀器,上海精科实业有限公司;高速冷冻离心机,上海菲恰尔分析仪器有限公司;氮吹浓缩仪,上海安谱;超声波仪器,上海科导超声仪器有限公司;MS204S电子天平,梅特勒托利多;XS105电子天平,梅特勒托利多。
1.2实验方法
1.2.1标准曲线的配制
准确称量金刚烷胺和金刚烷胺-D15标准品配制成需要且合理浓度的标准储备液和标准中间液体,再由标准中间液配制成金刚烷胺浓度为1.0 ng/mL、2.0 ng/mL、5.0 ng/mL、10.0 ng/mL、20.0 ng/mL,内标金刚烷胺-d15浓度为25.0 ng/mL的标准工作液。
1.2.2样品制备
称取2 g(精确到0.01 g)试样至50 mL离心管中,然后加入100 μL 的0.1 μg/mL金刚烷胺-D15内标,再加入15 mL乙腈提取液,涡旋振荡1 min,超声10 min,4000 r/min冷冻离心15 min,上清液转移至另一50 mL离心管中,重复上述操作,合并上清液,加入10 mL正己烷轻微振摇3 min,4000 r/min冷冻离心5 min,除去正己烷层,转移提取液到氮吹管,并氮吹至干,用1 mL水复溶,涡旋超声溶解残渣,过0.22 μm滤膜,供LC-MS/MS测定。
2 数学模型建立
样品中金刚烷胺含量计算公式如下:
式中:X——样品中金刚烷胺含量,μg/kg
A——样液中金刚烷胺的峰面积
Ci——样液中金刚烷胺-D15的浓度,ng/mL
Ais——标准物质中金刚烷胺-D15的峰面积
Cs——标准物质中金刚烷胺的浓度,ng/mL
Ai——样液中金刚烷胺-D15的峰面积
As——标准物质的峰面积
Cis——标准物质中金刚烷胺-D15的浓度,ng/mL
V——定容体积,mL
M——样品质量,g
df——稀释倍数
根据内标法的计算特点,可以知道样液中金刚烷胺与其内标物的质量浓度比C是由A,Ci,Ais,Cs,Ai,As,Cis各分量计算而来,因此由这几个分量产生的不确定度,可以归入C中,而又因为随机影响的重复性系数frep值为1,则上面的计算公式可简化为:
3 分析不确定度的来源[15-18]
通过测试过程步骤以及数学模型,可以确定不确定度的主要来源有:回收率产生的不确定度,液质联用仪器定量校准产生的不确定度,样品称量产生的不确定度,校准曲线拟合过程产生的不确定度,制备样液过程中的定容体积产生的不确定度,仪器定量重复性产生的不确定度,配制标准曲线过程产生的不确定度。
4 不确定度各分量的计算
4.1试样测试过程中由重复性引入的不确定度
在金刚烷胺样品中加标,重复测定6次,表1为测定结果。
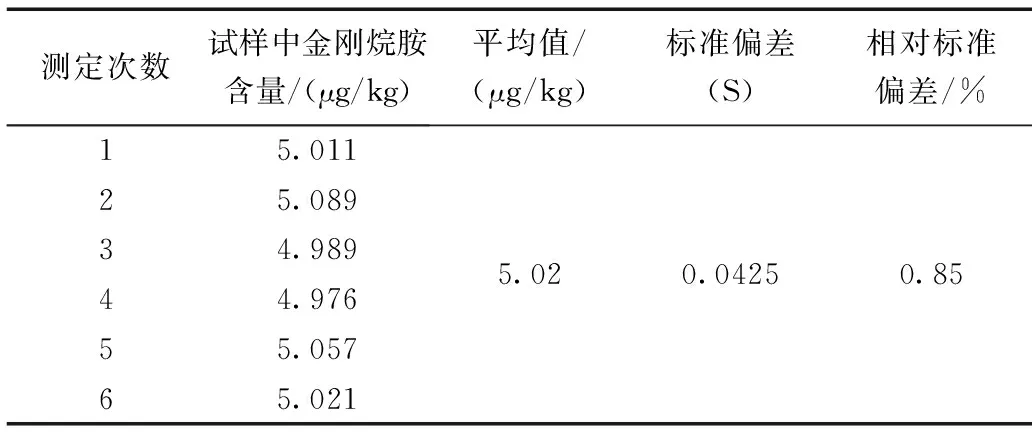
表1 重复测定加标样品的结果Table 1 Results of spiked sample determination
单次测量的试验标准偏差:
因此,由测量重复性引入的相对标准不确定度为:
4.2试样称量时产生的不确定度
准确称量样品2.0000g,所用天平校准允许的最大误差为±0.0001g,按均匀分布考虑,则称量试样产生的相对标准不确定度为:
4.3试样制备过程中定容体积引入的不确定度

4.4液质联用仪器定量校准引入的不确定度
测试所用仪器外校证报告给出扩展不确定度urel=6.8%,K=2,由此,液质联用仪器产生的相对标准不确定度为:
urel(LCMSMS)=0.068/2=0.034
4.5标准曲线配制过程产生的不确定度
4.5.1配制标准储备液产生的相对标准不确定度urel(C1)
(1)金刚烷胺和金刚烷胺-d15标准品证书给出纯度分别为98%和97.5%,由标准品纯度引入的不确定度为:
(2)天平允许的最大误差为±0.01 mg,称取标品金刚烷胺和金刚烷胺-d15分别是1.00 mg和10.00 mg,取矩形分布,产生的相对标准不确定度为:


(4)合成得到标准储备液配制的相对标准不确定度urel(C1)

4.5.2中间标准溶液配制所产生的相对标准不确定度urel(C2)
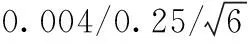
=0.00930
4.5.3由标准中间液稀释配制标准工作液产生的相对标准不确定度urel(C3)
配制标准工作液过程中主要是由玻璃量器带入的不确定度,根据规程JJG196-2006[19]的要求,并按三角分布考虑,则标准曲线配制过程中由玻璃量器所产生的不确定度见表2。
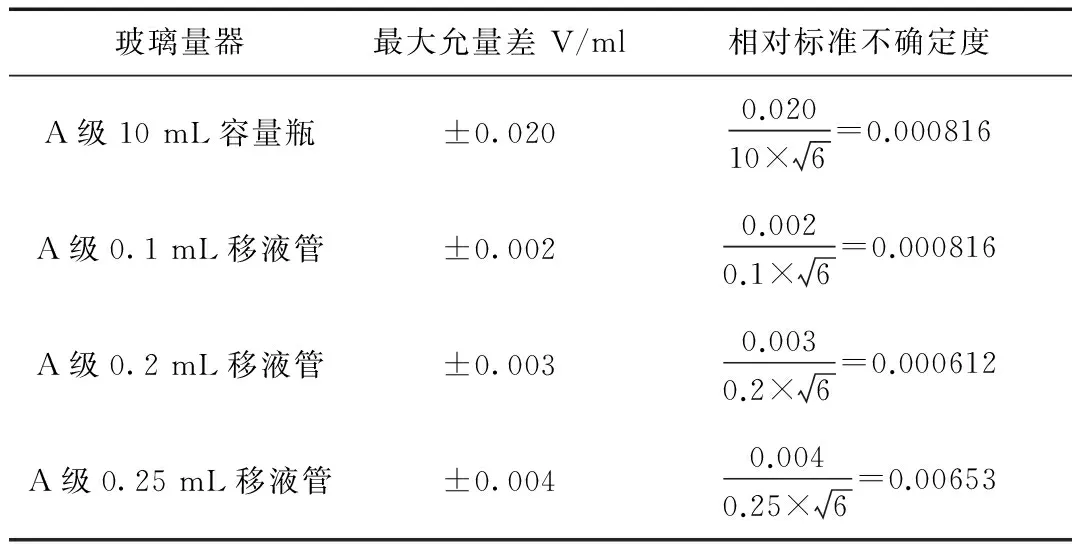
表2 标准曲线配制过程中玻璃量器所产生的不确定度Table 2 The uncertainty of the process of glass volume calibrationproduces standard working solution preparation
由于0.1 mL移液管在配制过程中使用了4次,0.25 mL移液管在配制过程中使用了5次,10 mL单标线容量瓶使用了5次,因此标准工作液配制过程玻璃量器产生的合成相对标准不确定度为:
=0.0148
古诗文中理的第二个层次是对生命启迪。曾经沧海难为水,除却巫山不是云。这句也是情理相融的经典代表诗句。为什么会这么说呢?据说写这首诗的作者,深深爱着他的家人,后来在他的家人离开他之后,他深深的怀念着。然后就写下了这两句诗“曾经沧海难为水,除却巫山不是云。”在作者妻子离开他之后,他看到生活中各种各样的人和事物,都已经无法动心了。“曾经沧海难为水”意思就是说,看到过很多很多的河水,直到见识过了沧海。从此以后,再看普通的水,就已经没有感觉了。“除却巫山不是云”意思是指巫山的云变化绮丽,所以见识过巫山的云之后,平平常常的云,再也无法激发起他心中的热情。作者以此来表示他对妻子的深深地怀念。
4.5.4金刚烷胺标准曲线配制过程所产生的相对标准不确定度urel(C)
4.6金刚烷胺标准曲线拟合过程所产生的不确定度
标准曲线一共由5个浓度点组成,每个浓度水平测定一次,根据所得到的相应的峰面积,用最小二乘法拟合,可得曲线方程Y=aC+b,以及相关系数R,y为金刚烷胺与内标物浓度的比值,x为金刚烷胺与内标物的峰面积比值,见表3。

表3 曲线各浓度点测定结果及拟合方程Table 3 The results of the determination of theconcentration point of the curve and fitting equation
注:a=0.10372,b=-0.01357,R=0.9995
对于同一试样,测定7次,由上述校准曲线计算所得结果见表4。
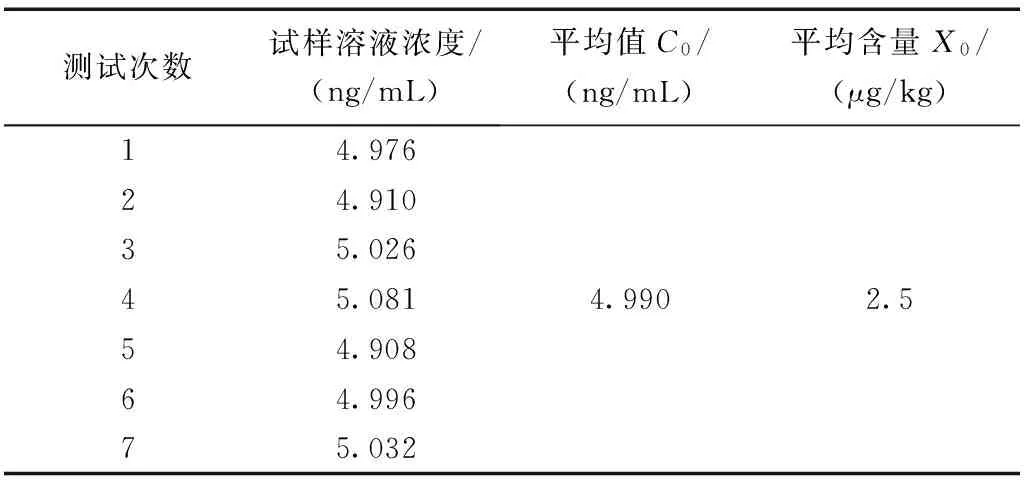
表4 试样溶液测定结果Table 4 Results of sample solution measurement
则校准曲线拟合引入的相对标准不确定度urel(C0)可由下式计算得到:
式中:a——校准曲线的斜率
p——试样测定次数
m——标准曲线各浓度点重复测定次数
Sy/c——标准曲线的标准偏差
Sc/c——标准曲线各个浓度点的离均差平方和
Yij——标准曲线各个浓度点的响应值
Yi——由线性方程计算所得的响应值
Ci——标准曲线各浓度点浓度值
C0——试样溶液的平均浓度
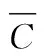
由上述公式计算得到的结果见表5。
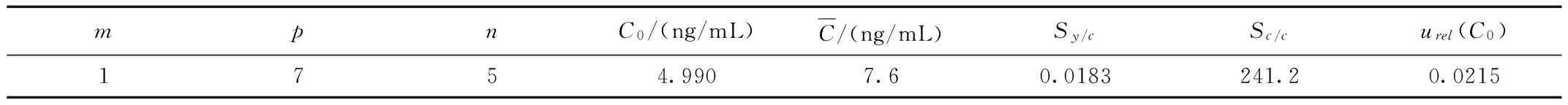
表5 标准曲线用最小二乘法拟合时产生的相对标准不确定度urel(C0)Table 5 The uncertainty urel(C0) of least square curve fitting
5 各个过程产生的相对标准不确定度的合成与扩展

由前面的试验结果可知,试样中金刚烷胺残留量为 2.5μg/kg,因此其标准不确定度为:
u(X)=urel(X)2.5=0.120
取包含因子k=2,则金刚烷胺扩展不确定度为:
U=K×u(X)=2×0.120 =0.24
6 结 论
由本试验得出,当k=2(95%置信度)时,金刚烷胺的测定结果可表示为(2.5±0.24)μg/kg,并且根据文中各个不确定度分量的计算,可知本方法测定金刚烷胺,不确定度的主要来源为所用仪器,其次是标准溶液的配制过程和校准曲线的拟合,因此平时测试工作中,应按规程定期的做好仪器的维护及校准,在配制标准溶液时,操作要规范,养成良好正确的习惯,使得测试结果更为可靠。
[1]ANTOINES,FRANCOISEP.Gaschromatographicdeterminationofamantadinehydrochloride(symmetrel)inhumanplasmaandurine[J].JChromatogrB:BiomedSciandAppl, 1980,183(1):33-39.
[2]李士敏,王玮.液相色谱-质谱联用法测定大鼠血浆中盐酸金刚烷胺浓度及体内药动力学研究[J].药物分析杂志,2007,37(1):66-68.
[3]WILLSRJ,FAROLINODA,CHOMAN,etal.Rimantadinepharmacokineticsaftersingleandmultipledoses[J].AntimicrobialAgents&Chemotherapy,1987,31(5):826-828.
[4]TOMINACKRL,WILLSRJ,GUSTAVSONLE,etal.Multiple-dosepharmacokineticsofrimantadineinelderlyadults[J].AntimicrobialAgents&Chemotherapy, 1988,32(12):1813-1 819.
[5]中华人民共和国农业部.农业部560号公告兽药地方标准废止目录[EB/OL].http://www.moa.gov.vn/zwllm/tzgg/gg/200511/t20051117_496523.
[6]USFDA.FDAprohibitsuseofantiviraldrugsinpoultrytohelpkeepdrugseffectiveforhumans[EB/OL].http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/2006/ucm108620.htm.
[7]修虹,黄榕珍,付梅春.HPLC-ELSD法测定复方氨酚烷胺胶囊中盐酸金刚烷胺及对乙酰氨基酚的含量[J].中国药品标准,2006(1):23-25.
[8]HIGASHIY,UEMORII,FUJIIY.SimultaneousdeterminationofamantadineandRimantadinebyHPLCinratplasmawithpre-columnderivatizationandfluorescencedetectionforpharmacokineticstudies[J].BiomedChromatogr,2005,19(9):655-662.
[9]HIGASHIY,FUJIIY.Simultaneousdeterminationofthebindingofamantadineanditsanaloguestosyntheticmelaninbyliquidchromatographyafterprecolumnderivatizationwithdansylchloride[J].JChromatogrSci,2005,43(4):213-217.
[10]CUI SJ,FENG F,LIU H,et al.New method for high-performance liquid chromatographic determination of amantadine and its analogues in rat plasma[J].J Pharm Biomed Anal,2007,44(5):1100-1105.
[11]REVILLA A L,HAMACEKJ,LUBAL P,et al.Determination of rimantadine in pharmaceutical preparations by capillary zone electrophoresis with indirect detection or after derivatization[J].Chromatogr,1998,47(7/8):433-439.
[12]TORSTEN A,BRUNHILDE G,AXEL H,et al.Determination of serum amantadine by liquid chromatography-tandem mass spectrometry[J].Clin Chim Acta,2005,359(1/2):125-131.
[13]WANG P,LIANG Y Z,CHEN B M,et al.Quantitative determination of amantadine in human plasma by liquid chromatography-mass spectrometry and the application in a bioequivalence study[J].J Pharm Biomed Anal,2007,43(4):1519-1525.
[14]云环,张朝晖,罗生亮,等.固相萃取/LC-MS/MS法检测动物源性食品中的金刚烷胺[J].现代仪器,2009,15(6):42-45.
[15]国家质量技术监督局.JJF 1059-1999 测量不确定度评定与表示[S].北京:中国计量出版社,1999.
[16]严凤,张文刚,李丹妮,等.液相色谱-串联质谱法测定动物源食品中氯霉素残留量不确定度分析[J].上海畜牧兽医通讯,2008(5):32-33.
[17]颜斌,曹军,陈勇,等.高效液相色谱/串联质谱法测定水产品中环丙沙星的不确定度[J].检验检疫学刊,2011(2):40-42.
[18]任雪冬,刘成雁,林雪征,等.液相色谱-串联质谱法测定畜禽肉中十种磺胺类兽药残留的不确定度评定[J].中国兽药杂志,2011,45(5):20-25.
[19]国家质量监督检验检疫总局.JJG 196-2006 常用玻璃量器检定规程[S].北京:中国计量出版社,2006.
Uncertainty Evaluation for the Determination of Amantadine Residues in Animal Derived Food by LC-MS-MS
YINLi-li
(Shanghai Intertek Testing Services Co., Ltd., Shanghai 200233, China)
A LC-MS-MS method was set up to detect amantadine residues in animal derived food and evaluated the uncertainty of this method. According to the principle and method in CNAS-GL06-Guidance on evluating the Uncertainty in Chemical Analysis and JJF1059.1-2012 Evaluation and Expression of Uncertainty in Measurement, the main influence factors of the uncertainty were analyzed, a mathematic model was established, and the report of the detect method’s uncertainty was created. The results showed that the major factors of uncertainty in measurement were the instrument, preparation of standard solution and fitting of calibration curve.
LC-MS-MS; animal derived food; amantadine; uncertainty
尹丽丽(1980-),女,硕士研究生,主要从事食品检测与分析。
TS207.7
A
1001-9677(2016)015-0137-04

