盐酸倍他司汀片加热降解杂质的定性检测
陈 红,朱 蓉,李 欣,谢 莉,张姮婕
(成都市食品药品检验研究院, 四川 成都 610045)
盐酸倍他司汀片加热降解杂质的定性检测
陈红,朱蓉,李欣,谢莉,张姮婕
(成都市食品药品检验研究院, 四川成都610045)
建立了盐酸倍他司汀片加热降解杂质的定性检测方法。样品粉末105 ℃下加热4 h后,用流动相溶解,滤过后采用二维液质联用(2D-LCMS-IT-TOF)杂质鉴定系统,对盐酸倍他司汀热降解杂质进行定性检查。结果表明:热降解杂质1和杂质2在质谱上没有响应。通过样品信息和多级高分辨质谱结果推断出杂质 3 可能的分子式,并推导其可能的质谱裂解规律,给出其可能的结构式。结论 本法准确、简便、快速,可用于盐酸倍他司汀热降解杂质定性检查。
盐酸倍他司汀;热降解杂质;定性检测
盐酸倍他司汀片(N-甲基-2-吡啶乙胺二盐酸盐,Betahistine Hydrochloride Tablets)主要用于美尼尔氏综合症,血管性头痛及脑动脉硬化,并可用于治疗急性缺血性脑血管疾病,如脑血栓、脑栓塞、一过性脑供血不足等;高血压所致直立性眩晕、耳鸣等亦有效[1-3],已列入国家基本药物目录。盐酸倍他司汀片质量标准收载于英国药典2013版[4]、中国药典2010年版二部[5]及国家药品标准等,根据药品评价抽验质量分析指导原则,2013年度对盐酸倍他司汀片按现行标准检验,合格率为100%。在研究中发现多批样品未知杂质含量高,现行标准收载的有关物质检查项,不能全面反应药品质量,查阅文献[6-8],建立了二维液质联用方法对热降解样品中杂质检查,对部分未知杂质定性测定。
1 实 验
1.1仪器与试剂
包括岛津公司提供的LC-20A液相色谱仪,二极管阵列检测器(SPD-M20A),高压流路选择阀(FCV-12AH×3),色谱柱切换阀(FCV-14AH×2),LCMS-IT-TOF(离子阱-飞行时间质谱)和 LCMSsolution Ver.3.60(工作站)。
盐酸倍他司汀对照由中国药品生物制品检定所提供,编号:100265-200602,杂质Ⅰ(乙烯吡啶)、杂质Ⅱ(2-羟乙基吡啶)、杂质Ⅲ(N-甲基-2吡啶乙胺)由德国LGC GmbH公司提供,选择四个4个生产企业(厂家A、B、C、D)的产品做热降解实验。乙腈为色谱纯;实验用水为超纯水;其余试剂为分析纯。
1.2实验方法
1.2.1色谱条件
(1)色谱柱(Inertsil ODS-4, 4.6 mm I.D.×250 mm, 5 μm);流动相:0.69 g 醋酸铵溶解于 1000 mL水中,用冰醋酸调 pH到 4.7,加入4.43 g十二烷基硫酸钠,混合均匀,过滤后取 600 mL与 400 mL乙腈混匀即得。流速:1 mL/min,柱温:40 ℃,进样体积:20 μL。
(2)色谱柱(Shim-pack XR-ODS 2.0 mm I.D.×50 mm, 2.2 μm);流动相:A-0.1% FA;B-ACN;梯度洗脱,流速:0.3 mL/min,柱温:40 ℃,进样体积:5 μL。
1.2.2质谱条件
离子源:ESI正负离子同时扫描,离子源电压:ESI+,4.5 kV; ESI-,-3.5 kV,检测器电压:1.6 kV。扫描范围:m/z 50~150;m/z 150~500。雾化气:氮气1.5 L/min,干燥气:氮气10 L/min,碰撞气:氩气。脱溶剂管温度:200 ℃,加热模块温度:200 ℃。校准方法:自动调谐优化电压,外标法校准质量数。
1.2.3 2D-LC-IT-TOF系统分析
2D-LC-IT-TOF系统过程如系统流路图1所示。
(1)LC 1stD 初始状态,药物样品进样,采用色谱条件(1)测试。保证了主成分和杂质的保留时间与建立方法一致,因此,准确确定目标杂质。
(2)收集 1stD 确定的杂质到 loop 1, 2, 3, 4, 5,然后通过色谱条件(2)输液泵将 loop环中的组分冲入到 2D色谱柱上分离,并洗脱到MS中进行分析。
(3)平衡 1stD 流路,准备进行溶剂的分析,得到空白数据。
(4)将得到的空白数据与药物的数据进行比较,找出杂质峰,并进行 MS 定性分析。
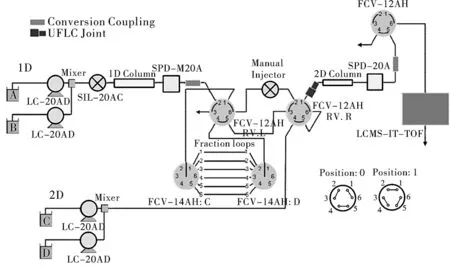
图1 系统流路图Fig.1 Diagram for system flow path
1.2.4溶液的制备
称取105 ℃加热4 h后样品(厂家B,批号20130401)细粉0.15 g,加流动相溶解并稀释制成每1 mL中约含0.4 mg的溶液,作为供试品溶液,测定,见图2。
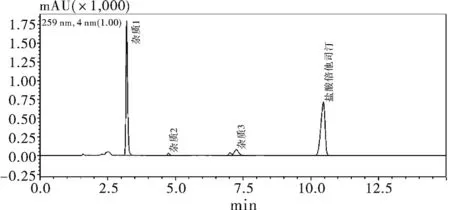
图2 105 ℃加热破坏后样品色谱图Fig.2 Chromatogramofthe sampleafter 105 ℃ heated
2 结果与讨论
2.1样品热降解实验
样品在40 ℃加速试验中发现,总杂质量增加,部分样品杂质1(相对保留时间0.28)和杂质3(相对保留时间0.70)增加量超过0.1%。样品粉末在60 ℃加热16 h后测定,按面积归一化法计算各杂质量,厂家A生产的样品单个杂质或总杂质量均未明显增加,杂质1增加量小于0.2%,其他杂质增加量小于0.1%。而其他三个生产厂家在相对保留时间0.36新增一个杂质(杂质2),杂质量约为0.07%~0.10%;杂质1明显增加,
增加量大于1.0%;在相对保留时间0.70的杂质3增加量大于0.1%。厂家B生产的样品在相对保留时间0.70的杂质增加量大于1.0%。
在未加热样品中杂质1、杂质3对总杂质量贡献较大,杂质2量小于0.1%,为了对样品中杂质1和杂质3定性研究,将四个生产厂家的样品粉末及原料分别进行高温破坏(105 ℃,3 h),使杂质量增加足以进行定性研究。结果原料未见明显杂质增加,4个样品粉末105 ℃加热3 h后颜色变黄,杂质1、杂质2、杂质3等处杂质含量都明显增加,见色谱图2。
2.2质谱图分析
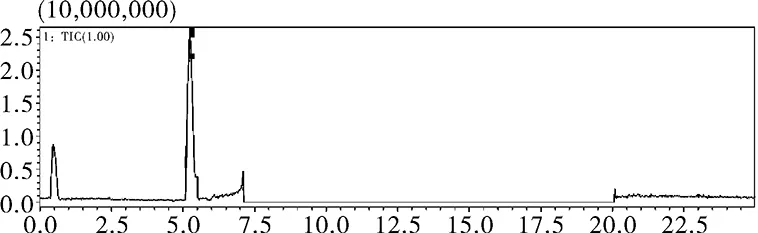
图3 杂质3二维 MS 色谱图Fig.3 Dimensional MS chromatograms of the impurity 3
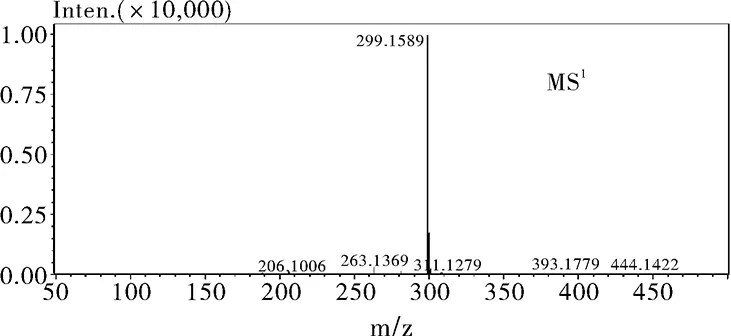
图4 杂质3一级质谱图Fig.4 MS1 spectrum of the impurity 3
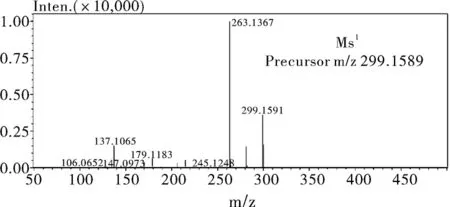
图5 杂质3二级质谱图Fig.5 MS2 spectrum of the impurity 3
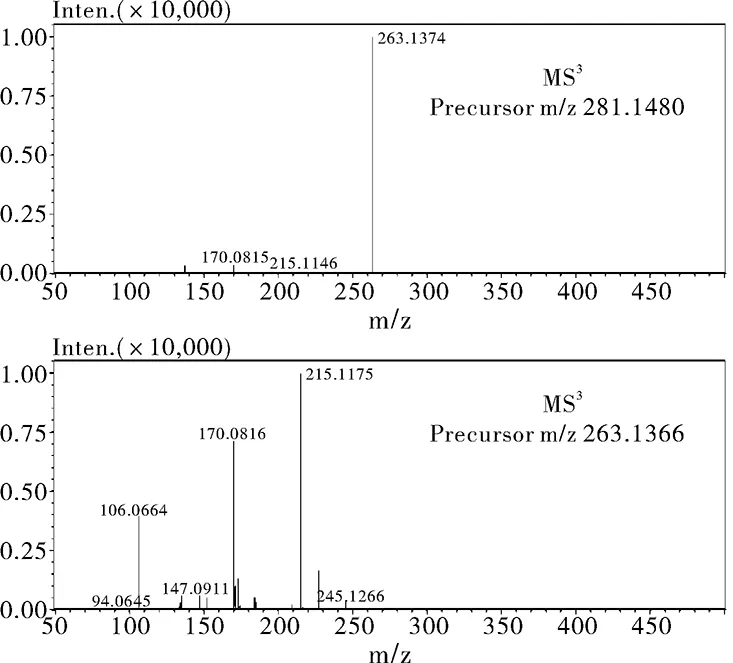
图6 杂质3三级质谱图1Fig.6 MS3 spectrum 1 of the impurity 3
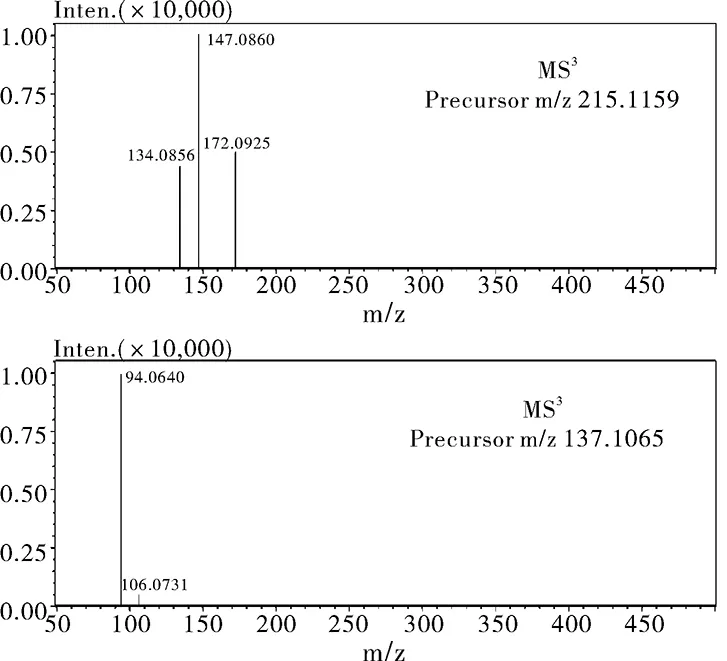
图7 杂质3三级质谱图2Fig.7 MS3 spectrum 2 of the impurity 3
盐酸倍他司汀及其已知3 个杂质(杂质Ⅰ(乙烯吡啶)、杂质Ⅱ(2-羟乙基吡啶)、杂质Ⅲ(N-甲基-2吡啶乙胺)),在质谱上均有很好的响应,但是未知杂质1和未知杂质2在质谱上却没有响应。未知杂质3二维 MS 色谱图(m/z 150~500),见图3,未知杂质3 的多级质谱图 ESI(+)见图4~图7。
3 结 论
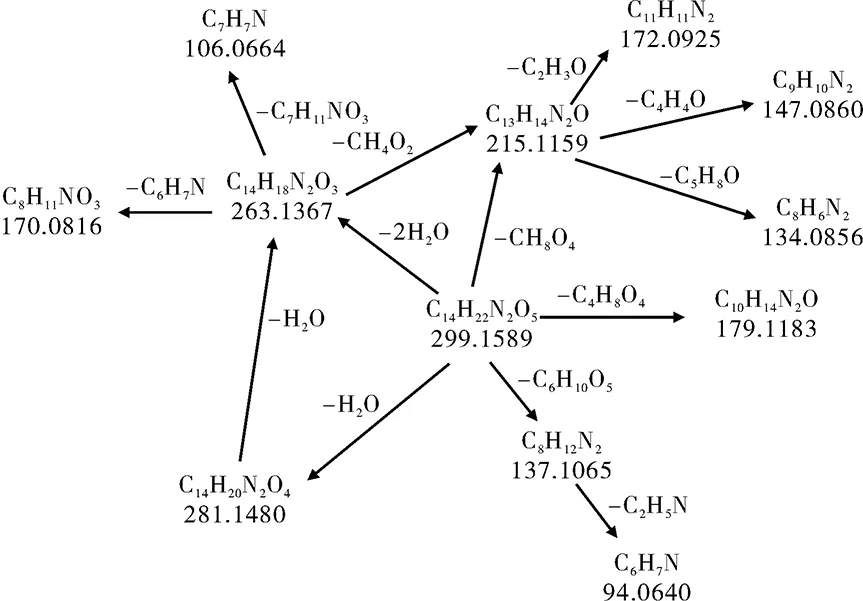
图8 杂质3的ESI(+)多级质谱碎裂方式分析Fig.8 ESI(+)MSn fragmentation pattern analysis of impurity 3
结合盐酸倍他司汀已知的三种杂质结构分析,用分子式预测软件分析,得到杂质3 可能的分子式为 C14H22N2O5。其碎片离子 m/z137.1065的分子式可能是 C8H12N2, 可能为倍他司汀。由杂质3的分子式裂解规律(见图8)推测出杂质3 可能的结构式见图9。考察盐酸倍他司汀片的辅料,由乳糖、蔗糖、淀粉、糊精、硬脂酸镁、羟丙基纤维素等组成,由此推测该杂质是在高温条件下由倍他司汀与样品辅料中的糖发生了缩合反应后产生的降解产物。
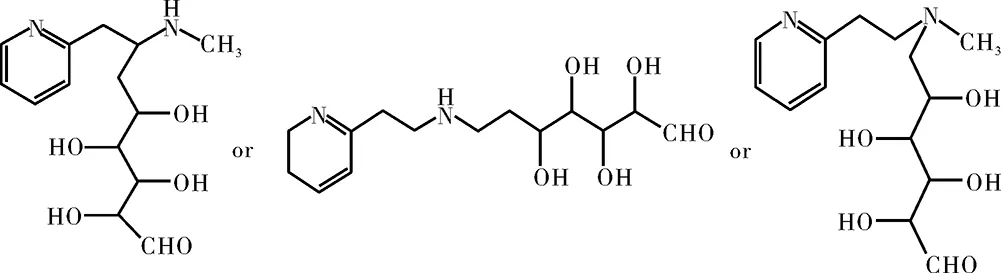
图9 杂质3可能的结构式Fig.9 Possible structural formula of impurity 3 参考文献
[1]张廷志.盐酸倍他司汀治疗眩晕症的临床效果分析[J]. 临床合理用药杂志, 2013,6(33): 25-26.
[2]杨远君.社区应用倍他司汀治疗椎基底动脉供血不足的临床观察[J]. 中国社区医师:医学专业,2013(8):11.
[3]沈新秀,祖军,魏叶,等. 盐酸倍他司汀联合葛根素治疗急性眩晕的临床观察[J]. 浙江临床医学, 2010,12(6):594-595.
[4]Betahistine Hydrochloride Tablets. British Pharmacopoeia 2013[S].2013:2469-2470.
[5]中华人民共和国国家药典委员会. 中国药典(二部)[S]. 北京:中国医药科技出版社,2010:769.
[6]王冬,董煜,钱小平,等. 高效液相色谱法测定盐酸倍他司汀片的有关物质[J]. 中国药业, 2013,22(12):93-94.
[7]吴随凤,宋尚龙,王传利. 高效液相色谱法测定盐酸倍他司汀片的有关物质[J]. 化学分析计量,2005,14(3):31-33.
[8]陆榕,孙进,方金玲,等. 离子对-HPLC法测定盐酸倍他司汀注射液中药物与有关物质含量[J].沈阳药科大学学报,2006,23(7):448-451.
Qualitative Analysis of Impurity in Betahistine Hydrochoride Tablets by Heat Treatment
CHENHong,ZHURong,LIXin,XIELi,ZHANGHeng-jie
(Chengdu Institute for Food and Drug Control, Sichuan Chengdu 610045, China)
A method for qualitative analysis of impurity in betahistine hydrochoride tablets by heat treatment was established. Betahistine hydrochoride tablets powder was heated in 4 h, and the degradation impurities were extracted by mobile phase. Qualitative analysis of the impurities was detected by 2D-LC-IT-TOF. Result showed that one of the three degradation impurities could be detected qualitatively. The molecular formula, fragmentation pattern and structure type possibly were inferred from by sample information and multistage high resolution mass spectrometry. The method is accurate and sensitive, and can be used for qualitative analysis of impurity in betahistine hydrochloride.
betahistine hydrochloride; impurities by heat treatment; qualitative analysis
陈红(1977-),女,副主任药师,硕士,主要研究方向为食品/药品监督检测和质量标准研究。
R917
A
1001-9677(2016)08-0123-03

