HPLC法测定利培酮中2-氨基吡啶残留
钱丽红
(无锡积大制药有限公司,江苏 无锡 214445)
HPLC法测定利培酮中2-氨基吡啶残留
钱丽红
(无锡积大制药有限公司,江苏无锡214445)
采用HPLC法测定利培酮原料药中2-氨基吡啶(具有潜在遗传毒性)的残留量。采用ODS-BP(4.6 mm×250 mm,5 μm)色谱柱,流动相为甲醇:醋酸盐=40:60,梯度洗脱,流速为1.0 mL/min,检测波长为290 nm。利培酮及其基因毒性物质2-氨基吡啶的线性范围分别为0.08~1.5 μg/mL,平均回收率分别为97.8%。本法简便、准确、可靠、适合于利培酮原料药中2-氨基吡啶(具有潜在遗传毒性)的残留量的测定。
利培酮;HPLC法;基因毒性;残留量
利培酮用于治疗急性和慢性精神分裂症,特别是对情感性抑郁症有较好的疗效[1-2]。2-氨基吡啶被认为是具有潜在的遗传毒性的物质,而遗传毒性杂质的毒理学评估和药物原料中此类杂质的可接受限度确定是难题,现有ICH Q3X指南中未充分说明。常用遗传毒性杂质数据库差异很大,而数据库是决定 (dictates)可接受限度评估所用方法的主要因素。当运用已建立风险评估方法所需资料缺乏时,包括致癌性长期试验资料或提供遗传毒性阈值机制证据的资料等,采用毒理学担忧阈值(TTC)所定义的普遍适用方法。根据EMEA人用药品委员会(CHMP)《遗传毒性杂质限度指导原则》[3],对大部分药物(Pharmaceuticals),认为TTC值为遗传毒性杂质摄入量1.5 μg/天时相关的风险可接受 (一生中额外的癌症风险1/100000)。根据该阈值,药物原料中2-氨基吡啶的允许水平可根据预计每日剂量计算得到,利培酮的日剂量为1.6 mg/天,计算的限度为93.75 ppm,为严格控制产品质量,2-氨基吡啶所定的限度为90 ppm,于是本文建立了HPLC法测定利培酮中2-氨基吡啶残留量的方法,方法简单,准确,灵敏。
1 仪器与试药
高效液相色谱仪,色谱柱ODS-BP(4.6 mm×250 mm,5 μm),美国Agilent公司。
2-氨基吡啶对照品,无锡积大制药有限公司(批号:130301);甲醇(色谱纯),德国默克;水为密理博制备的超纯水;其他试剂均为国药分析纯;利培酮(批号:130211),无锡积大制药有限公司。
2 方法与结果[4-5]
2.1溶液制备
2.1.1对照品溶液的制备
称取适量2-氨基吡啶对照品,精密称定,用甲醇溶解后定容,混匀,使成浓度为0.9 μg/mL的溶液。
2.1.2系统适用性溶液
称取适量利培酮样品,精密称定,加入适量2-氨基吡啶对照品储备溶液,加甲醇配成2-氨基吡啶浓度0.9 μg /mL,利培酮浓度10 mg/mL的混合溶液。
2.1.3供试品溶液
称取适量利培酮供试品,精密称定,用甲醇溶解后定容,混匀,使成浓度10 mg/mL的溶液。
2.2色谱条件及系统适用性
采用ODS-BP(4.6 mm×250 mm,5 μm)液相色谱柱,流动相组成为甲醇:醋酸盐=40:60;梯度洗脱;进样体积:20 μL;流速为1.0 mL/min;检测波长为UV290 nm;柱温为35 ℃;运行时间为30 min;稀释液为甲醇。在本条件下,系统适用性溶液中2-甲基吡啶与相邻峰之间分离度大于1.5,结果见图3。

图1 对照品储备溶液图谱

图2 供试品溶液图谱

图3 系统适用性图谱
2.3线性关系的考察
2-氨基吡啶贮备液:称取2-氨基吡啶对照品适量,精密称定,用甲醇溶解后定容,混匀,使成1.8 μg /mL的溶液。
线性溶液配制:分别精密量取2-氨基吡啶贮备液0.4 mL、0.5 mL、2.5 mL、4.0 mL、5.0 mL、6.0 mL、7.5 mL分别至10 mL 量瓶中,用甲醇溶解后定容,混匀,即为线性系列溶液。
分别精密吸取20 μL上述线性系列溶液注入液相色谱仪,记录各线性系列溶液的峰面积, 以Y(峰面积)为纵坐标,浓度X(μg/mL)为横坐标进行线性回归,线性回归方程为y=49.908X-0.3249。
结果表明2-氨基吡啶浓度在0.07~1.5 μg/mL的线性范围内,峰面积与溶液的浓度呈线性关系,线性相关系数为0.999。
2.4专属性试验
取本品,分别精密称定样品100 mg利培酮置10 mL量瓶中分别加入0.5 M氢氧化钠溶液1 mL、0.5 M盐酸溶液2 mL、双氧水(30%)各0.5 mL,分别放置1 h、2 h、0.5 h后,调节pH值至中性后,加入甲醇定容至10 mL,混匀,即为碱破坏、酸破坏和氧化破坏后的溶液,同时做空白试验。分别把1 g利培酮样品放置于4500 LUX光照、高温60 ℃和RH95%高湿的条件下,10天后,精密称定各破坏条件下的样品100 mg利培酮,加甲醇定容至10 mL,混匀,即得强光、高温和高湿破坏条件下的溶液。分别把上述6个破坏溶液各进样20 μL,记录峰面积。结果2-氨基吡啶均未检出,且各峰之间均达到基线分离,分离度均大于1.5。
取本品,分别精密称定样品100 mg利培酮置10 mL量瓶中分别加入0.5 M氢氧化钠溶液1 mL、0.5 M盐酸溶液2 mL、双氧水(30%)各0.5 mL,分别放置 h、2 h、0.5 h后,调节pH值至中性后,再分别加入2-氨基吡啶对照品溶液(0.09 mg/mL)0.1 mL后加甲醇定容至10 mL,混匀,即得碱破坏、酸破坏和氧化破坏后与2-氨基吡啶的分离度溶液,同时做空白试验。分别把1 g利培酮样品放置于4500LUX光照、高温60 ℃和RH95%高湿的条件下,10天后,精密称定各破坏条件下的样品100 mg利培酮,再分别加入2-氨基吡啶对照品溶液(0.09 mg/mL)0.1 mL后加甲醇定容至10 mL,混匀,即得强光、高温和高湿破坏条件下与2-氨基吡啶的分离度溶液。分别把上述6个破坏溶液各进样20 μL,记录峰面积。结果2-氨基吡啶与破坏溶液中的各峰之间的分离度均大于1.5,均达到基线分离,结果表明本法专属性良好。
2.5检测限和定量限
取2.3“线性关系的考察”项下的线性系列对照品溶液,取最低浓度为0.7 μg/mL的对照品溶液,逐步稀释,取信噪比(S/N)为3的对照品图谱作为检测限图谱,计算得出的检测限为0.03 μg/mL; 取信噪比(S/N)为10的对照品图谱作为定量限图谱,连续进样6针,计算得出的定量限为0.07 μg/mL,峰面积RSD为2.6%。
图4 检测限图谱

图5 定量限图谱
2.6稳定性试验
取利培酮(批号:130211)的供试品溶液,于(0、4、8、12、24 h)分别进样20 μL,得到各时间点的色谱图,分别记录峰面积,计算5个时间点的峰面积的RSD,结果利培酮峰面积的RSD为0.7%,且无生成新杂质,表明利培酮供试品溶液在24 h内基本稳定。
取2-氨基吡啶(批号:130301)的对照溶液,于(0、4、8、12、24 h)分别进样20 μL,得到各时间点的色谱图,分别记录峰面积,计算5个时间点的峰面积的RSD,结果2-氨基吡啶峰面积的RSD为2.2%,且无生成新杂质,表明对照溶液在24 h内基本稳定。
2.7精密度试验
(1) 分别配制对照溶液和供试品溶液,连续进样对照品溶液和供试品溶液各6针,分别记录对照溶液和供试品溶液的峰面积,计算对照溶液和供试品溶液峰面积的RSD,分别为1.2%、0.5%。
(2) 同一批利培酮样品(批号:130211)进行了不同人、不同仪器、不同天的测试,结果2-氨基吡啶的残留均未检出,RSD均为0。
精密度结果的RSD可接受标准为不得过10%,进行精密度实验后,结果均小于10%,表明本法精密度良好。
2.8准确度(回收率)试验
配制供试品溶液9份,分别加入杂质对照品贮备液配成含杂质0.7 μg/mL(3份)、0.9 μg/mL(3份)、1.1 μg/mL(3份)的准确度测试溶液,测定结果见表1。
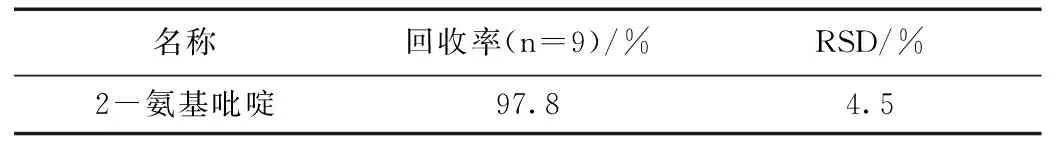
表1 准确度
准确度结果表明本法测试2-氨基吡啶的回收率良好。
3 讨 论
(1)检测波长的选择:配制对照品溶液,使用紫外分光光度计进行全波长扫描,扫描显示2-氨基吡啶的最大吸收波长为290 nm,所以选取290 nm 作为检测2-氨基吡啶的波长。
(2)流动相的选择:进行利培酮的溶解度测试后,结果表明利培酮在甲醇中溶解度较好,采用3种反向色谱条件进行分离,流动相分别为甲醇:醋酸盐=40:60;甲醇:磷酸盐=40:60;甲醇:水=40:60,3种反向色谱条件分别进行梯度洗脱,结果第一种流动相条件(甲醇:醋酸盐=40:60)的分离度符合要求。
(3)取2.4“专属性试验”项下的利培酮破坏性溶液进行主峰峰纯度检查,使用二极管阵列检测器在200~400 nm范围内进行扫描,各破坏性溶液中的主峰峰纯度均满足检测要求,结果表明本法能有效分离降解产物,不影响测定,可有效控制杂质含量。
[1]中国科学院上海有机化学研究所.化学数据库-药品数据库[S].
[2]陈新谦,金有豫,汤光.新编药物学.17版[M]. 北京:人民卫生出版社,2003:261.
[3]Guideline CHMP/QWP/251344/2006.
[4]中国药典2015附录9101 药品质量标准分析方法验证指导原则[S].
[5]ICH Q2.R1.Validation.Analytical.Procedures.
Determination of 2-aminopyridine Quantitative Determination of Risperidone by HPLC
QIANLi-hong
(Wuxi Jida Pharmaceutical Co., Ltd., Jiangsu Wuxi 214445, China)
An HPLC method for 2-aminopyridine(potential genotoxic)quantitative determination of riseperidone was established. The analytical column was HPLC ODS-BP(4.6 mm×250 mm,5 μm)column. The mobile phase was composed of methanol and acetate salt(40:60)at a flow rate of 1.0 mL/min. The wavelength of UV detector was 290 nm. The linear ranges of 2-aminopyridine was 0.08~1.5 μg/mL, the average recovery of riperidone was 97.8%. This method is rapid, accurate and reliable to determine the 2-aminopyridine content of risperidone.
risepridone; HPLC method; potential genotoxic; residue quantity
钱丽红(1975-),女,主要从事药物开发和分析。
R917
B
1001-9677(2016)012-0122-03

