法舒地尔对百草枯致大鼠肺纤维化的干预作用
周挺,夏菁,李增攀,徐丽艳,韩文文,方建江(宁波市医疗中心李惠利医院,浙江 宁波315000)
法舒地尔对百草枯致大鼠肺纤维化的干预作用
周挺,夏菁,李增攀,徐丽艳,韩文文,方建江*
(宁波市医疗中心李惠利医院,浙江 宁波315000)
目的观察急性百草枯(PQ)中毒大鼠肺组织转化生长因子-β1(TGF-β1)的表达水平及法舒地尔对其的干预作用。方法将72只SPF级SD大鼠随机分为正常对照组、法舒地尔对照组、PQ中毒组、法舒地尔干预组各18例,分别于灌胃后7、14、28天活杀大鼠留取标本。观察大鼠行为学改变,HE和Masson染色观察大鼠肺组织病理改变,实时荧光定量PCR及免疫组化法检测TGF-β1的表达水平。结果光镜下,PQ中毒组大鼠急性肺损伤及纤维化明显,法舒地尔干预组大鼠肺组织损伤程度较PQ中毒组减轻。与正常对照组比较,PQ中毒组大鼠肺组织7、14、28天TGF-β1 mRNA及蛋白的表达量显著增高,于28天达峰值,差异有统计学意义(均P<0.01);与同一时间PQ中毒组比较,法舒地尔干预组小鼠肺组织TGF-β1mRNA及蛋白表达量明显降低,差异具有统计学意义(P<0.01)。结论法舒地尔可以抑制百草枯中毒大鼠肺组织TGF-β1的表达,从而减轻大鼠肺纤维化程度。
百草枯;肺纤维化;转化生长因子-β1;法舒地尔
百草枯(paraquat,PQ)是目前全球使用最广泛的除草剂之一,口服中毒者短期内可出现多脏器功能障碍,数天内致死,度过急性期的患者最终多数死于肺纤维化[1]。转化生长因子-β1(transforming growth factorβ1,TGF-β1)是众多纤维化疾病发生发展的重要因子[2],日益引起大家重视。近年来发现法舒地尔作为一种高效的血管扩张药,可以干预多种器官纤维化进程。本研究通过PQ灌胃染毒建立大鼠肺纤维化模型,检测TGF-β1的动态变化,探讨法舒地尔对百草枯致大鼠肺纤维化的干预作用。
1 材料与方法
1.1材料动物:SPF级健康雄性SD大鼠72只,200~230g,10周龄左右,由浙江省实验动物中心提供,动物合格证号为:SCXK(浙)2014-0001,实验大鼠由宁波大学动物实验中心饲养,维持室温22~25℃,湿度45%~55%,喂食颗粒饲料,实验前8小时禁食,4小时禁水。试剂:注射用法舒地尔(批号: h20040356,天津红日药业股份有限公司生产),20%百草枯溶液 (山东济南天海科技有限公司,批号:4685-14-7);TGF-β1抗体、免疫组化试剂盒(上海士锋生物科技有限公司)。
1.2方法72只SPF级SD大鼠随机分为4组,即正常对照组、法舒地尔对照组、PQ中毒组及法舒地尔干预组。各组再按随机原则分为7、14、28天三个亚组,每个亚组6只大鼠。具体分组及方法见表1。各组大鼠于灌胃后第7、14、28天分批处死。开胸完整取出肺组织并观察整体肺的变化情况,左上肺置于4%甲醛中固定,制备石蜡切片供组织学检查、HE染色、Masson染色及免疫组化,其余肺组织入-70℃低温冰箱保存,待测时制备肺组织匀浆。观察各组大鼠行为学改变、肺组织病理学改变、TGF-β1mRNA的表达以及TGF-β1蛋白的表达。

表1 各组的实验方法
1.3检测指标
1.3.1病理学大鼠肺组织经4%甲醛固定后,脱水、包埋、连续切片,进行HE、Masson染色,光学镜下观察肺组织病理学改变;参照 Szapie等[3]方法,用Masson染色评定肺组织纤维化程度。
1.3.2TGF-β1mRNA的表达 严格按照 Realtime PCR操作流程操作,提取大鼠肺组织RNA进行检测。引物由上海基康生物有限公司合成。TGF-β1(长度95bp,上游5'-AGTCCCTGATGA CATTCCTTCTT-3'下游5'-CAAG TTTG AG A GGTGGTGTAAGC-3')。
1.3.3TGF-β1蛋白的表达采用链霉亲和素-过氧化物酶法(SABC)检测,实验步骤严格按照试剂盒说明书进行操作。TGF-β1免疫组化结果以胞质出现棕色或棕黄色为阳性,每张切片在400倍视野下随机取5个视野,用高清晰图像分析系统半定量分析阳性表达部位TGF-β1蛋白的表达水平,计算其平均吸光度值(MOD)作为表达水平的半定量参数。
1.4统计学处理采用SPSS19.0统计软件,计量数据以(±s)表示,多组间比较采用单因素方差分析,两两比较采用LSD-t检验,方差不齐则进行秩和检验。
2 结果
2.1大鼠行为学改变PQ中毒组染毒后大鼠出现呼吸急促、精神萎靡、反应迟钝、攻击性降低、鼠毛蓬松粗糙、色泽黯淡等表现,同时间段法舒地尔干预组大鼠其呼吸急促、精神萎靡、反应迟钝、毛发蓬松等表现相对较轻。
2.2肺组织病理学改变PQ中毒组光镜下可见明显肺泡炎,肺泡间隔水肿,间质内可观察到炎性细胞聚集充血,肺泡结构破坏,随时间延长,肺泡间隔增宽,成纤维细胞集聚(图1C);法舒地尔干预组肺泡炎较PQ中毒组减轻,渗出及充血减少,肺组织结构破坏减轻,肺泡间隔增宽不明显(图1D)。PQ中毒组大鼠肺组织蓝染部分明显,色暗质硬,部分区域表面凹凸不平,切片时韧度增加(图2C);法舒地尔干预组损伤程度较轻、范围较小,韧度较轻(图2D)。

图1 大鼠肺组织HE染色后的病理学改变(×400)(1A:正常对照组;1B:法舒地尔对照组;1C:PQ中毒组;1D:法舒地尔干预组)

图2 大鼠肺组织Masson染色后的病理学改变(×400)(2A:正常对照组;2B:法舒地尔对照组;2C:PQ中毒组;2D:法舒地尔干预组)
2.3TGF-β1mRNA的表达 正常对照组与法舒地尔对照组大鼠肺组织TGF-β1mRNA呈低表达,两组比较差异无统计学意义(P>0.05);与正常对照组比较,PQ中毒组大鼠肺组织 7、14、28天 TGF-β1mRNA表达量显著增高,于28天达峰值,差异有统计学意义(P<0.01);同一时间段法舒地尔干预组大鼠肺组织TGF-β1mRNA表达量较PQ中毒组明显降低,差异具有统计学意义(P<0.01)。详见表2。
表1 各组大鼠肺组织TGF-β1mRNA的表达(±s,×103)
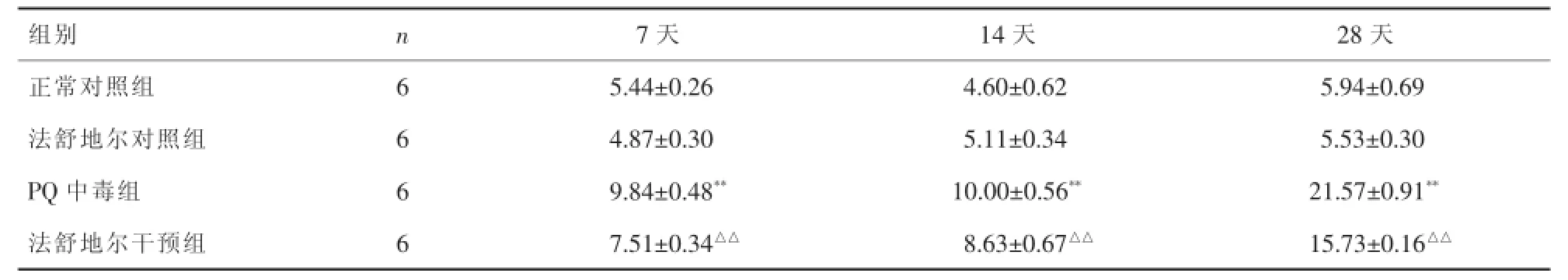
表1 各组大鼠肺组织TGF-β1mRNA的表达(±s,×103)
与正常对照组比较**P<0.01,与PQ中毒组比较△△P<0.01
?
2.4TGF-β1蛋白的表达正常对照组与法舒地尔对照组大鼠肺组织TGF-β1蛋白呈低表达,两组比较差异无统计学意义 (P>0.05);与正常对照组比较,PQ中毒组大鼠肺组织7、14、28天TGF-β1蛋白的表达量显著增高,于28天达峰值,差异有统计学意义(P<0.01);同一时间法舒地尔干预组小鼠肺组织TGF-β1蛋白表达量较PQ中毒组显著降低,差异具有统计学意义(P<0.01)。详见表3。
表3 各组大鼠肺组织TGF-β1蛋白的相对表达(±s)

表3 各组大鼠肺组织TGF-β1蛋白的相对表达(±s)
与正常对照组比较**P<0.01,与PQ中毒组比较△△P<0.01
?
3 讨论
百草枯是一种非选择性接触型除草剂,目前尚无特效解毒药,已成为农药中毒致死事件的常见病因。百草枯中毒可引起多脏器的损伤,尤以肺脏最为突出,早期主要以急性肺泡炎为主,细胞水肿,肺泡塌陷,肺毛细血管通透性增加,血细胞、体液大量进入肺泡腔内,影响通气功能[4]。随着百草枯诱导的急性肺泡炎进一步发展,成纤维细胞增生趋化,胶原蛋白沉积,最终导致肺纤维化[5],其致纤维化机制复杂,目前尚未完全阐明。TGF-β1是目前所知最强的致纤维化因子,是纤维化形成与发展的启动枢纽,能引起成纤维细胞趋化,促进胶原蛋白合成,改变细胞外基质成分[6]。有研究表明,PQ中毒时在氧代谢产物等作用下,大量释放各种TGF-β因子,启动肺组织的炎症和纤维化过程[7-8],促进肺成纤维细胞趋化和上调I、III型前胶原基因表达[9]。因而通过检测TGF-β1的表达可以间接反映肺组织纤维化的程度。法舒地尔是ROCK选择性阻断剂,是目前唯一应用于临床的抑制Rho/ROCK信号通路的药物,近年法舒地尔在抗纤维化方面的作用日益引起重视。王玉珍等[10]研究发现法舒地尔可以减缓肝脏纤维化的进程,在肾间质纤维化[11]及心脏纤维化[12]等方面也有干预作用。目前,法舒地尔对肺纤维化治疗方面的研究尚少,更无干预百草枯中毒致肺纤维化的研究报道。
本实验成功复制了百草枯中毒致肺纤维化的大鼠模型,光镜下可见PQ中毒组大鼠肺泡塌陷,肺间质水肿以及炎细胞浸润 (图1C),Masson染色显示蓝染部分明显,色暗质硬,部分区域表面凹凸不平,纤维蛋白沉积增加,同时肺组织TGF-β1mRNA和蛋白的表达增加(图2C),与正常对照组比较差异显著,而经法舒地尔干预后,大鼠肺组织TGF-β1mRNA和蛋白的表达与较PQ中毒组明显降低。上述结果表明,法舒地尔可以降低百草枯中毒大鼠肺组织TGF-β1的表达水平,改善百草枯致大鼠肺纤维化的严重程度,同时也提示Rho/Rho激酶信号通路可能参与了PQ致肺纤维化过程,但更为详细的机制还有待于进一步研究。
[1]YamashitaM.Along-termfollow-upoflungfunctioninsurvivors of araquat poisoning.Hum Exp Toxicol,2000,19(2):99
[2] Varga J,Pasche B.Antitransforming growth factor-beta in fibrosis:recent progress and implications for systemic sclerosis.Curr Opin Rheumatol,2008,20(6):720
[3] Szapiel SV,Elson NA,Fulmer JD,et al.Bleomycin-induced interstitial pulmonary disease in the nude,athymic mouse.Am Rev RespDis,1979,120(4):893
[4]Dinis-Oliveira RJ,Duate JA,Bastos ML,et al.Paraquat poisonings:Mechanisms of lung toxicity,clinical features,and treatment.Critical Review s in Toxicology,2008,38(1):13
[5]Nakamura T,U shiyama C,Shimada N,et al.Changes in concent rations of type IV collagen and tissue inhibitor of metalloproteinase-1 in patients with paraquat poisoning.Appl To xicol,2001,21(6):445
[6]Ihn H.Pathogenesis of fibrosis:role of TGF-beta and CTGF. Curr Opin Rheumatol,2002,14(6):681
[7]Nathan N,Thouvenin G,Fauroux B,et a1.Interstitial lung disease:physiopathology in the context of lung growth. Paediatr Respir Rev,2011,12(4):216
[8]黄敏,齐小娟,张平,等.结缔组织生长因在百草枯致大鼠子及α-平滑肌肌动蛋白肺纤维化中的作用.中华劳动卫生职业病杂志,2010,28(1):728
[9]蔡后荣,戴令娟,郑培德,等.肺纤维化大鼠肺组织转化生长因子-β1和前胶原基因的表达.中华医学杂志,2001,81 (4):247
[10]王玉珍,姜慧卿,扈彩霞,等.法舒地尔通过Rho/ROCK信号通路抑制肝星状细胞黏附、迁移和增殖.中华肝脏病杂志,2006,14(11):821
[11]Nishikimi T,Koshikawa S,Ishikawa Y,et al.Inhibition of Rho-kinase attenuates nephrosclerosis and improves survival in salt-loaded spontaneously hypertensive stroke-prone rats.J Hypertens,2007,25(5):1053
[12]Kagiyama S,Matsumura K,Goto K,et al.Role of Rho kinase and oxidative stress in cardiac fibrosis induced by aldosterone and salt in angiotensin type 1 a receptor knockoutmice. RegulPept,2010,160(1/3):133
,E-mail:fangjjiang@sina.com
宁波市医学科技计划项目(2013A03)
*为

