玉屏风散对变应性鼻炎模型大鼠血清IgE、IL-4 和IFN-r含量的影响
王芳胡晓艳
·实验研究·
玉屏风散对变应性鼻炎模型大鼠血清IgE、IL-4 和IFN-r含量的影响
王芳1胡晓艳2
目的 观察玉屏风散(YPFS)对变应性鼻炎(AR)大鼠的鼻腔分泌物中嗜酸性粒细胞(EOS)、血清中IgE、IL-4和IFN-r含量的影响。方法 建立AR大鼠模型,将40只大鼠分为正常组,模型组,阳性药对照组及YPFS组,记录每个实验组大鼠的行为表现,测定大鼠鼻腔分泌物中的EOS及血清中IgE、IL-4和IFN-r的含量。结果 模型组IgE、IL-4的含量明显升高,比正常对照组高(P<0.05),IFN-r的含量较正常对照组降低(P<0.05)。YPFS组大鼠鼻部症状明显减轻,血清IgE、IL-4的含量较模型组显著下降(P<0.05),IFN-r的含量较模型组升高(P<0.05)。YPFS组各项指标与阳性药对照组比较,差异之间无统计学意义。结论 YPFS能缓解AR大鼠的局部症状,通过调节宿主免疫功能,纠正Th1/Th2淋巴细胞亚群的失衡,从而产生抗过敏作用。
玉屏风散;变应性性鼻炎;免疫功能
1核工业416医院耳鼻咽喉科(成都,610051)
2四川泸州医学院病原生物学教研室
变应性鼻炎是由IgE介导的鼻腔黏膜变态反应性疾病,是耳鼻咽喉科头颈外科临床上常见的疾病,发病机制较复杂,较多数学者认为其Th1和Th2细胞之间的免疫失衡及其产生的多种细胞因子对IgE的调节是发病的免疫学基础。有研究发现Th1 和Th2之间通过分泌细胞因子保持着动态平衡,而IL-4和IFN-γ的表达异常提示Th细胞的分化偏移,导致了变应性鼻炎的发生发展[1]。玉屏风散由黄芪、白术、防风3味中药组成,是我国中医扶正固表的传统名方,源于元代朱震亨的《丹溪心法》。在临床上常用于预防和治疗呼吸道感染、风寒感冒以及支气管哮喘、变应性鼻炎等变应性疾病[2-4]。但玉屏风散治疗变应性鼻炎的作用方式及机制尚不明确,我们通过试验测定了玉屏风散对变应性鼻炎大鼠鼻部表现、EOS及细胞因子的影响,探索玉屏风散在变应性鼻炎大鼠中的可能的免疫调节方式和作用,为患者中医临床治疗提供试验依据。
材料与方法
1材料
1.1实验药物
玉屏风散药液(黄芪、白术、防风药材饮片均购自成都杏林大药房,批号20060902),依据《中国药典》(2010版)第一部玉屏风散项下标准配伍及制备工艺制备,生药含量2g/ml;氯雷他定(国药准字: H20070030,由西安杨森药业生产;规格:10mg/片)。
1.2实验动物
Sprague-Dawley(SD)大鼠40只由泸州医学院实验动物中心提供,许可证号SCXK(川)2014-028,SPF级,均为3月龄雌性,体重为160~200g,标准条件下适应性喂养1周。
1.3药物及试剂
卵白蛋白(美国Sigma公司,1001445093);氢氧化铝[Al(OH)3](上海桃浦化学试剂公司,070621);IgE试剂盒(美国BioLegend公司,AE9401Ra);IL-4和IFN-γ试剂盒(美国R&D公司进口分装),购自武汉博士德生物工程有限公司(EK0405、EK0374)。
2方法
2.1实验动物分组
SD大鼠40只随机分为正常组、模型组、阳性药对照组和YPFS组4组,每组10只。
2.2建立模型
建立模型组、阳性药对照组和YPFS组卵白蛋白(Ovalbumin,OVA)致敏模型[5]:第1天腹腔注射含10μg OVA及1mg[A1(OH)3]的无菌生理盐水0.5ml进行基础致敏,第5天腹腔注射含l0μg OVA的无菌生理盐水0.5ml强化致敏,第6天开始每日1次用50μl的2mg/ml OVA滴鼻,连续14天激发大鼠,观察其喷嚏、挠鼻的次数和流涕,参照文献[7]制定表1,评分大于5分造模为成功,30只大鼠均造模成功。正常组则用无菌生理盐水按照同样过程进行假致敏和假激发。

表1 大鼠变应性反应鼻部症状的评分标准
2.3给药
YPFS组给予玉屏风散药液12g/kg[6];阳性药对照组氯雷他定5mg/kg,用无菌生理盐水稀释,灌胃给药;正常对照组使用同等剂量的无菌生理盐水灌胃。给药期间仍给予持续局部抗原攻击,各组于滴鼻前1小时给药,每天1次,共7次。
2.4动物行为学观察
观察各组大鼠鼻痒、鼻涕和喷嚏的过敏反应行为,记录各组大鼠最后1次激发的24小时后评分。
2.5计数嗜酸性粒细胞(EOS)
鼻分泌物涂片检查。各组大鼠最后1次激发的24小时后微型小棉棒伸入大鼠鼻腔轻擦鼻甲表面3次,制作涂片,HE染色,光镜下(×100)观察并行EOS计数。每张切片观察5个视野,取平均值。
2.6细胞免疫因子的检测
各组大鼠最后1次激发的24小时后,用3%戊巴比妥钠(40mg/kg)腹腔注射麻醉大鼠由腹主动脉内抽血8ml,通过离心分离出血清,采用ELISA法检测各试验组大鼠血清IgE、IL-4和IFN-γ的含量。
3统计学处理
所有数据采用SPSS 16.0软件包进行分析,用ANOVA和Ridit分析,数据以(x¯±s)表示,P<0.05表示差异有统计学意义。
结果
1观察模型组行为
各组大鼠鼻痒、鼻涕和喷嚏的过敏反应行为评分比较(见表2)结果表明,模型组与正常组、阳性药对照组、YPFS组比较,差异有统计学意义(P<0.05);YPFS组与阳性药对照组比较,差异无统计学意义(P>0.05)。提示YPFS组大鼠鼻部过敏症状明显缓解,与阳性药对照组比较统计学上无差别。

表2 大鼠变应性反应鼻部症状的评分(x¯±s)
2各组大鼠鼻腔分泌物EOS计数、血清IgE、IL-4 和IFN-γ的含量比较(见表3、图1、图2和图3),模型组大鼠鼻腔分泌物EOS计数高于正常组;血清IgE和IL-4的含量升高,高于正常组;血清IFN-γ的含量降低,低于正常组,差异均有统计学意义(P<0.05)。YPFS组和阳性药对照组鼻腔分泌物EOS计数低于模型组,血清IgE和IL-4的含量降低,低于模型组;血清IFN-γ含量升高,高于模型组,差异均有统计学意义(P<0.05)。YPFS组与阳性药对照组鼻腔分泌物EOS计数、血清IgE、IL-4和IFN-γ的含量比较,差异无统计学意义(P>0.05)。

表3 大鼠鼻腔分泌物EOS计数、血清Ig E、IL-12和IFN-γ和含量比较(x¯±s)

图1 模型组鼻腔分泌物HE染色×20
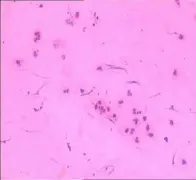
图2 YPFS组鼻腔分泌物HE染色×20

图3 阳性药对照组鼻腔分泌物HE染色×20
讨论
从免疫学角度来看,AR是体外环境因素作用于机体导致的异常免疫反应,造成Thl和Th2免疫反应失衡而引发的、以鼻腔黏膜Th2免疫反应为主的变应性炎症反应,其主要的免疫病理学特征是组织中大量表达Th2细胞因子的细胞浸润[8]。研究证据表明,通过诱导Thl型细胞的反应来调节Th2型细胞的细胞因子分泌谱可以改善与Th2相关的疾病[9]。Thl细胞的功能主要依赖IFN-γ实现,而Th2细胞功能主要依赖IL-4等。IL-4及其他Th2细胞因子,辅助招募可产生IgE抗体并能诱导过敏发生的B细胞、肥大细胞及嗜酸性粒细胞(EOS)等[10]。IgE抗体与嗜碱性粒细胞及肥大细胞相结合后能够激活被IgE致敏的细胞,分泌多种炎症介质引起相应的临床症状。本实验中模型组大鼠鼻腔分泌物EOS计数、血清IgE和IL-4含量明显高于正常组,IFN-γ含量低于正常组。提示Th1/Th2淋巴细胞亚群平衡及自身调节对变应性鼻炎的发生发展可能有着极其重要的作用。
玉屏风散由黄芪、白术和防风三味药组成,具有益气健脾、固表止汗的功效,用于治疗气虚基表不固兼感风寒之自汗症。因为该方疗效好,使用较广,被《中华人民共和国药典》所收载。随着研究的深入,其治疗作用和药理作用主要体现在对免疫功能的调节和影响。玉屏风散可以增强患者的体质,提高机体免疫功能,促进IgA、IgG、IgE和单核巨噬细胞的分泌[11]。观察玉屏风散对荷瘤小鼠免疫功能的影响,发现玉屏风散给药后小鼠脾脏T细胞增殖能力明显增强,IFN-γ、IL-2的产生明显升高,血清IL-4、IL-10含量下降[12];玉屏风散对小鼠气道变态反应性疾病中可以增强Th1细胞表达,同时提高Th1/Th2比值[13],提示玉屏风散可以通过调节细胞因子,促进免疫应答,改善机体情况。在本实验中,YPFS治疗组大鼠鼻部症状明显好于模型组,鼻腔分泌物EOS计数、血清IgE和IL-4含量明显低于模型组,IFN-γ含量高于模型组,而与阳性药物对照组无明显差别,提示玉屏风散可以调节Th1/Th2淋巴细胞亚群平衡,诱导Th向Th1分化,抑制Th2的表达,促进IFN-γ的产生,抑制IL-4的形成,并降低IgE的水平,从而减轻EOS的活化和浸润,以调节变应性鼻炎大鼠的免疫功能,减轻变应性鼻炎的炎症反应,达到治疗目的。该方剂是种复杂的混合药物,其药理作用的影响还需结合分子生物学与细胞生物学进一步研究,为其适应证提供充分的实验室依据。
1胡晓艳,姜梁.乳酸杆菌对过敏性鼻炎模型大鼠免疫功能的影响[J].重庆医学,2013,42(23):2752-2754.
2汪中宽.玉屏风散防治“哮喘病”的研究进展[J].菏泽医学专科学校学报,2006,18(1):91.
3高锐卿,苗相本.玉屏风散在呼吸系统疾病中的药理及临床研究进展[J].浙江中医杂志,2003,21(7)318-319.
4李兴平.玉屏风散的免疫药理研究[J].陕西中医学院学报,2000,23(2):36.
5陈忠,唐法娣.大鼠过敏性鼻炎模型建立及应用[J].浙江大学学报(医学版),2001,30(6):276-277.
6赵秀杰,董震,杨占泉,等.超敏反应实验模型的建立.中华耳鼻咽喉科杂志,1993,28(1)∶17-18.
7张仲林,钟玲,袁明勇等.玉屏风散对变应性鼻炎肥大细胞活性的抑制作用[J].中药药理与临床,2014,30(1):1-4.
8Kay AB.Allergy and allergic diseases:first of two parts[J].N Engl J Med,2001,344(3):330-337.
9Singh V K,Mehrotra S,Agarw ALS.The paradigm of Thl and Th2 cytokines:its relevance to autoimmunity and allergy[J].ImmunoI Res,1999,20(1):147-161.
10Maggi E.The TH1/TH2 paradigm inallergy[J].Immunotechnology,1998,3:233-244.
11张伟,周兆山,贾新华.养血益气温阳法治疗慢性支气管炎及其免疫指标影响[J].中华中西医杂志,2001,2(14):1266.
12张红军,唐小云,鞠宝玲,等.玉屏风散对S180荷瘤小鼠Th1/Th2型细胞因子的影响[J].热带医学杂志,2008,8 (4):346.
13顾珺,蒋瑾瑾,沈朝斌,等.玉屏风散对小鼠气道变态反应性疾病Th1/Th2平衡的影响 [J].上海中医药杂志,2005,39(7):50.
(收稿:2015-01-12修回:2015-02-02)
Effects of Yu ping feng san on allergic rhinitis rat models of the influence of the levels of IgE,IL-4 and IFN-r
WANG Fang,HU Xiaoyan
Department of Otolaryngology,416th Hospital,Ministry of Nuclear Industry,Chengdu,610051,China
Objective Explore the influence in YPFS on allergic rhinitis(AR)rates of the serum IgE,IL-4 and IFN-r levels. Methods With ovalbumin as sensibilisinogen,the rats allergic rhinitis model was established.Rats were divived into normal group,model group,YPFS group and positive drug control group.We observed the ethological perfmance of rats,examend oxyphile leukocytes in nasal secretion and the contents of IgE、IL-4 and IFN-r in blood serum.Results YPFS could obviously relieve allergic rhinitis symptoms of rhinocnesmus,and sneezing,clear nasal discharge,reduce EOS infiltration and nasal mucosal thickening in rat allergia models(P<0.05),model groupIgE、IL-4 content was significantly higher than normal control group(P<0.05),IFN-r levels are lower than the normal control group(P<0.05).YPFS group IL-4 content was significantly lower than the model group (P<0.05),IFN-r content increased higher than the model group(P<0.05).The index of lactobacillus group with positive drug compared difference was statistically significant.Conclusion YPFS can relieve the nasal symptoms in allergic rhinitis rats,adjust Th1/Th2 lymphocyte subsets balance,reduce nasal mucosa allergic inflammation.
YPFS;allergic rhinitis;immunologic function
胡晓艳,副教授.Email:huxiaoyan417@163.com
10.16542/j.cnki.issn.1007-4856.2016.02.001

