双水相体系萃取分离金属离子研究进展
张永强,孙体昌,郭 清,侯青霞,郭英超,卢铁强,燕春环
(1.北京科技大学土木与环境工程学院,北京100083;2.燕山大学环境与化学工程学院)
双水相体系萃取分离金属离子研究进展
张永强1,2,孙体昌1,郭清2,侯青霞2,郭英超2,卢铁强2,燕春环2
(1.北京科技大学土木与环境工程学院,北京100083;2.燕山大学环境与化学工程学院)
双水相体系是一种绿色环保的新型分离技术,应用领域相当广泛,是近年来的研究热点。论述了双水相体系用于萃取分离金属离子的研究现状。根据所使用萃取剂的不同分3种情况进行了论述:不添加任何萃取剂直接萃取金属离子;以无机阴离子为萃取剂,依靠金属阳离子与无机阴离子形成的阴离子配合物(螯合物)而转移到萃取相,萃取金属离子;采用有机试剂作为萃取剂,依靠金属离子与萃取剂反应形成的中性配合物(螯合物)而转移到萃取相,萃取金属离子。论述了双水相体系萃取分离金属离子的发展趋势:建立金属离子在双水相体系中分配的机理模型;双水相体系成相物质的回收及再利用;通过无机盐水化能力的差异,或者通过双水相体系的温度诱导相分离,实现无机盐的分离与常温制备;开展双水相体系萃取分离金属离子的工程研究。
双水相体系;研究进展;金属离子
1896年,M.W.Beijerinck通过混合一定浓度的明胶和琼脂的水溶液,观察到溶液由浑浊逐渐转变为澄清的两个水相,从而发现了双水相现象[1]。20世纪90年代,随着生物技术的不断发展及对分离技术的需求,双水相萃取才逐渐受到广泛重视。经过多年的发展,双水相体系在理论和应用研究方面均取得了令人瞩目的成就。双水相体系是指,在一定条件下某些水溶液自发形成两个互不相溶的水相,两相均为水溶液且具有清晰相界面,这样的体系称为双水相体系(Aqueous Two-Phase System,ATPS)[2]。与传统的有机溶剂液液萃取体系相比,双水相体系一般无毒无害、不易挥发、生物降解性好、两相大部分为水 (以摩尔分数计),不存在有机溶剂残留问题,是一项对环境友好的新型分离技术[3]。双水相体系应用十分广泛,到目前为止研究报道的萃取分离的溶质种类众多,如生物活性物质[4-5]、有机物[6]等。笔者重点讨论双水相体系在萃取分离金属离子中的研究现状及发展趋势。
1 双水相体系萃取分离金属离子研究进展
双水相体系萃取原理与传统的有机溶剂液液萃取类似,但与传统的液液萃取分配关系相比其影响因素更加复杂,这是由于双水相体系两相间的性质差异较小产生的。当溶质进入双水相体系后,由于电荷、质量(体积)、浓度以及存在形态等不同,在一定操作条件下不同溶质的疏水性产生差异,使其在上、下相中的分配比不同,从而实现溶质的提取浓缩以及不同溶质间的定量分离,其分配规律同样服从能斯特(Nernst)分配定律。影响溶质在双水相体系中分配性能的主要因素有成相物质的种类及浓度、溶质特性(如电荷、质量、浓度)、溶液中其他离子的种类及浓度、操作条件(如pH、温度)等。
在双水相萃取分离金属离子的研究中,金属离子在双水相体系中的分配方式根据所使用萃取剂的不同分为3种情况:1)在不添加任何萃取剂的条件下直接萃取金属离子;2)以无机阴离子为萃取剂,依靠金属阳离子与无机阴离子形成的阴离子配合物(螯合物)而转移到萃取相;3)采用有机试剂作为萃取剂,依靠金属离子与萃取剂反应形成的中性配合物(螯合物)而转移到萃取相。
1)不添加任何萃取剂。由于双水相体系的萃取相具有相对疏水环境,而绝大多数金属离子的极性较强、水化自由能较大(绝对值),因此在不添加适宜萃取剂的情况下金属离子很难被萃取。但是对于少数具有较大体积、较小荷质比的金属阴离子,因其具备一定的疏水性及较高的离液序列性,也有可能直接被萃取到萃取相中。该类萃取体系的特点是不使用任何无机或有机萃取剂,体系组成简单,有利于成相物质的循环利用。
锝、铼是与钨精矿、钼精矿伴生的稀散金属,含量极低且具有放射性,应用广泛,价格昂贵,因此从钨酸盐和钼酸盐溶液中回收锝、铼具有重要意义。此外,核废料中低浓度锝、铼的回收再利用也受到广泛重视。Rogers等[7-10]研究了TcO4-和ReO4-在双水相萃取体系中的分配行为。结果表明,在无任何萃取剂情况下TcO4-和ReO4-即可优先被分配到萃取相,而MoO42-和WO42-则留在富盐相。主要原因是TcO4-和ReO4-具有较大的疏水性和较小的吉布斯(Gibbs)水化自由能(绝对值)。成相盐和聚合物的种类及浓度对TcO4-的分配比具有较大的影响。6种成相聚合物聚丙二醇(PPG2000)、聚乙烯吡咯烷酮(PVP-K15)、聚 乙 二 醇(PEG2000、PEG3400、PEG12000)以及丙二醇嵌段聚醚L64,随其疏水性增加TcO4-分配系数呈减小趋势,但随(NH4)2SO4浓度增加而增大。随成相盐水化能力增强TcO4-分配系数增大。对PEG2000-无机盐[NaOH、K2CO3、(NH4)2SO4、K3PO4]双水相体系,TcO4-的分配系数随成相盐和聚合物浓度的增加而增大。在成相盐浓度相等的情况下,其对TcO4-萃取能力由大到小的顺序是PO43-> SO42->CO32->OH-;Na+>NH4+>Rb+>Cs+。这与上述盐的盐析能力的规律一致,表明成相盐阴离子(阳离子)的水化自由能ΔGhyd越小,其盐析能力越强,两相组成差异越大,对TcO4-在富PEG中的分配越有利。对于PEG2000-NaOH-H2O体系,TcO4-和ReO4-分配比均随NaOH储备液浓度的增加而增大。在低浓度Na2MoO4和Na2WO4溶液中,TcO4-和ReO4-的分配比与 Na2MoO4和 Na2WO4浓度无关;而在高浓度Na2MoO4和Na2WO4溶液中,TcO4-和ReO4-的分配比随Na2MoO4和Na2WO4浓度的增加而增大。TcO4-和ReO4-的分配比在ReO4-浓度大于0.1 mol/L之后均呈缓慢减小趋势。采用Kirchhoff定律对TcO4-分配热力学研究结果表明,萃取过程的标准吉布斯自由能ΔG0为负值,且随温度升高而减小[11]。此外,作者[12]还研究了TcO4-在离子液体1-丁基-3-甲基-氯化咪唑与无机盐(K3PO4、K2HPO4、K2CO3)组成的双水相萃取体系中的分配行为。结果表明,TcO4-在3种双水相萃取体系中均有较高的分配系数,且随双水相体系系线长度的增加而增大;当体系中加入SnCl2时,TcO4-的分配系数明显减小。但负载于离子液体中的TcO4-的反萃效果较差。牟婉君等[13]也研究了在PEGNaOH[K2CO3、(NH4)2SO4]双水相体系中 ReO4-与MoO42-的萃取分离行为。结果表明:在6 mol/L的NaOH体系下二者的萃取分离效果最好,在不添加任何萃取剂情况下ReO4-均可被定量萃取到富PEG相,最高萃取率达到96.8%(质量分数)。通过加入掩蔽剂酒石酸盐与MoO42-形成配合物的方法,可以有效降低MoO42-的萃取率,其萃取率低于10%(质量分数),实现了MoO42-与ReO4-的萃取分离。为研究ReO4-萃取机理,加入3种表面活性剂,即阳离子表面活性剂溴化十六烷基吡啶(CPB)、阴离子表面活性剂十二烷基硫酸钠(SDS)和非离子表面活性剂Triton X-100,其中只有阳离子表面活性剂CPB使ReO4-的萃取率明显减小,表明PEG相易萃取带负电荷的配合物阴离子,与一般有机溶剂萃取机制不同。Akama等[14]采用四丁基溴化铵(TBAB)-(NH4)2SO4-H2O双水相体系从Cr(Ⅲ)中萃取分离Cr(Ⅵ),并应用于废水样品中Cr(Ⅵ)的测定,结果较为准确。萃取机理分析认为,在酸性条件下HCrO4-和TBA+形成了中性离子对配合物[HCrO4-·TBA+]而被萃取到TBAB相。Safiulina等[15]在研究U(Ⅵ)的萃取性能时发现,随PEG分子量增加U(Ⅵ)的分配系数增大。萃取机理分析认为,在强碱性条件下U(Ⅵ)阳离子与PO43-形成了阴离子配合物,与PEG分子中的醚氧基团C—O—C和端羟基基团O—H依靠静电引力产生了相互作用。
2)无机阴离子作萃取剂。大部分过渡区金属阳离子均能与卤素阴离子、硫氰酸根等形成阴离子配合物,这些配合物具有较大的体积、较小的荷质比和离子势,因而疏水性显著提高,且能与有机分子中的O—H、C—O—C、C=O、COOH、COO等质子化基团依靠静电引力产生相互作用,从而被转移到萃取相中。该类萃取过程的特点是萃取效率高、分离性能优越;缺点是在萃余相中引入额外萃取剂阳离子,且一部分卤素、硫氰酸根阴离子也会残留在萃余相中,给后续分离过程带来不利影响。
Zvarova等[16]首次报道了部分金属离子在双水相体系PEG2000-(NH4)2SO4-H2O中的分配行为。在不添加任何萃取剂的情况下无机阳离子的分配系数均很小,而几种无机阴离子的分配系数则相对较大。在PEG2000质量分数为15%、(NH4)2SO4质量分数为14.4%的双水相体系中,部分无机离子 (浓度为1.0~5.0mol/L)的分配系数见表1。
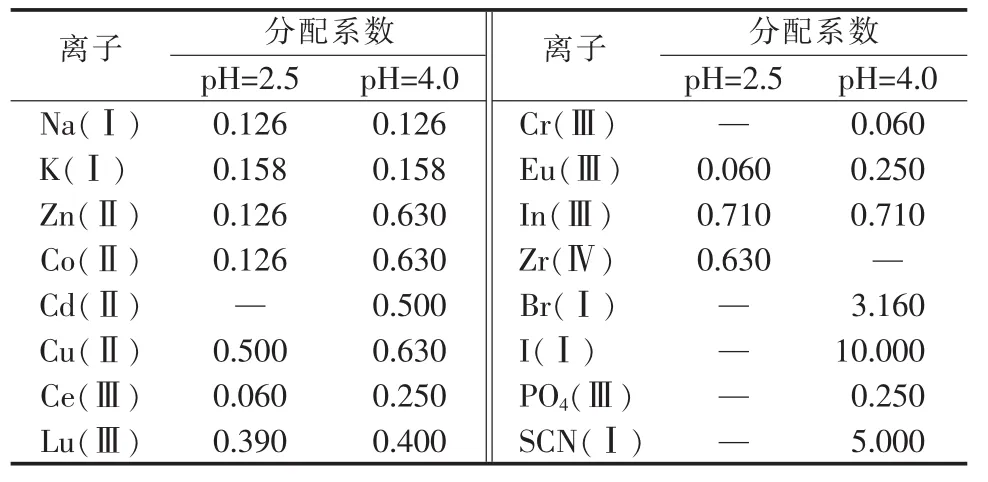
表1 在PEG2000-(NH4)2SO4双水相体系中部分无机离子分配系数
Wang等[17-18]采用异丙醇(i-PrOH)-(NH4)2SO4-H2O双水相体系,以 NH4SCN为萃取剂,分别对Cu(Ⅱ)、Cr(Ⅲ)的萃取工艺进行了优化,并用于测量血清中的Cu(Ⅱ)含量和血浆中的Cr(Ⅲ)含量。Akama等[19]采用四丁基溴化铵(TBAB)-(NH4)2SO4-H2O双水相体系,研究了从高浓度Co(Ⅱ)、Cu(Ⅱ)、Fe(Ⅲ)、Zn(Ⅱ)中萃取分离微量Cd(Ⅱ)的性能。结果表明,Cd(Ⅱ)能以[CdBr4]2-配合物阴离子形式被定量萃取到TBAB相,而Co(Ⅱ)、Cu(Ⅱ)、Fe(Ⅲ)的萃取率均小于1%(质量分数),Zn(Ⅱ)的萃取率为24%(质量分数),但对Cd(Ⅱ)的萃取率无影响。高云涛等[20-21]以卤素阴离子为萃取剂,较为系统地研究了双水相体系中贵金属Pt(Ⅱ)、Pd(Ⅱ)、Ir(Ⅱ)、Rh(Ⅲ)、Au(Ⅲ)等的萃取分离性能,实现了贵金属与碱金属的定量分离。红外光谱(FT-IR)分析表明,贵金属-卤素阴离子配合物与有机相中的C—O—C、O—H、C=O等基团存在一定的键合作用。张天喜等[22]在研究Au(Ⅰ)的萃取中,通过FT-Raman光谱分析发现[Au(CN)2]-阴离子配合物并未与PEG分子产生强烈作用。Shibukawa等[23]采用 PEGNa2SO4-H2O双水相体系,以KSCN和KI为萃取剂,研究了水溶液中Mn(Ⅱ)、Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)和Li(Ⅰ)的萃取分离性能。在所研究的金属离子中,除Li(Ⅰ)外,其他金属离子均能与SCN-和I-形成阴离子配合物而被萃取到富PEG相。Liu等[24]采用i-PrOH-(NH4)2SO4-H2O双水相体系,以NH4I为萃取剂,研究了Cd(Ⅱ)的萃取分离性能。在最优条件下,Cd(Ⅱ)的萃取率高达99.2%(质量分数),且能实现与Fe(Ⅱ)、Ca(Ⅱ)、Mg(Ⅱ)、Mn(Ⅱ)、Al(Ⅲ)、Pb(Ⅱ)和Zn(Ⅱ)的定量分离。萃取机理分析认为是[CdI4]2-配合物与质子化的i-PrOH2+相互作用的结果。da Silva等[25]在研究[Fe(CN)5(NO)]2-和[Fe(CN)6]3-阴离子配合物在双水相体系中的分配行为时发现,随着成相聚合物亲水性增强[L35(丙二醇嵌段聚醚)<F68(丙二醇嵌段聚醚)<PEO(聚环氧乙烷)],二者的分配系数逐渐增大;随着温度升高,二者的分配系数呈减小趋势。Van′t Hoff方程和量热测量结果表明,分配过程为焓驱动过程。在采用L35-Li2SO4-H2O双水相体系、以KI为萃取剂、研究废旧Cd-Ni电池盐酸浸出液中Cd(Ⅱ)和Ni(Ⅱ)的萃取分离性能的过程中[26],当KI用量在100 mmol/kg以上时,Cd(Ⅱ)的萃取率接近100%(质量分数),而Ni(Ⅱ)的萃取率低于1%(质量分数)。这是因为Cd(Ⅱ)和Ni(Ⅱ)与KI形成的阴离子配合物与L35中EO单元的亲和力不同所致,即EO-[Cd(I4)]2->>EO-[Ni(I4)]2-。同时Li+与EO单元能形成拟聚阳离子,也进一步促进了阴离子配合物依靠静电引力在L35相的分配。在采用4种双水相体系L35-Li2SO4-H2O、L35-(NH4)2SO4-H2O、PEO1500-Li2SO4-H2O和PEO1500-(NH4)2SO4-H2O,以KSCN为萃取剂,研究Co(Ⅱ)、Fe(Ⅲ)、Ni(Ⅱ)的萃取分离性能时[27],4种双水相体系中PEO1500+ (NH4)2SO4+H2O体系的分离性能最好,在 pH=4、KSCN用量为1.4 mmol时,Co(Ⅱ)、Fe(Ⅲ)、Ni(Ⅱ)的最高萃取率 (质量分数)分别为99.8%、12.7%和3.17%,分离因子SCo/Fe=3 440、SCo/Ni=15 300;在pH=2时,Fe(Ⅲ)、Ni(Ⅱ)的最高萃取率(质量分数)分别为99.5%和4.34%,分离因子SFe/Ni=4 380。成相聚合物的疏水性对金属离子的萃取分离性能也有较大影响,随着疏水性增大(L35>PEO1500),萃取率和分离因子均增大。Bulgariu等[4,28-29]采用 PEG-Na2SO4[(NH4)2SO4]-H2O双水相体系,以卤离子为萃取剂,系统研究了水溶液中 Zn(Ⅱ)、Cd(Ⅱ)、Hg(Ⅱ)、Pb(Ⅱ)、Au(Ⅲ)的萃取分离性能。FT-IR分析表明,对于Cd(Ⅱ)、Hg(Ⅱ)、Pb(Ⅱ)阴离子配合物与PEG之间并非因产生配位作用而被萃取到富PEG相,而是依靠水分子与PEG中的EO单元形成氢键从而使EO单元中的O原子带有正电荷,与阴离子配合物产生静电引力,萃取率按Cl-、Br-、I-配合物次序逐渐增大。而对于Zn(Ⅱ)则不同,其萃取过程是依靠固化于PEG相中的水分子与卤化锌分子形成氢键而被萃取,其分配系数按Cl-、Br-、I-配合物次序递减。在以Cl-为萃取剂萃取Au(Ⅲ)的研究中,在适宜条件下Au(Ⅲ)的萃取率超过98%(质量分数),而Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)、Pb(Ⅱ)则几乎不被萃取。
3)有机试剂为萃取剂。所用试剂一般为具有不同螯合基团的光度分析试剂,如甲基百里酚蓝(MB)、二甲酚橙(XO)、亚硝基R盐、7-氯-8-羟基喹啉-5-磺酸、偶氮胂Ⅲ(AZⅢ)、偶氮胂M、钍试剂、变色酸、磺基水杨酸、1-亚硝基-2-萘酚(1N2N)、1-(2-吡啶偶氮)-2-萘酚(PAN)、1-(2-噻唑偶氮)-2-萘酚(TAN)、4-(2-吡啶偶氮)-间苯二酚(PAR)、4-(2-噻唑偶氮)-间苯二酚(TAR)、双硫腙(DTZ)等,还包括一些碱性染料,如结晶紫、亮绿等。上述有机试剂与金属离子形成的配合物(螯合物)的稳定常数通常较高且具有一定的疏水性,因此很容易将金属离子配合物萃取到相对疏水的萃取相中。该类萃取体系的特点是分配系数高、分离因子大;缺点是萃取剂有毒有害、生物降解性差,有些试剂的水溶性较小,且大量使用时会对人体和环境造成危害。
Rogers等[30]综述了以光度分析试剂为萃取剂,镧系和锕系等稀土元素在PEG-盐双水相体系中的萃取分离研究进展。Visser等[31]以偶氮类染料PAN、TAN、PAR、TAR为萃取剂,系统研究了水溶液中Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)、Cs(Ⅰ)、Cd(Ⅱ)、Eu(Ⅲ)在PEG-(NH4)2SO4-H2O双水相体系中的分配行为。结果表明,Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)的分配比均较大且随着萃取剂浓度的增加而增大,而Cs(Ⅰ)、Cd(Ⅱ)、Eu(Ⅲ)的分配比均较小且与萃取剂浓度无关。萃取机理分析认为,去质子化的萃取剂阴离子与Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)阳离子形成了中性配合物,导致其疏水性增强,从而萃取到富PEG相。Rodrigues等[32-35]以1N2N和PAN为萃取剂,系统研究了水溶液中Fe(Ⅲ)、Co(Ⅱ)、Ni(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)的萃取分离性能。在适宜条件下,可以从Cd(Ⅱ)中分离Co(Ⅱ)、Ni(Ⅱ)、Fe(Ⅲ),从Fe(Ⅲ)、Zn(Ⅱ)、Cd(Ⅱ)混合水溶液中分离Co(Ⅱ);还可以实现Cu(Ⅱ)与伴生离子Zn(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)、Fe(Ⅲ)的分离。在研究Co(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)的分离性能时,采用L64-Na2C4H4O6-H2O和 L64-Li2SO4-H2O两种双水相体系,以1N2N为萃取剂。实验结果表明:在pH=1.00 时Co(Ⅱ)、Ni(Ⅱ)分离因子为826,在pH=3.00时Co(Ⅱ)、Cd(Ⅱ)和Ni(Ⅱ)、Cd(Ⅱ)分离因子分别为1 550和16 700;并且在Cd(Ⅱ)、Ni(Ⅱ)浓度20倍于Co(Ⅱ)时,Co(Ⅱ)也可以被定量萃取,而Cd(Ⅱ)、Ni(Ⅱ)的萃取率与低浓度时相同,均较低。在研究Cu(Ⅱ)、Zn(Ⅱ)的萃取分离性能时,采用L64-MgSO4-H2O、L64-Li2SO4-H2O、L64-Na2C4H4O6-H2O 3种双水相体系,以1N2N为萃取剂,在适宜条件下二者的萃取率(质量分数)均达到90%以上。在L64-Na2C4H4O6-H2O体系、溶液 pH=3、系线长度为41.28%(m/m)、1N2N与金属物质的量比为3的条件下,Cu(Ⅱ)、Zn(Ⅱ)分离因子达到最大值204。萃取机理分析认为是金属阳离子与萃取剂阴离子形成了中性配合物而被萃取。Das等[36]采用TX-100-Na2SO4-H2O和TX-100-Na3C6H5O7-H2O两种双水相体系,以DTZ为萃取剂,研究了Hg(Ⅱ)、Pb(Ⅱ)、Bi(Ⅲ)的萃取分离性能。结果表明,对于两种双水相体系,不管是否加入萃取剂,Bi(Ⅲ)均不能被萃取;对于TX-100-Na3C6H5O7-H2O体系,不加萃取剂时Hg(Ⅱ)、Pb(Ⅱ)的萃取率均随pH的升高而增大,加入萃取剂时Pb(Ⅱ)不被萃取而Hg(Ⅱ)萃取率的变化与不加萃取剂时相同,这是由于形成了Hg(Ⅱ)-Na3C6H5O7络合物且稳定性优于Hg(Ⅱ)-DTZ络合物;对于TX-100-Na2SO4-H2O体系,在不添加萃取剂的情况下,Hg(Ⅱ)的萃取率随pH升高而减小、Pb(Ⅱ)的萃取率随pH升高而增大。从而可以实现3种重金属离子的定量分离。
2 双水相体系萃取分离金属离子发展趋势
从上述论述中可以看出,双水相体系在萃取分离金属离子的研究中取得了为数众多的研究成果,几乎涵盖了从主族到副族的所有金属离子,为工业化应用奠定了良好的实验基础。但仍有一些问题需要解决。
1)分配模型。由于金属离子在双水相体系中分配行为的影响因素较多,目前的研究工作几乎都是建立在实验数据基础上,缺乏对金属离子在双水相体系中分配机理的研究以及分配系数的理论预测[37]。因此,建立金属离子在双水相体系中分配的机理模型将是下一步双水相体系相关研究的重点和难点。
2)成相物质的循环利用。双水相体系成相物质的回收及再利用是双水相体系获得工程应用的基础,可以有效降低成本、保护生态环境。目前这方面的研究报道较少[38-39],还需要进行大量的研究工作。
3)无机盐的制备。目前绝大部分无机盐的制备均采用蒸发浓缩、结晶工艺,需要消耗大量的能量。根据双水相体系的特点,通过无机盐水化能力的差异[40],或者通过双水相体系的温度诱导相分离[41],均有可能实现无机盐的分离与常温制备,这是无机盐工业未来的发展方向之一。
4)工程研究。双水相体系在萃取设备中的流体力学和传质性能是其工业化应用的关键,是萃取设备设计和操作的基础。目前的工程研究主要集中在生物活性物质方面[42-45],还没有关于双水相体系萃取分离金属离子的工程研究方面的报道。因此,有必要开展这方面的研究工作,为工程应用提供理论指导。
3 结论
双水相萃取作为一种绿色、环保的新型分离技术,具有操作条件温和、工艺及设备简单、溶质分配系数高、分离因子大、能耗低和环境污染小等特点,在湿法冶金、废水处理、生物化工、生物制药、无机盐制备等领域具有广阔的应用前景。
[1]HaghtalabA,AsadollahiMA.AnexcessGibbs energy model to study the phase behavior of aqueous two-phase systems of polyethylene glycol+dextran[J].Fluid Phase Equilibr.,2000,171(1/2):77-90.
[2]颜肖慈,罗明道.界面化学[M].北京:化学工业出版社,2005:79.
[3]Bulgariu L,Bulgariu D.Extraction of gold(Ⅲ)from chloride media in aqueous polyethylene glycol-based two-phase system[J].Sep. Purif.Technol.,2011,80(3):620-625.
[4]Nascimento C O,Soares P A G,Porto T S,et al.Aqueous two-phase systems:new strategies for separation and purification of lectin from crude extract of Cratylia mollis seeds[J].Sep.Purif.Technol.,2013,116:154-161.
[5]Tou B S Y,Neo K E,Tey B T,et al.Effect of phase inversion and separation on hepatitis B core antigen extraction from unclarified bacterial feedstock using aqueous two-phase system[J].Sep.Purif. Technol.,2014,130:45-55.
[6]Ingram T,Mehling T,Smirnova I.Partition coefficients of ionizable solutes in aqueous micellar two-phase systems[J].Chem.Eng.J.,2013,218:204-213.
[7]Rogers R D,Bond A H,Bauer C B.Partitioning behavior of99Tc and,129I from simulated Hanford tank wastes using polyethyleneglycol based aqueous biphasic systems[J].Solvent Extr.Ion Exch.,1995,13(4):689-713.
[8]Rogers R D,Zhang J H.Effects of increasing polymer hydrophobicity on distribution ratios of TcO4-in polyethylene/poly(propylene glycol)-based aqueous biphasic systems[J].J.Chromatogr.B,1996,680(1/2):231-236.
[9]Rogers R D,Bond A H,Bauer C B,et al.Metal ion separations in polyethylene glycol-based aqueous biphasic systems:correlation of partitioning behavior with available thermodynamic hydration data [J].J.Chromatogr.B,1996,680(1):221-229.
[10]Spear S K,Griffin S T,Huddleston J G.Radiopharmaceutical and hydrometallurgical separations of perrhenate using aqueous biphasic systems and the analogous aqueous biphasic extraction chromatographicresins[J].Ind.Eng.Chem.Res.,2000,39(9):3173-3180.
[11]Dilip M,Griffin S T,Spear S K,et al.Comparision of temperature effects on the salting out of poly(ethylene glycol)versus poly (ethylene oxide)-poly(propylene oxide)random copolymer[J]. Ind.Eng.Chem.Res.,2010,49(5):2371-2379.
[12]Bridges N J,Rogers R D.Can kosmotropic salt/chaotropic ionic liquid(salt/salt aqueous biphasic systems)be used to remove pertechnetate from complex salt waste?[J].Sep.Sci.Technol.,2008,43(5):1083-1090.
[13]牟婉君,李兴亮,刘国平.聚乙二醇双水相体系中铼、钼萃取性能研究[J].稀有金属材料与工程,2011,40(6):1102-1104.
[14]Akama Y,Sali A.Extraction mechanism of Cr(Ⅵ)on the aqueous two-phase system of tetrabutylammonium bromide and(NH4)2SO4mixture[J].Talanta,2002,57(4):681-686.
[15]Safiulina A M,Tananaev I G.Extraction of U(Ⅵ)with poly(ethylene glycol)in two-phase aqueous systems containing various anions[J].Radiochemistry,2004,46(5):457-460.
[16]Zvarova T I,Shkinev V M,Vorob′eva G A.Liquid-liquid extraction in the absence of usual organic solvents:Application of two-phase aqueous systems based on a water-soluble polymer[J].Microchim. Acta,1984,84(5):449-458.
[17]Wang Z H,Zeng Y,Ma H M,et al.Two-phase aqueous extraction of copper(Ⅱ)and its application to speciation analysis of serum copper[J].Microchem.J.,1998,60(2):143-152.
[18]Wang Z H,Song M,Ma Q L,et al.Two-phase aqueous extraction of chromium and its application to speciation analysis of chromium in plasma[J].Microchim.Acta,2000,134:95-99.
[19]Akama Y,Ito M,Tanaka S.Selective separation of cadmium from cobalt,copper,iron(Ⅲ)and zinc by water-based two-phase systemof tetrabutylammonium bromide[J].Talanta,2000,53(3):645-650.
[20]高云涛,王华兰,茶军伟,等.吐温80-硫酸铵-水的固液体系萃取分离Pt(Ⅳ)、Pd(Ⅱ)、Ir(Ⅳ)碘络阴离子[J].贵金属,2000,21(3):31-33.
[21]Gao Y T,Wang W.Distribution behaviors of Pd(Ⅱ)in PrOH-(NH4)2SO4aqueous biphasic system and its application in determination of Pd(Ⅱ)[J].Precious Metals,2006,27(3):45-49.
[22]张天喜,李文钧,周维金,等.基于双水相体系的KAu(CN)2分配行为[J].北京大学学报:自然科学版,2001,37(2):197-199.
[23]Shibukawa M,Nakayama N,Hayashi T,et al.Extraction behaviour of metal ions in aqueous polyethylene glycol-sodium sulphate twophase systems in the presence of iodide and thiocyanate ions[J]. Anal.Chim.Acta,2001,427(2):293-300.
[24]Liu X H,Gao Y T,Tang R S.On the extraction and separation of iodide complex of cadmium(Ⅱ)in propyl-alcohol ammonium sulfate aqueous biphase system[J].Sep.Purif.Technol.,2006,50(2):263-266.
[25]da Silva L H M,da Silva M C H,Junior J A,et al.Hydrophobic effect on the partitioning of[Fe(CN)5(NO)]2-and[Fe(CN)6]3-anionsinaqueoustwo-phasesystemsformedbytriblockcopolymers andphosphatesalts[J].Sep.Purif.Technol.,2008,60(1):103-112.
[26]Lacerda V G,Mageste A B,Santos I J B,et al.Separation of Cd and Ni from Ni-Cd batteries by an environmentally safe methodology employing aqueous two-phase systems[J].J.Power Sources,2009,193(2):908-913.
[27]da Rocha Patricio P,Mesquita M C,da Silva L H M,et al.Application of aqueous two-phase systems for the development of a new method ofcobalt(Ⅱ),iron(Ⅲ)andnickel(Ⅱ)extraction:A green chemistry approach[J].J.Hazard.Mater.,2011,193:311-318.
[28]BulgariuL,BulgariuD.Extractionofmetalionsinaqueouspolyethylene glycol-inorganic salt two-phase systems in the presence of inorganic extractants:Correlation between extraction behavior and stability constants of extracted species[J].J.Chromatogr.A,2008,1196-1197(4):117-124.
[29]Bulgariu L,Bulgariu D.Selective extraction of Hg(Ⅱ),Cd(Ⅱ)and Zn(Ⅱ)ions from aqueous media by a green chemistry procedureusingaqueous two-phase systems[J].Sep.Purif.Technol.,2013,118:209-216.
[30]Rogers R D,Bond A H,Bauer C B.Metal ion separations in polyethylene glycol-based aqueous biphasic systems[J].Sep.Purif.Technol.,1993,28(5):1091-1126.
[31]Visser A E,Griffin S T,Hartman D H.Naphthol-and resorcinolbased azo dyes as metal ion complexants in aqueous biphasic systems[J].J.Chromatogr.B,2000,743(1/2):107-114.
[32]Rodrigues G D,da Silva M C H,da Silva L H M.Liquid-liquid extraction of metal ions without use of organic solvent[J].Sep.Purif. Technol.,2008,62(3):687-693.
[33]de Lemos L R,Santos I J B,Rodrigues G D.Copper recovery from ore by liquid-liquid extraction using aqueous two-phase system[J]. J.Hazard.Mater.,2012,237-238:209-214.
[34]Rodrigues G D,de Lemos L R,da Silva L H M.Application of hydrophobic extractant in aqueous two-phase systems for selective extraction of cobalt,nickel and cadmium[J].J.Chromatogr.A,2013,1279:13-19.
[35]de Lemos L R,Campos R A,Rodrigues G D.Green separation of copper and zinc using triblock copolymer aqueous two-phase systems[J].Sep.Purif.Technol.,2013,115:107-113.
[36]Das D,Sen K.Species dependent aqueous biphasic extraction of some heavy metals[J].J.Ind.Eng.Chem.,2012,18(2):855-859.
[37]Graber T A,Andrews B A,Asenjo J A.Model for the partition of metal ions in aqueous two-phase systems[J].J.Chromatogr.B,2000,743(1/2):57-64.
[38]YanB,CaoXJ.Phasediagramofnovelrecyclingaqueoustwo-phase systems composed of two pH-response polymers:Experiment and modeling[J].Fluid Phase Equilibr.,2014,364:42-47.
[39]Edahiro J,Sumaru K,Takagi T,et al.Photoresponse of an aqueous two-phasesystem composed of photochromic dextran[J].Langmiur,2006,22(12):5224-5226.
[40]Chen J X,Shi X N,Li Y H,et al.Selective partition of potassium chlorideandammoniumchloridebyaqueoustwo-phasesystems[J]. Sep.Purif.Technol.,2013,108:1-5.
[41]Milosevic M,Staal K J J,Schuur B,et al.Extractive concentration of aqueous salt solutions in aqueous two phase systems[J].Desalination,2013,324:99-110.
[42]Igarashi L,Kieckbusch T G,Franco T T.Mass transfer in aqueous two-phase system packed column[J].J.Chromatogr.B,2004,807(1):75-80.
[43]Biazus J P M,Santana J C C,Souza R R.Continuous extraction of α-and β-amylases from Zea mays malt in a PEG4000/CaCl2ATPS[J].J.Chromatogr.B,2007,858(1/2):227-233.
[44]Novak U,Pohar A,Plazl I,et al.Ionic liquid-based aqueous twophase extraction within a microchannel system[J].Sep.Purif.Technol.,2012,97:172-178.
[45]Rode S,Durand A,Mabille I,et al.Flooding characteristics of an aqueous two-phase system in a counter-current Kuhni-type column[J].Chem.Eng.Sci.,2013,98:98-103.
联系方式:suntc@ces.ustb.edu.cn
Research progress on extraction and separation of metal ions with aqueous two-phase system
Zhang Yongqiang1,2,Sun Tichang1,Guo Qing2,Hou Qingxia2,Guo Yingchao2,Lu Tieqiang2,Yan Chunhuan2
(1.School of Civil and Environmental Engineering,Beijing Science and Technology University,Beijing 100083,China;2.College of Environmental and Chemical Engineering,Y anshan University)
Aqueous two-phase system(ATPS)is a green,environmentally friendly,new separation technology and is of wide application prospect,and becomes an advanced research hotspot in recent years.It is discussed about the application research situation in extracting and separating metal ions by ATPS,which is divided into three aspects according to different extracting agents:directly extracting metal ion without any extracting agent,extracting metal ion complex by forming anion complex (chelate)between metal cation and inorganic anion extracting agent and metal cation and organic reagent extracting agent. The development tendency of extracting and separating metal ions by ATPS is predicted from four aspects:the first is to establish mechanism model of metal ions partition by ATPS;the second is to recover and recycle phase-forming substance of ATPS;the third is to achieve separation and normal temperature preparation of inorganic salts by hydration ability difference of inorganic salts or by temperature-induced phase separation of ATPS;and the fourth is to develop engineering research of extracting and separating metal ions by ATPS.
aqueous two-phase system;research progress;metal ions
O658
A
1006-4990(2016)06-0010-06
2016-01-19
张永强(1963—),男,副教授,主要研究方向为绿色化学工艺与分离过程。
孙体昌

