响应曲面法对铝灰中AlN的水解行为
张 勇,郭朝晖,王 硕,肖细元(中南大学 冶金与环境学院,长沙 410083)
响应曲面法对铝灰中AlN的水解行为
张 勇,郭朝晖,王 硕,肖细元
(中南大学 冶金与环境学院,长沙 410083)
铝冶炼过程中会产生大量铝灰,铝灰中AlN对其综合利用和安全处置会产生显著影响。在系统分析AlN水解热力学基础上,以再生铝生产过程中产生的铝灰为原料,运用Design Expert软件设计二次正交旋转试验,研究铝灰中AlN的水解特征。结果表明:在303~373 K的温度范围内,铝灰中AlN的水解自发进行;液固比和水解时间对水解pH影响显著(P<0.01);水解温度和液固比间的交互作用影响明显(P<0.01)。水解pH值与水解温度、液固比和水解时间的二次回归方程理论预测值与试验值相对误差仅为1%,可以用来预测和指导铝灰中AlN水解行为。
铝灰;AlN;水解;响应曲面
铝冶金过程中产生大量铝灰[1−2]。铝灰中不仅含大量 Al2O3,还含有一定量的 AlN,在水溶液反应中会释放NH3。因此,铝灰堆放、填埋或作为路基材料受到雨水淋溶后有可能造成环境污染[3−4]。DAVID等[5]研究表明,铝灰在作为优质耐火材料或路基材料前必须进行预处理,否则其中AlN会释放大量潜在的有毒或易燃气体。DASH等[6]对铝灰进行酸浸提铝的研究也发现同样的问题。LI等[7]在研究CO2对铝灰中铝重熔过程的影响中发现铝灰在反应中释放NH3,对环境体系构成威胁同时导致材料性能不稳定。因此,研究铝灰中AlN水解行为对铝灰资源综合化、无害化和可持续利用具有重要意义。
国内外对AlN水解已有研究报道。FUKUMOTO等[8]研究表明,铝灰中AlN水解过程存在两个行为:1) 当温度小于351 K,AlN水解生成Al(OH)3并释放出NH3;2) 当温度大于 351 K,AlN水解生成无定型AlOOH并释放出NH3,无定型AlOOH可进一步水解转化为Al(OH)3,反应体系中HCl和NaOH都会促进铝灰中AlN水解。姜澜等[9]研究表明,铝灰中AlN水解pH随水解温度升高、水解时间延长而变大,在373 K水解24 h后,AlN几乎全部转为Al(OH)3,298 K下,液固比2.5~15,液固比越小,水解pH越大。张宇等[10]研究发现80 ℃下AlN水解产物为AlOOH,在pH=5条件下,AlN形成了一个保护层,在pH=12条件下,氨水会使水解产物形成团聚。ZHANG等[11]研究发现添加硅胶或有机酸等表面剂可以降低AlN水解,从而减少NH3的释放,水解192 h后生成无定型Al(OH)3,红外谱图未见明显O—H键;水解250 h后生成晶型Al(OH)3,红外谱图可明显见到O—H键的存在。AZIZI等[12]利用响应曲面法对低品位锰矿提锰工艺进行优化,再结合统计分析和方差分析,确定硫酸浓度、草酸浓度、溶出时间和温度的较佳工艺条件,使锰、铁浸出率分别达到93.44%和15.72%。LI等[13]对微波焙烧氧化锌烟尘脱氟、氯研究中采用响应曲面法,优化工艺的同时还得到焙烧温度、保温时间对氟、氯的去除影响最显著。YANG等[14]基于响应曲面统计学原理优化无氧条件下蔗渣焙烧还原低品位软锰矿工艺,结果表明渣矿比和焙烧温度对浸出过程影响高于焙烧时间,渣矿比和焙烧温度的线性项,二次项及之间交互作用影响显著,焙烧时间的影响却较小。LI等[15]同样利用响应曲面法优化微波干燥富硒渣脱水率并进行验证,结果表明,试验结果与回归方程预测较一致。
然而,铝灰中AlN水解过程中,水解温度、水解时间和液固比等因子对水解pH的影响及各因子间的交互作用如何暂未见系统的研究报道。本文作者在对AlN热力学进行系统计算基础上,采用响应曲面法对AlN水解进行二次正交旋转组合试验设计,研究水解温度、液固比和水解时间3个单因素的显著程度以及因素间交互作用影响,利用统计分析和方差分析得到AlN水解pH二次回归方程,并对方程准确性进行验证,相关显著性结论及回归方程为铝灰中AlN水解pH数据进行一定补充,为铝灰综合利用提供科学依据。
1 实验
1.1 铝灰
供试铝灰来自江西某再生铝企业熔炼工艺的二次铝灰。将供试铝灰置于刚玉研钵中磨细,过孔径为150 μm筛后保存备用。SEM和EDS分析表明,供试铝灰表面呈不均匀、疏松多孔状。X荧光光谱仪分析进一步表明铝灰主要成分为铝和氧,分别占铝灰质量的30.72%和31.30%,此外,还含有少量的Na、Mg、F和Si。
对供试铝灰进行XRD分析,其XRD结果如图1所示。从图1可看出,铝灰中主要成分为Al、Al2O3、MgAl2O4及AlN,同时含有NaCl、CaF2等成分。
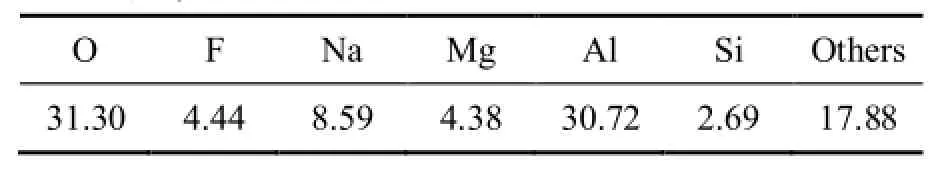
表1 铝灰主要化学成分Table 1 Chemical composition of aluminum dross (mass fraction, %)
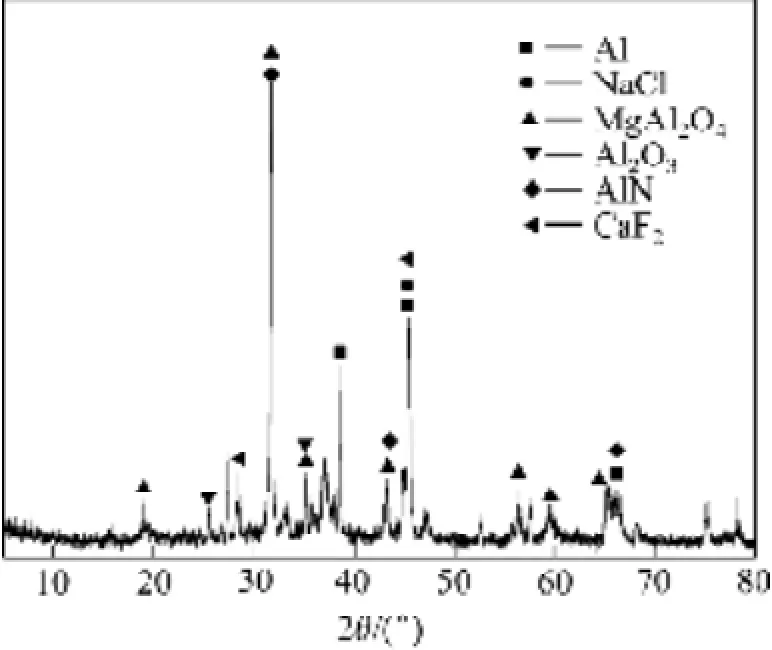
图1 铝灰的XRD谱Fig. 1 XRD pattern of aluminum dross

表2 AlN、H2O、Al(OH)3和NH3的热力学数据Table 2 Thermodynamic parameters for AlN, H2O, Al(OH)3and NH3, respectively
1.2 热力学计算原理
冶金热力学过程中,不同温度下反应的吉布斯自由能计算如下式所示:

n物质的化学计量数;(T)为n物质在温度T下的熵;cp为等压热容;(T)为T温度下生成熵与反应熵之差。AlN、H2O、Al(OH)3和NH34种物质热力学数据见表2[16−17]。
4种物质随温度变化的生成焓如下:


1.3 AlN水解二次正交旋转组合试验设计
采用Design Expert软件[18]设计铝灰中AlN水解反应试验,主要考察水解温度(A)、液固比(L/S,B)和水解时间(C) 3个因素对水解反应显著程度及三因素间交互作用的影响,具体设计见表3。

表3 反应因子编码表Table 3 Response factors code table
同时,采用3个单因素系列试验进行验证:固定水解温度30 ℃,液固比20,水解时间依次为10、30、50、70、90 min;固定液固比20,水解时间30 min,水解温度依次为 30、40、50、60 ℃;固定水解温度30 ℃,水解时间30 min,液固比依次为10、15、20、25。实验具体操作如下:称取5 g铝灰置于250 mL锥形瓶中,按试验设计液固比加入去离子水,然后将锥形瓶置于设定温度水浴锅(反应温度超过 100 ℃在油浴锅)中进行水解反应。
1.4 测试与分析
铝灰中AlN水解pH测定采用PHSJ−3FpH计(上海精科雷磁公司生产),铝灰微观形貌分析采用JSM−6360V扫描电子显微镜(日本电子公司生产),铝灰中主要元素及其含量分析采用AXIOS型X荧光光谱仪(荷兰 PANalytical生产),物相组成分析采用D/MAX 2500X型X射线衍射仪(日本理学公司生产)。
1.5 数据分析
为了确定自变量影响铝灰中AlN水解pH值,选择多项式模型对试验数据进行拟合,采用下面的多项式模型[19−20]:
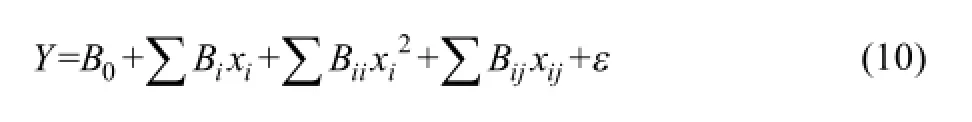
式中:Y为反应变量;B0因变量初始值;Bi、Bii、Bij分别为线性相、平方相、交互项的回归系数;xi、xj为不同变量的线性响应值(其中i≠j);为自变量非线性作用值;xij为两个独立变量交互作用值;ε为误差值。特别地,当优化目标是使独立变量最小化或最大化时,可分别采用如下最小或最大化公式:

式中:L和U分别为独立变量的上下限。
2 结果与讨论
2.1 AlN水解的热力学计算
常温条件下,铝灰中AlN水解方程:

AlN、H2O、Al(OH)3和NH34种物质随温度变化的生成焓如下:
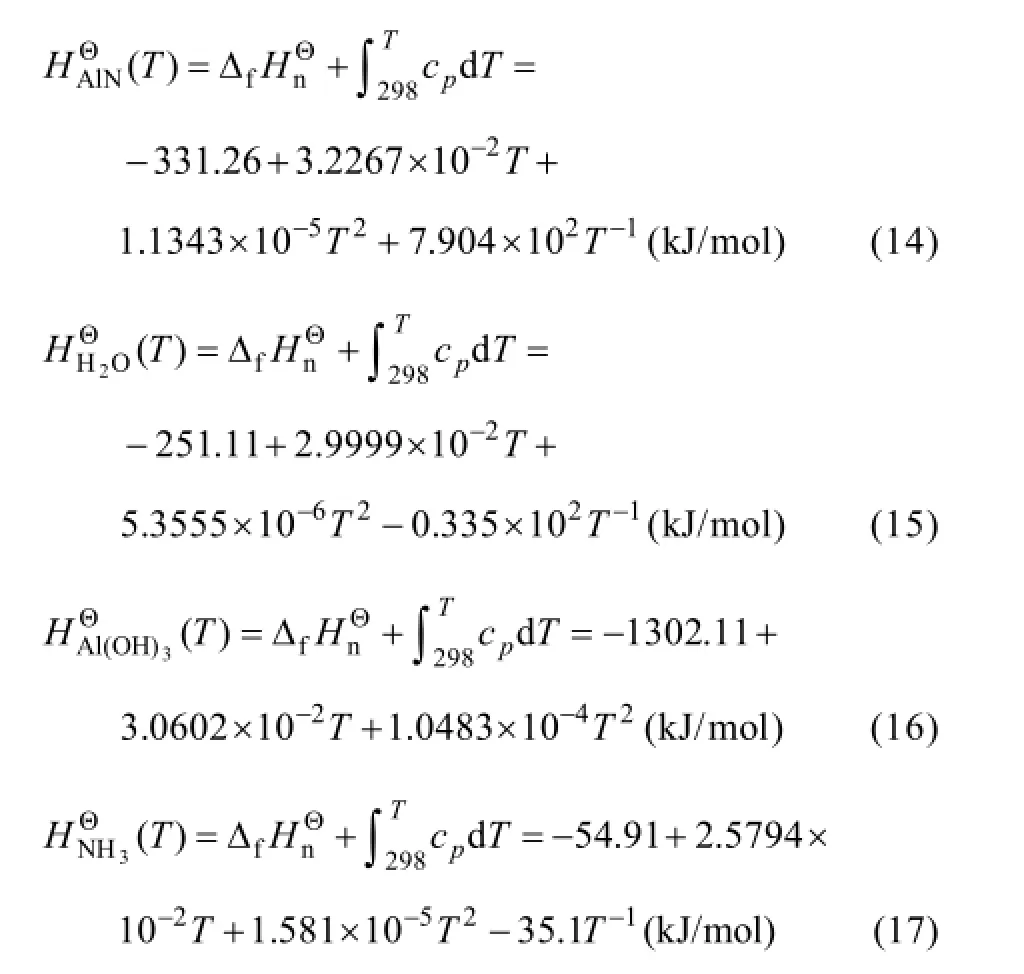
在303~373 K温度范围内采用4种物质298 K熵值进行近似计算:

计算303~373 K下AlN水解反应的标准Gibbs能值,如表4所列。由表4可知,在303~373 K范围内,铝灰中 AlN水解反应的吉布斯自由能在−217.54~−194.59 kJ/mol范围内,说明AlN水解反应热力学在标准条件下可自发进行。
2.2 AlN水解反应后铝灰XRD及SEM分析
对水解前后铝灰进行XRD分析,分析结果如图2所示。从图2可看出,原铝灰AlN在38°、44°和65°附近3条特征峰非常明显,水洗铝灰中难溶于水的尖晶石相和刚玉相依然存在。然而,经水解后铝灰在44°特征峰发生明显减弱,表明铝灰中AlN发生化学反应,水解后铝灰中AlN晶格常数a=3.111,小于原铝灰AlN晶格常数(a=4.045),水解后AlN含量降低;但38°和65°特征峰并未明显减弱,表明水解反应并非强烈的化学反应,水解后铝灰中依然存在部分AlN。在18.703°、20.368°和40.514°处可见Al(OH)3特征峰,可能由于生成Al(OH)3含量较低,导致其特征峰不明显所致。
供试铝灰与水解后铝灰 SEM 分析进一步表明,原铝灰形貌表面不均匀、疏松多孔状,水解后变为紧密颗粒团聚状,粒子之间出现一定的团聚,表明水解反应使水分子介入,促进AlN水解产物的晶粒长大,加强了产物的凝胶作用,这也与张宇等[10]的研究相一致。
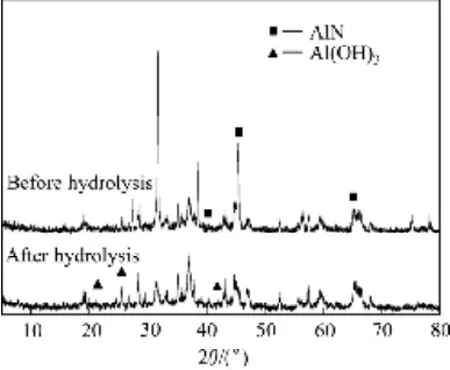
图2 水解前后铝灰XRD谱Fig. 2 XRD patterns of aluminum dross before and after hydrolysis

表5 铝灰与水洗后铝灰AlN的晶格常数Table 5 Lattice parameters (a, b, c) of AlN in aluminum dross before and after hydrolysis

表4 303~373 K下AlN水解反应的Gibbs能Table 4 Gibbs energy of AlN hydrolysis at temperature from 303 to 373 K

图3 水解前后铝灰的SEM像Fig. 3 SEM images of aluminum dross before(a) and after(b)hydrolysis

表6 二次正交旋转组合设计实验结果Table 6 Results based on the two orthogonal rotational experiments

表7 pH方差分析Table 7 Analysis of variance on pH
2.3 水解条件对AlN水解pH的影响及验证试验
由于铝灰中AlN在水解过程发生以下反应[8]:

水解产生OH−,使溶液pH变大,所以某种程度上,水解过程中pH值的变化可以用来表征AlN的水解程度。对铝灰中AlN水解开展二次正交旋转组合试验,其结果如表6所列。从表6可看出,AlN水解pH值在8.65~9.79范围内波动,铝灰中AlN水解呈现弱碱性。对AlN水解pH进行方差分析,其结果见表7。从表7看出,水解温度对AlN水解pH影响不显著,而液固比和水解时间则影响明显(P<0.01),且水解温度和液固比两者对水解 pH存在明显交互作用(P<0.01)。
利用响应曲面法对铝灰中AlN水解交互特性进行研究,得出部分等高线图呈现椭圆状交互作用明显(P<0.01)[21]。对于铝灰中AlN水解响应曲面研究,在固定某一影响因子的前提下,考虑其他两个因素间的交互作用。水解温度液固比响应曲面图及等高图见图4。从图4可看出,水解时间50 min、水解温度为30~100 ℃时,水解pH随水解温度整体变化趋势一致,随水解温度升高pH而增大,水解温度由 30 ℃增大到
65 ℃,水解pH逐渐增大,水解温度由65 ℃升高到100 ℃范围,水解pH继续增大但增幅更加明显,这是由于在pH缓慢上升的区域称为孕育区[8],在孕育区内pH上升的同时伴有NH3产生,NH3溶于水形成氨水,呈弱碱性,水分子不断冲击AlN表面,这一过程扩散起主要影响,溶液pH随反应进行不断升高。水解温度越低,溶液pH越低,温度升高,pH越高。高温有利于AlN+3H2O=Al(OH)3+NH3向右进行,升温有利于提高化学反应速率,提高传质过程。液固比 5~25范围内,水解pH随液固比的降低先降低后升高,当液固比由25降到12时,水解pH缓慢降低;当液固比由12降到5,水解pH变化趋势发生改变而出现明显增大。液固比较低条件下,整个体系体积小AlN局部浓度过高,此时产生的NH3大量溶解在小范围溶液内,导致水解pH偏高,宏观体现pH较大,但在响应曲面交互实验研究中,随着液固比降低,水解pH却呈现先降低后升高的过程,这是因为水解温度和液固比两者对水解 pH存在交互作用,且交互作用明显(P<0.01)。
水解温度、反应时间响应曲面图及等高图见图5。从图5可看出,AlN水解体系液固比为15时,水解温度30~100 ℃范围内,水解pH随水解温度增大先降低后升高。具体而言,水解温度在30 ℃到65 ℃时,水解pH逐渐降低,这与前人报道不一致,并非AlN水解 pH随水解温度升高而呈现增大趋势[9],这可能是NH3·H2O=NH3+H2O,伴随温度升高,锥形瓶内氨水在一定比例液固比条件下不断分解成NH3和H2O,破坏原有平衡,NH3挥发致使体系pH减小,这也表明AlN水解温度与液固比之间交互作用确实影响AlN水解pH;水解温度再由65 ℃上升到100 ℃时,水解pH增大,水解温度与液固比交互作用减弱,这可能是由于水解温度的升高,AlN+3H2O=Al(OH)3+NH3反应平衡向右进行,产生的NH3溶于溶液致使pH变大;当水解时间10~90 min范围内,水解时间由90 min降到10 min,水解pH不断减小,变化趋势明显。这可能是由于随着水解时间的延长,AlN表面薄层Al(OH)3逐渐被侵蚀而失去保护作用,AlN直接与水分接触,水解反应可能由原来的扩散过程控制转为化学反应控制的快速水解阶段,溶液中 OH−浓度增大,水解 pH变大,水解时间的减少,可能有利于AlN水解反应由快速地化学反应控制阶段向扩散控制阶段转化,这有利于抑制铝灰中AlN水解。液固比、反应时间响应曲面图及等高图见图 6。从图6可看出,水解温度65 ℃时,AlN水解体系液固比5~25范围内,水解pH变化随液固比降低而增大。液固比由25降到5,水解pH呈明显增大趋势;水解时间10~90 min范围内,水解pH随水解时间增加而逐渐增大。铝灰中AlN水解过程中,水解pH随水解温度升高、液固比减小、水解时间延长而增大趋势与前人研究报道一致[8−10],pH都呈现增大趋势,然而,由响应曲面法试验得到,在水解温度较低条件下,液固比较高,或水解温度变幅较大时,铝灰中AlN水解

图4 Y=F(水解温度,液固比)响应曲面图及等高图Fig. 4 Response surface plot(a) and contour plot(b) showing interactive effects of reaction temperature and liquid-solid ratio on pH

图5 Y=F(水解温度,反应时间)响应曲面图及等高图Fig. 5 Response surface plot(a) and contour plot(b) showing interactive effects of reaction temperature and reaction time on pH
pH受水解条件因子(水解温度,体系液固比)间的交互作用影响,而不再呈现单纯地随水解温度增大而变大趋势,可能会出现先降后增的变化规律。

对上述水解过程中水解pH与水解温度、液固比和水解时间的关系进行二次回归分析,得到如下二次回归方程:

通过单因素试验对上述二次回归方程准确性进行验证,具体结果见表8。从表8可看出,两者相对误差的绝对平均值仅为 1.00%,数据准确性较好,表明二次回归方程对铝灰中AlN水解pH值有一定的预测性。

表8 AlN水解pH实验值与理论值比较Table 8 Experimental and calculated pH values of AlN hydrolysis
3 结论
1) 303~373 K试验温度范围内,铝灰中AlN水解反应热力学在标准条件下可自发进行,液固比和水解时间对铝灰中AlN水解影响显著(P<0.01);水解温度和液固比之间存在交互作用明显(P<0.01)。
2) 铝灰中AlN水解pH值与水解温度、液固比和水解时间的二次回归方程为

该二次回归方程理论计算值与单因素试验结果值相对误差绝对平均值仅为1.00%,对铝灰中AlN水解pH有一定预测性。
REFERENCES
[1] MURAYMA N, MAEKAWA I, USHIRO H, MIYOSHI T,SHIBATA J, VALIX M. Synthesis of various layered double hydroxides using aluminum dross generated in aluminum recycling process[J]. International Journal of Mineral Processing,2012, 110/111: 46−52.
[2] 李远兵, 孙 莉, 赵 雷. 铝灰的综合利用[J]. 中国有色冶金,2008(6): 63−65. LI Yuan-bing, SUN Li, ZHAO Lei. Utilization of aluminum ash[J]. China Nonferrous Metallurgy, 2008(6): 63−65.
[3] 曾令可, 李得家, 刘艳春, 王 慧. 利用铝加工废渣制备堇青石材料[J]. 材料导报, 2009, 23(1): 90−92. ZENG Ling-ke, LI De-jia, LIU Yan-chun, WANG Hui. Application of industrial sludge of aluminum[J]. Factory in Producing Cordierite, 2009, 23(1): 90−92.
[4] SHINZATO M C, HYPOLITO R. Solid waste from aluminum recycling process characterization and reuse of its economically valuable constituents[J]. Waste Management, 2005, 25(1): 37−46.
[5] DAVID E, KOPAC J. Hydrolysis of aluminum dross material to achieve zero hazardous waste[J]. Journal of Hazardous Materials,2012, (209/210): 501−509.
[6] DASH B, DAS B R. Acid dissolution of alumina from waste aluminum dross[J]. Hydrometallurgy, 2008(92): 48−53.
[7] LI Peng, GUO Min. Leaching process investigation of secondary aluminum dross: The effect of CO2on leaching process of salt cake from aluminum remelting process[J]. Metallurgical and Materials Transactions B, 2012, (43): 1220−1221.
[8] FUKUMOTO S, HOOKABE T H. Hydrolysis behavior of aluminum nitride in various solutions[J]. Journal of Materials Science, 2000, (35): 2743−2748.
[9] 姜 澜, 邱明放, 丁友东, 苏 楠, 姚 泉. 铝灰中 AlN的水解行为[J]. 中国有色金属学报, 2012, 22(12): 3555−3557. JIANG Lan, QIU Ming-fang, DING You-dong, SU Nan, YAO Quan. Hydrolysis behavior of AlN in aluminum dross[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(12): 3555-3557.
[10] 张 宇, 刘 盟, 唐建成. pH值对AlN粉末水解产物的影响[J].陶瓷学报, 2011, 32(2): 231−233. ZHANG Yu, LIU Meng, TANG Jian-cheng. Influence of the pH on the hydrolysis product of AlN powder[J]. Journal of Ceramics,2011, 32(2): 231−233.
[11] ZHANG Yong-heng, BINNER J. Hydrolysis process of a surface treated aluminum nitride powder—A FTIR study[J]. Journal of Materials Science Letters, 2002, 21(10): 803−805.
[12] AZIZI D, SHAFAEI S Z, NOAPARAST M, ABDOLLAHI H. Modeling and optimization of low-grade Mn bearing ore leaching using response surface methodology and central composite rotatable design[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(9): 2295−2305.
[13] LI Zhi-qiang, LI Jing, ZHANG Li-bo, DENG Jin-hui, WANG Shui-xing, MA Ai-yuan, WANG Bao-bao. Response surface optimization of Fand Cl zinc oxide fume by microwave roasting[J]. Transactions of Nonferrous Metals Society of China,2015, 25(3): 973−980.
[14] YANG Ke-di, YE Xian-jia, SU Jin, LONG Yun-fei, LV Xiao-yan,WEN Yi-yuan, WANG Bao-bao. Response surface optimization of Fand Cl zinc oxide fume by microwave roasting[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(2): 548−555.
[15] LI Ying-wei, PENG Jin-hui, LIANG Gui-an, LI Wei, ZHANG Shi-min. Optimization of processing parameters for microwave drying of selenium-rich slag using incremental improved back-propagation neural network and response surface methodology[J]. Journal of Central South University of Technology, 2011, 18(5): 1441−1442.
[16] DEAN J A. 兰氏化学手册[M]. 北京:科学出版社, 2003. DEAN J A. Lange's chemistry handbook[M]. Beijing: Science Press, 2003.
[17] 戴永年. 有色金属冶金[M]. 北京:冶金工业出版社, 2009. DAI Yong-nian. Nonferrous metallurgy[M]. Beijing: Metallurgical Industry Press, 2009.
[18] YANG K D, TAN F X, WANG F. Response surface optimization for process parameters of LiFePO4/C preparation by carbothermal reduction technology[J]. Chinese Journal of Chemical Engineering, 2012, 20(4): 793−802.
[19] DEROSSI A, SEVERINI C, DEL MASTRO A, DE PILLI T. Study and optimization of osmotic dehydration of cherry tomatoes in complex solution by response surface methodology and desirability approach[J]. LWT-Food Science and Technology,2015, 60: 641−648.
[20] FAN Tao, HU Jian-guo, FU Li-dan, ZHANG Li-jin. Optimization of enzymolysis-ultrasonic assisted extraction of polysaccharides from Momordica charabtia L. by response surface methodology[J]. Carbohydrate Polymers, 2015, 115: 701−706.
[21] 徐 颖, 李明利, 赵选民, 卢凤纪. 响应曲面回归分析法——一种新的回归分析法在材料研究中的应用[J]. 稀有金属材料与工程, 2001, 30(6): 429−433. XU Ying, LI Ming-li, ZHAO Xuan-min, LU Feng-ji. The response curved surface regression analysis technique—The application of a new regression analysis technique in materials research[J]. Rare Metal Materials and Engineering, 2001, 30(6): 429−433.
(编辑 李艳红)
Hydrolysis behavior of AlN in aluminum dross with response surface methodology
ZHANG Yong, GUO Zhao-hui, WANG Shuo, XIAO Xi-yuan
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
A large quantities of aluminum dross are produced from aluminum smelting activities. The reuse or disposal of the dross is significantly affected by AlN in aluminum dross. The hydrolysis thermo-dynamic behaviors of AlN in the aluminum dross were studied through the Design Expert for two orthogonal rotational experiments, which is from the recycled aluminum process. The results show that the hydrolysis reaction of AlN in aluminum dross is spontaneous at the temperature from 303 K to 373 K. The pH value in hydrolysis system is significantly affected by the liquid-solid ratio (L/S ratio) and reaction time (P<0.01), respectively. The interaction between reaction temperature and L/S ratio is significant (P<0.01). Based on the quadratic regression equation between the pH of hydrolysis system and the parameters, such as hydrolysis temperature, L/S ratio and hydrolysis time, the relative error between the theoretical value and the trial value is only 1%, and the result shows that it is reliable to prospective the hydrolysis behaviors of AlN in aluminum dross.
aluminum dross; AlN; hydrolysis; response surface
date: 2015-05-19; Accepted date: 2015-11-05
GUO Zhao-hui; Tel: +86-731-88879325; E-mail: zhguo@csu.edu.cn
TF09
A
1004-0609(2016)-04-0919-09
2015-05-19;
2015-11-05
郭朝晖,教授;电话:0731-88879325;E-mail: zhguo@csu.edu.cn

