几种土壤粘粒对铅的吸附特性研究
钟 敏,林艳霞,黄 娅,魏世勇*
(1湖北省建始县林业局,湖北 建始 445300;2湖北民族学院 化学与环境工程学院,湖北 恩施 445000)
几种土壤粘粒对铅的吸附特性研究
钟敏1,林艳霞2,黄娅2,魏世勇2*
(1湖北省建始县林业局,湖北 建始 445300;2湖北民族学院 化学与环境工程学院,湖北 恩施 445000)
摘要:研究了4种土壤粘粒的基本性质及其对铅的吸附特性。结果表明,红砂土的有机质含量、阳离子交换量(CEC)和比表面积(SSA)都明显低于棕色石灰土,而等电点(IEP)高于棕色石灰土;红壤和黄棕壤的这些基本性质介于红砂土和棕色石灰土之间。吸附体系的pH为3~5时,土样对铅的吸附量随pH升高而缓慢增加;pH为5~7时,吸附量随pH升高而急剧增加。准1级动力学吸附模型对4种土样的吸附数据拟合度都较低(R2=0.798~0.863),准2级模型的拟合结果较好(R2=0.987~0.994)。红砂土、红壤、黄棕壤和棕色石灰土对铅的最大吸附量(qmax)分别为27.44,29.87,34.63和41.72 mg/g;Langmuir吸附模型可较好地拟合土样对铅的等温吸附数据(R2=0.984~0.993),而Freundlich模型的拟合度较低(R2=0.834~0.862)。土壤粘粒对铅的吸附主要属于单层吸附模式,化学吸附是其重要作用机制,不同粘粒的吸附量有较大差异。
关键词:土壤粘粒;表面性质;动力学吸附;等温吸附;铅
铅对人体和动物都有毒害作用,它可损害骨髓造血、生殖、内分泌、免疫、神经、消化、泌尿等很多系统[1-4]。表生环境中铅的主要来源有金属冶炼、矿山开采、汽车废气、燃煤、油漆和涂料等[4-8]。目前世界各地由于汽车尾气造成的铅污染逐年增加,排放大气中的铅尘和铅蒸气,经降雨、落尘而污染水体和土壤,因而污染范围广泛[5-8]。土壤及水体中的铅与人体健康及动植物生长关系密切,它们往往会通过食物链的传递进入生物体内,并在人体内蓄积达到有害的程度。当铅进入水体及土壤环境后,水体沉积物和土壤固相组分对它有较强的吸附作用,从而影响铅在表层环境中的固液分配和迁移转化行为,最终改变其生物有效性和生态危害作用[9-12]。可见,土壤固相对铅的吸附特性显著影响着铅在“土壤—水—植物—食物链”复合系统中的迁移和积累。因此,研究不同类型的土壤粘粒对铅的吸附作用,对于阐明铅在土壤中的形态和化学行为,以及对铅污染土壤的修复有着重要意义。
1材料与方法
1.1土样采集及粘粒提取
供试土样为红砂土、红壤、黄棕壤和棕色石灰土共4种,分别采集于湖北省巴东县、恩施市、咸丰县和建始县。土样均为0~15 cm的表层土,自然风干土样,过1 mm筛保存备用。根据文献[13],按以下主要程序提取土样粘粒(<2 μm)作为实验样品,用稀NaOH溶液调节土样悬液的pH至8.2左右,超声波分散后根据沉降虹吸法提取粒径小于2 μm的土壤粘粒组分,用CaCl2溶液絮凝悬浮液。离心分离沉淀物,并反复清洗至上清液中无Cl-存在。土样粘粒经60 ℃烘干,碾磨过60目筛,保存于干燥器备用。
1.2土壤粘粒的基本性质
土壤粘粒的pH、有机质含量和阳离子交换量均用常规法测定[13]。比表面积分析在Quantachrome Autosorb-1型全自动比表面分析仪上进行,样品80 ℃脱气处理约4 h,然后在77 k条件下进行N2等温吸附实验,根据多点BET方法计算样品的比表面积[9-10]。样品表面等电点用Zeta电位及纳米粒度仪(ZETAPALS)测定,称取7份0.01 g的供试样品,加入15 mL 0.01 mol/L KCl溶液,超声分散后,24 h内用0.01 mol/L KOH和HCl溶液将样品悬浮液的pH值分别调至3,4,5,6,7,8,9左右,用0.01 mol/L KCl溶液定容至20 mL,再次超声分散后取2 mL悬液测定其Zeta电位[10-12]。土壤粘粒中铅的本底含量采用硝酸-高氯酸-氢氟酸消解,原子吸收分光光度计法(天美原子吸收光谱仪AA-6000型,上海)进行测定[6]。
1.3吸附实验
1)储备液制备:称取4 g土壤粘粒样品于1 L塑料烧杯中,加入200 mL、0.01 mol/L KCl溶液,超声分散后用0.01 mol/L KCl溶液将悬浮液体积调至800 mL,搅拌条件下用0.01 mol/L KOH或HCl溶液将悬浮液的pH值调至5.0,然后用0.01 mol/L KCl溶液定容至1 L,获得4 g/L土壤粘粒悬浮液;然后用分析纯Pb(NO3)2配制含铅1 000 mg/L的铅离子储备液,并用KOH或HCl溶液调节其pH为 5.0,使用前根据需要将1 000 mg/L的铅离子储备液稀释至适当的浓度。
2)pH对吸附的影响:取若干份4 g/L的土样悬浮液10 mL注入50 mL离心管中,搅拌条件下加入5 mL、400 mg/L的铅离子溶液。用0.01 mol/L KOH或HCl溶液将离心管中混合溶液的pH值分别调节为3,4,5,6和7,然后将其总体积定容为20 mL。反应体系中土壤粘粒浓度为2 g/L,铅离子初始浓度为100 mg/L。在25 ℃、转速250 r/min条件下震荡24 h,然后在10 000 r/min的转速下离心分离,取上清液,用原子吸收光谱仪(Varian AAS240FS)测定吸附后溶液中铅的浓度。根据吸附前后反应体系中铅浓度之差计算土壤粘粒对铅的吸附量,实验设置重复3次取平均值。
3)反应时间对吸附的影响:取100 mL、4 g/L的土样悬浮液于500 mL烧杯中,搅拌条件下加入50 mL、400 mg/L的铅离子溶液,调节混合体系的pH至5.0,将反应体系的总体积定容为200 mL。反应体系中土壤粘粒浓度为2 g/L,铅离子初始浓度为100 mg/L。在25 ℃、转速250 r/min条件下持续震荡。设定的时间定期取样,立即在10 000 r/min的转速下离心分离,取上清液。其余实验步骤参照以上吸附实验。
4)铅浓度对吸附的影响:取若干份4 g/L的土样悬浮液10 mL注入50 mL离心管中,加入不同体积的600 mg/L的铅离子溶液,调节混合体系的pH至5.0,将各离心管中反应体系的体积定容为20 mL。悬浮液中土壤粘粒浓度均为2 g/L,铅离子初始浓度分别为5,10,20,30,50,100,150,200和300 mg/L。在25 ℃、转速250 r/min条件下震荡24 h,然后在10 000 r/min的转速下离心分离,取上清液。其余步骤参照以上吸附实验。
2结果与讨论
2.1土壤粘粒的基本性质
供试土壤粘粒的基本性质见表1。4种土壤粘粒的pH在4.6~7.4间,其中红砂土、红壤、黄棕壤为明显酸性,棕色石灰土为弱碱性。4种土样的有机质含量差异较大,棕色石灰土有机质含量接近红壤的3倍。不同土样的阳离子交换量(CEC)在8.3~14.6 cmol/kg间变化,其相对大小表现为:棕色石灰土>黄棕壤>红壤>红砂土。4种土壤粘粒的比表面积(SSA)比较接近,其中黄棕壤的SSA稍高(19 m2/g),红砂土的SSA最低(12 m2/g)。红砂土、红壤、黄棕壤和棕色石灰土的等电点(IEP)分别为4.5,4.3,3.6和3.2,表明自然环境条件下这4种土壤粘粒表面均为负电位状态。4种土壤粘粒中铅的本底含量较低(2.5~9.3 mg/kg),表明这4种土壤的铅污染不明显。
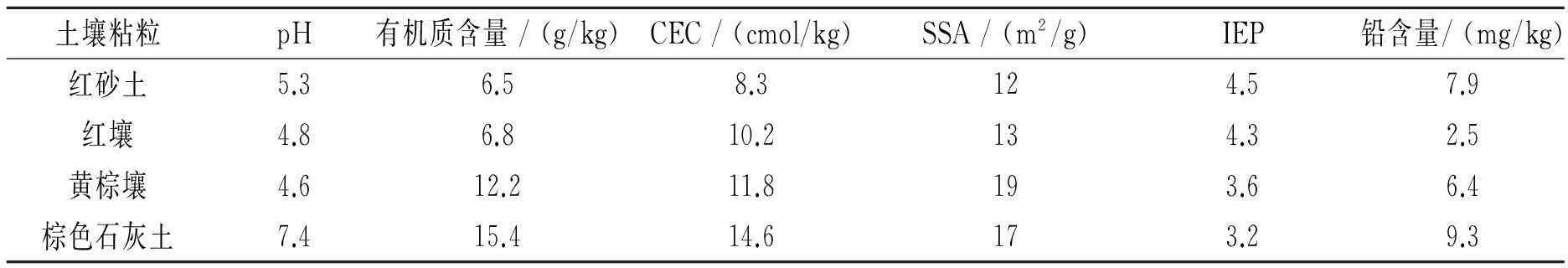
表1 供试土壤粘粒的基本性质
2.2土壤粘粒对铅的吸附
2.2.1pH对吸附的影响
反应体系的pH对4种土壤粘粒吸附铅的影响曲线见图1。由图1可知,当反应体系的pH在3~7范围内,随着pH的升高,4种土样的吸附量都不断升高。在低pH范围(<5),土样对铅的吸附量随pH升高而缓慢增加,这可归因于2个因素:①悬浮液的pH升高时土样表面负电荷将会增加,这有利于土样表面通过静电引力作用吸附金属阳离子;②反应体系的pH升高时,Pb2+可不断水解为Pb(OH)+、Pb(OH)20等羟基离子,也可促进铅在土样表面的吸附[11,14,15]。当吸附体系的pH升高至5以后,土样对铅的吸附量随pH升高而急剧增加,这可能是由于在接近中性的pH条件下,Pb2+高度水解形成了(氢)氧化铅沉淀而聚集于土壤粘粒表面,导致反应体系中可溶性铅的浓度剧烈下降,从而产生一种假吸附现象[15-18]。
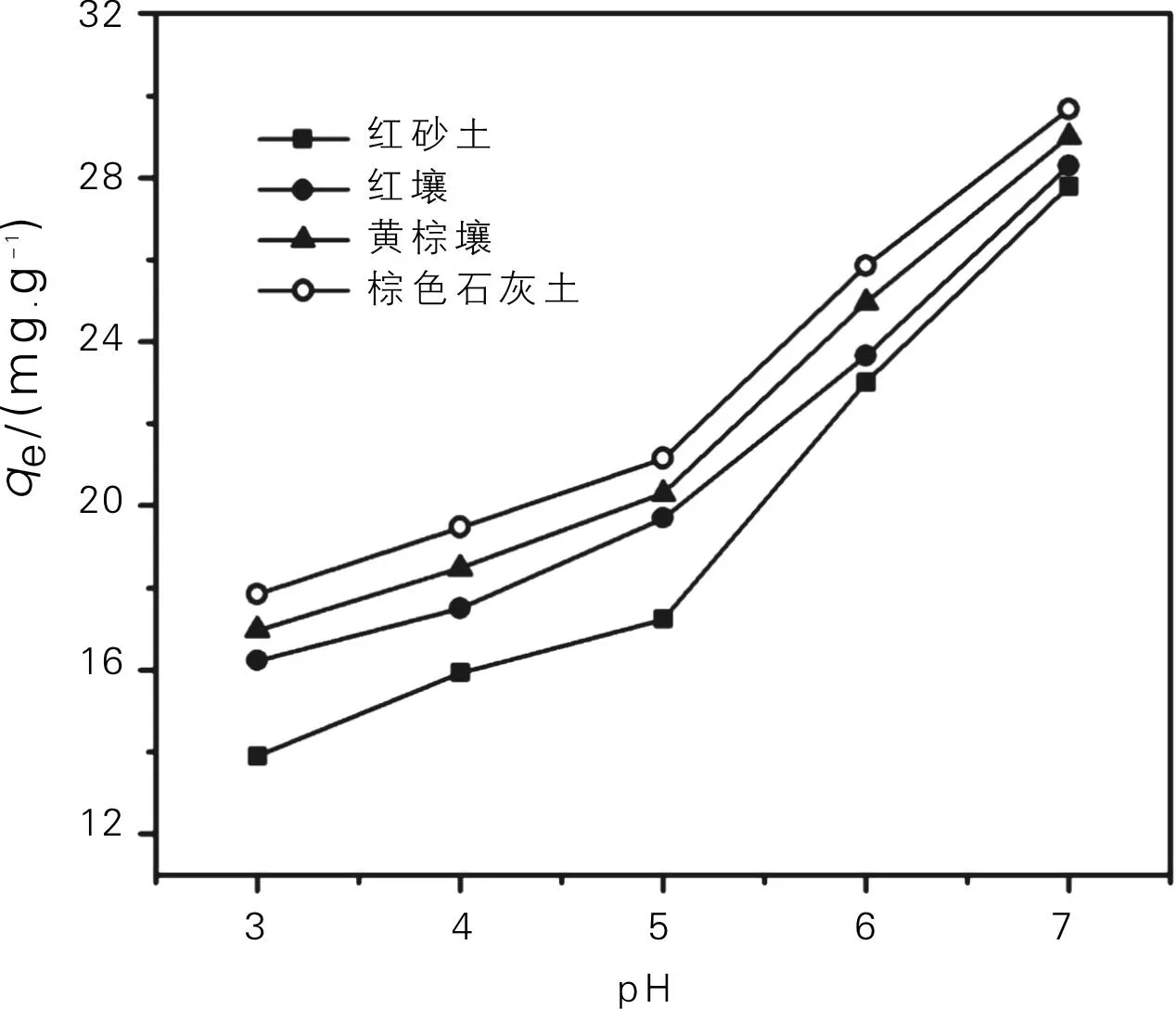
图1 pH对土壤粘粒吸附铅的影响
2.2.2反应时间对吸附的影响
反应时间对土壤粘粒吸附铅的影响见图2。在反应最初60 min内,土样对铅的吸附容量随时间延长而急剧升高;在60~120 min间,吸附容量随时间延长仍然不断升高,但其升高趋势逐渐变缓;吸附时间达120 min以后,吸附容量趋于平稳,达到吸附饱和状态。为了使吸附达到平衡状态,本研究中的等温平衡吸附实验设定吸附时间为24 h。
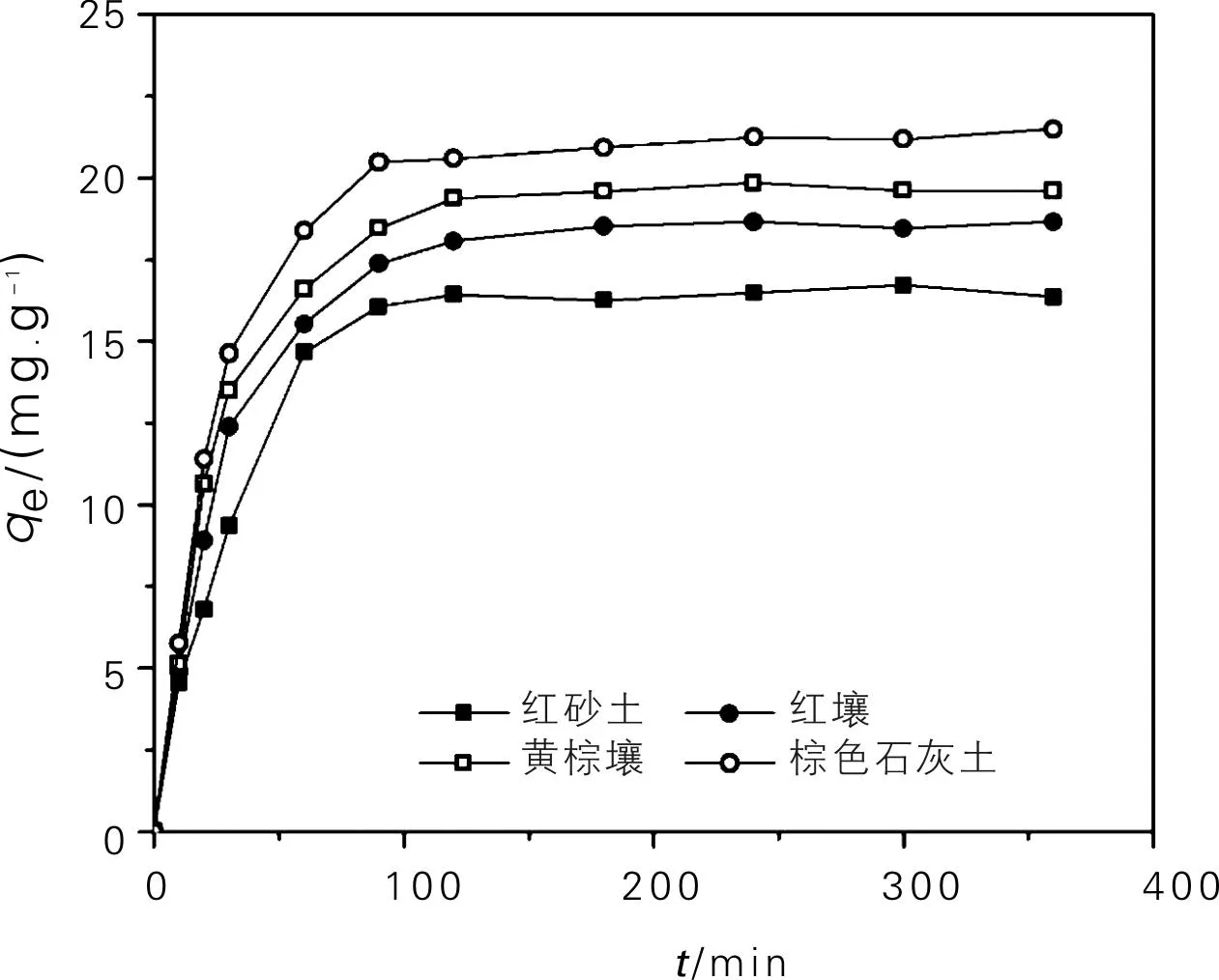
图2 反应时间对土壤粘粒吸附铅的影响
选用准1级和2级动力学模型对样品吸附铅的动力学数据进行了拟合。2种模型的表达式分别见方程(1)和(2):
lg(qe-qt)=lgqe-k1t/2.303
(1)
t/qt=1/(k2qe2)+t/qe
(2)
式(1)~(2)中,qt(mg/g)为反应时间t(min)时土壤粘粒对铅的吸附量;qe(mg/g)为吸附达饱和时的平衡吸附量;k1(min-1)和k2(g·mg-1·min-1)分别为准1级和2级动力学平衡速率常数[14-16]。
准1级和2级动力学模型对土壤粘粒吸附铅的动力学数据拟合参数见表2。准1级模型对4种土样的动力学吸附数据拟合度都较低(R2=0.798~0.863),拟合平衡吸附量(qe)都明显低于吸附饱和时的实验数据。可见,土样对铅的动力学吸附过程不符合准1级动力学模型。准2级模型可较好地拟合土样对铅的动力学吸附数据(R2=0.987~0.994),4种样品的拟合平衡吸附量qe也接近其吸附饱和时的实验数据,表明准2级动力模型可较好地描述4种土壤粘粒对铅的动力学吸附过程。根据文献[14,16]可知,悬浮液体系中固液界面的吸附平衡时间通常小于60 min。本研究中吸附动力学实验显示,土壤粘粒吸附铅达到吸附平衡状态时约需要120 min。可见,土样吸附铅是一个相对缓慢的作用过程。这些结果表明,表面物理吸附过程不是土壤粘粒吸附铅的主要速率控制步骤,化学吸附和颗粒内部扩散应该是土样吸附铅的重要机制[14-16]。
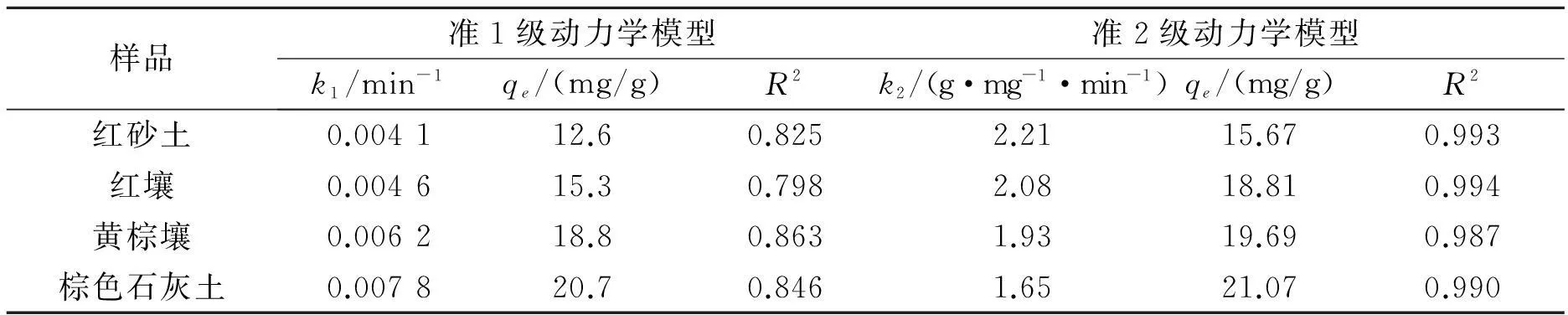
表2 供试样品吸附铅的动力学模型拟合参数
2.2.3铅初始浓度对吸附的影响
土样和铅的悬浮液体系中,铅的平衡浓度与土壤粘粒吸附容量的关系见图3。在吸附没达到饱和之前,土壤粘粒对铅的吸附量随铅平衡浓度的升高而不断增加。这是由于在固液体系中,增加可溶性铅的浓度使反应体系中的铅离子与土壤粘粒之间“有效碰撞”的几率增大所致。总体上看,4种土样的吸附量随铅平衡浓度变化的趋势比较类似。当铅离子的平衡浓度较低时(<20 mg/L),吸附量随平衡浓度的升高而急剧增加;铅离子的平衡浓度升高至20 mg/L以上时,吸附量随平衡浓度的升高仍然明显增加,但其变化趋势减缓。对红砂土和红壤2种土样而言,当平衡浓度达50 mg/L时,其吸附量趋于稳定,即达到吸附饱和状态;对黄棕壤和棕色石灰土而言,当平衡浓度达100 mg/L时,土壤粘粒的吸附量才趋于饱和。
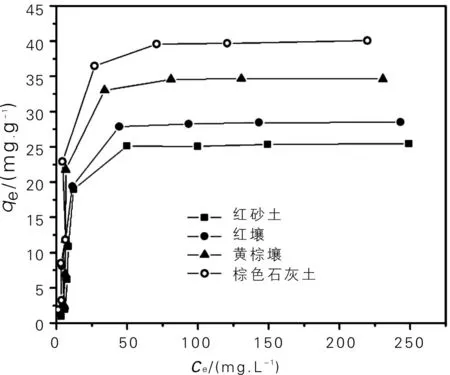
图3 土壤粘粒对铅的等温吸附曲线
选用Langmuir和Freundlich吸附模型对等温吸附数据进行了拟合。2种模型的表达式分别见方程(3)和(4):
qe=qmaxbce/(1+bce)
(3)
qe=kce1/n
(4)
式(3)~(4)中,qe表示单位质量土壤粘粒对铅的吸附量(mg/g);ce为铅离子的平衡浓度(mg/L);Langmuir模型中qmax表示最大吸附容量(mg/g),b为与吸附结合能及亲和力相关的常数(L/mg);Freundlich模型中k为与吸附容量有关的常数(mg1-(1/n)·L1/n·g-1),n为与吸附强度相关的经验系数[15-18]。一般认为,Langmuir方程适合描述匀质性表面单层吸附模式,而Freundlich方程适合描述异质性表面的多层吸附模式。
2种等温吸附模型对土壤粘粒吸附铅的实验数据拟合结果见表3。Langmuir模型拟合结果中,4种土样对铅的最大吸附量(qmax)在27.44~41.72 mg/g间,吸附亲和力常数(b)在0.049~0.072 L/mg间。4种土样的qmax和b的相对大小都表现为棕色石灰土>黄棕壤>红壤>红砂土,表明土样对铅的吸附亲和力越高则吸附容量越大。Langmuir模型对土样等温吸附铅的实验数据的拟合相关系数较高(R2=0.984~0.993),表明Langmuir模型较适合描述土样对铅的等温吸附过程。因此,土样对铅的吸附主要可归属于单层吸附模式。Freundlich模型拟合结果中,4种土样的吸附容量常数(k)在6.26~12.08 mg1-(1/n)·L1/n·g-1间,其相对大小与Langmuir模型拟合的最大吸附容量qmax一致。不同土样的Freundlich吸附强度系数n值在3.45~4.46间变化,说明4种土样表面对铅的吸附强度有一定差异;对4种土样等温吸附铅的拟合度都比较低(R2=0.834~0.862),表明Freundlich模型不适合描述土壤粘粒对铅的等温吸附过程,即多层吸附模型不是土样吸附铅的主要作用方式。
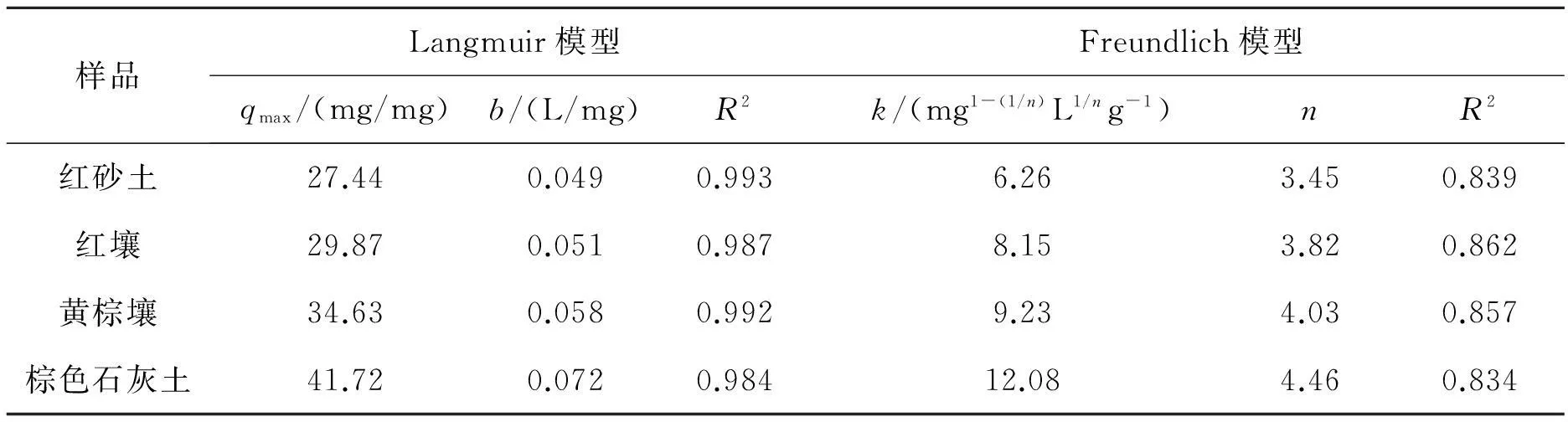
表3 供试土样吸附铅的等温模型拟合参数
4种土样粘粒对铅的等温吸附实验表明,不同土样的Langmuir最大吸附容量qmax和Freundlich吸附容量常数k都有较大差异,其中棕色石灰土这些吸附参数明显高于红砂土。根据文献[5,8,10,11,18,19]可知,其主要原因有:①土壤有机质富含羟基、羧基、醌基等活性官能团,它们都是结合铅离子的有效位点。由于棕色石灰土的有机质含量明显高于红砂土,因此它表现出更高的铅离子吸附容量;②棕色石灰土的CEC明显高于红砂土,表明棕色石灰土通过阳离子交换机制吸附的铅离子也较多;③棕色石灰土的SSA高于红砂土,表明它对铅的表面物理吸附量高于红砂土;④棕色石灰土和红砂土的IEP都小于5。当吸附体系的pH=5.0时,棕色石灰土和红砂土的表面电位均为负值,这有利于土样表面通过静电引力吸附铅离子。与红砂土比较,棕色石灰土的IEP更低,意味着其表面对铅离子的静电引力更强。
3结论
4种土壤粘粒对铅的吸附特性较相似,但其吸附容量差异较大,这与土样的基本性质密切相关。反应体系的pH对吸附作用有明显影响,pH在3~5时土样对铅的吸附量随pH升高而缓慢增加,pH为5~7时吸附量随pH升高而急剧增加。4种土壤粘粒对铅的动力学吸附不符合准1级动力学吸附模型,而准2级模型可较好地描述其动力学吸附过程。红砂土、红壤、黄棕壤和棕色石灰土的粘粒吸附铅的Langmuir最大吸附量依次增加,其中棕色石灰土的最大吸附量几乎达到红砂土的2倍。等温吸附模型Langmuir方程可较好地拟合土壤粘粒对铅的等温吸附数据,而Freundlich方程拟合的相关系数较低。4种土壤粘粒对铅的吸附主要属于单层吸附模式,化学吸附是其重要机制。
参 考 文 献
[1]吕玉桦,石小飞,刘珊渡,等.我国0~6岁儿童血铅水平及流行特征分析[J].实用预防医学,2015,22(2):149-154.
[2]唐昊翔,张湘江,宁丽丰,等.铅酸蓄电池企业建设项目职业病危害预评价[J].中国公共卫生管理,2015,31(5):747-752.
[3]陈雪琴,李红美,张爱红,等.血铅浓度对血压、心电图的影响[J].中国工业医学杂志,2015, 28(1):68-69.
[4]曾运良,周志洋.某铅蓄电池企业职业病危害综合治理效果分析[J].中国职业医学,2015,42(4):467-469.
[5]串丽敏,赵同科,郑怀国,等.土壤重金属污染修复技术研究进展[J].环境科学与技术,2014,37(120):213-222.
[6]罗小玲,郭庆荣,谢志宜,等.珠江三角洲地区典型农村土壤重金属污染现状分析[J].生态环境学报, 2014, 23(3): 485-489.
[7]宋伟,陈百明,刘琳.中国耕地土壤重金属污染概况[J].水土保持研究,2013,20(2):293-298.
[8]黄益宗,郝晓伟,雷鸣,等.重金属污染土壤修复技术及其修复实践[J].农业环境科学学报,2013,32(3):409-417.
[9]Tran HV,Tran LD,Nguyen TN.Preparation of chitosan/magnetite composite beads and their application for removal of Pb (II) and Ni (II) from aqueous solution[J].Mater.Sci.Eng.C,2010,30:304-310.
[10]Chang YC,Chen DH.Preparation and adsorption properties of monodisperse chitosan-bound Fe3O4magnetic nanoparticles for removal of Cu(II) ions[J].J.Colloid Interf.Sci.,2005,283:446-451.
[11]Adebowale KO,Unuabonah IE,Olu-Owolabi B I.The effect of some operating variables on the adsorption of lead and cadmium ions on kaolinite clay[J].J Hazard.Mater.,2006,34(s 1-3):130-139.
[12]Celis R,Hermosin MC,Cornejo J.Heavy metal adsorption by functionalized clays[J].Environ.Sci.Technol.,2000,34:4593-4599.
[13]鲍士旦.土壤农化分析[M].3版.北京:中国农业出版社,2000:30-34,154-169.
[14]Adebowale KO,Unuabonah IE,Olu-Owolabi BI.Kinetic and thermodynamic aspects of the adsorption of Pb2+and Cd2+ions on tripolyphosphate-modified kaolinite clay[J].Chem.Eng.J.,2008,136:99-107.
[15]Oubagaranadin JUK,Murthy ZVP.Adsorption of divalent lead on a montmorillonite-illite type of clay[J].Ind.Eng.Chem.Res.,2009,48:10627-10636.
[16]Singh SP,Ma LQ,Hendry MJ.Characterization of aqueous lead removal by phosphatic clay:equilibrium and kinetic studies[J].J. Hazard.Mater.,2006,136(3):654-662.
[17]周健,金诚,李晓林,等.熟污泥改性黄土对Pb2+的吸附解吸特征[J].环境化学,2015,34(9):1710-1715.
[18]孙红专,杨剑虹.新疆棕漠土无机胶体对Pb2+的吸附特征研究[J].土壤通报,2015(6):58-61.
[19]Liu JF,Zhao ZS,Jiang G B,et al.Coating Fe3O4magnetic nanoparticles with humic acid for high efficient removal of heavy metals in water[J].Environ.Sci.Technol.,2008,42:6949-6954.
(责任编辑高嵩)
收稿日期:2016-03-09
基金项目:国家自然科学基金项目(项目编号:41261060,41561053);生物资源保护与利用湖北省重点实验室开放基金项目(项目编号:PKLHB1315);湖北省高校优势特色学科群建设计划资助项目(鄂学位[2015]5号)。
作者简介:钟敏,工程师,本科。
*通讯作者:魏世勇,副教授,博士,研究方向:材料化学及应用。
doi:10.3969/j.issn.2095-4565.2016.03.003
中图分类号:X53
文献标识码:A
文章编号:2095-4565(2016)03-0010-06
Research on Adsorption Characteristics of Soil Clays on Lead(II)
Zhong Min1,Lin Yanxia2,Huang Ya2,Wei Shiyong2*
(1Jianshi Forestry Bureau,Jianshi Hubei 445300;2Department of Chemistry and Environmental Engineering,Hubei University for Nationalities,Enshi Hubei 445000)
Abstract:The basic properties of four soil clays and their adsorption characteristics on Lead (II) have been studied.Results show that the content of organic matter,cation exchange capacity,and specific surface area of red sand soil were obviously lower than those of brown calcareous soil,while the isoelectric point higher than that of brown calcareous soil.These basic properties of red soil and yellow-brown soil are between the red sand soil and brown calcareous soil. When absorbent's pH is 3~5,the adsorption capacities (qe) of the samples on lead (II) increases slowly with the growth of pH,when pH=5~7,the adsorption capacities grows significantly.According to pseudo-first-order model of (R2=0.798~0.863) of kinetics model of adsorption,the fitting degree of the four soil samples adsorption kinetic data are lower,while the better fitting results can be obtained by using the pseudo-second-order (R2=0.987~0.994).The isotherm adsorption capacity (qmax)of RSS,RS,YBS and BCS was 27.44,29.87,34.63 and 41.72 mg/g,respectively.Langmuir model was suitable to describe the isotherm adsorption (R2=0.984~0.993),and the R2 values of Freundlich model were low (R2=0.834~0.862).This indicated that the mono-layer adsorption with a chemisorption mechanism was important in adsorbing lead(II) onto the clays.
Key words:soil clays;surface properties;kinetic adsorption;isotherm adsorption;lead(II)

