氯化钙浸提—电感耦合等离子体发射光谱法快速测定石灰性土壤中的有效硫
蒋俊平++韩张雄++雒虹++李慧慧


摘要:在农业生产中,硫是一种作物必需且重要的营养元素。植物所吸收的硫素主要为土壤中的有效硫,因此,快速检测土壤中有效硫的含量,可以有效预警土壤硫素的缺失性。ICP-AES广泛运用于各种样品如生物、矿物、食品等的检测,具有灵敏度高、检出限低、操作简单、检测速度快等优点。本研究通过优化仪器和试验条件,选择出测定有效硫的最佳谱线为λ=182.034 nm,硫的质量浓度与发射光谱强的线性关系良好:y=1.255 4x-3.096 4(r=0.999 9),检出限为3.18 mg/kg。当试验用1.5 g/L CaCl2浸提剂在振荡速度为180 r/min的条件下,对5个标样进行振荡浸提 1 h 得到的有效硫含量与真实值接近,并且其准确度和精密度较高。同时对比了ICP-AES与比浊法,证实了ICP-AES法可以有效应用于石灰性土壤样品中有效硫的检测。
关键词:碱性土壤;ICP-AES;有效硫
中图分类号: S153.6文献标志码: A文章编号:1002-1302(2016)06-0500-03
收稿日期:2015-12-25
基金项目:国土资源部公益性行业科研专项(编号:201311096-02)。
作者简介:蒋俊平(1986—),女,重庆人,硕士,助理工程师,主要从事岩矿分析测试工作。E-mail:jiangjunping100@163.com。
通信作者:韩张雄,博士,工程师,主要从事土壤检测、污染治理及植物逆境培育方面的研究。E-mail:han10260@163.com。硫是作物生长发育不可缺少的16种营养元素之一。它在作物体内参与多种物质的合成,如蛋白质、氨基酸、酶、辅酶、硫胺类等活性物质,在作物体内的功能以及作物对其的吸收量与磷相似。作物体内的多种生理生化反应过程均与硫元素密不可分,如氮素代谢、脂类代谢、淀粉代谢、防御机制、生长调节机制、解毒机制、光合作用、呼吸作用、氧化还原反应等[1-3]。国际植物营养界对于硫在作物生长发育与生理代谢等过程中的重要性已经表示出高度的重视,而硫也被认定为仅次于氮、磷、钾的第4重要营养元素,与三者配合还可以使作物达到营养平衡[4]。研究表明越橘[5]、冬小麦[6-7]、油菜、大豆、四季萝卜[8]、水稻、玉米、油菜[9-10]、白菜[11]、烤烟[12]、生姜[13]等作物合理施硫,不仅增加产量,而且可以改善品质。而土壤中的有效硫是植物吸收利用土壤硫素的主要来源,因此正确快速地检测土壤中的有效硫含量,可以提前了解土壤的硫素情况及土壤的供硫能力,同时可及时预警作物缺硫情况,对硫肥的合理施用进行指导[14]。
目前,土壤样品中有效硫的常用检测方法有:还原法、比浊法、阴离子交换色层分析法(IC)、电感耦合等离子体原子发射光谱法等。其中还原法准确度高,但是分析速度慢,耗时费劳,试剂具有较强腐蚀性且试剂成本高;比浊法操作比较容易,成本费用较低,比还原法测定速度快,但是此方法受到土壤中有机胶体、分析条件及样品预处理的影响,从而准确度受到限制。IC法可以同时测定多种阴离子,灵敏度较高,但高浓度磷对硫的测定有干扰[15-16]。近年来,ICP-AES已经广泛运用于各种样品如生物、矿物、食品等的检测,具有灵敏度高、检出限低、操作简单、检测速度快,可以大批量应用等优点,其测定值与标准值相符,能较好应用于土壤中有效硫的测定[17-18]。本研究通过测定5个石灰性土壤的国家标准物质,对ICP-AES测定此类土壤中的有效硫进行研究。
1材料与方法
1.1主要试剂和标准溶液
氯化钙为分析纯,试验用水为艾科普纯化去离子水装备所制成的高纯水,国家标准物质GBW07459、GBW07460、GBW07461、GBW07413a、GBW07414a,为地球物理地球化学勘查研究所(IGGE)制备。
硫标准贮备液[ρ(S)=100 mg/L],准确称取0.543 6 g硫酸钾溶于去离子水,定容至1 L。硫标准二级贮备液[ρ(S)=20 mg/L]:准确吸取20 mL 100 mg/L 硫标准贮备液至100 mL容量瓶中,用去离子水定容并摇匀,将其逐级稀释制备成硫标准工作溶液。硫标准工作溶液浓度依次为:0.00、1.60、3.20、4.80、6.40、800、9.60 mg/L。
氯化钙浸提剂(CaCl2):准确称取3.00 g CaCl2溶于去离子水,定容至1 L。
1.2试验方法
准确称取10.00 g国家标准物质GBW07459、GBW07460、GBW07461、GBW07413a、GBW07414a 于250 mL塑料瓶中,加50.00 mL CaCl2 浸提剂,于20~25 ℃下振荡一定时间,过滤得待测溶液。在既定仪器工作条件下,对待测溶液进行ICP-AES测定,同时随试验测定空白3份。
1.3仪器设备及工作条件
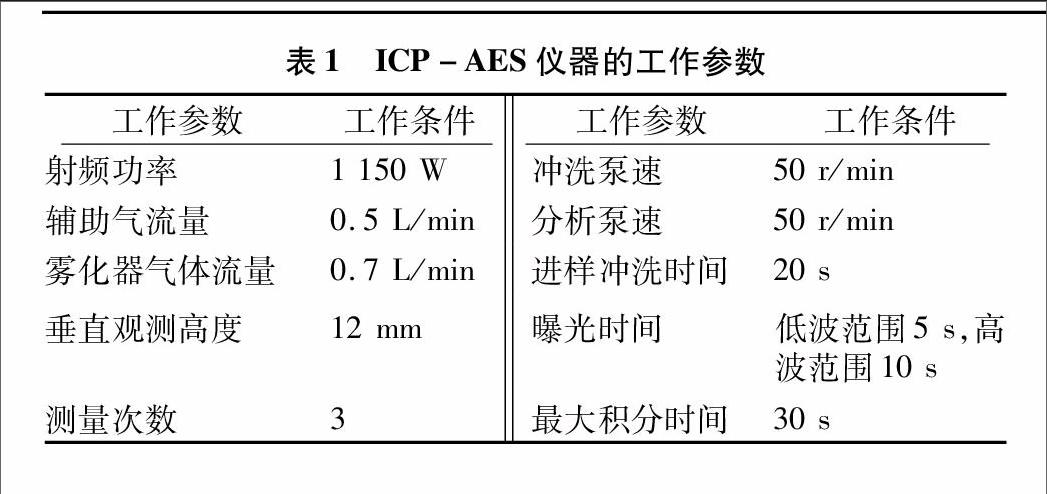
iCAP 6300 电感耦合等离子体发射光谱仪(美国Thermo公司),仪器的参数设置见表1。
2结果与讨论
2.1标准曲线和分析波长选择
本研究使用ICP-AES测定有效硫时,利用ICP-AES的软件及仪器性能,挑选了3条谱线对硫进行测定,分别为180.731、182.034、182.624 nm。最终根据峰谱线的发射强度、峰形、背景、检出限以及共存元素的干扰等因素,选择最佳的硫测定谱线波长182.034 nm。在波长λ=182.034 nm时,对硫标准工作溶液进行测定发现,硫的质量浓度与发射光谱强的线性关系良好:y=1.255 4x-3.096 4(r=0.999 9)。试验同时对12份样品空白进行测定,以3倍标准偏差计算得出硫的检出限,本试验硫元素的检出限为3.18 mg/kg。
2.2浸提剂浓度试验
土壤中有效硫的浸提剂主要有KCl、CaCl2、NaHCO3、Ca(H2PO4)2、NaH2PO4、KH2PO4、NH4AC等。根据目前的文献资料[17,19-21]以及笔者所在课题组多年来的实践经验,本试验选择CaCl2作为土壤有效硫的浸提剂,分别配制3.0、1.5、0.5 g/L CaCl2溶液作为浸提剂,此浸提所得溶液不需再加入其他试剂,用定量滤纸过滤后直接用ICP-MS测定,操作方便快捷。试验条件:振荡速度180 r/min,时间1 h。由表2可以看出,当CaCl2浸提剂浓度为0.5 g/L时,前3个标样中的有效硫测定值与标准值相近,但后2个稍微偏低,可能是由于后2个标样的有效硫含量比前3个高,而0.5 g/L 的CaCl2浓度对于稍高含量的有效硫提取能力不够导致的;1.5 g/L和3.0 g/L CaCl2都能较好地浸提出前3个标样中的有效硫,3.0 g/L CaCl2浸提出的后2个标样比标准值稍高,1.5 g/L的CaCl2浸提出5个标样有效硫测定值更接近标准值,因此本研究确定CaCl2的浓度为1.5 g/L。
2.3振荡时间试验
试验用1.5 g/L的CaCl2浸提液在180 r/min的条件下,对5个标样进行浸提,振荡时间分别为0.5、1.0、2.0 h。由表3可知,0.5 h的振荡时间得到的有效硫含量偏低,说明振荡时间较短,不能充分浸提出土壤标样中的有效硫,而2.0 h振荡浸提出的硫含量明显偏高,说明时间过长浸提液中除了有效硫外,其他状态的硫也有可能被浸提出来。试验选择1.0 h作为振荡时间得到的有效硫含量和真实值最为接近。
2.4振荡速率试验
本试验用1.5 g/L CaCl2浸提剂对5个标样中的有效硫进行振荡浸提1.0 h,振荡速度分别为120、180、240 r/min。由表4可知,当振荡速度为120 r/min,可能由于振荡速度较慢,导致浸提剂和标样混匀接触不充分,得到的有效硫含量偏低;当振荡速度为180 r/min和240 r/min都能较好地浸提出标样中的有效硫,所以选择耗能更低的180 r/min作为试验的振荡速度。
2.5方法准确度与精密度
按照试验得出的最佳方法(1.5 g/L浸提剂、振荡器振速180 r/h、浸提时间1.0 h),对5个标样浸提液中的有效硫进行测定,平行样品各6份。由表5可知:该方法的相对误差(RE)绝对值为1.04%~3.00%,精密度为4.09%~ 6.78%,均小于10%。该方法的准确度和精密度符合标准 DD 2005—03《生态地球化学评价样品分析技术要求(试行)》对有效硫的测定要求。
2.6对比试验
试验通过ICP-AES与比浊法分别测定5个标样浸提液中的有效硫含量,由表6可知,ICP-AES法与比浊法测定结果较为一致,可以用于快速测定土壤中有效硫的含量。
3结论
本试验采用CaCl2浸提-ICP-AES法快速测定石灰性土壤中的有效硫,通过优化仪器条件,选择合适的浸提剂浓度,振荡速度和振荡时间,对方法精密度、准确度、检出限进行了试验,并将其与传统比浊法进行对比,在提高了石灰性土壤中有效硫的检测速度、简化了操作步骤的同时,保证了检测结果的准确性,证实了该方法可以有效应用于大量石灰性土壤样品中有效硫的检测。
参考文献:
[1]李波. 硫肥作用应引起重视[N]. 农资导报,2015-11-17(C03).
[2]罗奇祥. 土壤硫素状况及其测试法[J]. 江西农业学报,1994,6(2):135-143.
[3]徐冬梅,刘广深,许中坚,等. 模拟酸雨对土壤酸性磷酸酶活性的影响及机理[J]. 中国环境科学,2003,23(2):176-179.
[4]李忠,刘思远,黄海涛,等. 烟草制品中硫含量测定的研究[J]. 光谱实验室,2000,17(5):534-535.
[5]唐雪东,李亚东,刘海广,等. 施用硫磺粉对越橘根域土壤酶活性的影响[J]. 华南农业大学学报,2012,33(2):183-187.
[6]赵玉霞. 氮硫配施对关中地区冬小麦氮硫吸收转运及产量影响[D]. 杨凌:西北农林科技大学,2014:8-15.
[7]李云杰,钟芳,赵霞,等. 硫肥施用对冬小麦影响的初步研究[J]. 天津农林科技,2015(2):26-27,37.
[8]魏珂萍. 鲁南兰山区主要土壤供硫状况与作物施硫效果[D]. 北京:中国农业大学,2004:7-10.
[9]肖厚军. 贵州主要耕地土壤硫素状况及硫肥效应研究[D]. 重庆:西南农业大学,2003:7-15.
[10]邹歧贵,黄平昌. 武宣县水稻施硫肥效试验研究[J]. 现代农业科技,2015(4):28-29,40.
[11]梁泰帅,刘昌欣,康靖全,等. 硫对镉胁迫下小白菜镉富集、光合速率等生理特性的影响[J]. 农业环境科学学报,2015,34(8):1455-1463.
[12]蔡赛男,周冀衡,张毅,等. 不同硫肥施用量对烤烟生长和生理生化指标的影响[J]. 作物研究,2015(2):170-172.
[13]罗振明,谢庆恩,王瑞芳,等. 安丘生姜增施硫肥试验初探[J]. 中国农学通报,2015(30):197-200.
[14]黎庆容,李汉涛,刘军仿,等. 土壤有效硫测试方法的探讨[J]. 湖北农业科学,2015(10):2343-2347.
[15]Jones M B. Sulfur in agriculture[J]. Agronomy Series,1986,27:549-566.
[16]Li Q R,Li H T,Liu J F,et al. Study on test method of soil available sulfur[J]. Hubei Agricultural Science,2015(10):533-537.
[17]Ketterings Q,Miyamoto C,Mathur R R,et al. A comparison of soil sulfur extraction methods[J]. Soil Science Society of America Journal,2011,75(4):1578-1583.
[18]Shirisha,K,Sahrawat,et al. Comparative evaluation of ICP-AES and turbidimetric methods for determining extractable sulfur in soils[J]. Journal of the Indian Society of Soil Science,2010,58:323-326.
[19]Virinder S,Sharma K,Veer S,et al. Suitability of extractants for available sulfur and relationship of Sulfur fraction with some soil properties in paddy soils of western UP[J]. Environment and Ecology,2009,27(4):1698-1703.
[20]Cui X Y,Wang SP,Yf W,et al. Suitability of extractants for predicting available sulfur in natural grassland in the Inner Mongolia Steppe of China[J]. Communications in Soil Science and Plant Analysis,2006,37:721-732.
[21]Cui Y S,Wang Q R,Dong Y T,et al. Correlation of different extractants with determination of soil extractable sulfur between[J]. Soils,2003(2):153-156.

