劳拉西泮片有关物质检查方法的比较
袁猛 余振喜 王慧文 王菲菲


[摘要] 目的 比较并讨论中国药典2015年版二部和美国药典39版中劳拉西泮片有关物质检查方法的异同,为选择合理有效的有关物质检测方法提供科学依据。 方法 比较两种检测方法在杂质分离能力、方法学以及检测结果一致性等方面的差异并进行评价。 结果 采用中国药典检测方法对劳拉西泮片中主要杂质之间的分离效果差,从而影响有关物质结果的判定;美国药典检测方法杂质分离好,灵敏度高,提高了分析方法的专属性和结果的准确性。 结论 美国药典有关物质检测方法更适合劳拉西泮片中杂质的控制,从而保证该产品的质量和安全。
[关键词] 劳拉西泮片;高效液相色谱法;有关物质;检测方法;分离度
[中图分类号] R917 [文献标识码] A [文章编号] 2095-0616(2016)09-40-05
[Abstract] Objective To compare and discuss the differences and similarities of related substances test method on lorazepam tablets between Chinese pharmacopoeia 2015 edition two and United States pharmacopoeia 39 edition. Methods The differences in the aspects of impurity separation capability, methodology and the consistency of test results etc between the two test methods were compared and evaluated. Results The separation effect of major impurities in lorazepam tablets by the test method of Chinese pharmacopoeia was bad, which could influence the determination of related substances result, while the impurity separation effect by the test method of United States pharmacopoeia was good, had high sensitivity and improved the specificity of analytical method and the accuracy of results. Conclusion The relative substances' test method of United States pharmacopoeia was more suitable for the impurity control in lorazepam tablets, which ensured the quality and safety of the product.
[Key words] Lorazepam tablets;High performance liquid chromatography method;Related substances;Test method;Separating degree
劳拉西泮属于苯二氮类精神安定药,具有镇静、催眠和抗癫痫等作用[1-3]。其常用口服固体制剂劳拉西泮片是一线抗癫痫持续状态的首选药物[4-7]。查阅各主要国家和地区药典,劳拉西泮原料药在欧洲药典8.0版(EP8.0)[8]、英国药典2016年版(BP2016)[9]、美国药典39版(USP39)[10]、日本药局方ⅩⅥ版(JP16)[11]和中国药典2015年版二部(ChP2015)[12]均有收载,其制剂劳拉西泮片在BP2016、USP39和ChP2015有收载。根据文献报道[13-15],劳拉西泮易受酸和热等条件影响降解产生出6-氯-4-(邻氯苯基)-2-喹唑啉甲醛(即USP39中杂质C)等杂质,因此,收载有本品及其制剂的药典中均设立了有关物质检查项。其中,在劳拉西泮片有关物质检查项下,BP2016采用薄层色谱(TLC)法,USP39和ChP2015采用高效液相色谱(HPLC)法。
在实际检验检测工作中发现,采用ChP2015色谱条件对劳拉西泮片中有关物质进行检查时,杂质C与相邻杂质不能有效分离,造成测定结果不准确甚至可能造成检验结论的误判。同时,通过试验发现,USP39中劳拉西泮片有关物质检测方法灵敏度高,专属性强,各杂质之间以及杂质与主成分之间分离度较好,该方法优于ChP2015中的检测方法,更适合劳拉西泮片有关物质的检测和控制。
1 仪器与试药
1.1 仪器
Agilent 1100型高效液相色谱仪;Sartorius CP225D型电子天平;GW-UP型普析通用超纯水器;天大天发科技有限公司YB-2型澄明度检测仪;上海一恒科学仪器有限公司HWS-24型电热恒温水浴锅。
1.2 试药
劳拉西泮片(A厂家,规格:1mg,批号:131002,140301,140402;B厂家,规格:1mg,批号:B140701,B140434);劳拉西泮片辅料由厂家提供;甲醇、乙腈为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 ChP2015有关物质检查方法(ChP法)
2.1.1 色谱条件 色谱柱:Agilent ZORBAX SB-C18柱(250mm×4.6mm,5μm);流动相:0.05mol/L磷酸二氢铵溶液(含0.5%三乙胺,用磷酸调节pH值至2.5)-甲醇-乙腈(40∶35∶30);流速:1.0mL/min,检测波长:230nm,柱温:30℃,进样量:20μL;稀释溶剂:乙腈。
2.1.2 测定方法 取本品细粉适量(约相当于劳拉西泮2mg),置10mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,滤过,取需滤液作为供试品溶液。精密量取供试品溶液20μL,注入液相色谱仪,记录色谱图至主成份保留时间的3倍。
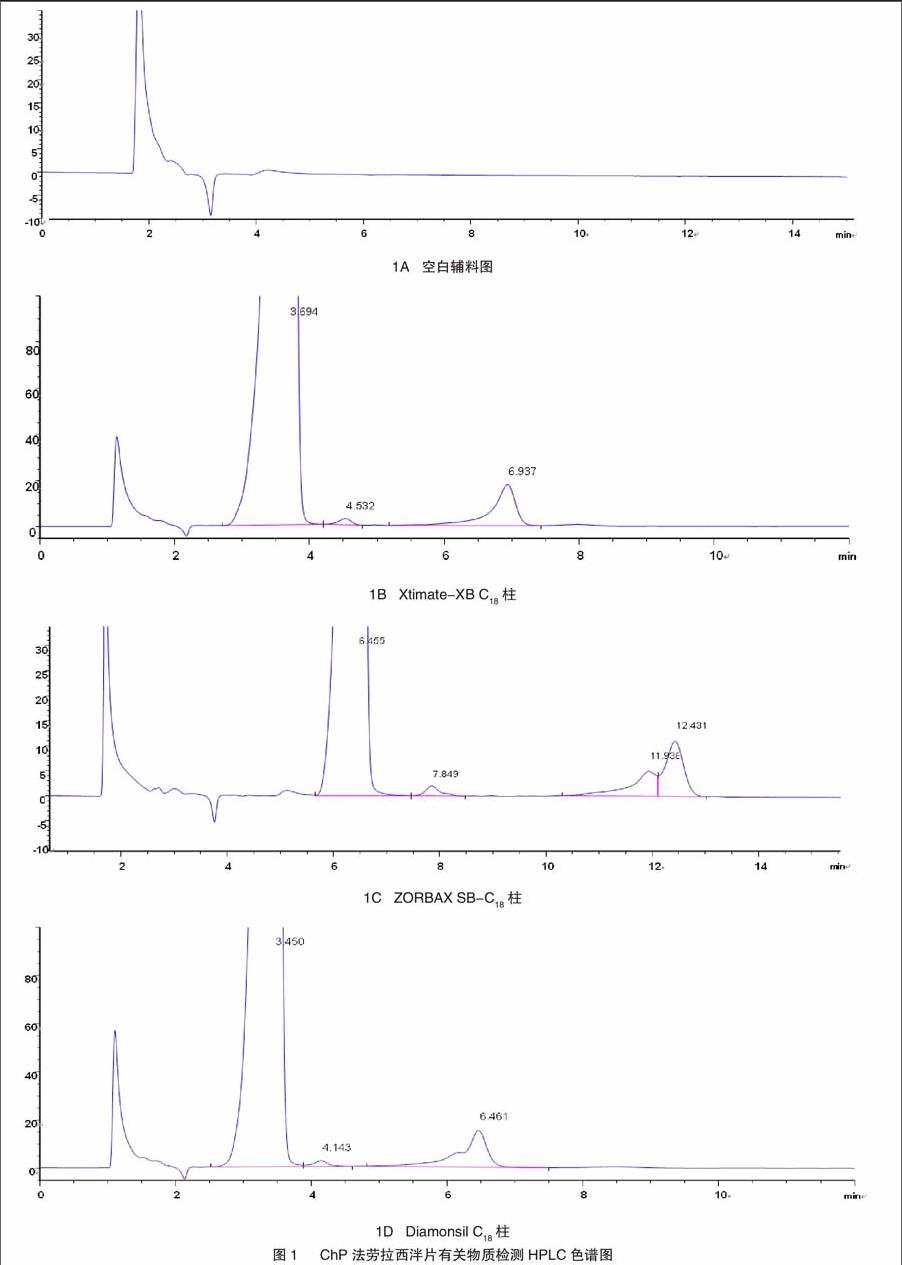
2.1.3 测定结果 杂质C与相邻杂质(相对保留时间分别约为1.9和1.8)不能有效分离(图1B),将色谱柱更换为Xtimate-XB C18柱(150mm×4.6mm,5μm)(图1C)或Diamonsil C18柱(图1D)(150mm×4.6mm,5μm),并通过改变流动相比例±5%、pH值±0.2、柱温±5℃等条件下均不能有效改善杂质分离情况,杂质C与相邻杂质重叠严重,甚至重合,影响了有关物质的指认和结果判定。
2.2 USP39有关物质检查方法(简称USP法)
2.2.1 色谱条件 色谱柱:Agilent ZORBAX SB-C18柱(250mm×4.6mm,5μm);流动相:水-乙腈-冰醋酸(50∶50∶1.2);流速1.0mL/min,检测波长:230nm,柱温:30℃;稀释溶剂:甲醇-缓冲液(三水合乙酸钠67.7g,加水1L溶解,用冰醋酸调pH值至5.0±0.05)(75∶25)。
2.2.2 测定方法 除稀释剂外,其余条件同“2.1.2”项。
2.2.3 测定结果 与ChP法杂质检出个数一致,均检出3个杂质,但本法色谱图中,杂质C与相邻杂质(相对保留时间分别为2.2和1.8)能完全分离,主峰和各杂质峰对称性良好,各杂质峰均能够准确积分。USP法条件下得到的典型色谱图见图2。
2.3 两种方法有关物质检查比较
2.3.1 USP法和ChP法检测两厂家劳拉西泮片的有关物质 由表1可知,两种方法检出的杂质个数一致,但USP法检出总杂质的总量更高。采用ChP法检测结果发现,在不同色谱柱上,杂质C均拖尾严重,不能与相邻杂质有效分离,因此不能分别对杂质C和相邻杂质进行准确积分和定量。而采用USP法检测结果发现,杂质C与相邻杂质分离效果好,并能准确积分和定量,且各杂质峰对称性和重现性均良好。
2.3.2 检测限 采用USP法,精密称取劳拉西泮对照品适量,用稀释剂溶解并制成0.0979μg/mL的溶液,测得检测限为1.958ng;采用ChP法,精密称取劳拉西泮对照品适量,用乙腈溶解并制成0.1857μg/ml的溶液,测得检测限为3.714ng。
2.3.3 溶液稳定性试验 分别取“2.1.2”和“2.2.2”项下供试品溶液,室温条件下放置,分别在第0、4、8h时进样,记录色谱图。结果表明,两种色谱条件下,供试品溶液在8h内均稳定。
2.3.4 耐用性试验 按USP法,将色谱柱更换为Xtimate-XB C18柱(150mm×4.6mm,5μm)和Diamonsil C18柱(150mm×4.6mm,5μm),采用“2.2.1”项下色谱条件,并通过改变流动相比例±5%、pH值±0.3、柱温±5℃的情况下,对本品进行有关物质测定。结果显示,在上述各种条件下,有关物质测定结果基本一致,劳拉西泮主峰与相邻杂质峰以及各杂质峰之间分离度良好,表明USP法耐用性良好。
2.3.5 专属性试验 按照企业提供的处方比例,取混合均匀的辅料适量(约相当于劳拉西泮2mg),置10mL量瓶中,加稀释剂溶解并稀释至刻度,摇匀,滤过,取滤液作为辅料溶液,进样测定,记录色谱图。结果表明,在两种色谱条件下,辅料均在相对保留时间约为0.4处出现色谱峰,应在积分和计算时加以扣除。
2.3.6 强制破坏试验 按USP法,称取劳拉西泮对照品约10mg,置25mL量瓶中,加稀释剂溶解并稀释至刻度,摇匀,作为对照品储备液。分别量取对照品储备液5.0mL,置5个10mL量瓶中,其中三个分别加入1mol/L盐酸溶液,1mol/L氢氧化钠溶液和3%双氧水溶液2ml,室温下放置2h,加稀释剂稀释至刻度;另两个先加稀释剂稀释至刻度,摇匀,一个置60℃水浴中加热2h,另一个于4500lx照度下放置24h。取上述各溶液分别进样,记录色谱图。结果表明,劳拉西泮在酸、碱、氧化、光照与热等强制性破坏条件下产生的降解产物均能与主峰有效分离。结合2.3.5专属性试验结果可知,各降解产物峰均在劳拉西泮峰之后,辅料峰不干扰降解产物峰的指认和计算。
3 讨论
通过试验发现,采用ChP2015法检查劳拉西泮片有关物质即使达到标准中系统适用性试验要求(杂质C与劳拉西泮峰分离度大于4.0),杂质C与相邻杂质仍不能有效分离。在劳拉西泮片有关物质限度控制的要求中,ChP2015标准对劳拉西泮片杂质C及总杂质的限度做出了规定,而USP39标准对劳拉西泮片的每一个杂质限度均做出了规定。作为劳拉西泮片的易降解杂质之一,杂质C是劳拉西泮片质量控制的重要内容。因此,劳拉西泮片有关物质检查项目中包含杂质C在内的主要杂质间的有效分离是保证其质量控制的前提条件。
通过试验比较,采用ChP2015法很容易将杂质C与其相邻杂质误判为一个杂质,进而造成检测结果的错误。若按药典规定范围内微调流动相组份等条件,杂质C拖尾严重,也无法达到与相邻杂质的有效分离,杂质C和相邻杂质均不能够准确积分和定量,对检测结果的判定有较大影响;而采用USP法杂质C与相邻杂质分离良好,能对各杂质准确积分和定量,方法灵敏度较高,色谱条件明显优于ChP2015法。因此,建议优化ChP2015中劳拉西泮片有关物质检查方法。
在ChP2015法与USP39法两种色谱条件下,辅料均在相对保留时间约为0.4处出现色谱峰,建议在质量标准有关物质检查项下限度规定时明确指出“扣除相对保留时间约为0.4之前的溶剂峰和辅料峰”。
[参考文献]
[1] 蔡喆.小剂量米氮平与劳拉西泮治疗慢性失眠症的临床分析[J].实用药物与临床,2013,16(9):821-823.
[2] 汤庆平,李宏,杨丽芬,等.文拉法新与劳拉西泮治疗广泛性焦虑症的比较[J].上海精神医学,2006,18(4):228-229.
[3] 李瑛.劳拉西泮的现状及前景展望[J].中国医药导报,2000,2(6):30-31.
[4] 王君,刘秀平,赵晓彦,等.精神科门诊一日精神药物使用情况调查[J].中国药物依赖性杂志,2015,24(4):276-279.
[5] 肖逸丽,左桂莲,刘满芬.门诊老年患者镇静催眠药的临床用药分析[J].今日药学,2015,25(9):666-668.
[6] 韦仕荣.癫痫持续状态治疗现状[J].中国医药指南,2011,9(27):39-41.
[7] 赵艳敏,王志敏,郑爱萍.苯二氮类药物药剂学研究新进展[J].中国新药杂志,2012,21(23):2771-2775.
[8] European Directorate for the Quality of Medicines and Healthcare(EDQM).European Pharmacopoeia 8.0th Edition[S].Nordlingen(German),2013:2639-2641.
[9] The British Pharmacopoeia Commission.The British Pharmacopoeia(2016)[S].London:the Stationery office,2015:765.
[10] The United States Pharmacopoeia Commission Inc.The United States Pharmacopoeia(39)[S].Rockville:the United States Pharmacopoeia Convention Inc,2015:4622-4624.
[11] Society of Japanese Pharmacopoeia.The Japanese Pharmacopoeia(16)[S].Toko(Japan),2011:1045.
[12] 中华人民共和国国家药典委员会.中国药典[S].2015年版二部,北京:中国医药科技出版社,2015:452-453.
[13] 王慧,陈华,南楠.劳拉西泮中杂质6-氯-4-(2-氯苯基)-2-喹唑啉甲醛的定位鉴别研究[J].药物分析杂志,2009,29(12):1985-1988.
[14] 程东升,陈蕾,南楠.劳拉西泮原料及其片剂中有关物质的检查[J].药物分析杂志,2006,26(12):1800-1803.
[15] 吕小丽,程鹏.劳拉西泮的合成[J].淮海工学院学报(自然科学版),2005,14(3):44-60.
(收稿日期:2016-03-07)

