一测多评法测定清热明目茶中大黄素、大黄酚与大黄素甲醚含量
周红艳,徐建东
(1.浙江省台州市第一人民医院 药剂科,浙江 台州 318020;2.上海市虹口区江湾医院 药剂科,上海 200080)
一测多评法测定清热明目茶中大黄素、大黄酚与大黄素甲醚含量
周红艳1,徐建东2Δ
(1.浙江省台州市第一人民医院 药剂科,浙江 台州 318020;2.上海市虹口区江湾医院 药剂科,上海 200080)
目的 建立清热明目茶中大黄素、大黄酚与大黄素甲醚含量的一测多评方法。方法 采用高效液相法采用一测多评法测定10批清热明目茶中大黄素、大黄酚和大黄素甲醚间的相对校正因子,考察其重现性,比较计算值与测得值的差异。结果 一测多评法测定10 批清热明目茶中大黄素、大黄酚与大黄素甲醚的含量,与外标法实测值基本一致。结论 该方法可靠,结果准确,可用于清热明目茶的质量控制。
一测多评;清热明目茶;大黄素;大黄酚;大黄素甲醚
清热明目茶由决明子(炒)、菊花和甜叶菊3味药材制得,具有平肝明目,清热祛风等功效, 临床常用于治疗高血压、头痛、头眩、目赤目糊等症状。其中决明子在我国古代就已入药,《神农本草经》就将决明子列为上品,称之“能治诸眼疾,久眼益精光,轻身。”经研究,决明子具有较好降血脂、降血压、抗氧化、抗衰老等疗效[1]。 据文献报道[2-4],决明子主要含有大黄酚、大黄素、大黄酸、大黄素甲醚、芦荟大黄素等成分。近年来,有不少研究对决明子成分做了相关研究,但均需要配制多种对照物质,实验操作过程繁琐,而且检验成本较高。而王智民等[5]最早提出建立利用一测多评法控制中成药多成分考察模式,随机在中成药领域大放异彩,得到极大推广。本实验以大黄素为参照物,建立其与大黄酚和大黄素甲醚间的校正因子,并计算各成分的量,通过考察不同色谱仪器和色谱柱对方法进行验证,并通过比较2种方法的差异来验证一测多评的准确性和可靠性。此种方法实现以一种对照物质(大黄素)对清热明目茶含有的多做有效成分进行质量控制,这为更真实评价清热明目茶质量提供全新模式,以便更好地控制清热明目茶的质量。
1 材料与方法
1.1 材料
1.1.1 药品与试剂:清热明目茶,规格: 3克/袋,共10个批次;大黄素对照品(批号:110756-200110,含量:100.0%)、大黄素甲醚对照品(批号:110758-201013,含量:99.8%)、大黄酚对照品(批号:110796-201017,含量:99.6%)均购自中国药品生物制品检定研究院;乙腈为色谱纯,水为纯化水,其他试剂为分析纯。
1.1.2 实验仪器:Agilent 1260高效液相色谱仪,检测器:1260VWD;色谱工作站:Agilent ChemStation for LC systems;色谱柱:sunfire ODS(4.6 mm×250 mm,5μm);AB-135S型电子天平(METTLER-TOLEDO)。
1.2 方法
1.2.1 色谱条件:色谱柱:sunfire ODS(4.6 mm×250 mm,5 μm);流动相:乙腈-0.1%磷酸, 梯度洗脱(程序:0 min时乙腈含量70%,0→20 min, 乙腈比例从70%→85%);检测器:1260VWD二极管阵列检测器,检测波长定为254 nm;柱温:30 ℃;进样量:20 μL。
1.2.2 溶液的配制
① 混合对照品溶液的制备:分别精密称取大黄素、大黄酚和大黄素甲醚对照品(P2O5真空干燥24 h)各适量,加甲醇制成每1 mL含大黄素5 μg、10 μg和大黄素甲醚5 μg的混合对照品溶液。
② 供试品溶液的制备:取混合均匀清热明目茶,研细,精密称取适量,置具塞锥形瓶中,精密加入甲醇25 mL,加热回流1 h,放冷,再称定质量,用甲醇补充减失的重量,摇匀,滤过,取续滤液,即得。
③ 阴性样品溶液的制备:按处方制备缺少上述3种成分的阴性样品,按②供试品溶液的制备步骤制得阴性样品溶液。

图1 对照品(A)、样品(B)和阴性样品(C)HPLC色谱图Fig.1 HPLC chromatograms of mixed standard(A),sample(B)and negative sample(C)
1.2.3 一测多评方法学考察
① 线性关系的考察:精密量取混合对照品溶液1、2、5、10、15、20、50 μL注入色谱仪,按照“1.2.1”项下给定色谱条件试验,以对照品进样量(X)为横坐标,峰面积积分值(Y)为纵坐标进行线性回归。
② 稳定性试验:取同一批供试品溶液,室温放置0、5、8、15、20、24 h,依照“1.2.1”项下色谱条件测定。
③ 精密度试验:取混合对照品溶液20 μL,连续进样6针,依照“1.2.1”项下色谱条件测定。
④ 加样回收率试验:取已知含量的清热明目茶6份,分别加入一定量的大黄素、大黄酚和大黄素甲醚对照品,依“1.2.1”项下色谱条件测定。
1.2.4 相对校正因子计算:本研究以大黄素为内参物,按文献给定公式[5]计算:
f=fs/fi=AsCi/AiCs
(注:As——内参物对照品峰面积,Cs——内参物浓度,Ai——待测成分峰面积,Ci——待测成分浓度)。
精密量取混合对照溶液2、4、8、15、20和25 μL,按“1.2.1”项下色谱条件测定。
1.2.5 相对校正因子重现性考察:分别考察型号分别为戴安UltiMate 3000 、SHIMADZU LC-10tvp和Waters 2695-2489等3台不同型号高效液相色谱仪,不同型号色谱柱Agilent C18(4.6 mm×250 mm,5 μm)、Thermo C18(4.6 mm×250 mm,5 μm)、SHIMADZU C18(4.6 mm×250 mm,4.5 μm)对相对校正因子的影响。
1.2.6 色谱峰专属性考察:色谱峰准确定位是保证一测多评法应用的前提,本实验中利用相对保留时间进行定位,采用大黄素与大黄酚和大黄素甲醚的相对保留时间结合色谱图整体特征来定位目标成分,并在不同高效液相色谱仪和色谱柱来考察方法耐用性。
1.2.7 样品测定:取10批清热明目茶,分别采用外标法和一测多评法计算清热明目茶中大黄素、大黄酚和大黄素甲醚。
2 结果
2.1 一测多评方法学考察结果
2.1.1 线性关系考察结果:大黄素、大黄酚和大黄素甲醚的回归方程分别为:
Y=3.25X+1.09,R2=1;Y=1.56X+0.45,R2=0.9999;Y=7.23X+3.88,R2=0.9999。
结果表明大黄素、大黄酚和大黄素甲醚进样量分别在0.531~2.582 ng、1.223~5.215 ng 、0.511~2.502 ng范围内与峰面积呈良好的线性关系。
2.1.2 稳定性试验结果:大黄素、大黄酚和大黄素甲醚峰面积的RSD分别为0.7%、0.5%和0.9%,表明供试品溶液在24h内稳定。
2.1.3 精密度试验结果:大黄素、大黄酚和大黄素甲醚峰面积的RSD分别为1.1%、0.4%和0.8%,表明仪器的精密度良好。
2.1.4 加样回收率试验结果:回收率结果见表1-3。
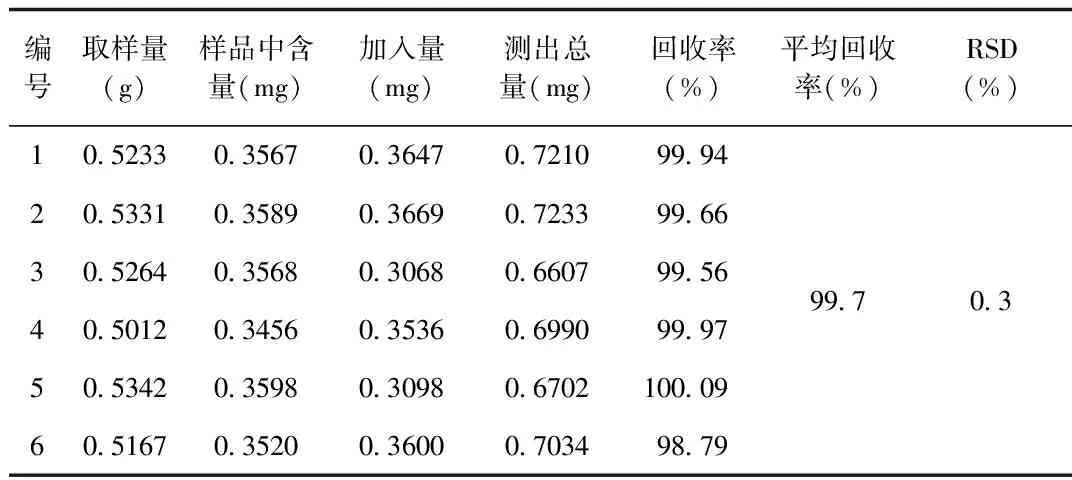
表1 大黄素回收率测定结果(n=6)

表2 大黄酚回收率测定结果(n=6)
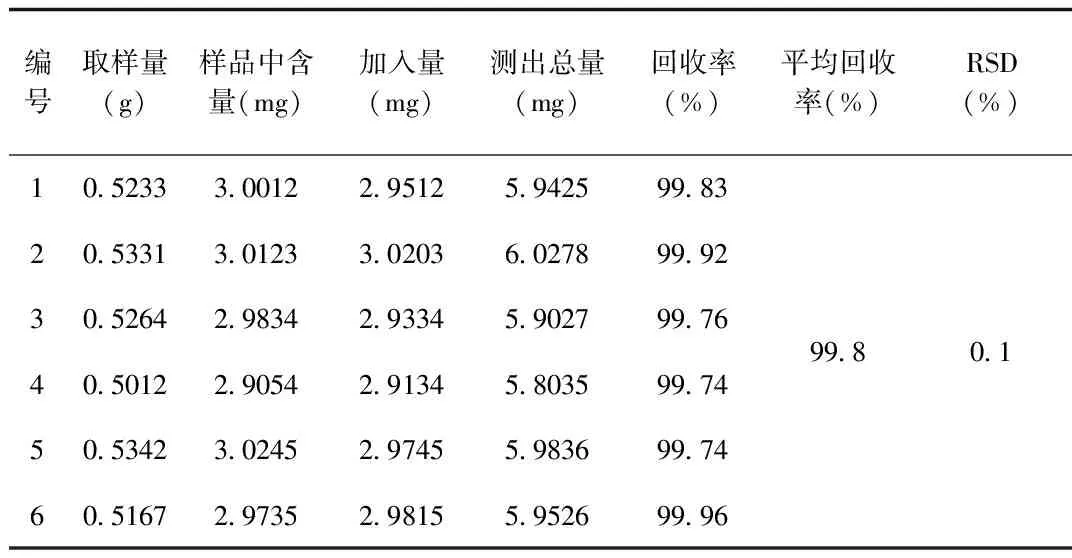
表3 大黄素甲醚回收率测定结果(n=6)
2.2 相对校正因子计算结果 大黄酚和大黄素甲醚的校正因子分别为0.694和3.596,RSD分别为0.4%和0.4%。
2.3 相对校正因子重现性考察结果 通过对3台不同型号的色谱仪和色谱柱进行交叉考察验证,相对校正因子比较稳定,大黄酚和大黄素甲醚RSD分别为0.6%和0.1%,可以看出一测多评法可以运用在检测清热明目茶中大黄素、大黄酚和大黄素甲醚成分中,方法耐用性强,简便可靠。见表4。
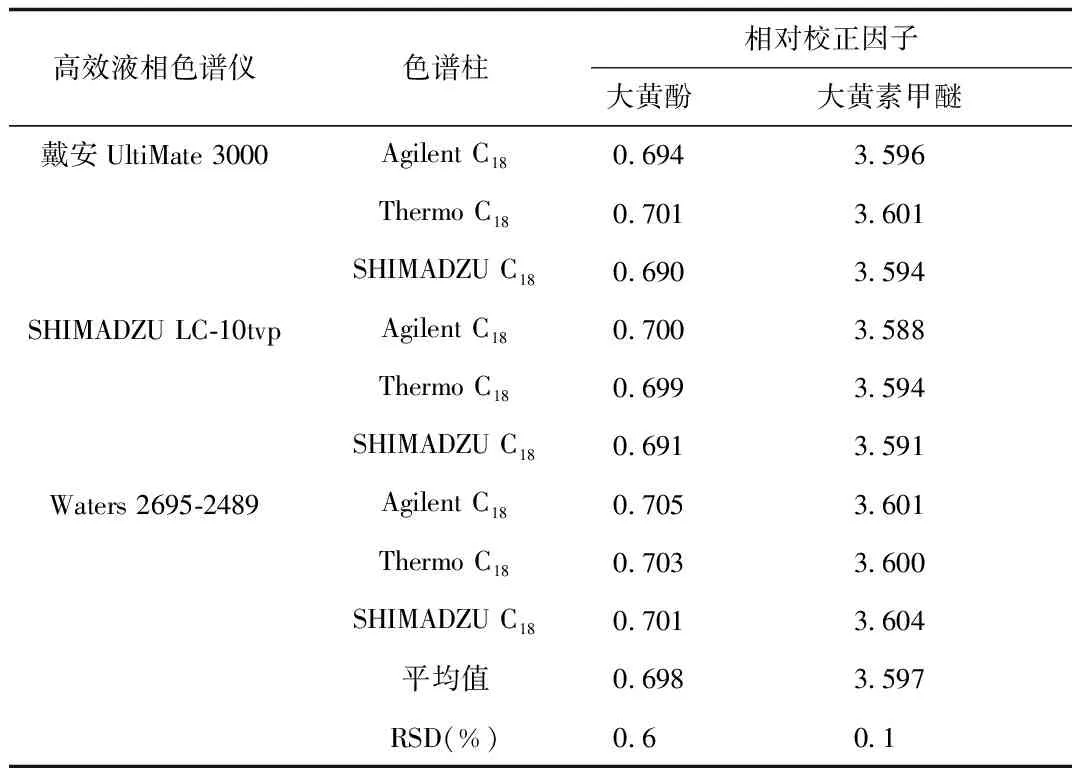
表4 高效液相色谱仪及色谱柱对相对校正因子的影响
2.4 色谱法专属性考察结果 大黄酚和大黄素甲醚相对大黄素保留时间的RSD分别为0.1%和0.2%,偏差很小,可以看出按照本实验方法试验,不同色谱仪和色谱柱对相对保留时间影响甚微,3种成分相对位置(色谱峰中相对保留时间)比较稳定,在已知一种成分保留时间的前提下可以将相对保留时间作为任2种成分的定性依据,结合其他相关鉴别方法对清热明目茶进行定性分析。见表5。

表5 不同色谱仪及色谱柱对相对保留时间的影响
2.5 样品测定结果 10批样品测定结果见表6。为比较外标法和一测多评法之间存在的差异,本研究采用2种方法进行考察:①比较外标法与一测多评法所测含量的夹角余弦值[5],大黄酚和大黄素甲醚夹角余弦值分别为0.9999和0.9995;②通过计算清热明目茶10批中2种成分分别采用2种方法所得结果,结果RSD值均小于1.0%,可以认为2种方法测得结果基本一致。通过2种方法对含量结果的比较,可以看出所测含量没有显著差异,一测多评法可以作为清热明目茶考察这3种成分的质控方法。见表6。
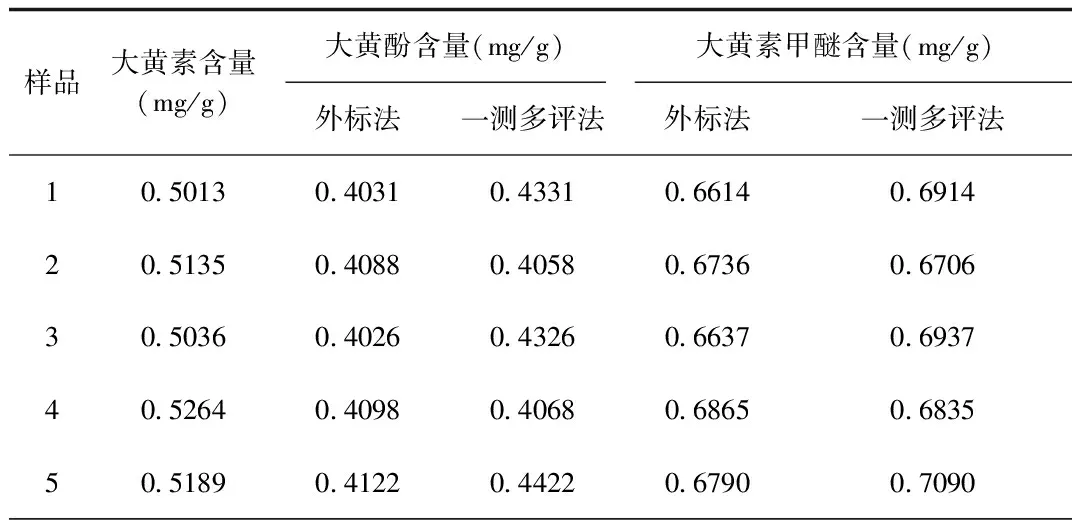
表6 样品的测定结果

续表
3 讨论
利用在外分光光法全波长扫描混合对照溶液发现,本实验涉及到的三种蒽醌类化合物在225 nm、255 nm及285 nm处均有都有较好的吸收。在225 nm处存在末端吸收故而舍去,而在285 nm处相比254 nm存在响应值低、色谱分离不理想等缺点,所以选择254 nm波长为本实验波长。
本实验共考察甲醇-水、乙腈-水、甲醇-0.1%磷酸溶液及乙腈-0.1%磷酸溶液等诸多流动相,结果只有采用乙腈-0.1%磷酸溶液是3个对照物质才同步出现信号并实现完全分离,但是大黄素甲醚保留时间过长,所以最终采用梯度洗脱程序。通过了解3种物质理化性质,样品提取介质选取甲醇,通过比较浸泡法、超声法和加热回流3种方法,最后发现只有加热回流1 h以上才能完全提取3种物质,达到实验制备要样品要求。
一测多评法(QAMS)比较传统外标法存在诸多优点,它可在待测成分对照品不易得到或不稳定等情况下,使用一种对照物质利用相对校正因子同时能测定多成分的含量。目前,一测多评法已在中药材及饮片质量评价中广泛应用[6-9]。此种方法不仅大大地节省了检验成本,同时也极大地简化实验操作,有效提高工作效率和实验准确性,方法有效可行,可以为制定本药品标准是提高参考。
[1] 郝延军,桑育黎,赵余庆,等.决明子的研究进展[J].中草药,2001,32(9):858-859.
[2]高钦,许惠琴,陈建伟,等.不同炮制的决明子保肝及润肠通便作用研究[J].中药新药与临床药理, 2007,18(3):194-196.
[3]励娜,杨荣平,张小梅,等.决明子不同清炒品中蒽醌类成分的含量测定[J].海峡药学,2007,19(8):42-43.
[4]李秋红.决明子的化学、药理与炮制研究进展[J].中医药学报,2006,34(6):48-50.
[5]王智民,高慧敏,付雪涛,等.一测多评法中药质量评价模式方法学研究[J].中国中药杂志,2006,31(23):1925-1928.
[6]冯伟红,王智民,张启伟,等.一测多评法测定秦皮药材与饮片中香豆素类成分的含量[J].中国中药杂志,2011,36(13):1782-1789.
[7]高慧敏,宋宗华,王智民,等.适合中药特点的质量评价模式— QAMS 研究概述[J].中国中药杂志,2012,37(4):405-416.
[8]陈建维,刘圆,刘晟楠,等.一测多评法测定枳实中4种黄酮类成分[J].中草药,2015,46(9):1374-1377.
[9]刘圆,魏惠珍,龚建平,等.一测多评法测定健脾丸中4 种黄酮类成分[J].中成药,2015,37(5):995-999.
(编校:王冬梅)
Content determination of emodin,chrysophanol and physcion in Qingre Mingmu Tea by quantitative analysis of multi-components by single-marker
ZHOU Hong-yan1, XU Jian-dong2Δ
(1.Department of Pharmacy, Taizhou First People’s Hospital of Zhejiang Province, Taizhou 318020, China; 2.Department of Pharmacy, Jiangwan Hospital of Shanghai Hongkou Distric, Shanghai 200080, China)
ObjectiveTo develop a method of quantitative analysis of multi-components by single marker(QAMS)for determination of emodin,chrysophanol,physcion in Qingre Mingmu Tea.MethodsBased on the HPLC, the relative correction factor of emodin was determined using magnolol as an internal reference substance, the method was evaluated for reproducibility, and the difference between calculated and measured values was compared.ResultsThe quantitative results of ten batches of Qingre Mingmu Tea by QAMS was basically consistent with that by external standard method.ConclusionThe QAMS method is reliable and accurate, which might be used for the quality control of Qingre Mingmu Tea.
quantitative analysis of multi-components by single marker(QAMS); Qingre Mingmu Tea; emodin; chrysophanol; physcion
周红艳,女,本科,副主任药师,研究方向:中药学,E-mail: 3369250235@qq.com;徐建东,通信作者,女,本科,副主任药师,研究方向:中药学,E-mail:2959198896@qq.com。
R284.1
A
10.3969/j.issn.1005-1678.2016.03.59

