阿苯达唑混悬剂的研制及其品质控制
党丽梅,崔耀明,冶冬阳,张 洁,李会芳,王炫博,李引乾
(1 西北农林科技大学 动物医学院,陕西 杨凌 712100;2 河南牧业经济学院,河南 郑州 450046)
阿苯达唑混悬剂的研制及其品质控制
党丽梅1,崔耀明2,冶冬阳1,张洁1,李会芳1,王炫博1,李引乾1
(1 西北农林科技大学 动物医学院,陕西 杨凌 712100;2 河南牧业经济学院,河南 郑州 450046)
[摘要]【目的】 对研制的阿苯达唑混悬剂的品质进行评价,为扩大其临床应用奠定基础。【方法】 采用分散法制备阿苯达唑混悬剂,以沉降体积比、再分散性和药物含量等混悬剂药剂学特性为指标,在单因素试验的基础上采用正交试验优选并确定最佳配方,对制备的阿苯达唑混悬剂进行品质评价。【结果】 阿苯达唑混悬剂的最佳配方为:每25 mL混悬剂中含有1.75 g阿苯达唑,0.3 g羧甲基纤维素钠,0.012 5 mL聚山梨酯-80,0.3 g柠檬酸,0.075 g苯甲酸钠。制备的阿苯达唑混悬剂沉降体积比为0.94,再分散性良好,平均回收率(99.60±1.47)%,变异系数1.48%。【结论】 确定的阿苯达唑混悬剂配方的药剂学特性稳定,制备的混悬剂物理稳定性良好,符合混悬剂的品质要求。
[关键词]阿苯达唑;混悬剂;药物研制;质量控制
阿苯达唑(Albendazole,ABZ)为苯并咪唑类广谱抗寄生虫药,是该类药物中驱虫谱较广、作用较强的药物之一,对线虫、吸虫、绦虫均有驱除作用,对包虫、泡球蚴病和细粒棘球蚴病也有较好的疗效,被广泛用于预防和治疗人及动物蛔虫病、钩虫病、鞭虫病、旋毛虫病以及粪类圆线虫病和棘球蚴病[1-4]。
阿苯达唑由于溶解度低,目前常用剂型以片剂和胶囊剂为主,这极大地限制了该药在临床上的应用。混悬剂是将难溶性固体药物以微粒状态分散于分散介质中形成的非均匀的液体剂型,药物以微粒状态分散,分散度较大,有利于延长药物作用时间及提高生物利用度[5-7]。本研究采用正交设计试验筛选配方,用分散法制备阿苯达唑悬液,考察其药剂学特征及稳定性,旨在为阿苯达唑兽用新剂型的研制奠定基础。
1材料与方法
1.1药品与试剂
阿苯达唑原料药,购自武汉祥华顺生物工程有限公司,批号:20130327;阿苯达唑对照品,购自中国兽医药品监察所,批号:20140415;阿拉伯胶,天津市天力化学制剂有限公司,批号:20120708;柠檬酸,天津博迪化工股份有限公司,批号:20121226;柠檬酸钠,天津市天力化学制剂有限公司,批号:20121108;聚山梨酯-80,天津市天力化学制剂有限公司,批号:20120907;冰乙酸,天津市百世化工有限公司,批号:20131026;无水乙醇,成都市科龙化工试剂厂,批号:20130619。
1.2仪器
SPECORD50紫外-可见分光光度计,德国耶那分析仪器有限公司;78-1型磁力加热搅拌器,江苏金坛保庆分析设备厂;PH-S3B型pH计,上海精密科学仪器有限公司;T25高速分散机,德国IKA公司;85-72型超速离心机,日本日立公司;BS-210S型电子分析天平,德国赛多利斯股份公司;QL-901型漩涡振荡器,其林贝尔仪器制造公司。
1.3阿苯达唑混悬剂的制备
1.3.1配方筛选以阿苯达唑为主药,按照混悬剂制备要求[8],通过单因素试验确定羧甲基纤维素钠为助悬剂、吐温-80为润湿剂、柠檬酸为絮凝剂、苯甲酸钠作为抗氧化剂。在单因素试验的基础上,选择L16(45)正交法进行设计,对羧甲基纤维素钠、吐温-80、柠檬酸、苯甲酸钠的用量进行筛选,以混悬剂的物理性状、沉降体积比、再分散性、药物含量等药剂学特性为评价指标,比较各配方的稳定性,以确定最佳配方[9]。正交试验各因素水平见表1。

表 1 阿苯达唑混悬剂配方正交试验的因素与水平
1.3.2制备方法采用分散法,用高速均质分散机制备混悬剂。按筛选确定的阿苯达唑混悬剂配方,先将助悬剂、润湿剂、絮凝剂、抗氧化剂溶于适量的蒸馏水中,待溶胀或溶解后备用。取润湿剂溶于少量的蒸馏水中,然后加入阿苯达唑润湿后,用高速均质分散机混匀,转移至25 mL量筒中,用蒸馏水冲洗均质机数次,将冲洗液转移至量筒,加蒸馏水至25 mL,密封筒口,混匀后在室温下静置保存备用[10-11]。
1.4混悬剂的质量评价
1.4.1颜色和pH变化观察记录混悬剂的外观、色泽、澄清度并测定其pH。
1.4.2沉降体积比的测定取阿苯达唑混悬剂25 mL置于量筒内,密塞后用力振荡1 min,记录混悬剂的总体积V0,静置1,2,3,4 h和2,3,4,7 d后,分别记录沉降物的体积V,然后计算混悬剂的沉降体积比F:F=V/V0[12-13]。
1.4.3再分散试验在室温环境下,将阿苯达唑混悬剂静置7 d后,以20 r/min的速度翻转量筒,观察混悬液的再分散性、物理性状以及絮凝性。
1.5阿苯达唑质量浓度测定方法的建立
1.5.1测定波长的选择精密称取105 ℃下干燥至恒质量的阿苯达唑标准品10.80 mg,置于100 mL容量瓶中,先加入2.0 mL冰醋酸溶解,再用无水乙醇稀释至刻度,振荡摇匀,作为标准品储备液。精密量取标准品储备液0.10 mL,置于50 mL容量瓶中,加无水乙醇稀释至刻度,摇匀,制成2.16 μg/mL的溶液备用。以无水乙醇作为空白对照,用分光光度计在190~450 nm波长处对阿苯达唑标准品进行扫描[14-15]。
1.5.2标准工作曲线的绘制用移液管分别精密吸取上述标准品储备液0.10,0.30,0.50,0.80和1.0 mL,置于10 mL容量瓶中,用无水乙醇稀释至刻度,配制成1.08,3.24,5.40,8.64,10.80 μg/mL的阿苯达唑系列对照品溶液备用。以无水乙醇作为空白对照,在1.5.1选择的波长处测定上述标准品的吸光度。以阿苯达唑标准品质量浓度(C)为横坐标(x),吸光度为纵坐标(y),绘制吸光度-质量浓度标准曲线,求其回归方程。
1.5.3样品处理将阿苯达唑混悬剂充分摇匀后准确移取0.5 mL于10 mL容量瓶中,用冰乙酸定容至刻度,充分摇匀。移取上述溶液0.5 mL于10 mL容量瓶,用冰乙酸定容至刻度,充分摇匀。重复上述操作2次后得测定样品。取该样品液用紫外分光光度计进行测定。
1.5.4回收率与精密度试验精密称取适量阿苯达唑和其他辅料,按1.3.2的方法制备成阿苯达唑理论质量浓度为10.0,30.0和70.0 mg/mL的混悬剂样品,转移至100 mL容量瓶定容,充分混匀。按上述样品处理方法处理后,在208 nm处测定吸光值,采用标准曲线计算阿苯达唑质量浓度,计算其回收率。
取标准品,按照1.3.2的方法配制成质量浓度为10.0,30.0和70.0 mg/mL的阿苯达唑混悬剂标样,分别在同一天测定3次;一周内隔天测定,共测定3次,分别计算日内精密度和日间精密度。
2结果与分析
2.1阿苯达唑混悬剂颜色和pH值的变化
试验制备的阿苯达唑混悬剂外观为乳白色,静置分层后,上清为无色透明液体,沉淀物为乳白色。放置时间较长时,上清液略呈淡黄色。放置过程中,上清液的pH无明显改变,介于5.5~6.2。
2.2阿苯达唑混悬剂沉降体积比的测定
阿苯达唑混悬剂在制备后7 d内的沉降体积比测定结果见表2。由表2可知,第9,10,15和16组药剂稳定性较好,不易沉降,符合药典规定的混悬剂品质控制标准。
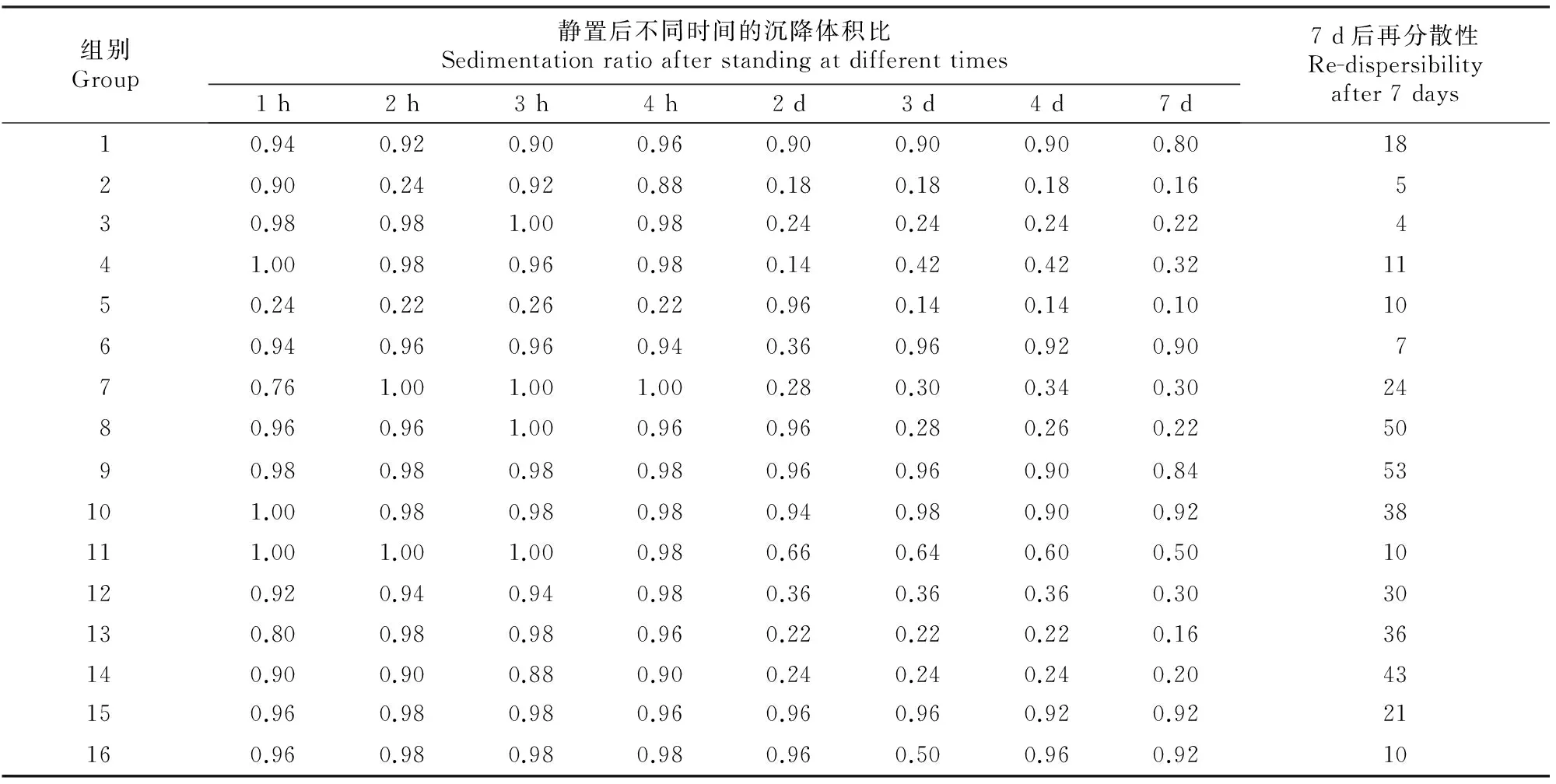
表 2 阿苯达唑混悬剂的沉降体积比和再分散性(V0=25 mL)
2.3阿苯达唑混悬剂的再分散性
在室温环境下,制备的阿苯达唑混悬剂静置7 d后可以重新分散,且瓶底无沉淀,混悬剂中无凝块,再分散性结果见表2。由表2可知,第2,3,4,5,6,11和16组药剂的再分散性较好。
2.4阿苯达唑混悬剂最佳配方的确定
通过对样品药剂学特性的考察,确定阿苯达唑混悬剂的最佳配方组成为第16组,即每25 mL混悬剂含1.75 g阿苯达唑、0.3 g羧甲基纤维素钠、0.012 5 mL吐温-80、0.3 g柠檬酸和0.075 g苯甲酸钠,利用该配方制备的阿苯达唑混悬剂稳定性、再分散性均良好。
2.5阿苯达唑含量的测定
2.5.1测定波长的选择图1结果表明,阿苯达唑标准品在208 nm波长处有最大吸收峰,故选择208 nm波长为阿苯达唑质量浓度的测定波长。
2.5.2标准工作曲线的绘制阿苯达唑标准曲线如图2所示。以吸光度(y)对阿苯达唑标准品质量浓度(x)进行线性回归,标准曲线方程为:y=0.040 9x+0.017 8(R2=0.998,n=5)。由此可见,阿苯达唑在质量浓度为1.08~10.80 μg/mL时线性关系良好。
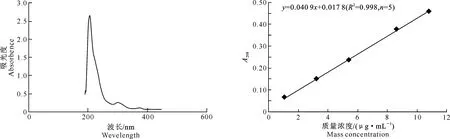
图 1 阿苯达唑的紫外吸收光谱
2.5.3回收率试验结果由表3可知,阿苯达唑混悬剂中阿苯达唑的平均回收率为(99.60±1.47)%,变异系数为1.48%。说明混悬剂中阿苯达唑的回收率高,测定方法的专属性好。

表 3 混悬剂中阿苯达唑的回收率
2.5.4精密度试验结果由表4可知,混悬剂中阿苯达唑的日内和日间平均精密度分别为0.45%和0.58%,日内和日间精密度(RSD)均小于5%,说明测定方法稳定性较好,测定结果真实可靠。
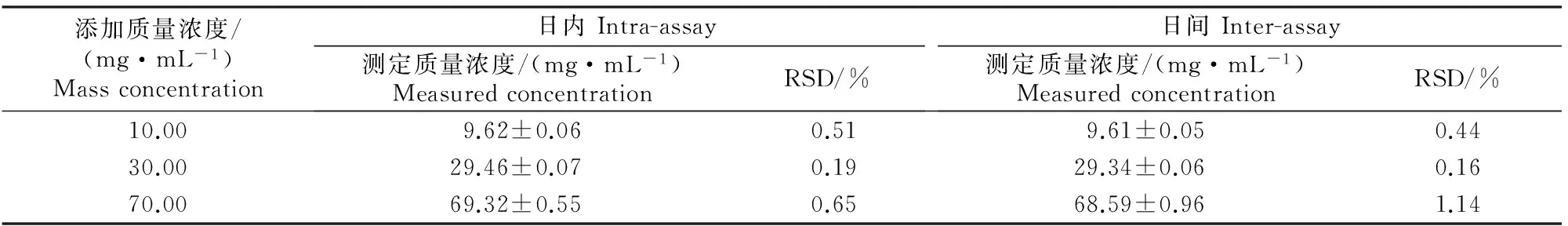
表 4 混悬剂中阿苯达唑的日内和日间精密度
3讨论
分析阿苯达唑混悬剂样品的各项药剂学特性可知,正交试验所涉及的几个因素中,影响混悬剂F值、再分散性等药剂学特征的主要因素是其自身的含量以及助悬剂、润湿剂的种类和含量。通过对配方组成进行单因素试验及正交试验,优选了制备阿苯达唑混悬剂的配方。在样品药剂学特性的考察中,沉降体积比试验结果显示,第9,10,15和16组稳定性较好,不易沉降,符合药典规定的混悬剂品质控制标准;再分散试验结果显示,第2,3,4,5,6,11和16组再分散性较好;故确定阿苯达唑混悬剂的最佳配方组成为第16组,即每25 mL混悬剂含1.75 g阿苯达唑,0.3 g羧甲基纤维素钠,0.012 5 mL聚山梨酯-80,0.3 g柠檬酸,0.075 g苯甲酸钠。
混悬剂的沉降体积比主要与助悬剂的特性有关,与药物含量的关系并不大。试验制备了阿苯达唑质量浓度为10.0,30.0,50.0和70.0 mg/mL的16组混悬剂,当助悬剂含量相同时,其沉降体积比基本一致,但在应用同一分散介质制备的不同质量浓度的混悬剂中,质量浓度为70 mg/mL的阿苯达唑混悬剂易出现药物凝集结块现象。为了增强混悬剂的稳定性,可适当增加助悬剂的质量浓度,以防药物凝集结块。本试验采用羧甲基纤维素钠为助悬剂,可有效增加药物再分散性并减缓混悬剂中的颗粒沉降速度,有效提高了该混悬剂的稳定性[16]。
本试验还尝试使用研钵法和均质法2种不同工艺来制备阿苯达唑混悬剂。结果表明,2种制备工艺所得样品在药剂学特征方面差异不大,但均质法所得样品的F值稍大,且操作简便,适当改进工艺和设备即可进行小规模生产。
[参考文献]
[1]Morris D L,Richard K S,Clarkson M J,et al.Comparsion of Albendazole and Praziquantel therapy ofEchinococcusgranulosusin naturally infexted sheep [J].Veterinary Parasitology,1990,36:1-2,83.
[2]万启惠.广谱驱蠕虫新药:丙硫咪唑 [J].遵义医学院学报,1988,11(1):73-74.
Wan Q H.Broad spectrum anthelmintic drugs:Albendazole [J].Journal of Zunyi Medical University,1988,11(1):73-74.(in Chinese)
[3]Skinner Adams T S,Davis T M,Manning L S,et al.The efficacy of benzimidazole drugs againstPlasmodiumfalciparuminvitro[J].Trans R Soc Trop Med Hyg,1997,91(5):580-584.
[4]中国兽药典委员会.中华人民共和国兽药典:兽药使用指南:化学药品卷 [M].北京:中国农业出版社,2011:135-136.
Commission of China Veterinary Pharmacopoeia.Veterinary pharmacopoeia of the People’s Republic of China:The veterinary drugs usage guide:Chemical medicine volume [M].Beijing:China Agriculture Press,2011:135-136.(in Chinese)
[5]朱仕铭.兽药缓释制剂 [J].兽药与饲料添加剂,1999,4(2):125.
Zhu S M.Sustained-release formulations of veterinary drugs [J].Veterinary Pharmaceuticals & Feed Additives,1999,4(2):125.(in Chinese)
[6]唐明义,耿奎士.高分子药物缓释材料 [J].化工新型材料,1999,26:26-28.
Tang M Y,Geng K S.Type of polymer drug delayed released materials [J].New Chemical Materials,1999,26:26-28.(in Chinese)
[7]王晓青,顾宗林,袁明月,等.阿苯达唑-壳聚糖纳米粒的制备及体内外评价 [J].中国新药杂志,2013,22(7):755-761.
Wang X Q,Gu Z L,Yuan M Y,et al.Preparation of albendazole-chitosan nanoparticles and its characteristicsinvivoandinvitro[J].Chinese Journal of New Drugs,2013,22(7):755-761.(in Chinese)
[8]毕殿洲.药剂学 [M].4版.北京:人民卫生出版社,1999:276-278.
Bi D Z.Pharmaceutics [M].Fourth Edition.Beijing:People’s Medical Publishing House,1999:276-278.(in Chinese)
[9]吴海坤,方炳虎,时书宁,等.恩诺沙星混悬液的研制及其在鸡组织中的残留研究 [J].动物医学进展,2010,31(4):47-52.
Wu H K,Fang B H,Shi S N,et al.Study on preparation of Enrofloxacin suspension and its residues study in chicken tissues [J].Progress in Veterinary Medicine,2010,31(4):47-52.(in Chinese)
[10]王敏儒,杨少林,杨鸿,等.恩诺沙星注射混悬剂的研制及药物含量测定 [J].中国兽医科技,2002,32(10):30-32.
Wang M R,Yang S L,Yang H,et al.Study on preparation of enrofloxacin suspension and measuring the content of enrofloxacin in suspensions [J].Chinese Journal of Veterinary Science and Technology,2002,32(10):30-32.(in Chinese)
[11]史同瑞,许腊梅,于万才,等.土霉素混悬剂的研制及药物质量指标测定 [J].现代畜牧兽医,2005,10(9):9-11.
Shi T R,Xu L M,Yu W C,et al.Preparation of Oxytetracycline suspension and determination of pharmaceutical quality index [J].Modern Journal of Animal Husbandry and Veterinary Medicine,2005,10(9):9-11.(in Chinese)
[12]中国药典委员会.中华人民共和国药典:Ⅱ部 [M].北京:化学工业出版社,2000:711.
Commission of China Pharmacopoeia.Pharmacopoeia of the People’s Republic of China:Part Ⅱ [M].Beijing:Chemical Industry Press,2000:711.(in Chinese)
[13]农业部新兽药评审委员会.兽药试验技术规范汇编 [S].北京:农业部新兽药评审委员会,2001.
The Review Committee on New Veterinary Drug of Ministry of Agriculture.The technical assembler about standards of veterinary drug test [S].Beijing:The Review Committee on New Veterinary Drug of Ministry of Agriculture,2001.(in Chinese)
[14]路宽,吴秀兰.药物阿苯达唑固体新剂型研究 [J].医药前沿,2012,6(3):4-5.
Lu K,Wu X L.Study on new forms of drug Albendazole solid [J].Health World,2012,6(3):4-5.(in Chinese)
[15]李华日,孙睿,李青梅,等.复方盐酸土霉素注射液的制备 [J].西北农林科技大学学报(自然科学版),2013,41(3):55-60.
Li H R,Sun R,Li Q M,et al.Preparation of compound Oxyteracycline hydrochloride injection [J].Journal of Northwest A&F University(Nat Sci Ed),2013,41(3):55-60.(in Chinese)
[16]中华人民共和国农业部.关于发布兽药稳定性试验技术规范(试行)的通知:农牧发[1999]13号 [S].1999-07-15.
Ministry of Agriculture of the People’s Republic of China.Circular on issusing technical standards of veterinary drug stability testing(for trinal implementation):Agriculture and Animal Husbandry Promulgated[1999] Thirteenth [S].1999-07-15.(in Chinese)
Preparation and quality control of Albendazole suspension
DANG Li-mei1,CUI Yao-ming2,YE Dong-yang1,ZHANG Jie1,
LI Hui-fang1, WANG Xuan-bo1, LI Yin-qian1
(1CollegeofVeterinaryMedicine,NorthwestA&FUniversity,Yangling,Shaanxi712100,China;2HenanUniversityofAnimalHusbandryandEconomy,Zhengzhou,Henan450046,China)
Abstract:【Objective】 The quality of prepared Albendazole suspension for veterinary use was evaluated to provide foundation for its application in clinical expansion.【Method】 Albendazole suspension was prepared using dispersion method.The optimal dispersion characteristics such as sedimentation volume,re-dispersibility and drug content were determined based on single factor experiments.Then the quality of prepared Albendazole suspension was evaluated.【Result】 The optimal preparation conditions for Albendazole suspension were Albendazole 1.75 g,sodium carboxymethyl cellulose 0.3 g,poly yamanashi ester-80 0.012 5 mL,citrate 0.3 g and sodium benzoate 0.075 g in a volume of 25 mL.The prepared suspension had the subsidence volume ratio of 0.94,fine re-dispersibility,the average recovery rate of (99.60±1.47)% and the variation coefficient of 1.48%.【Conclusion】 The prepared Albendazole suspension had good pharmaceutical and physical stability and meet the quality requirement of suspension.
Key words:Albendazole;suspension;drug development;quality control
DOI:网络出版时间:2016-05-03 14:0510.13207/j.cnki.jnwafu.2016.06.007
[收稿日期]2014-10-14
[基金项目]西北农林科技大学大学生创新创业训练计划校级重点项目(2201210712053)
[作者简介]党丽梅(1988-),女,陕西凤翔人,在读硕士,主要从事新兽药研发。E-mail:hjxniu7816@163.com [通信作者]李引乾(1962-),男,陕西岐山人,教授,博士,主要从事兽医药理学与毒理学研究。E-mail:liyinqian628@163.com
[中图分类号]S859.5+3
[文献标志码]A
[文章编号]1671-9387(2016)06-0040-06
网络出版地址:http://www.cnki.net/kcms/detail/61.1390.S.20160503.1405.014.html

