双加压法硝酸生产氧化和吸收效果计算及应用
白银慧(唐山中浩化工有限公司,河北唐山063611)
双加压法硝酸生产氧化和吸收效果计算及应用
白银慧
(唐山中浩化工有限公司,河北唐山063611)
摘要:根据双加压法硝酸生产的基本原理,结合实际推导出其两大主要过程——氨催化氧化和氮氧化物吸收效果的计算公式,应用该公式为判断铂催化剂活性,调整工艺指标,分析氨的消耗提供依据。
关键词:双加压法;硝酸生产;氨催化氧化;氮氧化物吸收
氨催化氧化和氮氧化物吸收是双加压法硝酸生产两大主要过程,氨氧化率反映了氨催化氧化效果,总吸收度反映氮氧化物(NO和NO2)的吸收效果。氧化和吸收效果的好坏综合反映了双加压法硝酸生产运行情况。计算、分析氨氧化率和总吸收度,对查找和解决双加压法硝酸实际生产问题有着重要的意义。
1 硝酸生产基本原理
双加压法硝酸生产基本原理主要有以下两个过程:氨在铂催化剂催化氧化为一氧化氮;一氧化氮氧化为二氧化氮,并被水吸收制得稀硝酸。可用下列反应方程式表示[1]:
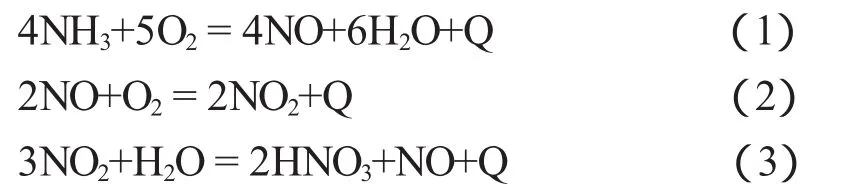
反应方程式(2)(3)的总反应方程式可以写成如下方程式:

反应方程式(1)(2)(3)的总反应方程式可以写成如下方程式:
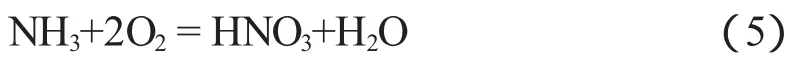
其中,氨在铂催化剂催化氧化的过程中还存在以下副反应:
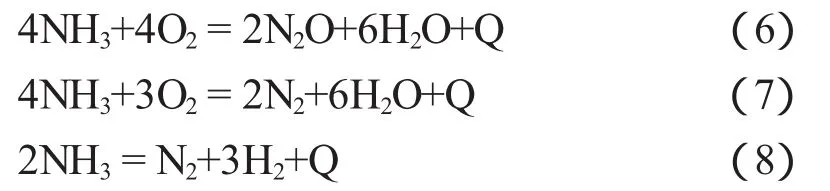
2 氨氧化率和总吸收效果计算
氨氧化率是指每摩尔的氨催化氧化生成NO的效率,用α表示,其大小反映了氧化效果的好坏。总吸收度是指气体中被吸收的氮氧化物的总量与进入吸收系统的气体中的氮氧化物总量之比,用β表示,其大小反映了吸收效果的好坏。
尾气中氮氧化物的摩尔含量为反应(1)生成的氮氧化物摩尔量减去未参与反应(4)吸收的氮氧化物摩尔量。由反应式(1)(4)可知NH3、NO和HNO3的对应关系为1mol NH3~αmol NO~αβmol HNO3。未参与吸收反应的氮氧化物摩尔量与尾气中的氮氧化物摩尔量相等,其关系式如下:
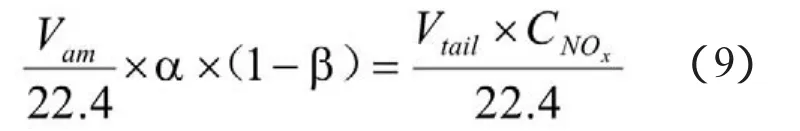
其中CNOχ表示系统的尾气中氮氧化物的摩尔含量;Vam表示正常生产气氨流量,Nm3/h;Vtail表示出系统的尾气体积流量,Nm3/h。
氨转化率是指每摩尔的氨转化生成硝酸的效率,用δ表示。同样由NH3、NO和HNO3的对应关系可以知道,δ=α×β。氨单耗是指每生产1吨折百硝酸需要消耗氨的重量,用η表示,单位为t/t。由反应式(5)结合氧化率(α)和总吸收度(β)的定义,可知1mol的NH3经氧化、吸收可得αβmol的HNO3,即1mol NH3~αβmol HNO3,则可以得到氨转化率与氨单耗的关系式如下:
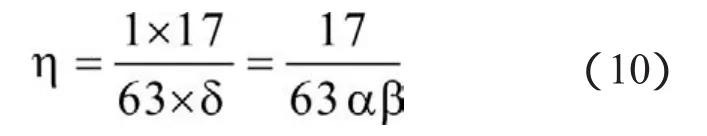
硝酸生产氨空比为氨空混合气中气氨的体积百分比,用γ表示。在双加压法硝酸生产中,氨空比值一般控制在9.6%左右,这里不妨取γ的值为9.6%。其表达式如下:
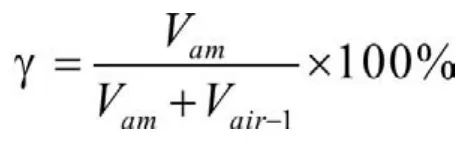
即

其中,Vair-1表示一次空气量,m3/h。
正常生产过程中,为保证反应式(11)生产的NO在吸收塔中按照反应式(10)合理地进行反应,要求尾气中氧含量控制在一定的范围,进一步要求二次空气量与一次空气量比例约为1∶5,则一次空气量与总空气量的关系如下:
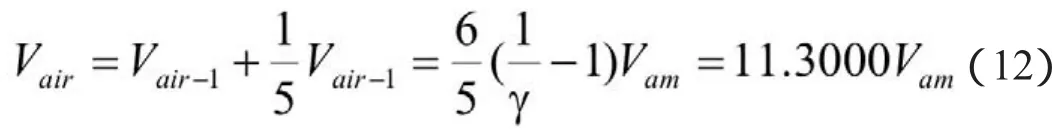
其中,Vair表示轴流压缩入口空气流量,Nm3/h。
由氨氧化率的定义可知,反应式(9)未转化生成NO的氨量为(1-α)Vam,不妨假设这些氨按照反应式(6)(7)(8)进行副反应,从这3个反应式来看,无论按照哪个(或哪几个)反应式,反应生成的N2O(或N2、或N2O和N2)均为参与反应氨的1/2,则可以知道参与副反应的氨量与生成的N2O(或N2、或N2O和N2)量对应关系式为1mol NH3~1/2mol N2O(这里不妨用N2O表示),则副反应生成的N2O量为(1-α)Vam/2mol;而且这些产物相对比较稳定,不再进行其它反应,并随尾气排出。空气中的氮气含量按79%计算,这部分气体不会参与反应,并随尾气排出,则进入系统氮气量与排出系统氮气量(不包括副反应生成的氮气)是相等的。其关系式如下:

其中,Co2表示出吸收塔尾气中氧气的摩尔含量。
将公式(12)代入公式(13),则:

由公式(9)(10)(14)可以求出氧化率(α)和总吸收度(β)的表达式:

3 氨氧化率和总吸收度应用
3.1判断铂催化剂活性
氨催化氧化是指氨在铂催化剂(网)的作用下按照反应式(1)氧化生产NO的过程,铂催化剂活性越高,氨参与副反应(6)~(8)比例就越少,相应地氨转化生成NO的比例(即氨氧化率)就越高;反之则相反。表1为某双加压法硝酸装置不同铂催化剂运行周期氧化率和总吸收度值。从表1可以看出,实际生产中随着铂催化剂运行周期的增加,因铂催化剂活性不断降低,相应的氨氧化率(α)也随之降低,这验证了上述分析。
因此,根据铂催化剂的活性与氨转化率的关系,生产中可以通过利用公式(15)计算氨氧化率,来分析判断铂催化剂的活性。铂催化剂在设计运行期内(一般180天),尤其是在运行初期,氨氧化率低于承诺的氧化率(一般大于96%),应该考虑是否中毒导致其活性降低,或其它原因(如催化反应温度控制)导致;在运行后期,考虑铂催化剂实际活性是否已降低,是否需要提前更换铂催化剂。
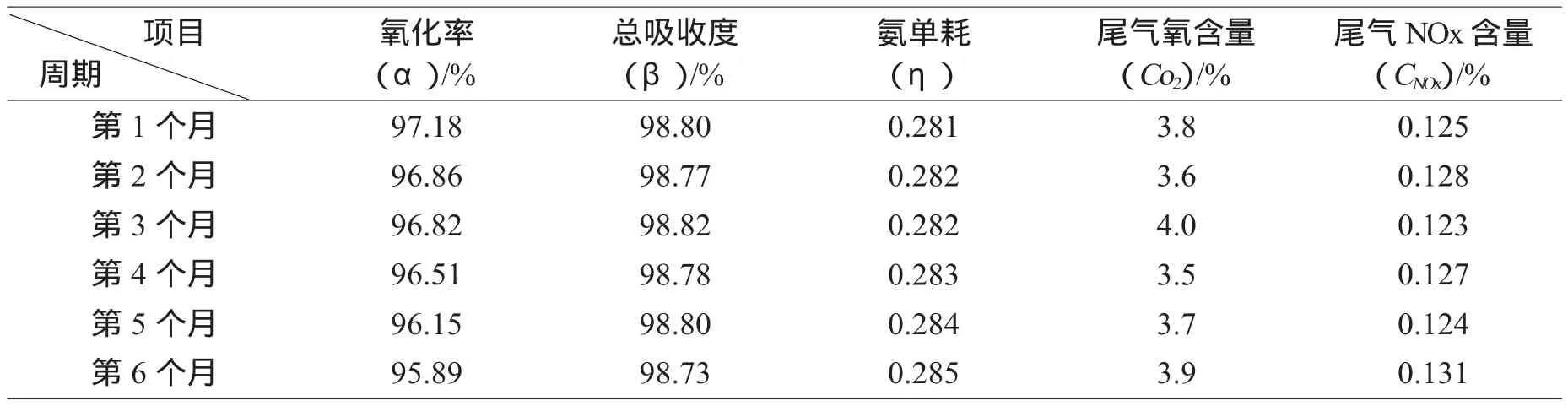
表1 某双加压法硝酸装置不同铂催化剂运行周期氧化率和总吸收度值
3.2工艺参数调整
反应式(2)(3)反映了氨催化氧化后生成的NO经转化生成硝酸的过程,由反应方程式可以知道上述两个过程是体积变小和放热反应,加压和降低温度能够促使反应向正反应方向进行,提高了NO氧化和NO2吸收的效率,进而提高了总吸收度。总吸收度的高低反映了反应式(2)(3)向正反应方向进行的效果,间接地反映了相关工艺参数控制是否合适。表2为某公司双加压法硝酸装置不同工况下氧化率和总吸收度值。从表2可以看出,实际生产中生产负荷越高,冷却水温度越低,相应的总吸收度(β)就越高,这是因为生产负荷越高,系统压力就越高;冷却水温度越低,温度梯度越大,高低压反应水冷却器和吸收冷却器所带走的反应热就越多,这两方面均有利于提高总吸收度(β)。
基于上述分析,在实际生产中当生产负荷较低时,为达到较好的吸收效果,可以通过降低冷却水温度或提高冷却水量,以带走更多的反应热量。生产负荷相同时,不同阶段的总吸收度(β)相差较大,或小于正常值(一般大于98%),应从强化吸收环节检查相关工艺参数(如冷却水温度、冷却水用量、吸收压力、吸收加水量等)控制是否合理,必要时进行调整。

表2 某公司双加压法硝酸装置不同工况下氧化率和总吸收度值
3.3分析氨单耗
硝酸生产涉及氨催化氧化和氮氧化物吸收两个过程,从公式(10)可知液氨单耗综合反映氧化和吸收的效果。实际生产中,如果液氨单耗偏高,则需要分析是氧化效果不好还是吸收效果不好导致,这就需要利用公式(15)(16)进行定量计算,并与指标值比较。
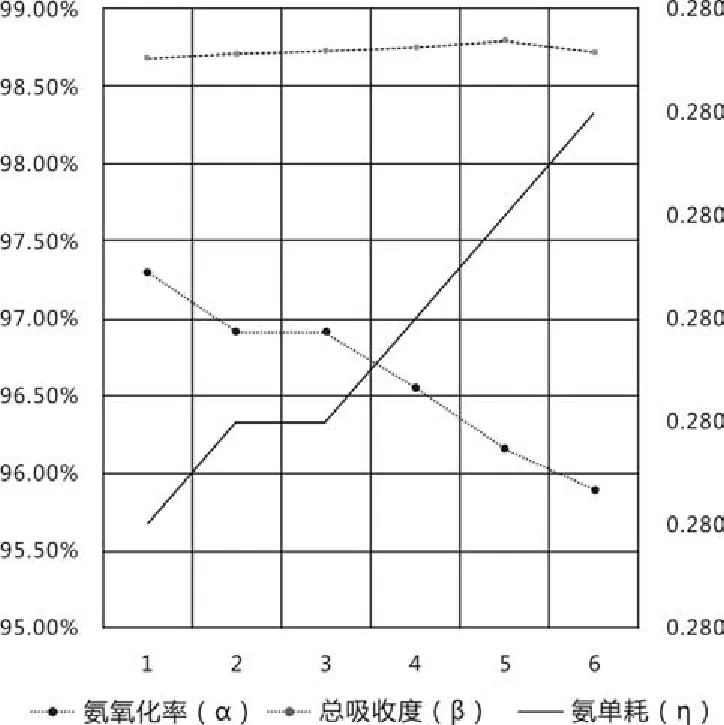
图1 氨单耗与氨氧化率和总吸收度对比曲线
根据表1数据绘制液氨单耗(η)与氨氧化率(α)和总吸收度(β)对比曲线,如图1。从图1可以看出,随着液氨单耗增加,氨氧化率(α)相应降低,但总吸收度(β)变化不太明显。这主要是因为:正常生产运行中,各工艺参数控制相对比较稳定,各项指标需要控制在一定范围内(如尾气氧含量Co2为3%~5%;尾气NOx含量CNOx为100~150mL/m3),经3.2分析可知在近似工况下总吸收度的影响不大,所以会导致上述结果。不妨取Co2=4%,CNOx=125mL/m3,则由公式(15)可得到氨氧化率(α)与氨单耗(η)之间的关系式:
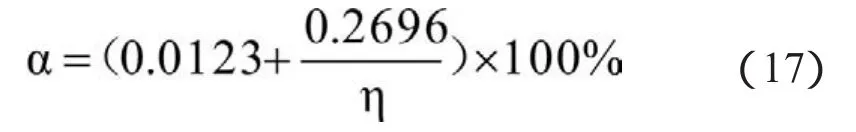
从公式(17)更容易看出氨氧化率(α)与氨单耗(η)的关系,实际生产中可以利用此公式估算氨氧化率。由3.1分析铂催化剂活性与氨氧化率相关,而氨氧化率又与液氨单耗有关,说明液氨单耗与铂催化剂活性相关。
4 结束语
氨氧化率和总吸收度计算公式(15)(16)是根据双加压法硝酸生产理论和实际推导出的一个半经验半理论公式。应用该公式计算出氨氧化率和总吸收度,为判断铂催化剂活性,调整工艺指标,分析氨的消耗提供依据。需要指出的是,在应用该公式时应结合实际情况,需要考虑各公式值及其参数的范围以及这些范围在实际生产中的意义。如氨单耗(η)其下限应该大于0.270t/t,即氨全部转化为硝酸(α×β=100%);其上限应该小于0.300t/t左右,超过该限值则生产成本可能会超过产品成本,实际生产意义不大。氨氧化率(α)和总吸收度(β)上限应分别小于100%;依据氨单耗(η)上限值,通过公式(10)可以算出其下限应分别大于90%,否则生产成本也可能会超过产品成本,实际生产意义也不大。因此,在计算时上述参数超过限值,应该考虑测量、分析数据和计算结果是否准确。
参考文献
[1]陈五平.无机化工工艺学(上册)(第三版)[M].北京:化学工业出版社,2002:315.□
Calculation and Application for Effect of Oxidation and Absorption of Dual-pressure Nitric Acid Production
BAI Yin-hui
(Tangshan Zhonghao Chemical Co.,Ltd.,Tangshan 063611,China)
Abstract:According to the basic principle of dual- pressure process of nitric acid production,deduced the formula for effect ofits twomain processes which were catalytic oxidation ofammonia and nitrogen oxides absorption actually. Application of the formula,provided the basis for determiningthe activityofa platinumcatalyst,adjustingprocess parameters process indicators and analyzingofconsumption ofammonia.
Key words:dual- pressure;nitric acid production;catalytic oxidation ofammonia;nitrogen oxides absorption
doi:10.3969/j.issn.1008- 553X.2016.03.018
中图分类号:TQ111.26
文献标识码:A
文章编号:1008- 553X(2016)03- 0051- 04
收稿日期:2016- 03- 22
作者简介:白银慧(1982-),女,助理工程师,从事己二酸和硝酸生产管理及技术开发工作,0315- 3034605,15103254143,he0zi@163.com。

