河北洨河人工湿地水体溶解性有机物性质的演化过程研究
马丽娜, 张 慧, 檀文炳, 虞敏达,黄智刚, 高如泰*, 席北斗, 何小松
1. 广西大学农学院,广西 南宁 530004 2. 中国环境科学研究院环境基准与风险评估国家重点实验室, 北京 100012 3. 中国环境科学研究院地下水与环境系统创新基地, 北京 100012
河北洨河人工湿地水体溶解性有机物性质的演化过程研究
马丽娜1, 2, 3, 张 慧2, 3, 檀文炳2, 3, 虞敏达2, 3,黄智刚1, 高如泰2, 3*, 席北斗2, 3, 何小松2, 3
1. 广西大学农学院,广西 南宁 530004 2. 中国环境科学研究院环境基准与风险评估国家重点实验室, 北京 100012 3. 中国环境科学研究院地下水与环境系统创新基地, 北京 100012
联合三维荧光光谱、紫外光谱和化学还原法,对洨河人工湿地水体DOC与COD的变化特征以及溶解性有机物(DOM)的来源、化学结构、腐殖化程度与氧化还原性质进行研究,以期为深入揭示DOM在人工湿地中的地球化学行为及其生态环境效应提供科学依据。结果显示,河流水体COD 60%以上来自DOC的贡献,而其经过人工湿地后含量的降低则主要是由有机物中的N,H,S,P元素更容易被去除所导致的,其贡献率可达65%。f470/520与BIX两种指数共同指示了水体DOM主要由微生物贡献,表明水体DOM明显受到微生物的降解作用。三维荧光光谱PARAFAC模型分析显示,人工湿地水体DOM包含类蛋白和类腐殖质组分,其中类富里酸和类胡敏酸组分比类蛋白质组分更容易被降解,类富里酸与类胡敏酸组分具有相似的分解命运。有色溶解性有机物(CDOM)与荧光溶解有机物(FDOM)具有共源性,均主要由类腐殖质组成,二者进入人工湿地后没有产生选择性降解。水体进入人工湿地后E2/E3,A240~400,r(A, C)与HIX指标没有发生显著变化,表明人工湿地对水体DOM的腐殖化程度不会产生显著影响。 然而,人工湿地环境不仅有利于形成还原态的DOM,促进水体三价铁的还原,而且可以提高DOM作为电子穿梭体的能力,这可能与DOM的芳香性碳在人工湿地中能够得以更好保存有关。
溶解性有机物;人工湿地;三维荧光光谱;紫外光谱;氧化还原
引 言
溶解性有机物(DOM)是一种由脂肪族和芳香族聚合物组成的非均相化合物,其在水生生态系统中扮演着十分重要的角色,其浓度、组成、结构以及氧化还原等性质均会对水生环境的生物学(例如微生物与浮游生物生态学[1])、化学过程(例如痕量重金属元素的形态与运输[2])以及物理性质(例如光学特性[3])产生直接或间接的影响。
人工湿地是由人工建造和控制运行的与沼泽地类似的水体地面,集合了土壤、人工介质、植物及微生物的物理、化学与生物三种协同功能,其独特的生态环境使得其水体DOM具有独特的性质和演化过程,并逐渐成为国内外研究热点。近年来,人们对人工湿地水体DOM的动态过程研究已有一些报道[4, 5],但仍存在许多方面的不足。第一,已有的研究结果主要是基于人工湿地模拟装置得出的,但这与实地的人工湿地不一定完全相符。第二,由于大多数研究所采用的分析方法较为单一,造成对人工湿地水体DOM浓度、组成、来源及结构的变化特征仍缺乏全面和深入的认识。第三,DOM参与的微生物活动、污染物降解与重金属转化迁移都涉及到了DOM的氧化还原性质[6],然而关于其在人工湿地中的演变机制研究还鲜有报道。
为此,选取河北洨河实地的人工湿地为研究区域,联合三维荧光光谱法、紫外光谱法和化学还原法,系统研究人工湿地中水体DOM各种性质的演化规律,以期为深入揭示DOM在人工湿地中的地球化学行为及其生态环境效应提供科学依据。
1 实验部分
1.1 研究区域概况
河北洨河人工湿地建于2013年6月,分布在衡井公路跨河桥上下游两侧,位于总退水渠和环城河下游,两条河流水体汇合后进入人工湿地(图1)。总退水渠的水除来源于天然水之外,还有相当一部分是来自桥东污水处理厂,环城河水主要是来源于黄璧庄水库与桥西污水处理厂。人工湿地总长度2 km,总面积368亩,其中植被面积232亩。人工湿地内水生植物近20种,主要是芦苇、棣棠、迎春、睡莲等喜水植物。

Fig.1 Location of the study area and sampling sites
1.2 样品处理
2014年8月在总退水渠、环城河与洨河人工湿地采集表层水样,其中总退水渠和环城河各采集2个样品,洨河人工湿地采集6个样品,具体采样点的分布情况见图1。采集样品时同时测定pH、溶解氧(DO)与水体温度(表1)。样品采集后立即用孔径0.45 μm的Millipore聚碳酸酯滤膜过滤,滤液中的有机物即为DOM,避光冷藏保存,备用。

Table 1 Basic parameters of water samples


1.4 亚铁与全铁含量的测定
亚铁含量采用邻菲罗啉分光光度法进行测定。全铁含量在测定之前,需预先加入10%的盐酸羟胺,将三价铁还原成二价铁,然后再采用邻菲罗啉分光光度法测定。
1.5 DOM化学还原容量的测定
取过滤后的样品置于棕色厌氧瓶中,调节pH为6.8,加入Pd/C作为催化剂,通入H2/N2(1/19)后密封,在25 ℃下振荡72 h,通入N2排出剩余的H2,在无氧环境下加入1 mmol·L-1K3[Fe(CN)6]溶液,密封后在25 ℃下振荡24 h,离心后取上清液,采用邻菲罗啉分光光度法测定二价铁的生成量,并根据还原1 mol三价铁需要1 mol电子计算电子转移数,其值与加入样品DOC总量的比值表示DOM的化学还原容量,与加入样品体积的比值表示单位体积水体的化学还原容量。
1.6 紫外光谱分析
紫外光谱分析采用日本岛津公司生产的UV1700紫外-可见分光光度计,扫描波长范围为200~400 nm,扫描间距为1 nm。测定254 nm处的吸光度值a(254),将其除以DOC浓度,记为SUVA254[L·(m·mg)-1];测定250和365 nm处的吸光度值a(250)和a(365),将a(250)与a(365)的比值记为E2/E3;对波长240~400 nm范围内进行面积积分,其值记为A240~400;计算波长275~295 nm和波长350~400 nm范围内吸收光谱斜率,分别记为S275~295和S350~400。
1.7 荧光光谱分析及其平行因子分析

三维荧光光谱的平行因子分析采用带有DOMFluor工具箱的MATLAB R2100a软件进行模拟。
2 结果与讨论
2.1 水体DOC浓度及COD的变化特征
总退水渠、环城河与洨河人工湿地水体DOC浓度分布在8~20 mg·L-1之间,环城河水体COD小于40 mg·L-1(图2),达到地表水环境质量Ⅴ类标准,总退水渠与人工湿地水体COD均分布在50~100 mg·L-1之间(图2),未达到地表水环境质量Ⅴ类标准。总退水渠水体DOC浓度和COD均明显高于环城河(图2),这可能是由桥东污水处理厂将未达到标准的尾水排入总退水渠所致。总退水渠与环城河从上游到下游约5 km,水体DOC浓度和COD均没有发生显著变化(图2),表明这两条河流在自然状态下水体有机物并不能得到有效去除。总退水渠与环城河汇合进入洨河人工湿地之后,水体DOC浓度和COD沿水流方向总体上呈现出逐渐降低的趋势(图2),表明人工湿地对污水厂尾水中有机物的去除具有一定的效果。以S1与S6分别作为人工湿地的进水口与出水口,估算人工湿地对水体有机物的去除效果,得出人工湿地DOC浓度和COD的降低率分别可达到12.0%和29.6%。

Fig.2 DOC concentration and COD value in waters of general waste canal, Huancheng River and Xiao River constructed wetland
水体中有机物(包括C,N,H,S,P元素)与还原性无机物(包括亚硝酸盐、硫化物与亚铁)都可以对COD做出贡献。本研究中所有水体样品均未检测出硫化物,因此仅将DOC、亚硝酸盐与亚铁含量换算成化学氧化所需氧量,估算这些还原性物质对COD的贡献,并将COD与这些还原性物质氧化所需氧总量的差值作为有机物中N,H,S,P元素对COD的贡献。如图3所示,总退水渠、环城河与人工湿地水体COD主要是来自DOC的贡献,其贡献值基本都在60%以上,大于有机物中N,H,S,P元素对COD的贡献,而亚硝酸盐与亚铁对COD的贡献极少。

Fig.3 Contributions of reducing substances to COD in waters
分析了人工湿地中DOC和有机物中N,H,S,P元素对COD沿水流方向减少量的贡献,结果如图4所示。从图4中可以看出,在人工湿地的上游,COD沿水流方向的减少量主要是由于DOC浓度的降低所引起的,而在人工湿地的下游,COD沿水流方向的减少量则主要是来自有机物中N,H,S,P元素含量降低的贡献。整个人工湿地从进水口(S1)到出水口(S6)有机物中N,H,S,P元素含量的降低对COD减少量的贡献值达到65%,要大于DOC浓度的降低对COD减少量的贡献值(图4)。由此可见,在人工湿地中,尽管COD主要是来自有机碳的贡献,但其沿水流方向的减少量则主要是来自有机物中N,H,S,P元素含量降低的贡献。

Fig.4 Contributions of DOC and elements N, H, S and P in organic matter to the decreased of COD along the stream in constructed wetland
2.2 水体DOM来源及组成的变化特征
总退水渠、环城河与洨河人工湿地水体DOM的f470/520与BIX值分别大于1.9与1.0(图5),两种指数共同指示了水体DOM主要由微生物贡献。人工湿地从S1~S2,BIX值下降显著(图5),这可能是由人为干扰所造成的,而从S2~S6,f470/520与BIX值均呈现逐渐增加趋势(图5),表明水体DOM明显受到微生物的降解作用。根据PARAFAC模型识别出总退水渠、环城河与洨河人工湿地水体DOM中四个荧光组分(图6)。C1(240, 300/380)为类色氨酸组分,C2(230, 275/340)为类酪氨酸组分,C3(250, 275, 350/410)为类富里酸类物质,C4(225, 260, 360/450)为类胡敏酸组分。总退水渠与环城河从上游到下游C1和C2组分与C3和C4组分在相对含量上分别呈现出增加与降低趋势(图7),表明水体DOM中类腐殖质组分比类蛋白质组分更容易被降解,类腐殖质在降解过程中逐渐向类蛋白质转化。人工湿地中除C1组分外,其他三种组分的相对含量沿水流方向总体上均表现出与总退水渠和环城河一致的变化趋势,但在人工湿地的上游区域这种变化趋势并不明显(图7),这主要是由于总退水渠与环城河汇合进入人工湿地之后水体环境发生了变化,微生物为了适应新环境或进行更替需要一个过程。S275~295和S350~400可用于半定量分析富里酸和胡敏酸含量的比值,总退水渠、环城河与洨河人工湿地水体S275~295和S350~400沿水流方向的波动均不大(图8),表明富里酸和胡敏酸具有一致的降解趋势,进一步证实了类富里酸组分与类胡敏酸组分在分解过程中具有相同的命运。
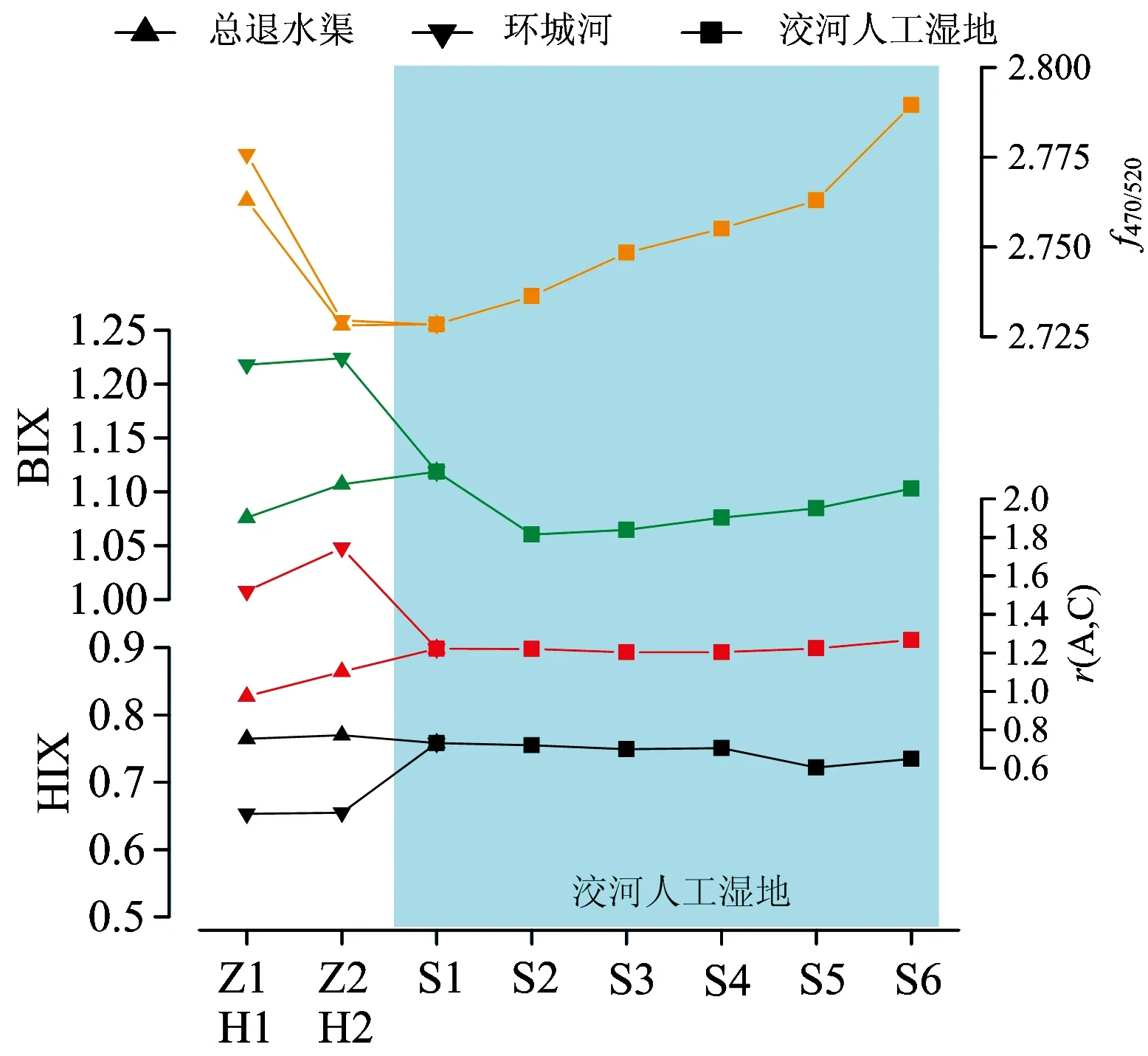
Fig.5 Indexs of fluorescence spectrum for waters DOM in general waste canal, Huancheng River and Xiao River constructed wetland
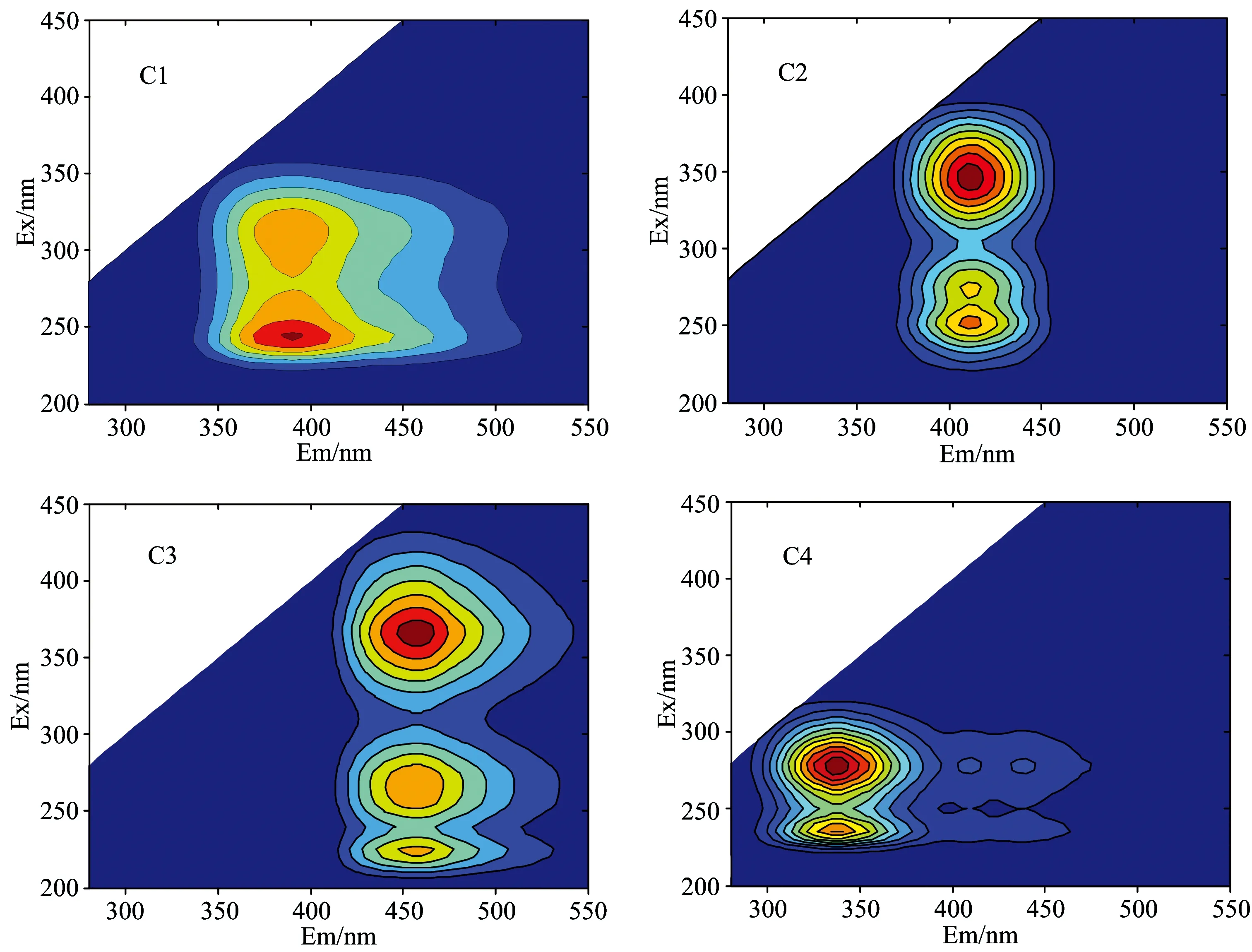
Fig.6 Four fluorescent components from parallel factor analysis

Fig.7 Percentages of C1, C2, C3 and C4 components in waters DOM
水体DOM中存在有色溶解性有机物(CDOM)与荧光溶解性有机物(FDOM),其相对浓度可分别以在355 nm处的吸光系数a(355)与荧光指标Fn(355)表征[7, 8]。a(355)和Fn(355)两种指标均与DOC浓度存在显著的正相关关系(图9),说明总退水渠、环城河与洨河人工湿地水体DOM中DOC浓度的变异可由CDOM与FDOM的变化来解释。此外,本研究还发现,不仅a(355)与Fn(355)之间存在显著的正相关关系(图9),而且上述两种指标分别与C3类富里酸组分和C4类胡敏酸组分的荧光得分值均存在显著的正相关关系(图9),表明总退水渠、环城河与洨河人工湿地水体CDOM与FDOM不仅具有共源性,都是由类腐殖质作为主要成分,而且二者在分解过程中没有选择性。

Fig.8 Indexs of ultraviolet spectrum for waters DOM in general waste canal, Huancheng River and Xiao River constructed wetland
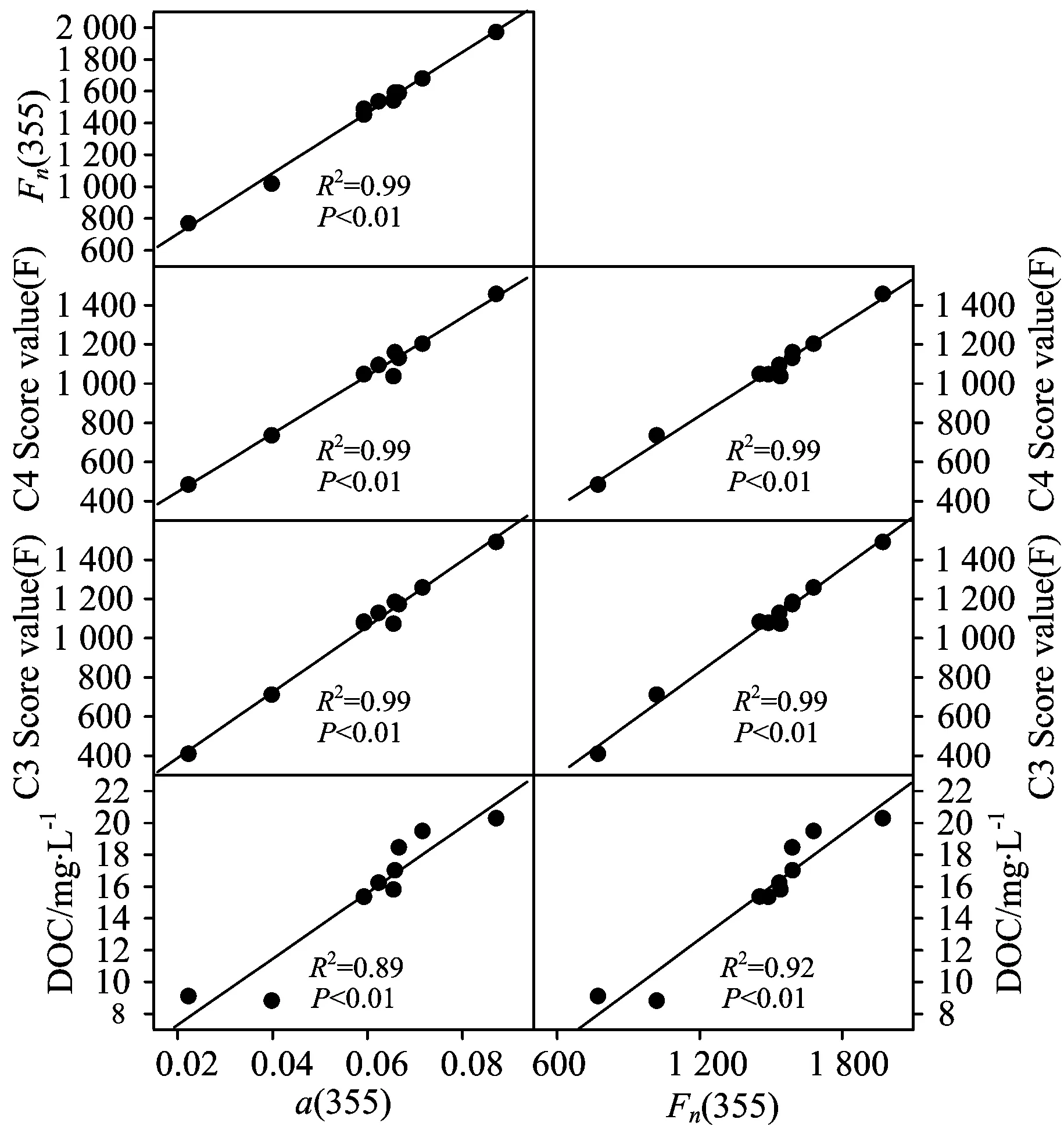
Fig.9 Relationships betweena(355) andFn(355), and betweena(355),Fn(355) and scores of C3, C4 components
2.3 水体DOM腐殖化程度及结构的变化特征
E2/E3,A240~400,r(A, C)与HIX腐殖化指数(humification index)指标在特定条件下都可以用于表征溶解性有机物DOM的腐殖化程度与分子量大小[9-12]。r(A, C)为DOM三维荧光光谱中类富里酸物质荧光峰强度与类胡敏酸物质荧光峰强度的比值,它与溶液pH存在一定的关系[11],然而本研究中所有水体样品之间pH差异并不大,均分布在7.13~7.45之间(表1),因此r(A, C)在本研究中主要是作为表征腐殖化程度的指标。在上述四个腐殖化程度指标中,E2/E3值与腐殖化程度和分子量成反比,其他三个指标值均与腐殖化程度和分子量成正比。从图5与图8可以看出,总退水渠与环城河从上游到下游E2/E3,A240~400,r(A, C)与HIX指标没有表现出一致的变化趋势,说明在总退水渠与环城河中,选用何种指标表征水体DOM的腐殖化程度需要进一步研究。然而,总退水渠与环城河汇合进入人工湿地之后,四种指标沿水流方向其波动均不明显(图5与图8),共同指示了人工湿地中水体DOM的腐殖化程度没有发生显著的变化。当HIX>0.8时,水体DOM具有显著的腐殖化特征[9, 10],但本研究中所有样品HIX均小于0.8(图5),表明水体DOM的腐殖化程度都较低,主要是来自于微生物的生命活动和死亡分解。
总退水渠水体SUVA254值明显高于环城河(图8),这可能是由总退水渠水体DOM具有更高的腐殖化程度所致。总退水渠与环城河从上游到下游SUVA254值明显下降(图8),表明水体DOM在流动过程中芳香性结构被破坏。然而,总退水渠与环城河汇合进入人工湿地之后,SUVA254值反而呈现出增加的趋势(图8),表明人工湿地环境有利于稳定DOM的芳香性结构。
2.4 水体DOM氧化还原性质的变化特征
有机物尤其是腐殖质中带有各种官能团的芳香性结构与未饱和脂肪结构发生氧化与还原时可引起π—π*键的形成与断裂,这对荧光强度具有显著的影响[13]。总退水渠与环城河汇合进入人工湿地之后水体DO值发生显著降低(表1),表明人工湿地是相对厌氧的环境。为了研究人工湿地这种相对厌氧的环境是否会对水体有机物的氧化还原特性产生影响,选定Em=450 nm,比较不同水体样品单位DOC浓度的Ex-荧光光强。从图10中可以看出,人工湿地水体Em=450 nm时不同激发波长下单位DOC浓度的Ex-荧光光强要显著高于总退水渠和环城河水体,尤其是在人工湿地的下游显得更为明显,这可能是由相对厌氧的人工湿地环境会使更多的DOM从原态转变成还原态所造成的,因为DOM被还原后可形成更多的π—π*键,从而使得DOM的荧光增强[13]。在厌氧条件下,被还原的DOM可以提供更多的电子给氧化还原电位更高的物质三价铁形成二价铁。由图11可见,人工湿地水体二价铁占全铁的百分含量明显要高于总退水渠与环城河,这进一步说明了人工湿地有利于还原态DOM的形成,同时也暗示着水体DOM可以很好地充当电子转移中介体的角色。

Fig.10 Ex fluorescent intensity per DOC concentration when Em=450 nm; the Ex fluorescent intensity per DOC concentration of different samples when Ex =350 nm is plotted in line symbol in the upper right
为了进一步定量研究水体DOM的电子穿梭能力,采用K3[Fe(CN)6]作为电子受体,对水体DOM的化学还原容量进行了分析。结果发现,总退水渠水体DOM的化学还原容量明显高于环城河,总退水渠与环城河从上游到下游水体DOM化学还原容量的变化均不显著,当两条河流汇合进入人工湿地之后,水体DOM的化学还原容量呈现出增加的趋势,但在人工湿地的下游逐渐趋于稳定(图11),表明人工湿地可以显著提高水体DOM的电子穿梭能力。水体DOM之所以具有氧化还原能力主要是由于其中的腐殖酸类物质含有芳香性结构的苯醌基团[14]。由此,对水体DOM的还原容量与SUVA254值之间做了相关性分析,发现二者存在显著的相关关系(r=0.73,p< 0.01),表明芳香性结构的确是影响DOM还原容量的主要因素。DOM中相对稳定的芳香性结构会随着其他不稳定结构的降解而逐渐暴露出来,这可能也是导致人工湿地水体DOM的还原容量沿水流方向逐渐增加的另一原因。此外,人工湿地水体DOM可能会络合更多的金属而形成氧化还原电对,这对增强DOM的电子穿梭能力亦具有一定的贡献[15]。沿人工湿地水流方向,尽管水体DOC浓度呈现出一定程度的降低,但DOM还原容量的增加却使得单位体积水体的还原容量仍然保持上升的趋势(图11),表明人工湿地在同时促进有机物降解与加速重金属还原迁移中具有重要作用。

Fig.11 Percentages of Fe2+, chemical reduction capacity of DOM per mol carbon and chemical reduction capacity of DOM per volume in waters
3 结 论
(1)人工湿地对水中有机物的去除具有一定的作用,从进水口到出水口,人工湿地DOC浓度和COD的降低率分别可达到12.0%和29.6%。总退水渠、环城河与洨河人工湿地水体COD 60%以上来自DOC的贡献,但人工湿地COD的减少量主要是由于N,H,S,P元素含量的降低引起,其贡献率可达65%。
(2)人工湿地水体DOM主要由微生物贡献,水体DOM中类腐殖质组分比类蛋白质组分更容易被降解,类腐殖质组分在降解过程中逐渐向类蛋白质转化,类富里酸组分与类胡敏酸组分具有相同的分解命运。CDOM与FDOM都是主要由类腐殖质组分构成,二者进入人工湿地后没有产生选择性降解。
(3)人工湿地相对厌氧的条件可以促进水体DOM的还原,从而加速了水中三价铁的还原。进入人工湿地后,尽管水体DOM的腐殖化程度没有发生显著变化,但芳香性碳却呈现出逐渐增加的趋势,这可能是导致水体DOM的电子穿梭能力不断增强的主要原因。
[1] Maie N, Yamashita Y, Cory R M, et al. Appl. Geochem., 2012, 27: 917.
[2] Fu P, Wu F, Liu C, et al. Appl. Geochem., 2007, 22: 1668.
[3] Nelson N B, Siegel D A. Annu. Rev. Mar. Sci., 2013, 5: 447.
[4] Mariot M, Dudal Y, Furian S, et al. Sci. Total Environ., 2007, 388: 184.
[5] Hijosa-Valsero M, Sidrach-Cardona R, Martín-Villacorta J, et al. Chemosphere, 2010, 81: 651.
[6] Zhang H C, Weber E J. Environ. Sci. Technol., 2009, 43(4): 1042.
[7] Guo W D, Stedmon C A, Han Y C, et al. Mar. Chem., 2007, 107: 357.
[8] Vignudelli S, Santinelli C, Murru E, et al. Estuar. Coast. Shelf S., 2004, 60(1): 133.
[9] Kimberly P W, Jason C N, George R A. Ecosystems, 2007, 10(8): 1323.
[10] Ohno T. Environ. Sci. Technol., 2002, 36(4): 742.
[11] Patel-Sorrentino N, Mounier S, Benaim J Y. Water Res., 2002, 36(10): 2571.
[12] Wang L Y, Wu F C, Zhang R Y, et al. J. Environ. Sci-China, 2009, 21: 581.
[13] Cory R M, Mcknight D M. Environ. Sci. Technol., 2005, 39: 8142.
[14] Nurmi J T, Tratnyek P G. Environ. Sci. Technol., 2002, 36: 617.
[15] Sposito G, Struyk Z. Geoderma, 2001, 102: 329.
*Corresponding author
Evolution of Dissolved Organic Matter Properties in a Constructed Wetland of Xiao River, Hebei
MA Li-na1, 2, 3, ZHANG Hui2, 3, TAN Wen-bing2, 3, YU Min-da2, 3, HUANG Zhi-gang1, GAO Ru-tai2, 3*, XI Bei-dou2, 3, HE Xiao-song2, 3
1. Agricultural College of Guangxi University, Nanning 530004, China
2. State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China
3. Innovation Base of Ground Water & Environmental System Engineering, Chinese Research Academy of Environmental Science, Beijing 100012, China
The evolution of water DOC and COD, and the source, chemical structure, humification degree and redox of dissolved organic matter (DOM) in a constructed wetland of Xiao River, Hebei, was investigated by 3D excitation-emission matrix fluorescence spectroscopy coupled with ultraviolet spectroscopy and chemical reduction, in order to explore the geochemical processes and environmental effects of DOM. Although DOC contributes at least 60% to COD, its decrease in the constructed wetland is mainly caused by the more extensive degradation of elements N, H, S, and P than C in DOM, and 65% is contributed from the former. DOM is mainly consisted of microbial products based on proxiesf470/520and BIX, indicating that DOM in water is apparently affected by microbial degradation. The result based on PARAFAC model shows that DOM in the constructed wetland contains protein-like and humus-like components, and Fulvic- and humic-like components are relatively easier to degrade than protein-like components. Fulvic- and humic-like components undergo similar decomposition in the constructed wetland. A common source of chromophoric dissolved organic matter (CDOM) and fluorescent dissolved organic matter (FDOM) exists; both CDOM and FDOM are mainly composed of a humus-like material and do not exhibit selective degradation in the constructed wetland. The proxiesE2/E3,A240~400,r(A, C)and HIX in water have no changes after flowing into the constructed wetland, implying that the humification degree of DOM in water is hardly affected by wet constructed wetland. However, the constructed wetland environment is not only beneficial in forming the reduced state of DOM, but also facilitates the reduction of ferric. It can also improve the capability of DOM to function as an electron shuttle. This result may be related to the condition that the aromatic carbon of DOM can be stabilized well in the constructed wetland.
Dissolved organic matter; Constructed wetland; three-dimensional excitation-emission matrix fluorescence spectroscopy; Ultraviolet spectroscopy; Redox
Oct. 8, 2014; accepted Jan. 29, 2015)
2014-10-08,
2015-01-29
国家水体污染控制与治理科技重大专项项目(2012ZX07203-003)资助
马丽娜,女,1988年生,广西大学农学院硕士研究生 e-mail: maln198810@126.com *通讯联系人 e-mail: grthu@126.com
O
A
10.3964/j.issn.1000-0593(2016)01-0206-07

