核黄素含量测定的实验室质量控制
刘丹天津市滨海新区塘沽街新港社区卫生服务中心,天津 300456
核黄素含量测定的实验室质量控制
刘丹
天津市滨海新区塘沽街新港社区卫生服务中心,天津300456
[摘要]实验室的质量控制在实验室测定中起到重要作用,该次实验采用960型荧光光度计测定核黄素的荧光强度,通过绘制标准曲线图,读出所含核黄素含量的浓度,分别进行精密度分析和准确度分析,进而判定实验的准确度,精密度符合要求。说明测定VB2药片中核黄素含量的实验方法可靠。
[关键词]质量控制;核黄素;测定
在测定VB2药片的核黄素含量的过程中,由于存在着由某些比较确定的原因引起的系统误差和各种随机因素引起的随机误差,使测得的结果不可能和真实值完全一致,误差愈小则结果愈准确。为了保证实验结果的可靠性,要采取减少误差的有效措施,并需要用统计学的方法将分析数据予以适当处理,以便能正确地评价分析结果的准确度、精密度。
1 材料与方法
1.1材料
以市售吉林鹿王药业生产的VB2为待测样品,测定其中核黄素的含量。
1.2仪器与试剂
1.2.1仪器(1)960型荧光光度计;(2)电子天平。
1.2.2试剂(1)酸性水:取浓硫酸1.5 mL加蒸馏水稀释至1 000 mL。(2)核黄素标准储备液(25 mg/L)精密称取25 mg的核黄素(分析纯),然后用酸性水定容至1 000 mL,用棕色瓶盛装,瓶子外用黑色塑料袋包裹,置于冰箱内冷藏,备用,每间隔两天重新配制;(3)核黄素标准应用液(1 mg/L)取核黄素标准储备液4 mL,用酸性水稀释到100 mL,用棕色容量瓶盛装,瓶子外用黑色塑料袋包裹,临用时配制;(4)维生素VB2片待测液取市售吉林鹿王药业生产的VB2片(5 mg/片),用酸性水稀释到1 000 mL,置于棕色容量瓶中,外面用黑色塑料袋包裹;(5)低亚硫酸钠(Na2S2O4);(6)维生素VB2片吉林鹿王药业生产。
1.3方法
(1)采用960型荧光光度计,测定各个比色管中核黄素的荧光强度。如①空白品:20 mL酸性水;②标准品:取10 mL应用液稀释到100 mL后取20 mL。(0.1 mg/L);③待测品:VB2稀释到1000 mL(A液),取A液20 mL稀释到1 000 mL后取20 mL。(0.1 mg/L);④加标样品:10 mL标准+10 mL样品,每天做一个批次,每次两个平行样,共做20批次。绘制标准曲线图,在标准曲线上读出所含核黄素含量的浓度,分别进行精密度分析和准确度分析,并绘制准确度控制图与精密度控制图。
(2)操作步骤。①配制标准系列溶液:取7个50 mL容量瓶,用黑色塑料袋包裹后分别加入1~7 mL的核黄素标准应用液(1 mg/L),用酸性水稀释到刻度,摇匀。②标准系列的荧光强度测定:严格按程序开启荧光光度计后预热20 min,依次按照浓度从低到高的顺序测量其荧光强度及加入低亚硫酸钠后的荧光强度。③测定VB2药片中核黄素含量:a.取8个25 mL的比色管用黑色塑料袋包裹至20 mL刻度线,分别标注空白品、标准品、加标样品、待测品,分别取平行样。b.严格按程序开启荧光光度计后预热20 min,依次测定各个比色管的荧光强度及加入低压硫酸钠后的荧光强度。

2 结果
2.1核黄素标准溶液的荧光强度测定值
以标准核黄素浓度为横坐标、荧光强度为纵坐标绘制的标准曲线(如图1),VB2片待测液的浓度平均值C(VB2)为0.101 mg/L,则原待测液的浓度C(VB2)原=C(VB2)×100 mL/2 mL=5.05 mg/L。则药片中VB2的含量就为C(VB2)原×1000 mL=5.05 mg/片。由核黄素标准系列得出回归方程(r=0.997 52 P<0.001)。

图1 核黄素标准曲线图
2.220批次不同样品的浓度
依次测定空白品,标准品,如标样品,待测品,并记录数值。见表1。
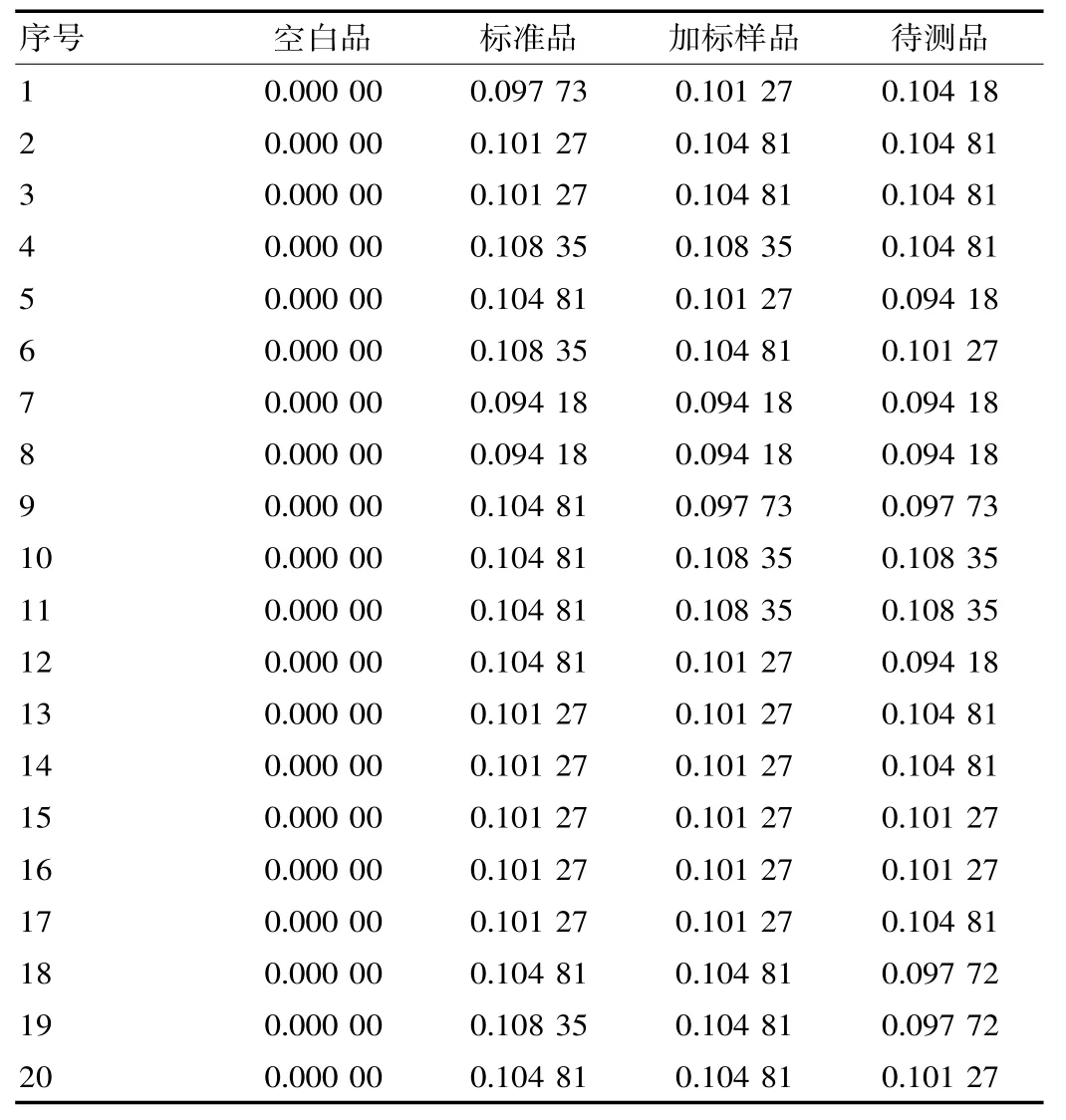
表1 20批次不同样品的浓度(mg/L)
2.3精密度分析
通过精密度控制图分析该次实验精密度是否符合要求。精密度控制图的绘制:记录20批次样品测定值,求出平均值)、标准差(S),并计算出中心线是纵坐标为的、平行于横轴的直线;分别为上下控制限;与-2S分别为上下警告限;以测定值为纵坐标、样品测定序号为横坐标绘图。
2.4准确度分析
通过待测样品中核黄素含量的加标回收率来判定该次实验中准确度是否在控制之中。平均回收率=101.83%。经测定1号样品加标回收率为100%,2号样品加标回收率为103.5%,3号样品加标回收率为103.55,4号样品加标回收率为103.3%,5号样品加标回收率为103.4%,6号样品加标回收率为100%,7号样品加标回收率为100%,8号样品加标回收率为100%,9号样品加标回收率为103.3%,10号样品加标回收率为103.4%,11号样品加标回收率为103.4%,12号样品加标回收率为103.4%,13号样品加标回收率为96.5%,14号样品加标回收率为95.6%,15号样品加标回收率为100%,16号样品加标回收率为100%,17号样品加标回收率为104.9%,18号样品加标回收率为105.8%,19号样品加标回收率为103.2%,20号样品加标回收率为103.4%。
3 讨论
实验室的质量控制虽然会增加一定的工作量,但它所换来的是数据可信性。所以要建立较全面的质量控制,把所做的实验都加以控制,数据准确性就十分有把握。样品总标准差S(0.004 6)<目标值W(0.101),加标样总标准差S(0.004 9)<目标值W(0.005);标准品总标准差S(0.005 5)>目标值W(0.005),但标准品总均方S2(0.3×10-4)/目标值W2(0.0052)<F(19,∝),所以加标样和标准品、样品的精密度均符合要求,平均加标回收率为101.83%,在95%~105%之间。由准确度控制图可看出各点的分布情况:18个点的位置在中心线附近、上下控制限的区域内浮动,说明测定工作的质量处于较好控制水平;其中有2个点的位置在下警告限之外,但仍在下控制限的区域内,提示可能存在误差,但样品测定结果尚可保留,准确度符合要求。由精密度控制图可看出各点的分布情况:20个点的位置在中心线附近、上下警告限之间的区域内浮动,说明测定工作的精密度符合要求。实验中出现的可能影响核黄素荧光强度的因素:
①溶剂:该次实验所用溶剂为酸性水,主要考虑到核黄素极易分解,其在酸性条件下比较稳定。
②温度影响:在该次实验过程中,实验室配有遮阳窗帘,所用到的容器都已用黑色塑料袋包裹,避免实验过程中核黄素的分解,避光措施较好。
③激发光的照射对荧光强度的影响:实验测定过程中,要在放入比色皿前打开盖门,放入后立即读数,以减少核黄素受激发光照射的时间,取出后立即关闭盖门。
④溶液的pH值:该次实验所用的酸性水由于所需剂量较大,故如果多次配制易产生误差,使酸性水的pH有所改变,会影响到测定结果。因此在该次实验中,实验前应配好足够的酸性水,保持酸性水的pH在5.6。由于浓硫酸比较粘稠,吸取浓硫酸时要尽量让刻度吸管里的浓硫酸全部流下后再移走刻度吸管,以免浓硫酸残留,影响测定结果。
⑤样品浓度的影响:荧光分析应在低浓度溶液中进行。
⑥试剂的配制对荧光强度的影响:由于实验中需要配制大量的溶液,故溶液配制的是否准确直接影响到实验结果。能否准确无误地配制溶液,就需要实验人员具有良好的操作技能及耐性。
4 结语
由准确度控制图、精密度控制图可看出,实验的准确度、精密度符合要求。说明测定VB2药片中核黄素含量的实验方法可靠、测定结果具有一定的准确性和可靠性。
[参考文献]
[1]许哲荣.卫生实验室的质量控制[J].口岸卫生控制,1999(2):11-12.
[2]张雪梅,张岚.实验室质量管理[J].中国公共卫生,2002,18(6):7-9.
[3]Lichtenstein AH.Soy protein,isoflavones and cardiovascular disease risk[J].J Nutr,1998,128:1589.
[4]吴志宏.水质分析中的质量控制[J].科技情报开发与经济,2002,12(4):22.
[5]鄂学礼,祝军.疾病控制系统实验室计量认证[J].中国卫生检验杂志,2003,7(3):49-51.
[6]孙要武,祁艳波.预防医学实验教程[M].黑龙江科学技术出版社,2000,4:38-39.
[7]王淑亭.食品卫生检验手册[M].3版.化学工业出版社,1995:121.
[8]俞汀.卫生防疫机构实施全面管理工作探讨[J].中国公共卫生管理,1999,15(4):226-227.
[中图分类号]R927.2
[文献标识码]A
[文章编号]1672-5654(2016)03(b)-0108-03
DOI:10.16659/j.cnki.1672-5654.2016.08.108
收稿日期:(2015-12-19)