Mn3O4的室温制备及其对高氯酸铵热分解的催化性能
钱石川,王桂萍,王利航
(沈阳理工大学 装备工程学院,沈阳110159)
Mn3O4的室温制备及其对高氯酸铵热分解的催化性能
钱石川,王桂萍,王利航
(沈阳理工大学 装备工程学院,沈阳110159)
摘要:以MnCl2、NaOH、H2O2为原料,以十二烷基苯磺酸钠(SDBS)为分散剂,制备纳米Mn3O4。通过XRD表征产物。采用差示扫描量热法(DSC)和热重分析(TG)考查纳米Mn3O4对高氯酸铵(AP)热分解的催化作用。结果表明:在MnCl2(0.25mol/L)用量100mL的条件下,制备纳米Mn3O4的最佳工艺为:NaOH(0.5mol/L)100mL;H2O2(2.5mol/L)14mL;SDBS(0.025mol/L)6mL;室温下,制备前驱物,对前驱物的热处理温度为300℃,热处理时间为2h,该条件下制备出的纳米Mn3O4的产率为77.50%,粒径为14.52nm。纳米Mn3O4对AP热分解的催化活性很高,可使AP的高温热分解温度显著降低,分解放热量显著增加,粒径越小其催化活性越高。
关键词:四氧化三锰;纳米粒子;高氯酸铵;热分解;催化性能
四氧化三锰具有优越的性能和广泛的用途,越来越引起人们的关注。四氧化三锰是新一代软磁铁氧体材料和微波铁氧体材料的主要原料,可作为处理汽车尾气(分解碳、氮氧化物)的催化剂和选择性还原硝基苯的催化剂,此外还可作为某些油漆或涂料的色料[1]。纳米粒子由于特殊的结构,导致它具有一系列新奇的物理、化学特性,随着纳米技术的不断发展,纳米锰氧化物的制备与应用也成为研究热点[2]。纳米四氧化三锰粉末可作为还原氮氧化物、氧化甲烷的催化剂等[3],还可作为廉价易得的清除 CO 高效催化剂[4]。有研究表明,纳米四氧化三锰可以在氧化反应中作为绿色催化剂[5]。目前见报道纳米四氧化三锰的制备方法有水热法[6]、溶剂热法[1]、微乳液法[7]、沉淀法[8]等。这些方法概括起来存在工艺复杂,反应时间长,对反应容器要求高,需要有机溶剂等缺点,所以研究纳米四氧化三锰制备的简单高效工艺具有意义。高氯酸铵(AP)是复合固体火箭推进剂中应用最广的氧化剂,含量占60%~80%,其热分解特性与推进剂的燃烧特性密切相关.已报道纳米CuO[9]、纳米Fe2O3[10-11]、Cu/Co/Fe水滑石衍生的复合氧化物[12]、二茂铁功能化石墨烯氧化物[13]、纳米Cu2O[14-15]等对高氯酸铵热分解的催化作用,至今未见有关纳米Mn3O4对催化高氯酸铵热分解性能影响的报道.本文参考文献[16]的方法,以MnCl2、NaOH、H2O2为原料,采用室温液相直接沉淀法,以期寻找纳米Mn3O4制备的简单工艺条件;并用差示扫描量热法(DSC)和热重分析(TG)考察纳米Mn3O4对高氯酸铵热分解的催化作用。
1实验部分
1.1纳米Mn3O4的制备
所用药品:氯化锰(沈阳化学试剂厂),氢氧化钠,双氧水,十二烷基苯磺酸钠(沈阳东陵区精细化学厂),乙醇、高氯酸铵(国药集团化学试剂有限公司),以上药品均为分析纯;实验用水均为蒸馏水。
首先配制MnCl2溶液(0.25mol/L),NaOH溶液(0.5mol/L),H2O2溶液(2.5mol/L),十二烷基苯磺酸钠溶液(SDBS 0.025mol/L);向MnCl2溶液中加入H2O2溶液,用磁力搅拌器搅拌至混合均匀得A;向NaOH溶液中加入SDBS溶液,混合均匀作为沉淀剂B。室温下,控制一定滴加速度,将B滴加到A或A滴加到B中,滴加完且反应溶液颜色均匀后,静止陈化,抽滤;将沉淀用蒸馏水洗涤3次,再用无水乙醇洗涤1次,70℃条件下烘干2h得到固体前驱物;研磨前驱物,一定温度下在马弗炉中焙烧前驱物粉体得到目标产物。
1.2纳米Mn3O4的表征
采用Rigaku Ultima Ⅳ型X射线衍射仪(日本株式会社理学北京事务所)对制备的产物进行表征。测试条件:工作电压40kV,工作电流40mA;步长扫描,步长0.02°;扫描范围10°~80°(2θ);采用Cu靶Kα辐射(λ=1.54056Å)。测得数据使用Jade 5.0衍射数据分析软件进行分析。
1.3纳米Mn3O4对高氯酸铵热分解催化性能评价
采用STA 409 C/CD综合热分析仪(德国NETZSCH)进行差示扫描量热 (DSC)与热重分析(TG),评价纳米Mn3O4对高氯酸铵热分解催化性能。测量范围为50℃~500℃,升温速率为20℃/min,参比物为α-Al2O3,氩(Ar)气气氛,Ar气流速50mL/min,样品装在常压开口铝坩埚中。制得的纳米Mn3O4样品与AP按质量比2∶98的比例充分研磨混合,制备试样,取试样1.5mg进行测试。
2结果与分析
2.1沉淀反应方式的影响
采用3种沉淀反应方式:(Ⅰ)正滴法:将NaOH滴加到MnCl2中;(Ⅱ)反滴法: MnCl2滴加到NaOH中;(Ⅲ)同时滴加法:将两者同时滴加到水中。其它条件: MnCl2溶液100mL ,NaOH溶液100mL,H2O2溶液10mL,十二烷基苯磺酸钠溶液12mL,滴加速度2mL/min,制得前驱物;将前驱物在300℃下焙烧2h,制得目标产物。三种沉淀方式制得的前驱物及目标产物的XRD图谱见图1a和图1b,目标产物的颜色分别为棕色、黑色、深棕色。
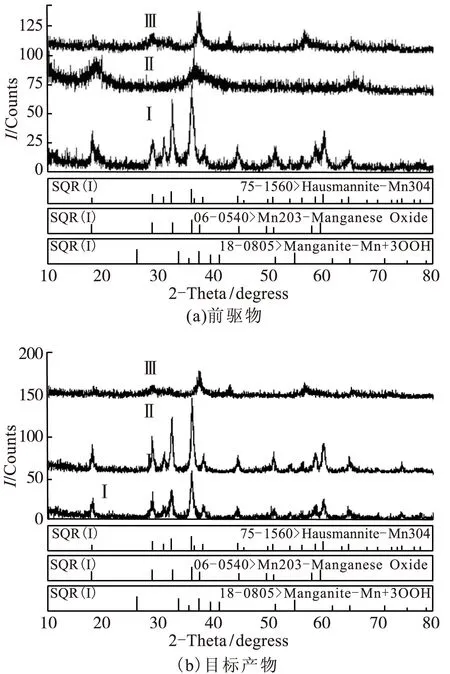
图1 3种沉淀方式制得的前驱物和终产物的XRD
从图1a可见,前驱物(I)在18.0°、28.9°、32.3°、36.1°、59.8°五处有明显的衍射峰与Mn3O4(ICDD PDF No.75-1560)衍射峰对应;在44.6°、59.6°处有强度较弱的宽化峰与Mn2O3(ICDD PDF No.06-0540)衍射峰对应;在33.8°、54.8°处有强度较弱的宽化峰与MnOOH(ICDD PDF No.06-0540)衍射峰对应。可见前驱物(Ⅰ)结晶程度较高,以Mn3O4为主相,含有少量Mn2O3和MnOOH。前驱物(Ⅱ)、(Ⅲ)衍射峰强度较弱,衍射峰严重宽化,表明其晶化程度低,实验制得的前驱物均为氧化物和氢氧化物的混合物。由图1b可见,终产物(I)和(II)在32.3°、36.1°、59.8°三处有明显的衍射峰,是结晶性较好的Mn3O4;终产物(III)只有在37.4°处有明显的衍射峰,其它位置的衍射峰严重宽化,其晶化程度较小,不是Mn3O4。综上,实验采用正滴定法。
2.2NaOH用量的影响
其余条件固定如1.1,改变NaOH用量,所制得的前驱物颜色均为褐色粉体。不同NaOH用量制得的目标产物的产率见表1。可见,当NaOH用量在70~100mL范围内,目标产物的产率随NaOH用量增加而显著增加,用量达到100mL后,增加缓慢。产物A1、A5和A9的XRD图谱见图2,3种产物均为结晶性较好的纳米Mn3O4,粒径分别为26.35nm,28.23nm、27.84nm。所以NaOH溶液的最佳用量为100mL,即NaOH和MnCl2的物质的量比为2∶1。
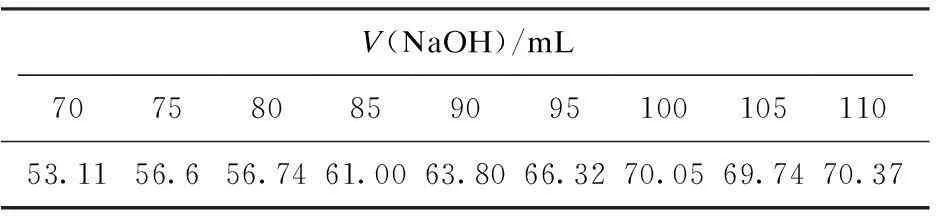
表1 不同NaOH用量制得的前驱物和目标产物的产率 %
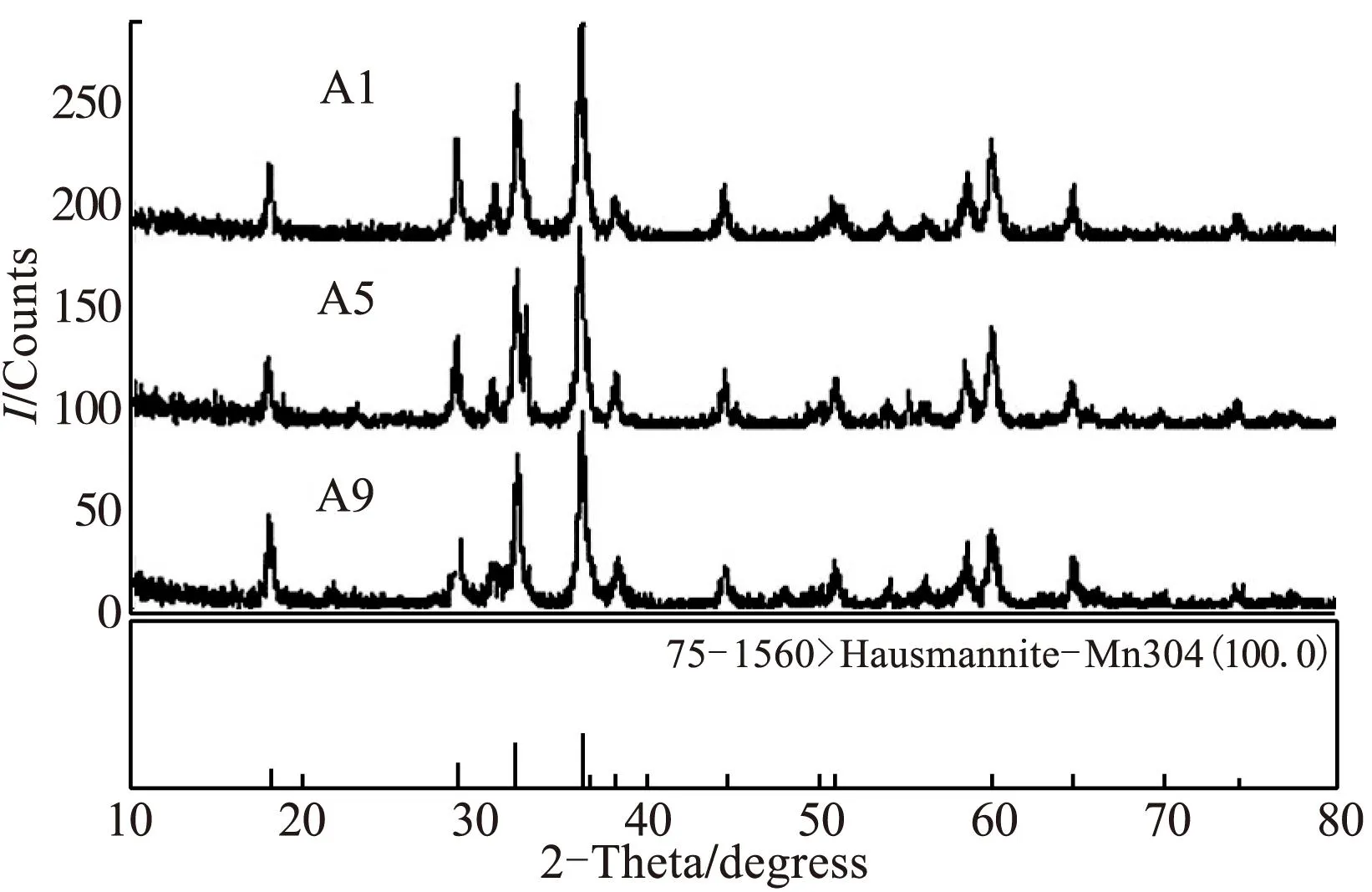
图2 不同NaOH用量制得的目标产物的XRD
2.3H2O2用量的影响
其它条件如上,H2O2用量分别取4、8、12、16、20mL,制得的目标产物B1、 B3、 B5、 B7 、B9的XRD图谱见图3。
由图3可见,目标产物B1、B3在23.1°、38.2°、55.2°处出现不明显且严重宽化的衍射峰,含结晶性较差的Mn2O3,目标产物B5、B7和B9没有其它杂峰出现,是纯净的Mn3O4。综上可知, H2O2溶液的最佳用量为12mL。
2.4焙烧温度的影响
对前驱物焙烧温度分别取400(T1)、500(T2)、600(T3)、700(T4)、800℃(T5),焙烧2h制得目标产物的XRD图谱见图4. 由图4可见,随温度升高,产物中除Mn3O4,还含有杂质。比较图3中B5可知,制备纳米Mn3O4,前驱物最佳的焙烧温度为300℃。

图3 不同H2O2用量制得的目标产物的XRD

图4 不同焙烧温度制得的目标产物的XRD
2.5焙烧时间的影响
分别将前驱物在300℃焙烧1、2、3、4、5h,制得目标产物H6、H7、 H8、 H9、H10的XRD图谱见图5,其平均粒径分别为38.5nm、16.92nm、18.68nm、23.75nm、30.24nm。
由图5可看出,产物H7、H8、H9和H10在18.0°、28.9°、32.3°、36.1°、59.8°五处有明显的衍射峰,是纯净的、结晶性较好的Mn3O4,产物H6还在32.6°、37.5 °、59.5°处出现不明显且严重宽化的衍射峰,是结晶性较差的Mn2O3,产物H6含Mn2O3。在300℃条件下,随焙烧时间增加,反应物先发生物质转化,使反应物粒径迅速减小,在焙烧2h时,粒径最小,16.92nm;当焙烧时间增加到3h后,产物粒径明显增大。所以前驱物最佳焙烧时间为2h。

图5 300 ℃不同焙烧时间产物的XRD
2.6最佳工艺验证
按照上述最佳制备工艺:NaOH溶液(0.5mol/L)100mL,H2O2(2.5mol/L)10mL,十二烷基苯磺酸钠(0.025mol/L)12mL为原料,采用正滴法将NaOH以2mL/min滴加到MnCl2溶液中;焙烧温度300℃,焙烧时间2h。制备纳米Mn3O4,产率为77.50%,制得样品的XRD图谱见图6。由图6可以看出,在18.0°、28.9°、32.3°、36.1°、59.8°五处有明显的衍射峰,且无杂峰出现,是结晶性良好的Mn3O4,通过软件Jade5.0计算,制得的纳米Mn3O4的粒径为14.52nm。

图6 最佳工艺制得的纳米Mn3O4的XRD
2.7纳米Mn3O4对高氯酸铵热分解催化性能
选择制得的粒径为23.75nm(H9)和14.52nm的Mn3O4样品为AP热分解的催化剂,DSC 和TG实验结果见图7。
从图7可见,含2%的粒径为23.75nm和14.52nmMn3O4的AP试样的DSC曲线分别在247.6℃和247℃出现了吸热峰,与纯AP吸热峰值差别不大[17],属于纯AP的晶型转变。可见,纳米Mn3O4对AP的晶型转变没有明显影响;在图7的DSC曲线上,247~500℃范围内,含23.75nm和14.52nmMn3O4的AP试样均只出现了一个放热峰,分别在329.5℃和326.4℃,属于AP的高温分解放热峰, 表观分解热分别为1088J/g和1201J/g,可见纳米 Mn3O4使AP的高温分解温度显著降低(纯AP高温分解温度约453℃[18]),高温分解峰分别降低了123.5℃和126.6℃;表观分解热显著增加(纯AP的表观分解热515J/g[14]),分别增加了573J/g和686J/g。 纳米Mn3O4对AP的热分解催化作用显著,催化效果与粒径有关,粒径越小,催化活性越高。这是因为,起催化作用的Mn3O4粒子首先要与AP接触,相同含量下,Mn3O4的粒径越小,表面积越大,与AP直接接触的面积越大,因而催化活性越高。与纳米Fe2O3比较[14],纳米Mn3O4使AP高温分解峰降低更多(纳米Fe2O3使AP高温分解峰最多降低67.3℃),表观分解热增加较少(纳米Fe2O3使AP表观分解热增加785 J/g)。

图7 含纳米Mn3O4的AP的DSC和TG曲线
由图7中TG曲线可见,加入纳米Mn3O4使AP的分解速度更快,在300~350℃范围内,含23.75nm Mn3O4的样品失重约70%,含14.52nm Mn3O4的样品失重约75%,可见Mn3O4的粒径越小,催化作用越强。
3结论
(1)沉淀反应方式对纳米锰氧化物的种类有影响,使用正滴法可制得纳米Mn3O4。
(2)通过单因素实验确定的制备纳米Mn3O4的最佳制备工艺:MnCl2(0.25mol/L)100mL,NaOH(0.5mol/L)100mL;H2O2(2.5mol/L)12mL,SDBS(0.025mol/L) 6mL;热处理温度为300℃,热处理时间为2h。该条件下制备出的纳米Mn3O4的产率为77.50%,粒径为14.52nm。
(3)纳米Mn3O4对AP的热分解具有很高的催化活性,可使AP的高温分解温度显著降低,分解放热量显著升高,粒径越小其催化活性越高。
参考文献:
[1] 杨则恒,张卫新,许俊.溶剂热合成法制备Mn3O4纳米粉体[J].应用化学,2005,22(7):722-725.
[2]黄开金.纳米材料的制备及应用[M].北京:冶金工业出版社,2009.
[3]Chen L,Horiuchi T,Mori T. Catalytic reduction of NO over a mechanical mixture of NiGa2O4spinel with manganese oxide: influence of catalyst preparation method[J].Applied Catalysis A: General,2001(209):97 -105.
[4]Liu Yun-ping,Yuan Jun-jun,Lin Pei-yan,et al.Catalytic activity of nanocrystalline manganese oxides for CO oxidation[J]. 物理化学学报,1999,12(1) :82-86.
[5]孙华银.纳米四氧化三锰催化的氧化反应及纳米铋促进的烯丁基化反应研究[D].合肥:中国科学技术大学,2011.
[6]Fang Z,Tang K B,Gao L S,et al. Facile and large-scale synthesis of single-crystalline manganese oxyhydroxide/oxide nanostructures [J]. Mater Res Bull,2007, 42(9): 1761-1768.
[7]王积森,孙金全,鲍英,等.氧化锰纳米带的合成研究[J].山东科技大学学报:自然科学版,2003,22(2):27-29.
[8]周叶青,程翔.Mn3O4纳米颗粒的制备及改性[J].应用化工,2008,37(11):1335-1337.
[9]罗元香,陆路德,刘孝恒,等.纳米CuO的制备及对NH4ClO4热分解的催化性能[J]. 无机化学学报,2002,18(12):1211-1214.
[10]马振叶,李凤生,陈爱四,等.纳米Fe2O3/高氯酸铵复合粒子的制备及其热分解性能研究[J]. 化学学报,2004,62(13):1252-1255.
[11]李小红, 江向平,文思逸,等.不同形貌纳米α-Fe2O3粉体水热合成及其催化高氯酸铵热分解研究[J].人工晶体学报,2013(6):1132-1137.
[12]刘洪博,黄志勇,郭冰之,等.Cu/Co/Fe水滑石衍生的复合氧化物催化高氯酸铵热分解的研究[J].无机化学学报,2013(5):1077-1083.
[13]周磊,王立,俞豪杰,等.二茂铁功能化石墨烯氧化物的制备、表征及对高氯酸铵热分解的催化性能[J].材料科学与工程学报,2013(3):323-330.
[14]朱俊武, 陈海群, 谢波,等.纳米Cu2O的制备及其对高氯酸铵热分解的催化性能[J].催化学报,2004,25(8):637-640.
[15]罗小林, 韩银凤, 杨德锁.溶剂热合成Cu2O微球及其对高氯酸铵热分解的催化作用[J].物理化学学报,2012,28(2):297-302.
[16]Chen Z W,Lai J K L, Shek C H.Shape-controlled synthesis and nanostructure evolution of single-crystal Mn3O4nanocrystals[J].Scripta Mater, 2006(55):735-738.
[17]Fu T M,Liu F Q,Liu L.Catalytic thermal decomposition of ammonium perchlorate using manganese oxide octahedral molecular sieve (OMS)[J].Catalysis Communications,2008(10):108-112.
[18]刘建勋,李凤生,陈爱四.纳米Fe2O3的制备及其对AP热分解的催化作用[J].推进技术,2006,27(4):381-384.
(责任编辑:马金发)
Preparation of Mn3O4Nanocrystalline and Its Catalytic Effect on Thermal Decomposition of Ammonium Perchlorate (AP)
QIAN Shichuan,WANG Guiping,WANG Lihang
(Shenyang Ligong University,Shenyang 110159,China)
Abstract:Mn3O4 nanocrystalline was prepared by MnCl2,NaOH, and H2O2 as the starting materials and surfactant sodium dodecyl benzene sulfonate?(SDBS)as dispersant,and it was characterized by X-raydiffraction (XRD).The catalytic properties of. Mn3O4 nanocrystalline on the thermal decomposition of ammonium perchlorate(AP) were investigated by differential scanning calorimetry(DSC) and thermogravimetric analysis (TG). The experimental results indicated that the optimum conditions for preparing Mn3O4 nanocrystalline are as follows: At room temperruture,precursor is prepared by NaOH(0.5mol/L)100mL, H2O2(2.5mol/L)14mL,SDBS(0.025mol/L)6mL; the precursor is calcined at 300℃ for 2h.the average diameter of the product.Mn3O4 is 14.52nm,the yield is 77.5% . Mn3O4 nanocrystalline shows strong effect on thermal decomposition of ammonium perchlorate,it can decrease the higher thermal decomposition temperature of AP and increase the exothermic heat significantly, and the smaller size it was, the higher catalytic activity it had.
Key words:Mn3O4;nanocrystalline;ammonium perchlorate; thermal decomposition; catalytic activity
中图分类号:O614.7+11
文献标志码:A
文章编号:1003-1251(2016)02-0075-05
作者简介:钱石川(1993—),男,本科生;通信作者:王桂萍(1963—),女,教授,研究方向:纳米材料。
收稿日期:2014-04-29

