单侧肾上腺切除术治疗双侧肾上腺大结节增生疗效分析
魏 文,汤坤龙,陈文轩,李黎明,林 毅
(1.天津医科大学研究生院,天津300070;2.天津医科大学总医院泌尿外科,天津300052)
论著
单侧肾上腺切除术治疗双侧肾上腺大结节增生疗效分析
魏 文1,2,汤坤龙2,陈文轩2,李黎明2,林 毅2
(1.天津医科大学研究生院,天津300070;2.天津医科大学总医院泌尿外科,天津300052)
目的:探讨单侧肾上腺切除术治疗双侧肾上腺大结节增生(AIMAH)的可行性。方法:回顾性分析确诊为AIMAH的19例患者(男性11例,女性8例)的临床表现、实验室及影像学检查、病理结果、治疗及预后。结果:内分泌检查血浆皮质醇昼夜节律变化消失,24 h尿游离皮质醇升高,促肾上腺皮质激素释放激素(ACTH)受抑制或正常,小剂量地塞米松抑制试验均不受抑制,8例大剂量地塞米松抑制试验受到抑制。18例行单侧肾上腺切除术治疗,病理示肾上腺皮质结节性增生。10例临床型库欣综合征患者单侧肾上腺切除术后3~6个月库欣综合征消失,平均随访3年,库欣综合征无复发。另外2例临床型库欣综合征患者术后复发分别予对侧肾上腺全切除术、次全切除术,术后库欣症状缓解,给予糖皮质激素替代治疗。6例亚临床库欣综合征患者,术后高血压高血糖均有改善。结论:单侧肾上腺切除术治疗双侧肾上腺大结节增生是有效安全的手段。
双侧肾上腺大结节增生;库欣综合征;单侧肾上腺切除术
双侧肾上腺大结节增生(AIMAH)是导致皮质醇增多的一种罕见原因,以往认为采取双侧肾上腺切除治疗可以获得根治,但这种方法近年来已少用。因患者术后需要终身服用糖皮质激素替代,并且容易出现肾上腺皮质功能低下。目前普遍认为单侧肾上腺切除术治疗双侧AIMAH效果确切,术后皮质醇增多症表现消失,而且不用长期激素替代,同时提高了生活质量,为多数患者所接受。本文回顾性分析我院2000年1月-2013年12月确诊为双侧AIMAH的19例患者的临床资料,进一步探讨单侧肾上腺切除术治疗双侧AIMAH的可行性。
1 对象与方法
1.1 一般资料 本组19例,术前肾上腺CT提示双侧肾上腺多发大小不等结节,最大侧肾上腺直径大于3 cm。肾上腺内分泌检查提示促肾上腺皮质激素非依赖型皮质醇增多。术后病理回报结节样或腺瘤样增生,确诊为双侧肾上腺大结节增生。男性11例,女性8例,年龄40~73岁,平均年龄52岁,其中12例患者以满月脸、水牛背、向心性肥胖、皮肤紫纹等典型库欣综合征表现就诊,另外7例患者因影像学检查发现双侧肾上腺病变伴有高血压或糖尿病、四肢乏力等非典型库欣综合征表现就诊,临床上将缺乏典型库欣综合征表现的患者称为亚临床型。19例患者收缩压150~190 mmHg,舒张压110~130 mmHg。
1.2 辅助检查
1.2.1 实验室检测 8∶00血浆皮质醇:476~1320nmol/L,平均值:865.05 nmol/L,标准差:235.95 nmol/L;夜间0点血皮质醇:384~1100nmol/L,平均值:700.42nmol/L,标准差:172.56nmol/L(正常值:138~688nmol/L)。24 h尿游离皮质醇:247~3250nmol,平均值:973.31nmol,标准差:794.60 nmol(正常值:80~294 nmol/24 h)。促肾上腺皮质激素释放激素(ACTH):2.7~19 pmol/L,平均值:11.68 pmol/L,标准差:4.97 pmol/L(正常值:0~10 pmol/L)。小剂量地塞米松抑制试验均不受抑制,8例大剂量地塞米松抑制试验受到抑制。其中6例患者伴有低血钾,血钾:2.4~3.4 mmol/L,平均值:2.87mmol/L,标准差:0.38 mmol/L;卧位血浆醛固酮范围:409.96~678.65 pmol/L,平均值:462.59 pmol/L,标准差:116.34pmol/L(正常值:138.5~484.75pmol/L);血浆肾素:0.4~0.76ng/mL,平均值:0.66 ng/mL,标准差:0.08 ng/mL(正常值:0.05~0.79 ng/mL)
1.2.2 影像学检查 19例患者均行肾上腺CT平扫及强化,均显示双侧肾上腺多发软组织结节密度影,最大结节直径为7 cm,其中7例患者单侧肾上腺结节大于4 cm,失去了正常肾上腺的形态。CT强化表现为:轻度均匀强化,早期强化后迅速廓清。见图1。
1.3 治疗方法 19例患者中18例行后腹腔镜下单侧肾上腺全切术,依据CT检查结果,择有最大肾上腺结节侧做首次肾上腺切除。双侧肾上腺结节大小差别不大时(<1 cm),择右侧肾上腺切除作为首次肾上腺切除。其中2例单侧肾上腺切除术后分别予对侧肾上腺切除术、次全切除术治疗。1例拒绝行手术治疗,行密切随访观察治疗。

图1 双侧肾上腺CT强化表现
2 结果
术后剖开肾上腺标本,见金黄色均匀一致多发结节,其内未见到色素沉着。一侧肾上腺标本重量23~65 g(正常肾上腺重量约5 g),见图2。术后病理回报:肾上腺组织切面可见多个大小不等金黄色结节,结节直径2.8~7 cm,肾上腺皮质结节样增生。光镜下可以见到增生的结节主要由大透明细胞及小致密细胞组成。结节间皮质未见萎缩。
18例患者行CT检查提示较大侧肾上腺切除术,其中10例临床型库欣综合征患者,术后3个月到半年内,库欣综合征表现消失,平均随访3年,未再出现满月脸、水牛背、皮肤紫纹等典型的库欣表现,复查血尿皮质醇均恢复正常。术后3个月、之后1年复查1次CT,对侧肾上腺较前无显著改变(肾上腺结节直径改变<0.5 cm);另外2例临床型患者分别术后2个月、1年库欣综合征复发,分别给予对侧肾上腺全切术、次全切除术,随访至今,未出现库欣综合征及肾上腺皮质功能低下的表现,如恶心、呕吐等。术后均给予口服糖皮质激素替代治疗。双侧肾上腺全切除患者未出现尼尔森综合征。6例患者为亚临床型库欣综合征,以高血压或糖尿病控制差等症状为主,术后5例患者血压恢复到正常范围,1例患者降压药物的使用剂量下调。其中3例伴有糖尿病,2例空腹血糖恢复正常范围,1例继续胰岛素治疗。1例患者为老年73岁亚临床型双侧肾上腺大结节增生,首次CT检查发现右侧肾上腺结节大小约3.0 cm,左侧肾上腺结节大小约2.5 cm,该患者行保守密切观察治疗,随访至今6年,复查双侧肾上腺CT未见结节明显增大。患者仍未出现典型的库欣综合征表现。尿24 h皮质醇检测结果为683 nmol/L。血浆皮质醇昼夜节律变化消失。
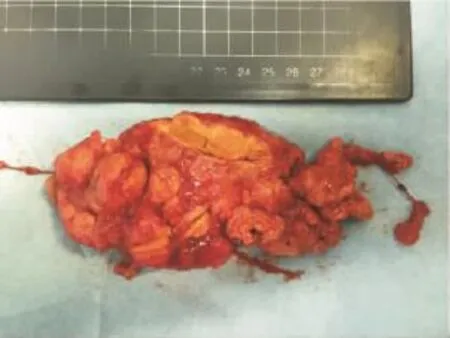
图2 AIMAH患者一侧肾上腺切除大体标本
3 讨论
双侧肾上腺大结节增生是导致皮质醇增多症中的一种罕见的病因类型[1]。作为促肾上腺皮质激素释放激素非依赖型的一种,其在促肾上腺皮质激素非依赖型库欣综合征患者中占到<2%。发病机制尚不明确,研究表明可能与多种异位受体的表达及遗传有关。其中包括抑胃肽、儿茶酚胺、血管升压素、促黄体生成素、5羟色胺等受体的异常激活[2]。男女发病比例大致为1∶1。在本研究中,男女比例分布大致符合。
临床上根据有无典型的库欣综合征表现,如满月脸、皮肤紫纹、向心性肥胖、多血质面容分为临床型及亚临床型,肾上腺内分泌通常有血浆皮质醇昼夜节律消失,血皮质醇升高,24 h尿游离皮质醇超出正常范围,小剂量地塞米松抑制试验不被抑制;由于受到来自双侧肾上腺过度分泌的皮质醇的负反馈调节,垂体分泌的ACTH多处于抑制状态,实验室检查表现为小于5 pmol/L。血浆ACTH是随着皮质醇分泌的升高而逐渐被抑制的,当ACTH完全被抑制时,ACTH<5 pmol/L,此时大剂量地塞米松抑制试验不被抑制[3]。本组ACTH2.7~19 pmol/L,平均11.7 pmol/L,其中11例>10 pmol/L,这些患者受到皮质醇升高的负反馈,ACTH未完全受到抑制,大剂量地塞米松抑制试验未完全受到抑制。对于具有典型临床表现的双侧肾上腺大结节增生患者,通过肾上腺内分泌检查可以确诊。由于B超及CT查体的普及,肾上腺偶发瘤的患者逐渐增加。因影像学检测发现双侧肾上腺结节,不伴有典型的库欣综合征的表现,多出现高血压或糖尿病等非典型表现,仍可以发现血浆皮质醇昼夜节律、尿24 h游离皮质醇、ACTH、大小剂量地塞米松抑制试验出现异常加以诊断。因为缺乏库欣综合征的临床表现,亚临床型双侧肾上腺大结节增生的病人是临床诊断工作中的一个难题,此类病人ACTH不完全受到抑制,在进行CRH试验时ACTH升高。有报道由亚临床进展到临床型历时很长,可以7年[4],有可能造成延误治疗。因此定义亚临床型为血皮质醇轻中度升高,尿24 h游离皮质醇升高,小剂量地塞米松抑制试验不受抑制,ACTH可以大于10 pmol/L[5]。肾上腺皮质分泌亢进主要是由于肾上腺皮质细胞数目的增多而并非单个细胞皮质醇合成能力旺盛。在AIMAH中,糖皮质激素合成相对来说是低效率的过程,这缘于在类固醇合成过程中几个关键酶表达水平下降,同时我们发现血浆中皮质醇合成的前体物质增加,这证明了单个肾上腺细胞合成激素的过程是低效率的[3,6]。尽管双侧肾上腺多发结节样增生,但是单个皮质细胞的激素合成效率降低,这种不协调可以解释那些缺乏临床表现的亚临床型患者。
影像学检查可见到双侧肾上腺受累,CT检查可以显示双侧肾上腺弥漫性增厚,侧肢增厚,面积增大,并且可以见到多发结节,整体观类似“生姜样”[7]。当双侧肾上腺结节大于5 cm,正常肾上腺形态通常消失,表现为肾上腺极不规则。肾上腺增生通常需要与垂体微小腺瘤引起促肾上腺皮质激素释放激素的过度分泌导致的双侧肾上腺增生及原发性色素性肾上腺结节性增生(PPNAD)相互鉴别,前者通过检测ACTH及垂体MRI可以鉴别。对于后者,肾上腺结节的大小一般1 cm左右,发病年龄较轻,多见于青春后期或成年早期[8],术中标本剖面可见到色素沉着,不同于原发性肾上腺大结节增生的均匀一致的金黄色。除此之外,与非ACTH依赖最常见的肾上腺皮质腺瘤的区别在于,由于一侧肾上腺皮质醇激素分泌旺盛,继发引起对侧肾上腺的皮质功能低下,切除肾上腺皮质腺瘤术后需要常规补充糖皮质激素,而对于原发性肾上腺大结节性增生,切除一侧肾上腺后,由于对侧肾上腺皮质醇分泌处于分泌增强,无需使用激素替代。本研究对象中16例行单侧肾上腺切除术,15例术后均未行糖皮质激素的补充,术后1年内均未出现皮质醇功能低下的症状。复查尿24 h游离皮质醇110~173 nmol,只有1例亚临床型患者,术后出现了乏力、恶心、呕吐的症状,行静脉补充氢化可的松治疗,症状改善,分析其原因,术前对侧肾上腺最大结节大小约1.8 cm,与首次切除侧肾上腺最大结节大小2.8 cm相比,增生程度较轻有关。原发性肾上腺大结节增生行双侧肾上腺切除术后,不会发生尼尔森综合征,此种现象间接证明了其为非ACTH依赖性这一特点[9]。
双侧肾上腺大结节增生导致肾上腺皮质分泌功能增强,主要表现在束状带过度分泌糖皮质激素,其次当肾上腺皮质功能亢进时,也会导致盐皮质激素的过度分泌,由于醛固酮的保钠排钾作用,患者可以伴有低血钾。本组研究患者中有6例患者伴有四肢乏力的表现,血钾最低2.4 mmol/L。卧位血浆醛固酮范围:409.96~678.65 pmol/L,血浆肾素:0.4~0.76 ng/mL。分析其原因,与醛固酮水平正常高值或高于正常有关,血浆肾素无明显减低。
双侧肾上腺切除术一直以来被认为是治疗双侧肾上腺大结节增生的金标准,国外学者Venanzi[10]报道了45例双侧肾上腺大结节增生患者,行腹腔镜双侧肾上腺切除术后,库欣综合征表现消失,无手术相关并发症出现。术后给予终身糖皮质激素替代治疗,效果满意。国内学者钟山[11]报道了3例双侧肾上腺切除治疗AIMAH患者,其中1例术后7 d内发生皮质功能危象死亡,另外2例患者术后终身糖皮质激素替代治疗。但是随着研究的深入,其安全受到挑战。众所周知,糖皮质激素替代和增加疾病的发病率及降低预期寿命有关,并且不会消除由于压力因素导致肾上腺危象的风险[12]。本研究中18例患者行单侧肾上腺切除术,其中12例有临床型库欣综合征的表现,10例术后3个月到半年内,满月脸、皮质紫纹、向心性肥胖等库欣症状消失,平均随访3年,库欣综合征的表现无复发,复查血尿皮质醇均恢复正常。另外2例临床型库欣患者单侧肾上腺切除术后复发分别予对侧肾上腺全切术、次全切除术。此2例患者术前CT检查双侧肾上腺大结节最大直径相差不大,其中1例保留侧肾上腺最大结节大小(6.5 cm)与首次切除一侧肾上腺大小(7.0 cm)相比体积明显超出正常范围,仍保持皮质醇分泌过度升高,继而导致库欣综合征复发。因为AIMAH中,皮质醇增多主要由于肾上腺皮质细胞数目增多引起,而非单个肾上腺细胞类固醇激素合成功能亢进所导致。6例亚临床患者,术后5例患者血压恢复到正常范围,1例患者降压药物的使用剂量下调,其中3例伴有糖尿病患者,2例空腹血糖恢复正常范围,1例血糖仍需胰岛素治疗,可能与原发性2型糖尿病有关。术后1年内未出现肾上腺皮质功能低下。复查尿24 h游离皮质醇及血浆皮质醇昼夜节律变化均正常。所有单侧肾上腺切除术后患者复查CT均未见到对侧肾上腺进行性增大。我们可以认为单侧肾上腺切除术是安全有效的治疗双侧肾上腺大结节增生的手段。双侧肾上腺切除术最大的弊端在于迫使患者终身服用糖皮质激素替代治疗,并且使得他们很容易出现肾上腺皮质不全危象。
双侧肾上腺切除已不再是双侧肾上腺大结节增生外科治疗的唯一手段,通过研究发现,单侧肾上腺切除术后,患者疗效确切,通过切除一侧肾上腺可以将肾上腺皮质醇的分泌降低到正常范围,术后少有对侧复发的情况,并且此术式保留了一侧肾上腺器官,不用担心糖皮质激素替代的问题。综合上述可见,单侧肾上腺切除术在治疗双侧肾上腺大结节增生中是有效安全的。
[1]张学斌,李汉忠.肾上腺大结节增生的外科治疗[J].中华泌尿外科杂志,2007,28(2):80
[2] Maghrabi A,Yaqub A,Denning K L,et al.Challenges in the diagnostic work-up and management of patients with subclinical Cushing’s syndrome and bilateral adrenal masses[J].Endocr Pract, 2013,19(3):515
[3] Lacroix A.ACTH-independent macronodular adrenal hyperplasia [J].Best Pract Res Clin Endocrinol Metab,2009,23(2):245
[4] Ohashi A,Yamada Y,Sakaguchi K,et al.A natural history of adrenocorticotropin-independent bilateral adrenal macronodular hyperplasia(AIMAH)from preclinical to clinically overt Cushing’s syndrome[J].Endocr J,2001,48(6):677
[5] Albiger N M,Ceccato F,Zilio M,et al.An analysis of different therapeutic options in patients with Cushing’s syndrome due to bilateral macronodu lar adrenal hyperplasia:a single-centre experience[J].Clin Endocrinol(Oxf),2015,82(6):808
[6] Shen W T,Lee J,Kebebew E,et al.Selective use of steroid replacement after adrenalectomy:lessons from 331 consecutive cases[J].Arch Surg,2006,141(8):771
[7]宋琦,周薇薇,苏颈为,等.ACTH非依赖性大结节样肾上腺增生的多层螺旋CT表现[J].中华内分泌代谢杂志,2012,28(4):335
[8] Xu Y,Rui W,Qi Y,et al.The role of unilateral adrenalectomy in corticotropin-independent bilateral adrenocortical hyperplasias[J]. World J Surg,2013,37(7):1626
[9] Louiset E,Duparc C,Young J,et al.Intraadrenal corticotropin in bilateral macronodular adrenal hyperplasia[J].N Engl J Med,2013, 369(22):2115
[10]De Venanzi A,Alencar G A,Bourdeau I,et al.Primary bilateral macronodular adrenal hyperplasia[J].Curr Opin Endocrinol Diabetes Obes,2014,21(3):177
[11]钟山,孙福康,刘定益,等.促肾上腺皮质激素非依赖性肾上腺皮质大结节样增生的外科治疗[J].中华泌尿外科杂志,2011,32(11):746
[12]Grossman A,Johannsson G,Quinkler M,et al.Therapy of endocrine disease:Perspectives on the management of adrenal insufficiency: clinical insights from across Europe[J].Eur J Endocrinol,2013,169 (6):R165
(2015-11-17收稿)
R736.6
A
1006-8147(2016)03-0262-04
魏文(1988-),男,硕士在读,研究方向:肾上腺肿瘤的诊治;通信作者:林毅,E-mail:linyi6312@hotmail.com。

