2-乙酰吡啶缩L-蛋氨酸铜(Ⅱ)配合物的合成、表征及与DNA相互作用
王强,林结双
(广西民族师范学院,广西崇左532200)
2-乙酰吡啶缩L-蛋氨酸铜(Ⅱ)配合物的合成、表征及与DNA相互作用
王强,林结双
(广西民族师范学院,广西崇左532200)
将2-乙酰吡啶与L-蛋氨酸在乙醇作为溶剂的情况下混合,并用氢氧化钾调节其pH,二者通过缩合反应,得到2-乙酰吡啶缩L-蛋氨酸配体。在此基础上,将配体与三水合硝酸铜进行反应,合成了铜配合物,使用紫外和红外光谱等手段对其进行表征。此外,选用紫外和荧光光谱法对配合物与DNA相互作用进行研究,结果表明配合物和DNA作用的模式是插入模式。
2-乙酰吡啶;L-蛋氨酸;结构表征;DNA作用
研究表明,医学上研究的某些有机物在抗癌、抗菌、抗炎等诸多方面发挥着越来越重要的作用,这类有机物通常都是含有-N=CH-基团。然而,当这些有机化合物与某些金属盐在温和条件下进行回流反应时,所得产物的抗癌作用将会大大增强[1]38-39,研究人员对此产生了浓厚的兴趣,并在此基础上进行了深入的研究,给医学领域、药物领域等的创新和发展,提供了不可或缺的作用,开辟了新的途径。氨基酸是人类必需的营养物质之一,可以用来合成蛋白质、酶和激素等物质,它是重要的两性物质,既含有氨基也有羧基,它这一特殊的结构决定了它具有很强的生理活性,可以和很多物质结合,进而得到理想的产物,给人类的生产生活以及生物化学过程带来了极大的帮助[2]74-78。本实验所用的氨基酸是甲硫氨酸也叫蛋氨酸,是组成人体的必需氨基酸之一,参与蛋白质的合成,但不能在体内自动合成,必须从外部获取。研究人员根据蛋氨酸所特有的氨基,将其与含羰基类的化合物如醛或酮在既定的条件下发生反应,即可得到具有多个强电负性的配位原子如N、O等的配体希夫碱,又将希夫碱配体和过渡金属盐进行配合,所得配合物的生物活性及其催化作用,经过不断的验证后发现,该配合物对生物化学和医药化学的研究意义非凡[3-4]118-119,422-424。例如,桂自其、田君濂合成的甲酰基甲酸氨硫脲希夫碱配合物对细菌的杀灭效果非常明显,而且形态各异,各有所长;华中师范大学化学系与湖北肿瘤医院合作,通过持续不断的研究后发现,希夫碱类化合物对人体各种癌症的抑制作用效果显著,为推动我国抗癌事业的进一步发展做出了极大的贡献[5]43-46。
正因为氨基酸希夫碱及其金属配合物具有良好的杀菌抗癌性能,研究人员对这方面的研究热度颇高。近年来,人们对希夫碱进行了更深层次的探讨后发现,氨基酸希夫碱同时还具有抗超氧离子自由基的特性,而且我们知道有些肿瘤、癌症正是因为人的体内超氧离子自由基O2-过多而引发的,此外,O2-过多也会造成某些炎症和衰老。一些研究专家通过不断的试验后发现,某些金属盐与希夫碱所形成的配合物对超氧离子自由基有很明显的抑制性能,而且,希夫碱本身也能对超氧离子自由基起到清除的效果。除此以外,部分希夫碱和它的金属配合物特有的发光性、光致变色性等诸多性质标志着这类有机物在科技和材料的研发方面前景非常广阔,很多科学家也在不断地进行这方面的研究,成果显著[6-7]65-69,98-100。
吡啶类物质生理活性较好,研究价值非常高,一直以来都是科研人员青睐的对象[8]451-460,其中,在众多吡啶类物质中,2-乙酰吡啶是一种非常优良的有机化合物,它与蛋氨酸化合形成的希夫碱配体及其金属配合物,操作简洁明了,反应温和,应用广泛涉及多个领域[9]266-267,270。文章采用L-蛋氨酸和2-乙酰吡啶,通过回流冷凝法,在非常温和的条件下,合成了2-乙酰吡啶缩L-蛋氨酸希夫碱配体,并将配体与三水合硝酸铜进行化合,合成了四种金属配合物,然后通过测定摩尔电导率、以及运用紫外可见光光谱法、红外光谱法分别对四种金属配合物进行表征。另外,DNA与配合物之间的作用,选用紫外可见吸收光谱和荧光光谱法对其进行研究。
一、实验部分
(一)主要仪器与试剂
DDA-11A型电导率仪(上海金万仪器表有限公司);RF-5301PC荧光分光光度计(日本岛津有限公司);UV 6100S型紫外可见分光光度计(上海元析仪器有限公司);红外光谱仪(天津拓普仪器有限公司)。
所用试剂均为市售分析纯或化学纯试剂,未进一步纯化。
(二)配体与金属配合物的合成
1.配体的合成
称取质量为1.3690 g的L-蛋氨酸和0.5038 g的氢氧化钾固体置于150 mL的圆底烧瓶中,并向烧瓶中加入20 mL无水乙醇,2滴蒸馏水,之后将烧瓶放到磁力搅拌器中,调节温度为40℃,加热搅拌0.5 h后,趁热过滤。随后将滤液倒入另一烧瓶中,用恒压滴液漏斗向其缓慢滴加1 mL(1.0812g)的2-乙酰吡啶的无水乙醇(20 mL)溶液,在65℃下搅拌回流3 h。回流结束后冷却至室温,静置2天,过滤,用无水乙醇洗涤2-3次,得到浅黄色固体,常温下干燥保存。
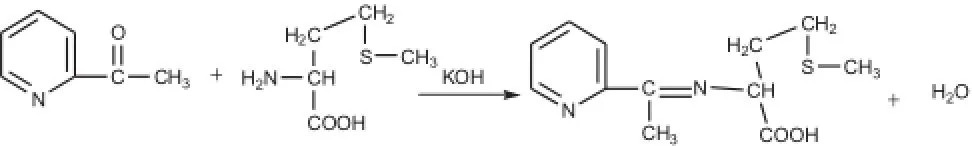
2.金属配合物的合成
称取三水合硝酸铜(Cu(NO3)2·3H2O)固体0.5973 g放入250 mL的圆底烧瓶中,并向其加入10 mL的无水乙醇,用玻璃棒搅拌溶解。用量筒量取15 mL配体溶液于恒压滴液漏斗中,以每秒2-3滴的速度滴入烧瓶,然后将烧瓶置于磁力搅拌器中,调节温度为65℃,搅拌回流6小时。回流结束后,将溶液趁热倒入100 mL烧杯中,冷却静置两天后,过滤,得到浅黄色固体,常温下真空保存。
(三)配合物的结构表征
1.摩尔电导率的测定
分别取少量金属配合物的固体溶解于无水乙醇当中,使其浓度约为l.02×10-4mol·L-1时,使用电导率仪进行测定,其摩尔电导率为15.52 S·cm2·mol-1。其值小于35 S·cm2·mol-1,可以判断出这些金属配合物为非电解质,而金属硝酸盐中的硝酸根参与了配位[10]73-79。
2.紫外-可见吸收光谱扫描
分别取少量配体及金属配合物固体,溶解于无水乙醇中,在比较温和的条件下,用无水乙醇作参比溶液,设置扫描波长为200nm~600 nm,使用UV-6100S型紫外可见分光光度计分别对上述溶液进行扫描,所得光谱图如图1所示。
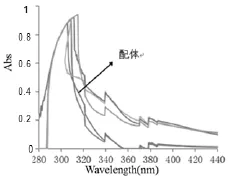
图1 配体与配合物UV光谱图
从图1中可知,2-乙酰吡啶缩L-蛋氨酸配体的吸收曲线在305.5nm处有最高峰,并且该峰非常强烈,而碳氮单键(C=N)的紫外吸收峰范围在200~400nm,该配体的吸收峰恰好出现在这个范围内,因此能够解释该配体已经形成了碳氮单键(C=N),属于希夫碱类物质。当吡啶缩L-蛋氨酸和铜金属盐溶液进行作用后,其吸收曲线的吸收峰发生了一定的红移,均有向右移动的趋势。在第一个吸收峰处,移动9nm;而第二个吸收峰处,移动10.5nm、,进一步表明,2-乙酰吡啶缩L-蛋氨酸希夫碱配体与铜离子发生了配位,希夫碱配合物已经形成。
3.红外光谱扫描
设置波长的扫描范围为4000~450 cm-1,对配体与配合物分别进行红外光谱扫描,所得谱图如图2、图3所示。
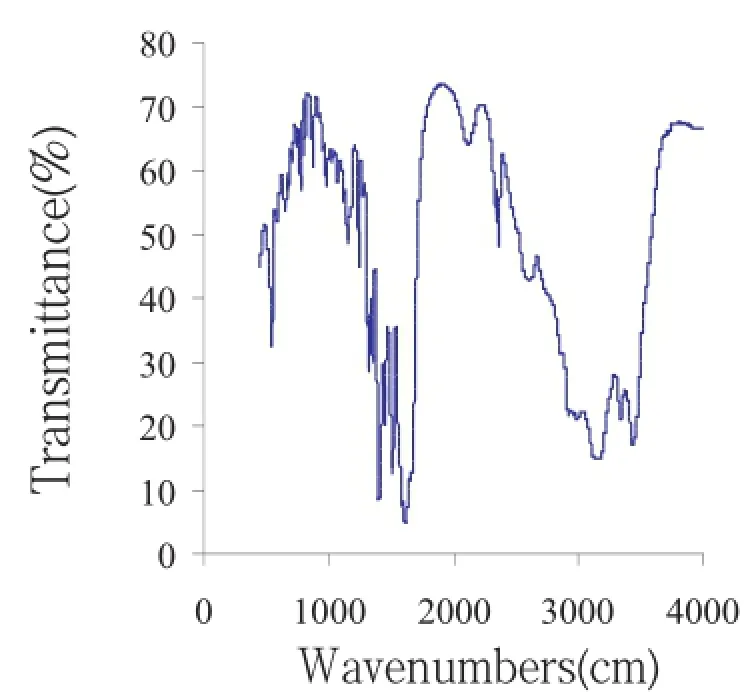
图2 IR配体的红外光谱图
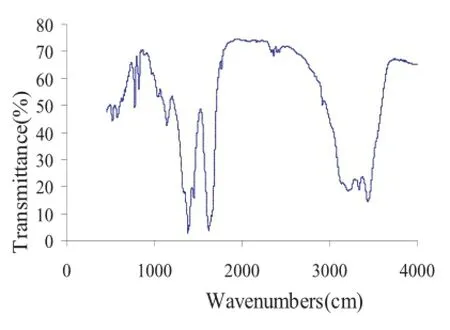
图3 IR铜配合物的红外光谱图
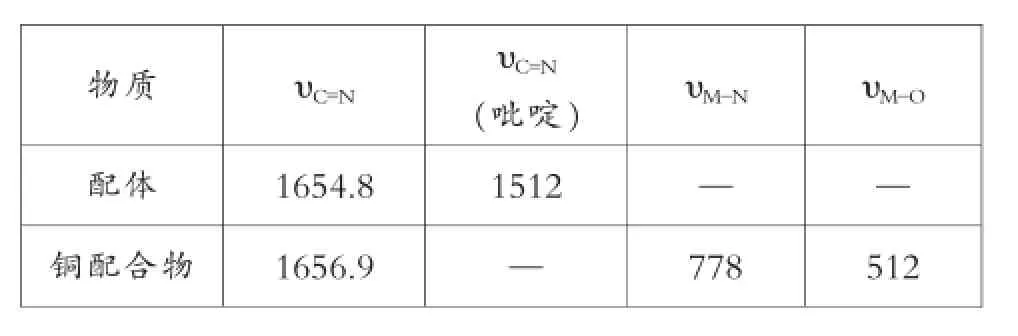
表1 配体和配合物主要的红外光谱峰值(cm-1)
结合图2、3以及表1中的数据可得知:
(1)配体及其配合物在3300cm-1处并没有出现类似马鞍形的两个吸收峰,因此可以断定,在配体及其配合物中并不存在伯胺基、仲氨基这样的结构。但在3000-3500 cm-1范围内却出现较宽的峰,由此可推测,这峰可能是合成碳氮双键时,脱去的水分子中的羟基发生振动所致,但也有可能是乙醇中的羟基发生振动[11-12]92,463-466。另外,在1000-800cm-1范围内出现了较明显的峰,这说明配合物中有水产生。
(2)与此同时,在2820-2729cm-1处,没有明显的吸收峰,说明吡啶环上的醛基已经与蛋氨酸上的氨基发生了反应,有可能产生碳氮双键。
(3)经查阅资料可知,碳氮双键(亚氨基)在1690-1630cm-1范围内存在较强的吸收峰,而本次实验合成的配体当中,碳氮双键的峰值为1654.8cm-1,刚好在这个范围内,并且,在配体与金属盐结合后,形成的配合物中,出现的碳氮双键峰值为1656.9cm-1,相对于配体而言,发生了一定的位移[13]58-60。
(4)配体和金属盐反应后,所得金属配合物出现了新的吸收峰,也就是M-N的伸缩振动,峰值为:778 cm-1,除此以外,又在512 cm-1处出现了配体中未出现的新的谱带为M-O的特征吸收峰,由此可以说明这四种金属离子都分别与2-乙酰吡啶缩L-蛋氨酸希夫碱配体中的N、O原子发生了配位。综上所述,该反应合成了希夫碱配体,并且该配体与金属盐发生了配位反应。
4.配合物可能的结构
根据以上的数据及其图表分析,可以初步得出配合物的结构可能为:

图4 金属配合物可能的结构图
二、配合物与DNA作用的研究
(一)溶液的配制
1.缓冲溶液的配制:用电子天平称量质量为0.6057g的三羟甲氨基甲烷固体,以及2.9220g的氯化钠,放入1000mL烧杯中,加入适量蒸馏水,搅拌溶解后,立即用pH计测定溶液的pH,滴加少量事先配制好的1mol/L的盐酸,用以调节溶液的pH,直至其pH为7.2。随后,将溶液通过玻璃棒引流,转入到1000mL的容量瓶中,用蒸馏水定容,摇匀便可。
2.鱼精DNA溶液的配制:用电子天平量取质量为0.0122g的鱼精DNA固体于100mL的烧杯中,立即倒入适量的事先配制好的缓冲溶液,将其快速溶解,随后将溶液转入100mL容量瓶中,用缓冲溶液进行定容,摇匀即可。
3.金属配合物溶液的配制:用电子天平分别称量0.0015 g的金属配合物固体,用事先配好的缓冲溶液进行溶解,使各金属配合物的浓度接近2.80×10-4mo l/L,以缓冲溶液定容于100mL容量瓶中,摇匀即可。
(二)配合物与DNA相互作用的研究方式
1.紫外-可见吸收光谱扫描
用规格为5mL的吸量管分别量取2.5mL金属配合物溶液于五个25mL的容量瓶中,然后,向五个容量瓶中分别加入不同浓度的鱼精DNA溶液:以0.0mL的DNA溶液为起点,做空白试验,以1mLDNA溶液为梯度,不断增加DNA溶液的体积,直至DNA溶液的体积增至5mL时,用事先准备好的缓冲溶液依次进行定容,摇匀后,把配制好的溶液放到阴暗处保存12小时。随后,使用紫外-可见吸收光谱进行扫描,选取缓冲溶液作为参比溶液,设置扫描波长为200~600nm,分别进行扫描。
IPA重要性和表现性分析法是1977年由Martilla 和 James所提出一种满意度评测模型工具,其基本思想是顾客对产品/服务的满意度来自于其对于该产品/服务各属性的重视程度,以及对各属性绩效表现程度的评价[5].IPA分析法有助于理解顾客满意度并明确服务质量应优先改进的领域,方法简单实用,分析结果易于理解,自上个世纪90年代开始被广泛运用到服务业之中用以分析产品或服务优劣势,提升服务质量和提高顾客满意[6].
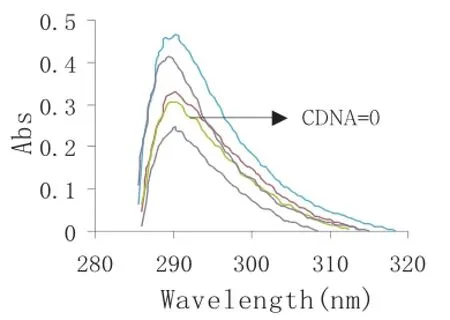
图5 铜配合物在CDNA/CComplex增大体系中的UV谱图
2.荧光光谱扫描
用规格为5mL的吸量管分别量取2.5mL金属配合物溶液于五个25mL的容量瓶中,然后,向五个容量瓶中分别加入不同浓度的鱼精DNA溶液:以0.0mL的DNA溶液为起点,做空白试验,以1mL DNA溶液为梯度,不断增加DNA溶液的体积,直至DNA溶液的体积增至5mL时,用事先准备好的缓冲溶液依次进行定容,摇匀后,把配制好的溶液放到阴暗处保存12小时。随后,使用荧光分光光度计进行扫描,选取缓冲溶液作为参比溶液,设置5nm的裂缝,二维为240nm/min,发射波长为350nm~450nm,激发波长为300nm~400nm,分别进行荧光扫描。
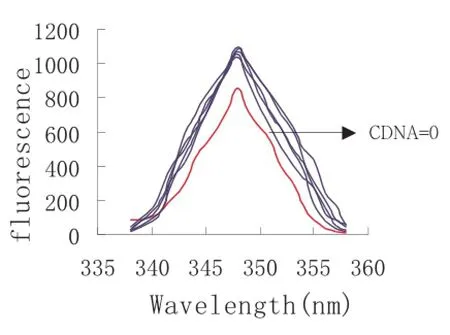
图6 铜配合物在CDNA/CComplex增大体系中荧光激发图
(三)配合物与DNA相互作用结果的讨论和分析
1.配合物与DNA作用的紫外-可见吸收光谱扫描和分析
从图5可发现,金属配合物的紫外吸收峰在不断升高,而且落在了285nm到290nm之间。另外,在加入DNA,并且随着DNA溶液浓度逐渐增大,曲线的红移现象越发明显,因此,可以说明,上述金属配合物都DNA发生了插入作用[14]86-88。
2.配合物与DNA相互作用的荧光光谱扫描分析
在保证金属配合物浓度一致的情况下,逐渐增加DNA溶液的浓度,分别测定溶液的发射光谱和激发光谱。据图6可知,随着加入DNA的浓度不断增加,配合物溶液的发射光谱和激发光谱也存在着逐渐增加的趋势,并且,与空白溶液即未加DNA的溶液进行比较后发现,加入DNA的配合物溶液的发射峰产生了微小的红移,由此可以说明,配合物与DNA进行了相互作用,导致DNA的结构发生了一定的变化。而此时,配合物的荧光强度在不断增加,说明配合物的基团由亲水性转入了疏水性,从而可以推测出金属配合物与DNA作用的方式是插入模式。
结语
经过不断的试验,发现了2-乙酰吡啶缩L-蛋氨酸配体及其金属配合物的最佳合成路线,即在一定条件下,先固定温度为40℃,并不停地进行搅拌,等L-蛋氨酸在无水乙醇溶液中逐渐溶解后,再缓慢滴加2-乙酰吡啶的无水乙醇溶液,随后把温度升高到65℃,回流反应3h即得到目标配体。将配体静置两天后,调节磁力搅拌器的温度为65℃,将配合物的无水乙醇溶液滴加到配体的无水乙醇溶液中,回流反应6h,便可制得配合物。选用紫外、摩尔电导率以及红外等的检测方式,推测出了配合物可能的结构。根据DNA浓度的不同对配合物的活性进行了探究,最后发现DNA与金属配合物的作用方式是插入模式。
[1]李晓萍.氨基酸席夫碱配合物的合成及性能研究进展[J].中国科技信息,2014,17.
[2]张然.氨基酸席夫碱金属配合物的研究进展[J].滨州学院学报,2010,26(3).
[3]SchiffH.Annalen.MittheilungenausdemUniversits laboratoriuminPisa:EineneueReiheorganischer Basen[J].1864,3.
[4]党元林,谢海泉,卓立宏.氨基酸席夫碱铬、钼配合物的合成与表征[J].信阳师范学院学报(自然科学版),2004,17(4).
[5]席晓岚,黎植昌.氨基酸Schiff碱及其金属配合物的抑菌抗癌活性的研究进展[J].氨基酸和生物资源,1998,20(4). [6]梁芳珍,江崇球,黄汝骐.新型荧光试剂N-2-噻唑基水杨醛亚胺Schiff碱的合成及荧光性质[J].合成化学,1999,7(2).
[7]赵建章,赵冰,徐蔚清,等.N-水杨醛缩-1-十六胺光致变色过程的光谱研究[J].光谱学与光谱分析,2001,21(1).
[8]计亮年,张黔玲,巢晖.多吡啶配合物在大分子DNA中的功能及其应用前景[J].科学通报,2001,46(6).
[9]杨名辉,李新生,陈义朗,等.新型含吡啶环大环席夫碱与铬离子配合物的合成及其生物活性[J].化学试剂,2002,24(5).
[10]戴寰,耿志明,韩志坚.2,6-二乙酰吡啶类双希夫碱及Mn (Ⅱ)、Fe(Ⅱ)、Fe(Ⅲ)配合物的合成和表征[J].无机化学学报,1989,5(3).
[11]中本一雄著,黄德如,汪庆仁译,等.无机和配位化合物的红外和拉曼光[M].北京:化学工业出版社,1986.
[12]范玉华,张栋梅,毕彩丰,等.异双希夫碱与La(Ⅲ)配合物的合成、热分解反应动力学和抑菌活性[J].中国海洋大学学报(自然科学版),2005,35(3).
[13]王强,范玉华,邱诗铭,等.邻香草醛缩L-蛋氨酸Zn(Ⅱ)配合物的合成与表征[J].广州化工,2013,41(6).
[14]侯琳熙,魏丹毅,干宁,等.新型Schiff碱双核铜配合物与DNA相互作用的光谱研究[J].光谱实验室,2007,24(2).
责任编辑:李凡生
Study on the Synthesis,Characterization and Interaction with DNA from 2-acetyl Pyridine Condensing L-methionine Cu(Ⅱ)Complexes
WANG Qiang,LIN Jie-Shuang
(Guangxi Normal University for Nationalities,Guangxi Chongzuo,532200)
Under the condition of mixing 2-acetyl Pyridine with L-Methionine in ethanol as solvent,and with potassium hydroxide to adjust its pH,2-aceto-pyridine condensation L-Methionine ligands can be obtained by the condensation reaction.On this basis,complexes of different synthesis can be obtained by the ligand respectively with Cu(NO3)2o3H2O,and Cu(Ⅱ)complexes was characterized by IR and UV spectra method.In addition,using IR and UV spectra method to study the interaction between the complexes and DNA,the results show that DNA and metal complexes of action is in insert mode.
2-acetyl Pyridine,L-Methionine;structural characterization,interaction with DNA
O621.4
A
1674-8891(2016)03-0007-04
2016-04-11
2013年度广西高等学校科学技术研究项目(编号:2013YB265);广西民族师范学院人才科研启动项目(编号∶2012RCBS001)。
王强(1973-),男,广西玉林人,博士,广西民族师范学院化学与生物工程系副教授,研究方向:有机合成、功能配合物。

