浅谈如何利用胶头滴管演示铜与硝酸的反应
浅谈如何利用胶头滴管演示铜与硝酸的反应
◇山东张丽波
在普通高中课程标准实验教学书人教版必修教材中,有一课时主要讲述稀硝酸与浓硝酸的化学性质,但是教材内容却只是简单地对铜和稀硝酸、铜和浓硝酸的化学反应方程式进行了介绍,并没有较详细的课堂实验演示.关于铜和硝酸的化学反应及其实验演示对于高中生在整个学习过程中都非常关键、重要.因此,笔者认为很有必要在以后的课堂教学中,将“铜与硝酸反应的装置设计”纳入到教学内容当中,并根据实际教学需要,适时的对实验设计及其实验方法进行创新.
1选择实践教学方法、确立教学设计思想
无论是人教版高中化学《必修1》教材还是苏教版《必修1》教材,在内容上都比较详细的介绍了铜与硝酸(浓硝酸、稀硝酸)之间的化学反应,但是关于实验探索的方法却不尽相同.
1.1实践教学指导思想
为了能够最大限度地克服此实验教学在课程体系中的缺陷,本次关于利用胶头滴管演示铜与硝酸反应的实验教学设计,主要还是以所使用的课本教材内容为背景来进行探究式、创新性的实践教学.
对于此次实验装置的设计以及操作实施,考虑到为了加深学生的理论认识以及巩固知识体系,决定将此次实验设计放到自习时间来进行,也就是将其安排在“硝酸的性质”学习之后.在实验过程中,并不是教师来主导,而是以全班学生为主体,根据铜与硝酸反应的实验目的以及实验原理,与学生一起对现行课本教材内容中关于实验设计进行研究分析,经历一番课堂探讨之后,教师提供实验器具,引导学生进行实验演示(实验操作以及实验装置设计根据教材内容进行创新、优化).此次实验的重点、难点就是让学生通过实践验证来充分思考硝酸的性质,进而培养学生分析问题、解决问题的思维能力、创新能力.
1.2实践教学框架设计(表1)
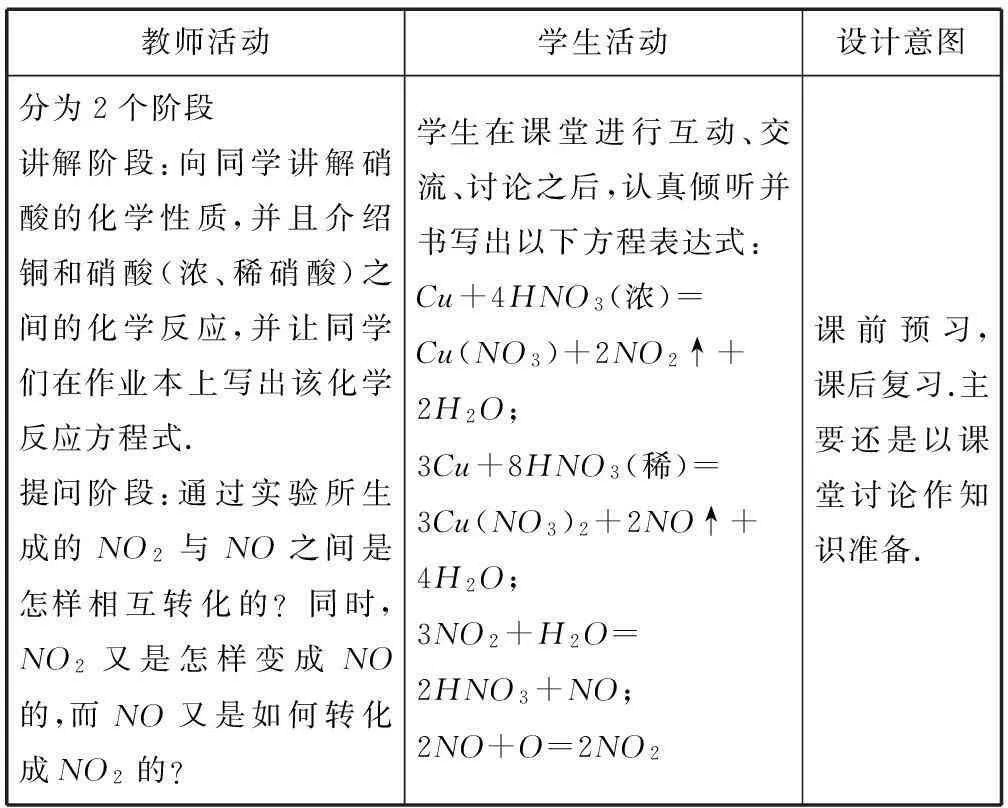
表1
2实验操作
2.1设计实验装置(图1)
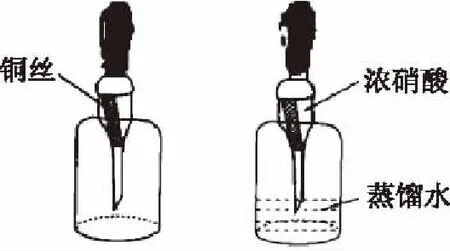
图1
2.2选取相关的实验设备、仪器、药品
本次实验需要准备的实验用品有烧杯、粗铜丝、浓硝酸、胶头滴管、乳胶管、滴瓶、NaOH溶液、蒸馏水、镊子、止水夹等.
2.3观察实验操作过程中的现象

图2
1) 铜和浓硝酸产生的化学反应.
图2是新型实验胶头滴管,主要是将常用的胶头滴管从中间部位切开,如图所示,之后再使用乳胶管将其连接.再如图1所示,选取一个准备好的洁净的,并且带有乳胶头滴管的的空滴瓶,然后再拔掉实验滴管上的胶头,从最上头的入口处装入弯曲的铜丝,最后将试管胶头紧紧的套牢(见图1左边的实验装置).在完成以上实验步骤之后,再用之前装有铜丝的乳胶头滴管,从烧杯中吸取出2滴管的蒸馏水,并并入到备好的滴瓶当中(见图1右边的实验装置),最后一步就是使用乳胶头滴管吸入一滴管的浓硝酸,并将其安全放入到滴瓶之中.
该实验操作化学反应对应的方程式,
Cu+4HNO3(浓)=Cu(NO3)+2NO2↑+2H2O.
在教师的引导下,让学生观察此次实验反应现象.观察到胶头滴管内浓硝酸液面迅速下降,瞬间变成了绿色液体,而胶头滴管内充满红棕色气体,其中的绿色液体为硝酸铜溶液,而红棕色气体为NO2气体.
2) 铜和稀硝酸产生的化学反应.
该实验步骤同上,当铜与稀硝酸开始发生反应时,此时会观察到在胶头滴管内所放置的铜丝,其表面明显有气泡逸出,此时胶头滴管内的气体表现为无色状态;片刻之后,再进行观察,发现铜丝表面上的气泡,其逸出的速度开始减慢,同时胶头滴管内的溶液也开始下降,溶液转变成无色气体.
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O.
3)H2O与NO2反应的化学方程式
3NO2+H2O=2HNO3+NO.
NO2与蒸馏水发生反应后,生成了无色气体NO,同时滴管内产生了硝酸铜的稀溶液.
4)O2与NO反应的化学方程式
2NO+O=2NO2.
反应产生出来的是红棕色的NO2;此时铜丝表明不再产生气泡,而乳胶头滴管内充满着大量的气体.在实验操作过程中,将胶头滴管慢慢提起,并顺势挤出滴管内的部分气体,之后再适当的吸入空气,通过观察,如4)的方程式所要表达的一样.
3实验总结
关于利用胶头滴管在课堂上演示铜与硝酸的反应实验,实验目的以及实验效果都得到了最大化的体现.本次实验操作装置是一种微型化的实验设计,是新课标教育改革下的一种教学创新,通过利用改进后的微型化实验装置进行的课堂实验演示,所起到的课堂教学效率是常规化学实验无法比拟的.
1) 反应装置比常规性实验装置小,在课堂上操作方便,节省课堂教学时间,节省试剂.
2) 在同一个实验装置当中能够同时实现铜和稀硝酸以及铜和浓硝酸的反应效果,O2和NO的反应、H2O与NO2的反应,并且其反应现象比常规性实验效果更为明显.
3) 本次实验过程中所产生的NO2、NO等污染物不会扩散,且方便收集,对于整个教学课堂的环境、人体的安全都不会产生危害,这也是在为学生宣传一种“绿色化学”的思想,极大地启迪了学生的学习思维以及培养学生环保、节约的理念意识.
(作者单位:山东省邹平县长山中学)

